En los pacientes con dislipidemia se deben alcanzar los objetivos terapéuticos para obtener la máxima reducción del riesgo de padecer eventos cardiovasculares, sobre todo de infarto de miocardio. A pesar de disponer de guías de práctica clínica y de fármacos hipolipidemiantes potentes, difícilmente se alcanzan los objetivos de colesterol de las lipoproteínas de baja densidad (cLDL), siendo una de las causas la inercia terapéutica. Para evitarla existen herramientas que permiten planificar el tratamiento y facilitar las decisiones. Sin embargo, uno de los problemas que se plantea en la clínica diaria para aplicarlas es desconocer el porcentaje de reducción de cLDL que se pretende conseguir para seleccionar el medicamento más adecuado. Eso es así tanto en la instauración del tratamiento como cuando se necesita modificar por no alcanzar el objetivo buscado. Este artículo propone un método práctico que puede ayudar a resolver estas cuestiones.
In patients with dyslipidemia, there is the need to reach the therapeutic goals in order to get the maximum benefit in the cardiovascular events risk reduction, especially myocardial infarction. Even having guidelines and some powerful hypolipidemic drugs, the goals of low-density lipoprotein-cholesterol (LDL-c) are often not reached, being of special in patients with a high cardiovascular risk. One of the causes is the therapeutic inertia. There are tools to plan the treatment and make the decisions easier. One of the challenges in everyday clinical practice is to know the needed percentage of reduction in LDL-c. Moreover: it is hard to know which one is the treatment we should use in the beginning of the treatment but also when the desired objective is not reached. This article proposes a practical method that can help solving these questions.
En el año 2001 se puso de relieve, en la literatura científica, la ausencia de toma de decisiones en el manejo terapéutico de trastornos crónicos en fases asintomáticas, como la hipertensión, la dislipidemia y la diabetes. Se denominó ‘inercia clínica’ la situación en que no se inicia, ni se intensifica ni modifica el tratamiento a pesar de estar indicado en las guías de práctica clínica (GPC)1. Posteriormente, se definió como ‘inercia terapéutica’ (IT) y, actualmente, el concepto de inercia clínica se ha ampliado a la falta de diagnóstico o seguimiento de los pacientes a lo largo del tiempo2. De hecho, podemos interpretar 2 tipos de IT: la de inicio, que se refiere al paciente no tratado y no controlado, y la de cambio, que hace referencia al paciente tratado pero no controlado.
Un caso especialmente paradigmático de inercia terapéutica es el control de la dislipidemia. Estudios realizados en Europa3 y en España4 ponen de manifiesto el escaso control del colesterol de las lipoproteínas de baja densidad (cLDL) especialmente relevante en pacientes con riesgo cardiovascular elevado.
Un ejemplo ilustrativo es el estudio poblacional DARIOS4, que analizó el grado de control alcanzado para los principales factores de riesgo cardiovascular modificables en población general de 35-74 años. Utilizó las categorías de riesgo coronario (RC) medido con la función calibrada REGICOR5, tras excluir a pacientes con cardiopatía isquémica (infarto de miocardio y angina). Se consideró buen control a partir de 2 tipos de criterios: a) los de las sociedades europeas (SE)6; cuando el cLDL era < 100mg/dl en diabéticos y en pacientes con alto-muy alto RC o si era < 115mg/dl en los demás (bajo-moderado RC); y b) los del Programa de Actividades Preventivas y Promoción de la Salud (PAPPS)7: cuando el cLDL era < 100mg/dl en diabéticos; si era < 130mg/dl en los pacientes con moderado, alto-muy alto RC y si era < 160mg/dl en los de bajo RC. Alcanzaron buen control menos del 3% de los pacientes en ambos sexos según criterios de las SE6, siendo insignificante la cifra de pacientes de alto y muy alto riesgo que alcanzó los objetivos. Con los criterios del PAPPS, la proporción de participantes bien controlados mejoró notablemente: un 46% de los varones y el 52% de las mujeres. Entre otros, el porcentaje de varones en los que no se inició tratamiento hipolipidemiante y que no estaban controlados, de alto y muy alto riesgo, según criterios menos ambiciosos del PAPPS, fue del 47 y 46% respectivamente. El 49% de varones de alto riesgo recibió tratamiento y, de estos, un 73,5% no estaban controlados. Se puso de manifiesto que cuanto más exigentes eran los objetivos, peores fueron los resultados.
Una publicación reciente, el estudio EDICONDIS-ULISEA8, realizado en pacientes remitidos por dislipidemia y riesgo cardiovascular a las unidades de lípidos y riesgo vascular de la Sociedad Española de Arteriosclerosis (SEA), analiza el grado de control de los objetivos terapéuticos de cLDL, de acuerdo con la guía europea de prevención cardiovascular 20076 (cLDL < 100mg/dl para los pacientes con enfermedad cardiovascular [ECV] o diabetes tipo 2 [DM2]). Los resultados indican que solo el 40,4% de los pacientes con ECV y el 35,8% de los que padecían DM2 cumplían con dichos objetivos al llegar a la unidad de lípidos. Los resultados registrados en la última visita un año después fueron del 65,3 y 50,4%, respectivamente, observándose una mejora tras el control de la unidad especializada. Cuando se aplican los criterios de las guías europeas más recientes9 solo el 17,9% de los pacientes con ECV y el 16,5% con DM2 alcanzaron una concentración de cLDL inferior a 70mg/dl. Tal cosa indica que existe una mejora en el grado de consecución de los objetivos respecto a estudios previos, realizados en otros ámbitos asistenciales. Sin embargo, pone también de manifiesto la necesidad de un control más eficaz de los pacientes dislipidémicos.
Las causas identificadas que pueden explicar el escaso control del cLDL, según estudios que analizan la IT, son atribuibles a la organización del sistema sanitario, al paciente y al médico2,10 (20, 30 y 50% de los casos, respectivamente)2. Como origen de la IT relacionada con la actuación médica se destacó: la insuficiente formación, el desconocimiento y bajo seguimiento de las GPC, la exigencia creciente de objetivos terapéuticos, la infrautilización de los tratamientos disponibles y la sobrestimación del control por parte del profesional2,3,10. Una causa posible, no descrita y que puede contribuir a no modificar el tratamiento, es la dificultad del cálculo rápido del porcentaje de cLDL que se debe reducir para llegar al objetivo.
El acto médico es una toma de decisiones constante y para facilitarlo es preciso contar con GPC sustentadas en la evidencia científica. Es necesario que estén adaptadas a la realidad, dirigidas a la consecución de objetivos terapéuticos, que ostenten credibilidad y cuyo fin sea facilitar la toma de decisiones. Además, para mayor facilidad, deberían estar integradas en los programas de historia clínica electrónica o de gestión de las consultas11.
Dado que en la actualidad estos recursos aún no están implementados en la práctica clínica diaria, proponemos un método sencillo que contribuye a afrontar y ayudar a evitar de forma práctica la IT.
Metodología aplicable en la consulta diaria para alcanzar los objetivos terapéuticos en colesterol de las lipoproteínas de baja densidadPara evitar la IT, desde un punto de vista teórico, los autores proponemos seguir los siguientes apartados en toda visita de un paciente con dislipidemia12.
- 1)
Realizar el diagnóstico de la dislipidemia, como indican las GPC.
- 2)
Determinar el RCV utilizando escalas de riesgo validadas, priorizando la identificación del paciente con alto RCV.
- 3)
Marcar el objetivo terapéutico de acuerdo con la GPC.
- 4)
Establecer el plan terapéutico para conseguir el objetivo terapéutico.
- 5)
Seguimiento y evaluación de resultados.
Así, desde un punto de vista práctico, en la clínica se presentan habitualmente 2 situaciones bien definidas:
A) Paciente no tratado y no controlado
Este caso correspondería a una IT de inicio. Para evitarla, se recomienda ofrecer de entrada el tratamiento a la dosis óptima para alcanzar el objetivo terapéutico12. Para ello existen herramientas que pueden facilitar la toma de decisiones, como por ejemplo las tablas de planificación terapéutica de la hipercolesterolemia13. Estas relacionan el nivel inicial de cLDL con el porcentaje de reducción de cLDL según el objetivo recomendado y las reducciones teóricas de cLDL proporcionadas por los hipolipidemiantes, estatinas y ezetimibe, en todo su rango de dosis.
B) Paciente tratado y no controlado
Partimos del cLDL en la visita actual en el paciente ya tratado con una estatina en monoterapia o asociada a ezetimibe y que no alcanza objetivos de control de acuerdo con la GPC.
Para evitar la IT de cambio sería conveniente seguir los siguientes pasos:
- 1.
Identificar las causas potenciales de no alcanzar el objetivo terapéutico12: las atribuidas al paciente (como el incumplimiento terapéutico) y las que dependen del fármaco (como las interacciones, efectos adversos y la falta de potencia).
- 2.
Modificar el tratamiento cuando sea posible, siguiendo una de las estrategias que permita alcanzar el objetivo terapéutico, como son: aumentar la dosis de la estatina que ya se está utilizando14, cambiar a una estatina más potente o combinar la estatina con otro fármaco hipolipidemiante12,13.
Dado que cada una de las estrategias consigue a priori un porcentaje de reducción diferente y, para evitar múltiples pasos que alargarían el tiempo hasta la consecución del objetivo terapéutico, sería de interés conocer el cLDL inicial y, de acuerdo al riesgo del paciente, el porcentaje que es necesario reducir13.
Una estrategia que facilitaría rediseñar el tratamiento sería disponer de una herramienta sencilla que permitiera conocer el cLDL previo al inicio del tratamiento y así poder aplicar las tablas de planificación terapéutica de la hipercolesterolemia. Posteriormente visualizaríamos el tratamiento que se precisa para llegar al objetivo terapéutico, escogiendo una modificación de las que se puedan realizar en el caso de haber más de una opción13.
¿Cómo disponer del colesterol de las lipoproteínas de baja densidad inicial previo al tratamiento?Cuando se presenta un paciente nuevo que ya recibe tratamiento pero está mal controlado, hay 2 supuestos sobre su cLDL inicial:
- 1.
El cLDL se conoce por tener acceso a la historia clínica y a la analítica del paciente13.
- 2.
El cLDL inicial no se conoce. En este caso se podría hacer una estimación teórica partiendo genéricamente del cLDL de la analítica actual, de 2 maneras posibles:
- a.
Adaptar el tratamiento a partir de un valor de cLDL un 30% superior al que presenta en la analítica actual, después de la intervención terapéutica, como recomiendan algunos autores13.
- b.
Pero, dada la diversidad de estatinas y teniendo en cuenta la diferente potencia de cada una de ellas, sería razonable añadir al valor de la analítica actual de cLDL el porcentaje de reducción teórico que ha proporcionado el tratamiento utilizado. Así tendríamos el cLDL de inicio calculado.
- a.
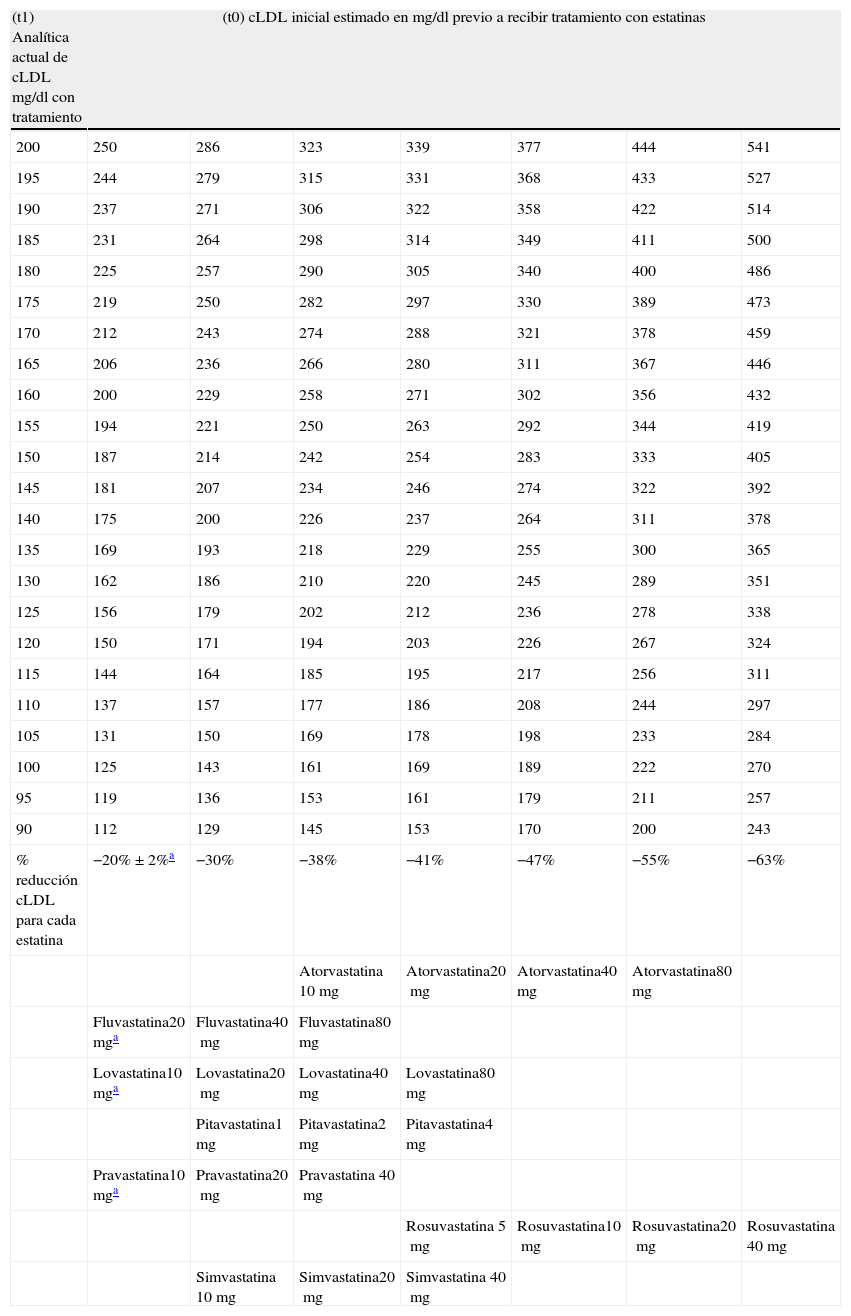
Para ello proponemos 2 tablas de uso sencillo en la consulta. En la tabla 1 se muestra el cLDL inicial estimado en pacientes en tratamiento con las estatinas disponibles y el porcentaje de reducción proporcionado en todas las dosis recomendadas15,16. Para confeccionarla hemos optado por utilizar los datos publicados por la FDA15 y, en aquellos casos en que no los había, hemos utilizado datos obtenidos de publicaciones relevantes16. En la misma no aparece ezetimibe por no estar recomendado en monoterapia de inicio sino solo recomendado como alternativa12.
Cálculo del cLDL inicial estimado en pacientes en tratamiento con estatinas en monoterapia
| (t1) Analítica actual de cLDL mg/dl con tratamiento | (t0) cLDL inicial estimado en mg/dl previo a recibir tratamiento con estatinas | ||||||
| 200 | 250 | 286 | 323 | 339 | 377 | 444 | 541 |
| 195 | 244 | 279 | 315 | 331 | 368 | 433 | 527 |
| 190 | 237 | 271 | 306 | 322 | 358 | 422 | 514 |
| 185 | 231 | 264 | 298 | 314 | 349 | 411 | 500 |
| 180 | 225 | 257 | 290 | 305 | 340 | 400 | 486 |
| 175 | 219 | 250 | 282 | 297 | 330 | 389 | 473 |
| 170 | 212 | 243 | 274 | 288 | 321 | 378 | 459 |
| 165 | 206 | 236 | 266 | 280 | 311 | 367 | 446 |
| 160 | 200 | 229 | 258 | 271 | 302 | 356 | 432 |
| 155 | 194 | 221 | 250 | 263 | 292 | 344 | 419 |
| 150 | 187 | 214 | 242 | 254 | 283 | 333 | 405 |
| 145 | 181 | 207 | 234 | 246 | 274 | 322 | 392 |
| 140 | 175 | 200 | 226 | 237 | 264 | 311 | 378 |
| 135 | 169 | 193 | 218 | 229 | 255 | 300 | 365 |
| 130 | 162 | 186 | 210 | 220 | 245 | 289 | 351 |
| 125 | 156 | 179 | 202 | 212 | 236 | 278 | 338 |
| 120 | 150 | 171 | 194 | 203 | 226 | 267 | 324 |
| 115 | 144 | 164 | 185 | 195 | 217 | 256 | 311 |
| 110 | 137 | 157 | 177 | 186 | 208 | 244 | 297 |
| 105 | 131 | 150 | 169 | 178 | 198 | 233 | 284 |
| 100 | 125 | 143 | 161 | 169 | 189 | 222 | 270 |
| 95 | 119 | 136 | 153 | 161 | 179 | 211 | 257 |
| 90 | 112 | 129 | 145 | 153 | 170 | 200 | 243 |
| % reducción cLDL para cada estatina | −20% ± 2%a | −30% | −38% | −41% | −47% | −55% | −63% |
| Atorvastatina 10mg | Atorvastatina20mg | Atorvastatina40mg | Atorvastatina80mg | ||||
| Fluvastatina20 mga | Fluvastatina40mg | Fluvastatina80mg | |||||
| Lovastatina10 mga | Lovastatina20mg | Lovastatina40mg | Lovastatina80mg | ||||
| Pitavastatina1mg | Pitavastatina2mg | Pitavastatina4mg | |||||
| Pravastatina10 mga | Pravastatina20mg | Pravastatina 40mg | |||||
| Rosuvastatina 5mg | Rosuvastatina10mg | Rosuvastatina20mg | Rosuvastatina 40mg | ||||
| Simvastatina 10mg | Simvastatina20mg | Simvastatina 40mg | |||||
cLDL: colesterol de las lipoproteínas de baja densidad.
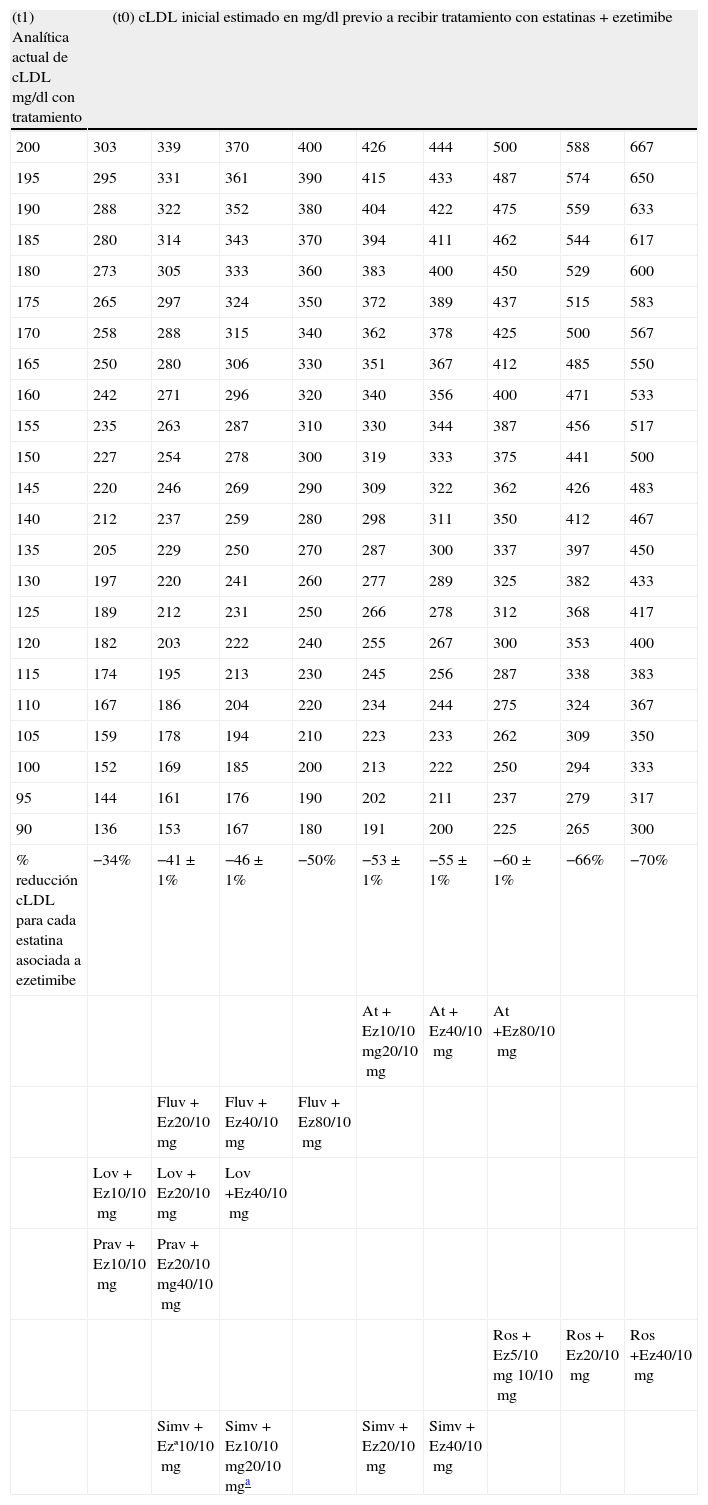
La tabla 2 muestra el cLDL inicial estimado en pacientes en tratamiento con estatinas en combinación con ezetimibe en todo su rango de dosis conocido15,16. Es posible que, en aquellos que reciben estatinas de alta potencia asociadas con ezetimibe, sea de escasa utilidad conocer su cLDL inicial estimado ya que, aunque no alcancen el objetivo terapéutico, posiblemente se habrá reducido más del 50% su cLDL y difícilmente se plantearía un cambio de medicación12.
Cálculo del cLDL inicial estimado en pacientes en tratamiento con la combinación de estatinas y ezetimibe
| (t1) Analítica actual de cLDL mg/dl con tratamiento | (t0) cLDL inicial estimado en mg/dl previo a recibir tratamiento con estatinas+ezetimibe | ||||||||
| 200 | 303 | 339 | 370 | 400 | 426 | 444 | 500 | 588 | 667 |
| 195 | 295 | 331 | 361 | 390 | 415 | 433 | 487 | 574 | 650 |
| 190 | 288 | 322 | 352 | 380 | 404 | 422 | 475 | 559 | 633 |
| 185 | 280 | 314 | 343 | 370 | 394 | 411 | 462 | 544 | 617 |
| 180 | 273 | 305 | 333 | 360 | 383 | 400 | 450 | 529 | 600 |
| 175 | 265 | 297 | 324 | 350 | 372 | 389 | 437 | 515 | 583 |
| 170 | 258 | 288 | 315 | 340 | 362 | 378 | 425 | 500 | 567 |
| 165 | 250 | 280 | 306 | 330 | 351 | 367 | 412 | 485 | 550 |
| 160 | 242 | 271 | 296 | 320 | 340 | 356 | 400 | 471 | 533 |
| 155 | 235 | 263 | 287 | 310 | 330 | 344 | 387 | 456 | 517 |
| 150 | 227 | 254 | 278 | 300 | 319 | 333 | 375 | 441 | 500 |
| 145 | 220 | 246 | 269 | 290 | 309 | 322 | 362 | 426 | 483 |
| 140 | 212 | 237 | 259 | 280 | 298 | 311 | 350 | 412 | 467 |
| 135 | 205 | 229 | 250 | 270 | 287 | 300 | 337 | 397 | 450 |
| 130 | 197 | 220 | 241 | 260 | 277 | 289 | 325 | 382 | 433 |
| 125 | 189 | 212 | 231 | 250 | 266 | 278 | 312 | 368 | 417 |
| 120 | 182 | 203 | 222 | 240 | 255 | 267 | 300 | 353 | 400 |
| 115 | 174 | 195 | 213 | 230 | 245 | 256 | 287 | 338 | 383 |
| 110 | 167 | 186 | 204 | 220 | 234 | 244 | 275 | 324 | 367 |
| 105 | 159 | 178 | 194 | 210 | 223 | 233 | 262 | 309 | 350 |
| 100 | 152 | 169 | 185 | 200 | 213 | 222 | 250 | 294 | 333 |
| 95 | 144 | 161 | 176 | 190 | 202 | 211 | 237 | 279 | 317 |
| 90 | 136 | 153 | 167 | 180 | 191 | 200 | 225 | 265 | 300 |
| % reducción cLDL para cada estatina asociada a ezetimibe | −34% | −41±1% | −46±1% | −50% | −53±1% | −55±1% | −60±1% | −66% | −70% |
| At+Ez10/10mg20/10mg | At+Ez40/10mg | At +Ez80/10mg | |||||||
| Fluv+Ez20/10mg | Fluv+Ez40/10mg | Fluv+Ez80/10mg | |||||||
| Lov+Ez10/10mg | Lov+Ez20/10mg | Lov +Ez40/10mg | |||||||
| Prav+Ez10/10mg | Prav+Ez20/10mg40/10mg | ||||||||
| Ros+Ez5/10mg 10/10mg | Ros+Ez20/10mg | Ros +Ez40/10mg | |||||||
| Simv+Ezª10/10mg | Simv+Ez10/10mg20/10 mga | Simv+Ez20/10mg | Simv+Ez40/10mg | ||||||
At: atorvastatatina; cLDL: colesterol de las lipoproteínas de baja densidad; Ez: ezetimibe; Fluv: fluvastatina; Lov: lovastatina; Prav: pravastatina; Ros: rosuvastatina; Simv: simvastatina.
En ambas tablas se diferencian las siguientes partes:
- 1.
En la primera columna de la izquierda se sitúan los niveles de cLDL en la visita actual del paciente tratado (tiempo t1).
- 2.
En el resto de columnas hacia la derecha se muestra la estimación del cLDL inicial sin recibir tratamiento (tiempo t0). Este se ha calculado a partir del cLDL de la analítica actual (tiempo t1) y del porcentaje de reducción teórico del tratamiento realizado (en la parte inferior de la tabla) con la siguiente fórmula: cLDL t0=cLDL t1+(%↓ cLDL teórico9 del tratamiento realizado en t0).
- 3.
En la parte inferior, aparecen las diversas estatinas con sus diferentes dosis y en combinación con ezetimibe, con el porcentaje de reducción teórico del cLDL.
Relacionando en la tabla el cLDL actual y el tratamiento recibido, podremos estimar el cLDL inicial y así podremos rediseñar el plan terapéutico óptimo para alcanzar el objetivo terapéutico13.
Un ejemplo práctico del uso de las tablas a modo ilustrativo:
Varón, de 67 años, con diabetes tipo 2 y cardiopatía isquémica establecida, remitido a la unidad de lípidos por presentar en su última analítica cLDL de 105mg/dl, en la actualidad está recibiendo tratamiento con simvastatina 20mg/día.
Ante un paciente de estas características, de muy alto riesgo vascular y una vez confirmado que sigue los consejos en hábitos de vida saludables, cumple adecuadamente con el tratamiento farmacológico y se ha descartado cualquier interacción que pueda interferir en la respuesta farmacológica, es preciso superar la inercia e instaurar una acción terapéutica. Es importante recordar que el objetivo aconsejado por las GPC9,12 es un cLDL < 70mg/dl. Para que resulte más fácil saber qué tratamiento es el óptimo, sería de utilidad disponer del cLDL que tenía antes de iniciar el tratamiento farmacológico. Si conocemos el valor por historia clínica, rediseñamos el tratamiento13. En el caso de no conocerlo, se puede buscar en la tabla 1 y relacionar el cLDL actual (105mg/dl) y el porcentaje de reducción teórico de simvastatina 20mg (−38%), el valor que se obtiene es de 169mg/dl. Según la tabla de planificación terapéutica se precisa una reducción de un 58% para llegar al objetivo terapéutico aconsejado13, por lo que deberíamos modificar el tratamiento. Si se observa la parte inferior de las tablas 1 y 2 también orientan sobre cuál serían las posibles estrategias a seguir para reducir al menos un 55%: atorvastatina 80mg, rosuvastatina 20mg, atorvastatina 40 mg combinada con ezetimibe 10 mg o simvastatina 40mg combinada con ezetimibe 10mg.
Por tanto, debemos saber qué paciente tenemos en nuestra consulta y estar dispuestos a evaluar nuestros resultados. En cada visita, debemos ser capaces de responder a las siguientes preguntas: ¿Qué tipo de dislipidemia tiene el paciente? ¿Qué riesgo vascular presenta? ¿Qué objetivo terapéutico tiene para su nivel de riesgo? ¿Lo cumple? ¿Está recibiendo el tratamiento óptimo? Si no lo cumple, ¿cuál es la causa? ¿Hemos iniciado el tratamiento a la dosis óptima o intensificado o modificado al no alcanzar los objetivos?
Para llevar a cabo todo esto, facilitaría la toma de decisiones disponer de herramientas de fácil manejo. Solo así podremos tratar adecuadamente a cada paciente y garantizar que estamos haciendo todo lo posible para anticipar las causas que favorecen la IT.
Las tablas que se presentan tienen la limitación de la variabilidad en la respuesta individual a las estatinas, que está bien documentada en la literatura15,16. Del mismo modo en la práctica diaria tenemos la misma limitación, ya que los datos que se utilizan para la planificación del tratamiento son los mismos en que nos hemos basado para su elaboración.
En conclusión, presentamos unas tablas con la intención de que sean un instrumento de manejo sencillo en la consulta diaria, que puede contribuir al mejor ajuste del tratamiento hipolipidemiante del paciente y a reducir nuestra propia IT.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.