Más allá del control de la glucemia existen otros objetivos importantes a la hora de brindar atención integral a pacientes con diabetes mellitus. Se realizó una revisión bibliográfica con el objetivo de identificar el papel que desempeñan los nuevos fármacos antidiabéticos en la prevención cardiovascular y la insuficiencia cardiaca. El uso de SGLT2i y GLP-1a acarrea una disminución significativa de eventos cardiovasculares, sin diferencias entre ambos, exceptuando las hospitalizaciones por insuficiencia cardiaca, en donde es evidente la superioridad de estos últimos (en especial dapaglifozina y empaglifozina). La evidencia actual respecto al efecto de los DPP-4i es diversa, aunque se observa un aumento del riesgo de hospitalizaciones por insuficiencia cardiaca con el consumo de algunos fármacos de esta clase (saxagliptina).
Beyond glucemic control there are other important goals when it comes to providing integral care to patients with diabetes mellitus. A bibliographic review was made in order to identify the role played by new antidiabetic drugs in cardiovascular prevention and heart failure. The use of SLGT2i and GLP1a leads to a significant decrease in cardiovascular events, with no difference between the two, except when it comes to hospitalizations for heart failure, where the superiority of the last ones (especially dapaglifozin and empaglifozin) is evident. The current evidence regarding the effect of dpp-4i is diverse, although an increased risk of hospitalizations for heart failure is observed with the use of some drugs of this class (saxagliptin).
La diabetes mellitus (DM) es una enfermedad crónica compleja que requiere cuidados médicos continuos con estrategias multifactoriales para la reducción de riesgo a través del control glucémico1.
Más allá del control de la glucemia existen otros objetivos importantes a la hora de brindar atención integral a pacientes con esta afección. Debido a la gran repercusión macrovascular y microvascular de este desorden, en la actualidad se hace mucho énfasis en la prevención e intervención en la enfermedad renal crónica (ERC), cardiopatía Isquémica (CI) e insuficiencia cardiaca (IC), las 3 asociadas con esta patología base1.
Existen 3 grupos farmacológicos más recientemente introducidos en la práctica cotidiana que han sido estudiados con este último propósito: los inhibidores del cotransportador sodio/glucosa tipo 2 (SGLT2i), los agonistas del receptor del péptido similar al glucagón tipo 1 (GLP-1a) y los inhibidores de la peptidil dipeptidasa 4 (DPP-4i)1,2.
Independientemente de la presencia de lesiones coronarias existe una relación directa entre la DM y la IC. Un término que se ha acuñado para referirse a esto es el de miocardiopatía diabética. Sus bases fisiopatológicas son la presencia de enfermedad microvascular, fibrosis, inflamación y alteraciones metabólicas miocárdicas3.
Un reciente estudio publicado en Circulation demostró que la presencia de DM en pacientes con factores de riesgo cardiovasculares adicionales representa un aumento significativo del riesgo de presentar CI de entre el 21% y el 111% según el número de factores de riesgo asociados. De la misma forma, el aumento del riesgo de hospitalizaciones por IC fue de entre el 31% y el 182%4.
Debido a lo planteado anteriormente, los autores del presente artículo se propusieron realizar una revisión bibliográfica con el objetivo de identificar el papel que desempeñan los nuevos fármacos antidiabéticos en la prevención cardiovascular y la IC.
Material y métodosSe realizó una búsqueda bibliográfica en las bases de datos Pubmed/Medline, ScienceDirect y AHA/ASA Journals complementado con el buscador Google Académico (fecha de última consulta 1 de diciembre de 2020).
Para la recuperación de la información se aplicó una estrategia de búsqueda utilizando las palabras clave Sodium-glucose co-transporter 2 inhibitor (SGLT2i), Glucagon-like peptide-1 receptor agonists (GLP-1 RA), Dipeptidylpeptidase-4 inhibitor (DPP-4i), Heart failure, Myocardial Ischemia y Type 2 Diabetes Mellitus. Se filtró por relevancia y se priorizaron los artículos originales, revisiones y metaanálisis
Se preseleccionaron 83 artículos los cuales fueron revisados en profundidad por los autores y se utilizaron en la confección del informe final un total de 53 referencias bibliográficas.
DesarrolloInhibidores del cotransportador sodio/glucosa tipo 2Los SGTL2i son fármacos que actúan inhibiendo el cotransportador sodio-glucosa en el túbulo contorneado proximal de las nefronas. De esta manera inhiben la reabsorción de glucosa en el riñón, originando glucosuria, con la consecuente disminución de la glucemia1,5.
Independientemente de este mecanismo existen otros más que intervienen en el beneficio cardiovascular que producen estos fármacos. Se han descrito efectos miocárdicos, efectos renales hemodinámicos y no hemodinámicos, efectos metabólicos no glucémicos, disminución de la hipoxia renal, aumento del hematocrito, efecto hipotensor y uricosuria5,6.
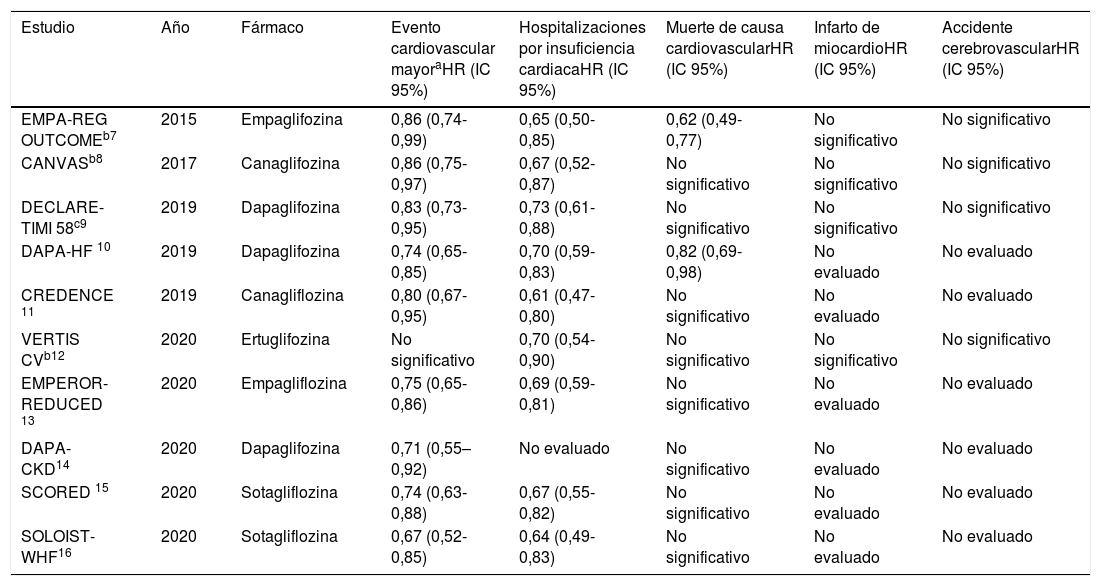
Hasta la fecha se han publicado un total de 10 ensayos clínicos aleatorizados multicéntricos relevantes, que han demostrado el beneficio real de estos fármacos en reducir eventos cardiovasculares mayores, hospitalizaciones por IC y muerte de causa cardiovascular (tabla 1).
Ensayos clínicos que evalúan la influencia de SGLT2i en resultados cardiovasculares
| Estudio | Año | Fármaco | Evento cardiovascular mayoraHR (IC 95%) | Hospitalizaciones por insuficiencia cardiacaHR (IC 95%) | Muerte de causa cardiovascularHR (IC 95%) | Infarto de miocardioHR (IC 95%) | Accidente cerebrovascularHR (IC 95%) |
|---|---|---|---|---|---|---|---|
| EMPA-REG OUTCOMEb7 | 2015 | Empaglifozina | 0,86 (0,74-0,99) | 0,65 (0,50-0,85) | 0,62 (0,49-0,77) | No significativo | No significativo |
| CANVASb8 | 2017 | Canaglifozina | 0,86 (0,75-0,97) | 0,67 (0,52-0,87) | No significativo | No significativo | No significativo |
| DECLARE-TIMI 58c9 | 2019 | Dapaglifozina | 0,83 (0,73-0,95) | 0,73 (0,61-0,88) | No significativo | No significativo | No significativo |
| DAPA-HF 10 | 2019 | Dapaglifozina | 0,74 (0,65-0,85) | 0,70 (0,59-0,83) | 0,82 (0,69-0,98) | No evaluado | No evaluado |
| CREDENCE 11 | 2019 | Canagliflozina | 0,80 (0,67-0,95) | 0,61 (0,47-0,80) | No significativo | No evaluado | No evaluado |
| VERTIS CVb12 | 2020 | Ertuglifozina | No significativo | 0,70 (0,54-0,90) | No significativo | No significativo | No significativo |
| EMPEROR-REDUCED 13 | 2020 | Empagliflozina | 0,75 (0,65-0,86) | 0,69 (0,59-0,81) | No significativo | No evaluado | No evaluado |
| DAPA-CKD14 | 2020 | Dapaglifozina | 0,71 (0,55–0,92) | No evaluado | No significativo | No evaluado | No evaluado |
| SCORED 15 | 2020 | Sotagliflozina | 0,74 (0,63-0,88) | 0,67 (0,55-0,82) | No significativo | No evaluado | No evaluado |
| SOLOIST-WHF16 | 2020 | Sotagliflozina | 0,67 (0,52-0,85) | 0,64 (0,49-0,83) | No significativo | No evaluado | No evaluado |
El estudio CANVAS de 2017 evaluó a la canaglifozina en pacientes con DM tipo 2. Comparado con placebo, este fármaco redujo la incidencia del compuesto primario conformado por muerte de causa cardiovascular, infarto de miocardio (IM) y accidente cerebrovascular (ACV). Además redujo las hospitalizaciones por IC8.
En concordancia con estos resultados, los ensayos CREDENCE, EMPEROR REDUCED, SCORED y SOLOIST-WHF mostraron una disminución de las hospitalizaciones por IC entre un 31% (EMPEROR REDUCED) y un 39% (CREDENCE). Sin embargo, estos estudios evidenciaron una reducción de la mortalidad cardiovascular en los compuestos primarios pero no al evaluar en solitario esa variable11,13,15,16.
Iborra-Egea et al.17, en un estudio preclínico, demostraron que la empaglifozina realiza un bloqueo directo en el intercambiador sodio-hidrógeno tipo 1, lo cual disminuye la apoptosis de cardiomiocitos en ratas con IC, sin diferencias entre diabéticos y no diabéticos.
Esto podría explicar el claro beneficio que se obtiene con los SGLT2i en individuos con IC y fracción de eyección reducida.
Otro estudio preclínico evidenció que en ratones con falla cardiaca y fracción de eyección del ventrículo izquierdo preservada la empaglifozina disminuye la masa ventricular izquierda, mejorando la función diastólica18.
Este resultado refrendaría la hipótesis de que el beneficio de los SGLT2i también puede observarse en pacientes con IC con disfunción diastólica como mecanismo fisiopatológico predominante. En estos momentos se encuentra en curso el estudio EMPEROR-Preserved (NCT03057951) para comprobar dicha hipótesis.
Ademas, Januzzi et al.19 comprobaron que el consumo de SGLT2i en individuos entre 55 y 80 años con DM se asocia de forma estadísticamente significativa con concentraciones séricas menores de péptidos natriuréticos y de troponinas i a los 2 años de seguimiento.
Solo 2 ensayos clínicos han demostrado una reducción significativa de la mortalidad cardiovascular al evaluar esta variable en solitario.
El EMPA-REG OUTCOME comparó empaglifozina vs. placebo en individuos con DM tipo 2. La empaglifozina redujo la incidencia de un compuesto primario conformado por muerte de causa cardiovascular, IM y ACV. Además redujo la incidencia de hospitalizaciones por IC y la mortalidad de causa cardiovascular7.
El ensayo DAPA HF publicado en 2019 en New England Journal of Medicine evaluó dapaglifozina vs. placebo tanto en individuos diabéticos como en otros sin esta patología de base. Este SGLT2i se asoció a una reducción en el endpoint primario (muerte de causa cardiovascular u hospitalización por IC). Además redujo las hospitalizaciones por IC y la mortalidad cardiovascular10.
Lo más llamativo de los resultados de ese estudio es que evidenciaron una reducción de la mortalidad cardiovascular y de las hospitalizaciones por IC tanto en diabéticos como en no diabéticos.
El estudio EMPA-TROPISM demostró que la empaglifozina en pacientes no diabéticos con IC y fracción de eyección reducida produce una mejora significativa de los volúmenes ventriculares izquierdos, masa ventricular izquierda, fracción de eyección, capacidad funcional y calidad de vida al compararse con placebo, a los 6 meses de la aleatorización20.
Estos resultados justifican la reducción de la mortalidad cardiovascular y las hospitalizaciones por IC arrojadas por el DAPA HF.
En una cohorte de pacientes diabéticos con alto riesgo cardiovascular realizada por Udell et al.21 el inicio de tratamiento con SGLT2i se asoció con un menor riesgo de 2 objetivos primarios compuestos por muerte de cualquier causa y hospitalizaciones por IC y por muerte de cualquier causa, IM y ACV.
Couselo-Seijas et al.22 en un reciente estudio demostraron que la dapaglifozina mejora el metabolismo de oxidación de la glucosa, sin cambios en los genes involucrados en el almacenamiento de los lípidos, con una reducción significativa del lactato liberado y la acidosis en la grasa pericárdica.
Este beneficio metabólico puede justificar el efecto de los SGLT2i en la reducción de la incidencia de IM y en la mortalidad de causa cardiovascular.
En contraste con esos resultados, los ensayos DECLARE TIMI 58 y VERTIS CV no arrojaron una reducción significativa de la mortalidad cardiovascular sola o evaluada en un objetivo primario compuesto con IM o ACV. El DECLARE TIMI 58 mostró entre sus resultados una disminución de un 27% en las hospitalizaciones por IC comparando dapaglifozina vs. placebo en individuos diabéticos, mientras que en el VERTIS CV esta reducción fue de un 30% con ertuglifozina. Además, en el DECLARE TIMI 58 hubo reducción en un objetivo secundario compuesto por muerte de causa cardiovascular y hospitalizaciones por IC9,12.
El estudio DAPA-CKD evaluó dapaglifozina vs. placebo, notificándose en el brazo del SGLT2i una disminución de la incidencia de ERC terminal, descenso mayor de un 50% del filtrado glomerular basal y/o muerte de causa cardiovascular o renal, así como una reducción del compuesto entre muerte de causa cardiovascular y hospitalizaciones por IC14.
Lo anteriormente planteado demuestra un claro beneficio del uso de los SGLT2i en la reducción de hospitalizaciones por IC. Tanto dapagliflozina como empagliflozina se han asociado con reducción de la mortalidad cardiovascular. Existe evidencia de que estos fármacos suponen un beneficio respecto a eventos cardiovasculares y cerebrovasculares mayores, aunque no se observa reducción significativa de las incidencias de IM o ACV al evaluar estas variables de forma individual, pese a que dentro de variables compuestas sí se ha observado esta ventaja.
Agonistas del receptor del péptido similar al glucagón tipo 1El péptido similar al glucagón tipo 1 (GLP 1) es una hormona incretina, sintetizada por células L del íleon distal y el colon, que estimula la secreción pospandrial de insulina de manera dependiente de la glucosa sanguínea, suprimiendo la secreción posprandial de glucagón, disminuyendo el vaciamiento gástrico y reduciendo la ingesta de alimentos2,23.
El efecto favorable de los agonistas del receptor de GLP1 sobre la función endotelial, el aumento de la entrega de oxígeno al músculo esquelético, la disminución de la tensión arterial, los valores de proteína C reactiva, el activador del plasminógeno tipo 1, el péptido natriurético cerebral, además de posibles efectos directos sobre el miocardio y la función sistodiastólica ventricular motivaron la realización de estudios para evaluar su efecto protector en los pacientes con DM tipo 2 y enfermedades cardiovasculares2,24.
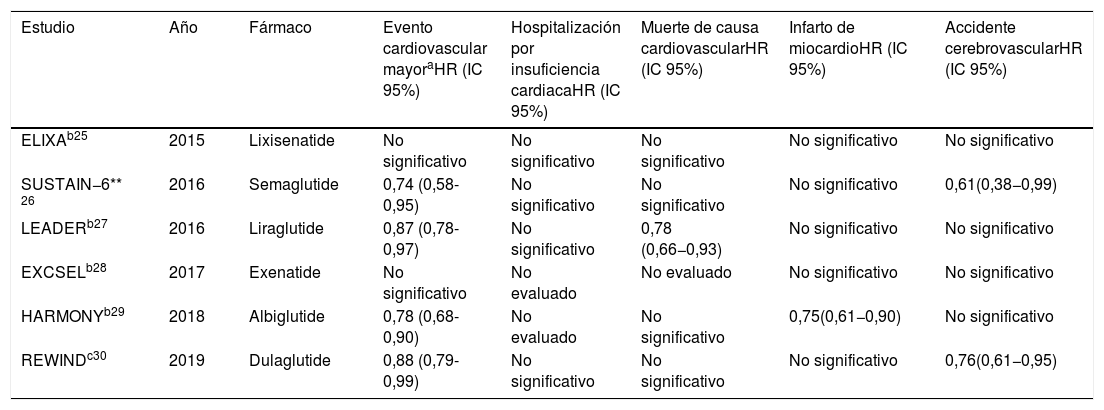
Hasta la fecha han sido publicados un total de 5 ensayos clínicos aleatorizados multicéntricos relevantes con resultados favorables de estos fármacos en la reducción de eventos cardiovasculares mayores (tabla 2).
Ensayos clínicos que evalúan la influencia de GLP-1a en resultados cardiovasculares
| Estudio | Año | Fármaco | Evento cardiovascular mayoraHR (IC 95%) | Hospitalización por insuficiencia cardiacaHR (IC 95%) | Muerte de causa cardiovascularHR (IC 95%) | Infarto de miocardioHR (IC 95%) | Accidente cerebrovascularHR (IC 95%) |
|---|---|---|---|---|---|---|---|
| ELIXAb25 | 2015 | Lixisenatide | No significativo | No significativo | No significativo | No significativo | No significativo |
| SUSTAIN−6** 26 | 2016 | Semaglutide | 0,74 (0,58-0,95) | No significativo | No significativo | No significativo | 0,61(0,38−0,99) |
| LEADERb27 | 2016 | Liraglutide | 0,87 (0,78-0,97) | No significativo | 0,78 (0,66−0,93) | No significativo | No significativo |
| EXCSELb28 | 2017 | Exenatide | No significativo | No evaluado | No evaluado | No significativo | No significativo |
| HARMONYb29 | 2018 | Albiglutide | 0,78 (0,68-0,90) | No evaluado | No significativo | 0,75(0,61−0,90) | No significativo |
| REWINDc30 | 2019 | Dulaglutide | 0,88 (0,79-0,99) | No significativo | No significativo | No significativo | 0,76(0,61−0,95) |
En el año 2015 se publicaron los resultados del estudio ELIXA, el cual evaluó lixisenatide en pacientes con diagnóstico de DM tipo 2 y antecedentes de evento coronario agudo en los 180 días previos; comparado con placebo no demostró reducción de ninguno de los objetivos evaluados25.
En contraposición a estos resultados, los ensayo SUSTAIN−6 y LEADER publicados al año siguiente, sí obtuvieron una reducción en los eventos cardiovasculares y cerebrovasculares mayores en pacientes con DM tipo 2 y riesgo cardiovascular alto (en el caso de estudio LEADER) al comparar el tratamiento con semaglutide y liraglutide respecto a placebo. Además este último fármaco mostró una disminución en la incidencia de muerte de causa cardiovascular y en el ensayo SUSTAIN−6 se evidenció una reducción en la incidencia de ACV no fatal26,27.
Lambadiari et al.31 en un ensayo clínico publicado en Cardiovascular Diabetology que comparaba el uso de metformina y liraglutide, demostraron diferencias significativas en cuanto a la rigidez arterial, strain longitudinal global del ventrículo izquierdo, valores de NT−pro BNP así como otros parámetros de motilidad y deformación ventricular izquierda con reducción del estrés oxidativo en pacientes con nuevo diagnóstico de DM tipo 2 que fueron sometidos a tratamiento con GLP-1a, lo cual evidencia hasta cierto punto algunos de los efectos protectores cardiovasculares de estos nuevos fármacos antidiabéticos.
En contraposición a algunos de estos resultados, la investigación de Kumarathurai et al.32 no mostró diferencias significativas en el tratamiento con liraglutide respecto a placebo en cuanto a incremento de la función sistólica del ventrículo izquierdo en pacientes diabéticos tipo 2 y enfermedad arterial coronaria estable sometidos a ecocardiografía de estrés con dobutamina, ni aumento en la capacidad de ejercicio.
Estos datos muestran lo diversos que han sido los hallazgos en múltiples estudios que abordan el uso de los GLP-1a en pacientes diabéticos con enfermedades cardiovasculares.
En 2017 el estudio EXCSEL evaluó el fármaco exenatide administrado semanalmente (vs. placebo) en pacientes diabéticos tipo 2 con o sin antecedentes de enfermedad cardiovascular previa. No arrojó diferencias significativas en el compuesto primario conformado por muerte de causa cardiovascular, IM no mortal y ACV. El ensayo no evaluó la incidencia de hospitalizaciones por IC28.
Paralelo a esto Scalzo et al.24 en otro estudio encontraron resultados favorables con el uso de exenatide respecto a placebo en pacientes diabéticos tipo 2 no complicados, con mejora en la función diastólica y reducción de la rigidez arterial, pero estos no estuvieron acompañados de aumento en la capacidad de realizar ejercicio.
Si bien no fueron evaluados objetivos primarios similares en ambos ensayos clínicos, los resultados de cierto modo se contraponen, pues es conocida la asociación entre rigidez arterial y la mayoría de los factores de riesgo cardiovascular, y por tanto su reducción así como la mejora de la función cardiaca debería conllevar una menor incidencia de eventos cardiacos mayores y una mejor calidad de vida, disminuyendo el número de eventos coronarios agudos a largo plazo. Una mayor capacidad para la realización de ejercicios físicos y en consecuencia una mejor capacidad funcional, hipotéticamente implicaría una reducción de las hospitalizaciones por IC, pero no fue evaluada en ninguno de estos estudios.
El ensayo HARMONY determinó la superioridad del fármaco albiglutide respecto a placebo en la reducción de eventos cardiovasculares mayores sin evaluar las hospitalizaciones por IC y no mostró superioridad al valorar la muerte de causa cardiovascular en solitario, pero sí arrojó una disminución en la incidencia de IM fatales o no29.
Un ensayo clínico realizado por Lepore et al.33 y publicado en Journal of American College of Cardiology reveló que comparado con placebo no hubo incremento de la función cardiaca medida por ecocardiografía ni reducción del consumo miocárdico de oxígeno o uso de glucosa por el músculo cardiaco en individuos tratados con albiglutide.
De forma similar al HARMONY, el estudio aleatorizado multicéntrico REWIND demostró la superioridad de dulaglutide comparado con placebo en pacientes diabéticos mayores de 50 años con diagnóstico previo de enfermedad cardiovascular o factores de riesgo, en cuanto a disminución de la incidencia de eventos cardiacos mayores, sin diferencias significativas en lo referente a muerte de causa cardiovascular u hospitalización por IC, aunque sí mostró reducción de la incidencia de ACV no fatal al evaluar la variable de manera independiente30.
Los grandes estudios que han involucrado a los fármacos GLP-1a en el tratamiento de la DM tipo 2 han puesto en evidencia disímiles resultados y se han mostrado seguros en el tratamiento de pacientes con enfermedades cardiovasculares concomitantes o factores de alto riesgo para las mismas. Los ensayos clínicos SUSTAIN−6, LEADER, HARMONY y REWIND reflejaron una reducción de eventos cardiovasculares y cerebrovasculares mayores, con efectos neutros sobre la mortalidad de causa cardiovascular (excepto el estudio LEADER), muerte por cualquier causa, IM no fatal, ACV no fatal, así como las hospitalizaciones por IC.
Inhibidores de la peptidil dipeptidasa 4Los DPP-4i son fármacos antidiabéticos que actúan inhibiendo la enzima peptidil dipeptidasa 4; estas aumentan los niveles y potencian la acción de las incretinas endógenas, produciendo un aumento de la secreción de insulina y disminución de la secreción de glucagón2.
La inhibición de dicha enzima potencia las acciones de los GLP1, y además modula las actividades de varios péptidos vasculares asociados con efectos protectores cardiacos2.
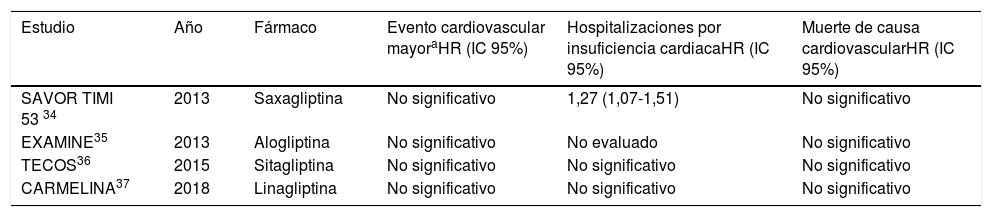
Sin embargo, ninguno de los múltiples ensayos clínicos aleatorizados realizados ha demostrado beneficio real en la reducción de los eventos cardiovasculares mayores, hospitalizaciones por IC y muerte de causa cardiovascular (tabla 3).
Ensayos clínicos que evalúan la influencia de DPP-4i en resultados cardiovasculares
| Estudio | Año | Fármaco | Evento cardiovascular mayoraHR (IC 95%) | Hospitalizaciones por insuficiencia cardiacaHR (IC 95%) | Muerte de causa cardiovascularHR (IC 95%) |
|---|---|---|---|---|---|
| SAVOR TIMI 53 34 | 2013 | Saxagliptina | No significativo | 1,27 (1,07-1,51) | No significativo |
| EXAMINE35 | 2013 | Alogliptina | No significativo | No evaluado | No significativo |
| TECOS36 | 2015 | Sitagliptina | No significativo | No significativo | No significativo |
| CARMELINA37 | 2018 | Linagliptina | No significativo | No significativo | No significativo |
El estudio SAVOR- TIMI 53 realizado en 2013, que evaluó saxagliptina contra placebo en pacientes con DM tipo 2, mostró un aumento de hospitalizaciones por IC, sin embargo, no se obtuvieron diferencias significativas en la incidencia del compuesto primario conformado por ACV,IM y muerte de causa cardiovascular34.
Un reciente metaanálisis evaluó a pacientes diabéticos tratados con DPP-4i. Este mostró un aumento de las hospitalizaciones por IC, en concordancia con el SAVOR TIMI 5338.
En contraposición, los otros grandes ensayos clínicos con DPP-4i no revelaron diferencias significativas respecto a la incidencia de hospitalizaciones por IC36,37.
Los estudios EXAMINE, TECOS y CARMELINA evaluaron alogliptina, sitagliptina y linagliptina respectivamente en pacientes diabéticos. Estos no mostraron diferencias respecto a placebo de un objetivo primario compuesto por muerte de causa cardiovascular, IM o ACV35–37.
Un metaanálisis realizado en 2017 evaluó el efecto de los DPP-4i en la IC, sin aumento significativo de hospitalizaciones por la misma en los pacientes tratados con vildagliptina, sitagliptina o saxagliptina, pero la alogliptina fue asociada a un mayor riesgo de este evento, resultados contrarios a los obtenidos en los estudios SAVOR TIMI 53 y EXAMINE39.
Por otro lado, el estudio ESPECIAL-ACS valoró el efecto de la sitagliptina sobre los cambios de la placa coronaria en pacientes diabéticos con síndrome coronario agudo tratados mediante intervencionismo coronario. Utilizando ultrasonidos intravasculares seriados se comparó el tratamiento con sitagliptina, dieta y ejercicios, frente a dieta y ejercicios solamente. El ensayo mostró una reducción significativa en cuanto al volumen lipídico de la placa de ateroma en los pacientes tratados con sitagliptina, pero no se hallaron diferencias significativas en la disminución del volumen total de la placa coronaria entre un grupo y otro40.
El estudio PROLOGUE evaluó la progresión de la ateroesclerosis carotídea a través del cociente íntima media en pacientes con DM tipo 2 tratados con sitagliptina vs. terapia convencional mediante la realización de doppler carotídeo, sin revelar diferencias significativas en la reducción de la progresión de la ateroesclerosis entre ambos subgrupos41.
Estos resultados indican un probable beneficio fisiopatológico de estos fármacos en la CI, aunque en la práctica no se ha podido corroborar.
Un subanálisis del PROLOGUE evaluó durante 2 años la progresión de la rigidez arterial en pacientes diabéticos tratados con sitagliptina vs. antidiabéticos convencionales, a partir de la medición de la velocidad de la onda de pulso. Los cambios en este parámetro fueron similares en pacientes de ambos grupos, demostrando que los pacientes con un pobre control glucémico experimentaron un mayor aumento de esta cuantificación42.
Otro subanálisis del PROLOGUE evaluó la función diastólica mediante la relación E/é mostrando una disminución significativa de esta relación en los pacientes tratados con sitagliptina a los 2 años de seguimiento43.
En correspondencia con estos estudios, un subanálisis del ensayo REASON evaluó los efectos de anagliptina y sitagliptina en la concentración de la adipocina FABP4, cuya elevación se asocia con obesidad, resistencia a la insulina y aterosclerosis. El estudio se realizó en pacientes diabéticos tipo 2 con alto riesgo de eventos cardiovasculares. Los niveles de FABP4 en plasma disminuyeron un 7,9% en los pacientes tratados con anagliptina, sin disminución significativa en los pacientes que recibieron sitagliptina44.
Esto último pone en duda si los probables beneficios fisiopatológicos de algunos DPP-4i en las afecciones cardiovasculares tienen efecto clase y por tanto no son atribuibles al resto de fármacos del grupo.
Comparación entre los grupos farmacológicosTodo lo planteado previamente demuestra el claro beneficio de los SGLT2i y de los GLP-1a en la reducción de eventos cardiovasculares mayores, así como la aparente falta de utilidad de los DPP-4i para este fin. Sin embargo hay contextos clínicos en los que es útil seleccionar entre uno y otro grupo farmacológico en base al beneficio específico deseado.
Kramer et al.45 en un metaanálisis de 9 ensayos clínicos compararon los 3 grupos en base al riesgo de hospitalizaciones por IC. Los SGLT2i comparados con placebo redujeron este evento en un 44%, a diferencia de las otras 2 clases farmacológicas, lo cual era esperable teniendo en cuenta los resultados de los ensayos clínicos disponibles.
En concordancia con lo anterior, otro metaanálisis evidenció que tanto los SGLT2i como los GLP-1a se asociaron a una disminución de la mortalidad al compararlos con placebo y con un DPP-4i46.
Otra revisión sistemática y metaanálisis que evaluó los GLP-1a y los DPP-4i concluyó que ambos no acarrean incremento del riesgo de eventos cardiovasculares, aunque sin reducción significativa de los mismos47. Este resultado contrasta con lo observado en la mayoría de los ensayos clínicos que han estudiado a los GLP-1a con este fin (tabla 2).
El estudio de Fei et al. 48 comparó los 3 grupos de fármacos en base al riesgo de eventos cardiovasculares. Los SGLT2i redujeron las muertes de causa cardiovascular comparados con placebo y con los DPP-4i. Tanto los SGLT2i como los GLP-1a redujeron la incidencia de eventos cardiovasculares mayores, renales y hospitalizaciones por IC, con superioridad de los SGLT2i en estos 2 últimos acápites. En discordancia, en el estudio de MacKee et al.49 ambos grupos redujeron la incidencia de eventos renales.
Otro metaanálisis que evaluó los SGLT2i y los GLP-1a obtuvo resultados similares a los de Fei et al. en cuanto a la superioridad de los primeros en la prevención de eventos renales y hospitalizaciones por IC. Cabe destacar que ambos grupos disminuyeron la incidencia del compuesto primario (muerte de causa cardiovascular, IM y enfermedad cerebrovascular) en similar magnitud, sin diferencias tampoco en el subgrupo con enfermedad cardiovascular aterosclerótica establecida50.
Estos resultados podrían estar relacionados con diversos efectos sobre la función endotelial y la rigidez arterial mostrados por estos fármacos, asociándose los SGLT2i con un efecto predominante en la función endotelial mientras los GLP-1a tienen acción predominante sobre la rigidez arterial51.
La guía de práctica clínica de la American Diabetes Association de 2021 recomienda en el tratamiento farmacológico a pacientes con DM tipo 2 considerar la presencia de IC, ERC y CI. En el caso de pacientes con IC o ERC establecida, recomienda iniciar con un SGLT2i como primer escalón. Sin embargo, en pacientes con CI o cualquier otro desorden aterosclerótico establecido se muestran a los GLP-1a y los SGLT2i como las 2 alternativas iniciales sin prioridad evidente a favor de uno u otro grupo1.
Los autores del presente artículo concuerdan con estas recomendaciones pues ambos grupos farmacológicos han demostrado una reducción significativa de estos eventos en los objetivos primarios compuestos, aunque al evaluarlos de forma individual no se ha evidenciado, en los ensayos clínicos, reducción de la incidencia de IM o ACV con el empleo de los SGLT2i, y algunos resultados indican que los GLP1-a sí pueden ocasionar estos beneficios. No hay diferencias respecto a estos parámetros en los metaanálisis revisados (excepto en ACV en el artículo de Fei et al.). Sería conveniente evaluar este tema en un ensayo clínico que compare a ambos grupos farmacológicos.
El estudio EMPRISE comparó empaglifozina vs. sitagliptina en pacientes con DM tipo 2, mostrando una reducción de las hospitalizaciones por IC por parte del primer fármaco52.
Este resultado (tabla 1) no sorprende debido al evidente beneficio de los SGLT2i en la reducción de este evento contrariamente a los DPP-4i que incluso se han asociado en algunos casos con un aumento del mismo.
En concordancia con los resultados del EMPRISE, el estudio CVD-REAL 2 incluyó a individuos con DM tipo 2 comparando a los SGLT2i con otras terapias antidiabéticas, determinando que los primeros disminuyeron el riesgo de muerte de causa cardiovascular, hospitalizaciones por IC, y un compuesto formado por estas 2 variables más IM e ictus53.
ConclusionesEn individuos con DM resulta seguro el uso de SGLT2i y GLP-1a en cuanto a eventos cardiovasculares mayores. El empleo de estos 2 grupos de fármacos se asocia a una disminución significativa de los mismos. Los SGLT2i (en especial dapaglifozina y empaglifozina) muestran una disminución de la mortalidad cardiovascular y las hospitalizaciones por IC. La evidencia actual respecto al efecto de los DPP-4i es diversa, aunque se observa un aumento del riesgo de hospitalizaciones por IC con el consumo de algunos fármacos de esta clase (saxagliptina). Existen pocas diferencias en cuanto a la reducción de eventos cardiacos entre GLP-1a y SGLT2i, exceptuando las hospitalizaciones por IC, en donde es evidente la superioridad de estos últimos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.