La preeclampsia es una de las principales causas de mortalidad materna a nivel mundial. El diagnóstico oportuno de esta enfermedad es en muchas ocasiones un reto para el profesional, ya que se basa en criterios clínicos y pruebas de laboratorio poco específicas. Además, en ocasiones la clínica no se correlaciona con la severidad de la enfermedad. Recientemente se ha estudiado el uso de algunas sustancias angiogénicas y antiangiogénicas que tienen un rol clave en la fisiopatología de la disfunción placentaria y, consecuentemente, en el desarrollo de las manifestaciones clínicas de la preeclampsia. El factor soluble de la tirosincinasa-1 (sFLt-1) y el factor de crecimiento placentario (PlGF) tienen hoy en día un rol protagónico en el manejo de las pacientes con sospecha clínica de preeclampsia. Se presenta en esta publicación un algoritmo de manejo para los trastornos hipertensivos del embarazo utilizando como ayuda diagnóstica la relación sFLt-1/PlGF.
Pre-eclampsia is one of the main causes of maternal mortality worldwide. The timely and accurate diagnosis of this disease is, in many cases, a challenge for the clinician, due to the fact that the diagnosis is mainly based on non-specific clinical criteria and laboratory results. In many cases the clinical manifestations do not correlate appropriately with the severity of the disease. Recently, the use of angiogenesis related factors and their relationship with placental dysfunction and the consequent development of hypertensive disorders has been studied. The soluble FMS-like tyrosine kinase-1 (sFLt-1) and placental growth factor (PlGF) currently have a leading role in the management, diagnosis, and prognosis of hypertensive disorders during pregnancy. The current publication presents a clinical algorithm to aid the management of pregnant women with the clinical suspicion of PE using the sFLt-1/PlGF ratio.
La hipertensión en el embarazo se considera una enfermedad común, aproximadamente el 10% de los embarazos se complican con algún trastorno hipertensivo del embarazo. Un retraso en el diagnóstico y un manejo inadecuado de esta enfermedad puede llevar a complicaciones graves tanto para la madre como para el feto1. Dentro del espectro de los trastornos hipertensivos del embarazo, la preeclampsia sigue siendo por excelencia una de las entidades con mayor morbimortalidad para la población embarazada, pues complica de un 2 a un 5% los embarazos a nivel mundial, con una incidencia mayor en países de bajos recursos. Anualmente, se estima que causa 76.000 muertes maternas y 500.000 muertes neonatales2.
Las complicaciones asociadas a los trastornos hipertensivos del embarazo han ido en aumento: de un 5,3% de las hospitalizaciones en el año 1993 a un 9,1% en el año 2014, según la Sociedad Americana de Ginecología y Obstetricia3. El embarazo se considera en la actualidad como un periodo de ventana, en el que la mujer experimenta un nivel de estrés natural, secundario, del cual podemos obtener muchísimos datos de la salud cardiovascular de la mujer. Tanto la diabetes gestacional como la preeclampsia y los otros trastornos hipertensivos del embarazo son considerados hoy en día factores de riesgo para enfermedad cardiovascular futura4.
Tomando en cuenta la prevalencia de esta enfermedad, su alta morbimortaliad y su peso como factor de riesgo para enfermedad cardiovascular, es cada día más importante un diagnóstico oportuno para disminuir sus complicaciones asociadas. Los biomarcadores son considerados hoy en día como una herramienta con una alta especificidad para el diagnóstico de las pacientes con sospecha de preeclampsia. El objetivo de este protocolo es hacer una breve reseña con respecto al rol de los marcadores angiogénicos en la fisiopatología de la enfermedad y presentar un algoritmo de manejo utilizando esta prueba para la toma de decisiones clínicas.
Preeclampsia, disfunción placentaria y el rol de los marcadores angiogénicosLa preeclampsia es un desorden multisistémico y su patogénesis es aún solo parcialmente comprendida2. Sin embargo, se ha identificado como la causa principal de esta enfermedad la disfunción placentaria, que es el denominador común para una serie de condiciones, además de la preeclampsia: la restricción del crecimiento intrauterino (RCIU) y el abrupto placentae. Esta placentación deficiente se caracteriza por una invasión trofoblástica defectuosa y una remodelación inadecuada de las arterias uterinas, lo que resulta en una perfusión placentaria subóptima. Las consecuencias de la remodelación vascular inadecuada generan subperfusión del espacio intervelloso y esto, como consecuencia, lleva a un daño crónico en las vellosidades, lo cual tiene como principal efecto un aporte inadecuado para el feto, que resulta en RCIU y, a largo plazo, en desprendimiento de placenta debido a que la profundidad de la placentación es inadecuada5.
La disfunción placentaria también conlleva un desbalance entre los factores angiogénicos y antiangiogénicos en la circulación materna. Entre los factores antiangiogénicos más estudiados se encuentra el factor soluble de la tirosincinasa-1 (sFLt-1), que se produce en cantidades aumentadas en las placentas disfuncionales. La función principal de esta sustancia es generar vasoconstricción generalizada para asegurar un aumento en la perfusión de sangre oxigenada al espacio intervelloso5. Estudios histopatológicos de las placentas de fetos con RCIU han demostrado una serie de hallazgos que se engloban dentro del término «malperfusión vascular materna». Uno de estos hallazgos es la presencia de nudos sinciciales, los cuales son los responsables de producir el sFLt-16.
El otro factor importante que considerar dentro de la disfunción placentaria es el factor de crecimiento placentario (PlGF por sus siglas en inglés). El PlGF se produce en las vellosidades placentarias y es detectable en sangre materna desde que se establece la circulación útero-placentaria en las semanas 11-13. Las concentraciones bajas de esta sustancia se relacionan con RCIU y se correlacionan directamente con la severidad de la disfunción placentaria6. El PlGF y otros factores angiogénicos como el factor de crecimiento endotelial son los encargados de estimular la formación de nuevos vasos, así como de propiciar la proliferación y mantenimiento del endotelio vascular. Los factores angiogénicos son capturados e inhibidos por el sFLt-1 y es este desbalance entre los factores angiogénicos y antiangiogénicos lo que lleva a las manifestaciones clínicas de la preeclampsia5. Este desequilibrio podría, inclusive, evidenciarse un mes antes de las manifestaciones clínicas de la enfermedad7.
Implementación clínica de la relación sFLt-1/PlGFLa relación sFLt-1/PlGF ha demostrado ser muy útil como una ayuda diagnóstica para el manejo de las pacientes con sospecha clínica de preeclampsia5,7. Un estudio reciente titulado PROGNOSIS se encargó de validar el punto de corte para determinar la presencia o ausencia de preeclampsia en las siguientes 4 semanas en mujeres con sospecha clínica de esta enfermedad y embarazos entre las 24 y 36,6 semanas de edad gestacional. Este estudio incluyó a un total de 1.050 mujeres en 14 centros hospitalarios en todo el mundo. Se determinó que una relación sFlt-1/PlGF ≤ 38 tenía un valor predictivo negativo para descartar preeclampsia del 94,3% en las siguientes 4 semanas. Este mismo estudio demostró que la relación sFlt-1/PlGF es útiles para establecer con mayor precisión el diagnóstico de preeclampsia, con valores de corte según la edad gestacional: para preeclampsia temprana (<34 semanas) un valor >85, con una especificidad del 99,5% y para preeclampsia tardía (≥34 semanas) valores >110, con una especificidad del 95,5%8.
Otro de los hallazgos valiosos que se documentaron en este estudio fue lograr determinar que antes de las 34 semanas la relación sFlt-1/PlGF no aumenta significativamente en las mujeres con hipertension crónica e hipertensión gestacional en comparación con mujeres normotensas, y que se mantuvo debajo del punto de corte de 85 en un 95% de las mujeres con trastornos hipertensivos del embarazo sin preeclampsia. En el caso de los embarazos de más de 34 semanas, sí se logró observar un aumento significativo en la relación sFlt-1/PlGF en las mujeres sin preeclampsia, pero solo una pequeña proporción de los casos (<10%) alcanzaron valores superiores a 1108. Estos datos lograron demostrar que los marcadores angiogénicos son útiles, además, para el diagnóstico diferencial de los trastornos hipertensivos del embarazo, sobre todo cuando se presentan tempranamente5,8.
De acuerdo con los puntos de corte establecidos en PROGNOSIS, se establecen 3grupos de pacientes que se exponen en la tabla 19.
Clasificación de pacientes según nivel de corte de la relación sFlt-1/PlGF
| Grupo 1 | Grupo 2 | Grupo 3 |
|---|---|---|
| Relación sFlt-1/PlGF <38 | Relación sFlt-1/PlGF > 85 (inicio temprano) o > 110 (inicio tardío) | Relación sFlt-1/PlGF 38-85 (inicio temprano) o 38-110 (inicio tardío) |
| Pacientes que no van a presentar PE en los próximos 7 días | Pacientes con alta probabilidad de tener PE o alguna otra manifestación de disfunción placentaria | Pacientes con alta probabilida de PE en las siguientes 4 semanas |
PE: preeclampsia.
Es utilizando estos distintos punto de corte como el clínico puede guiarse para tomar decisiones clínicas. Las pacientes que se incluyen en el grupo 1 se considera que no tienen preeclampsia al momento de la toma de la muestra, con una alta probabilidad de que no desarrollen la enfermedad en los siguientes 7 días, independientemente de la edad gestacional. Un 80% de las pacientes se van a encontrar en este grupo. En este escenario el clínico puede con seguridad egresar a la paciente y repetir la prueba solo si la sospecha clínica de preeclampsia vuelve a surgir5,9.
Las pacientes del grupo 2 son aquellas que tienen una altísima probabilidad de desarrollar la enfermedad. En este grupo específico, cuando los valores son >655 con edad gestacional de 34 semanas o >201 con edad gestacional de ≥34, se recomienda iniciar la maduración pulmonar debido a que existe una alta probabilidad de descompensción materna o fetal en las siguientes 48 h, con necesidad de alguna intervención de urgencia. En este grupo de pacientes, además, se recomienda repetir la medición de la relación cada 2-4 días para observar la tendencia y ayudar en la toma de decisiones. Debido al alto riesgo de descompensación a corto plazo, estas pacientes deben mantenerse internadas5,9,10.
Las pacientes del grupo 3 son las que una gran parte de los autores consideran que se encuentran en una zona gris; sin embargo, este grupo de pacientes tienen una alta probabilidad de desarrollar preeclampsia en las siguientes 4 semanas y solo un 20% permanecen embarazadas después de un mes. Por esta razón, se debe aumentar la vigilancia en este grupo de pacientes y, en ausencia de criterios de severidad o compromiso fetal, podría considerarse el manejo ambulatorio y repetir el examen al cabo de 1 o 2 semanas5,9.
La medición de los marcadores angiogénicos debe reservarse para aquellas pacientes con sospecha clínica de preeclampsia, con los criterios clínicos que se han utilizado tradicionalmente9 y que son avalados por las distintas sociedades internacionales1-3,11, los cuales se resumen en la tabla 2.
Criterios clínicos para sospecha de preeclampsia
| PAS ≥140 mmHg* |
| PAD ≥ 90 mmHg* |
| Hipertensión crónica que empeora |
| Proteinuria de novo |
| Sintomatología |
| Dolor epigástrico |
| Cefalea |
| Alteraciones visuales |
| Alteraciones auditivas |
| Datos de disfunción orgánica |
| Elevación de transaminasas |
| Trombocitopenia |
| Alteración de la función renal |
| RCIU |
| Doppler de arterias uterinas > P95 |
* Dos tomas en un período de 4 horas en paciente previamente normotensa.
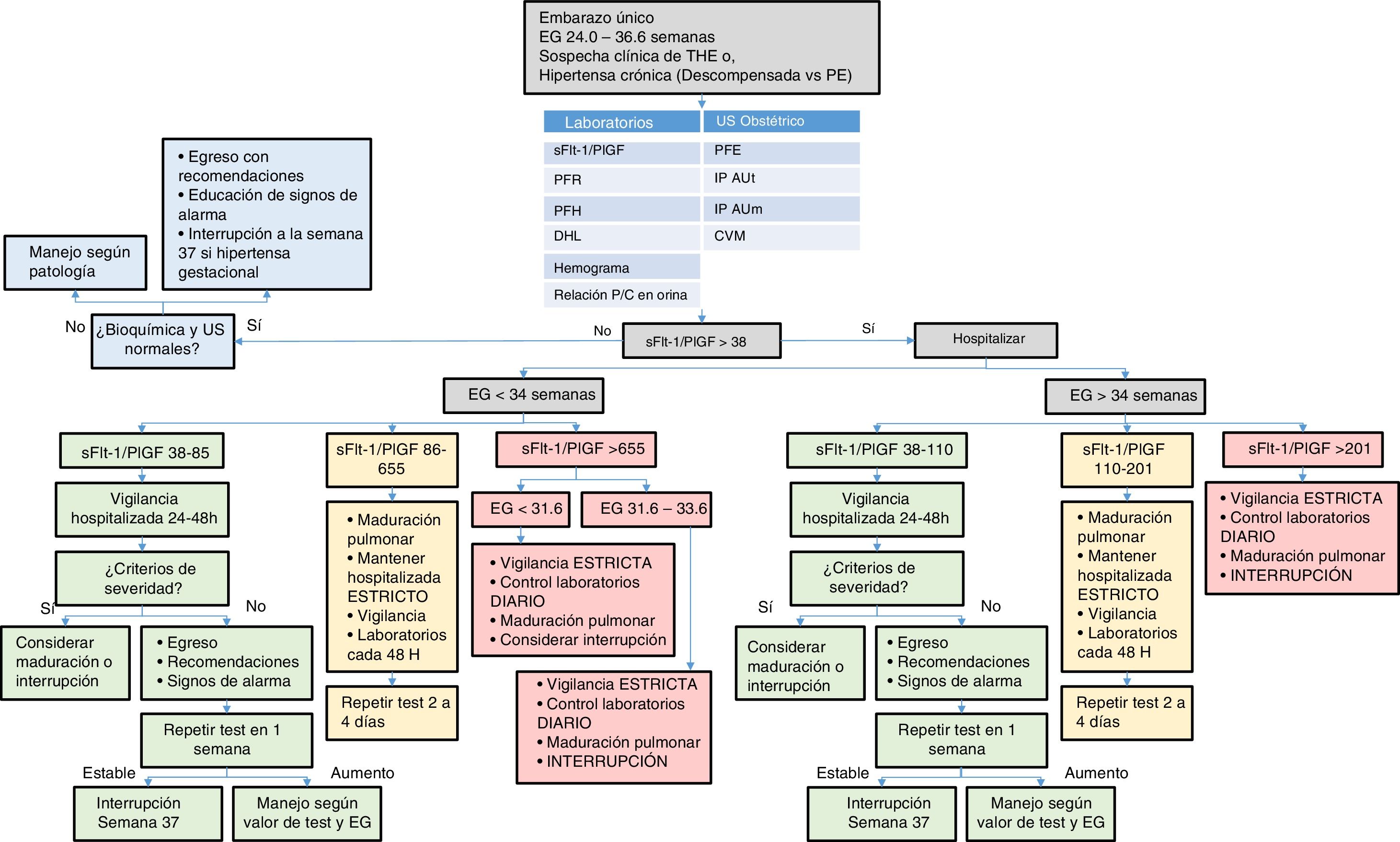
Es importante recalcar que, hasta la fecha, ninguna asociación internacional ha incluido los marcadores angiogénicos como criterio diagnóstico de la preeclampsia, sin embargo, su utilidad como ayuda diagnóstica es ampliamente reconocida. Es por estas razones por lo que presentamos el algoritmo de la figura 1 para guiar al clínico en la toma de decisiones y protocolizar el uso de la relación sFlt-1/PlGF en la práctica clínica.
Algoritmo de manejo de los THE utilizando la relación sFLt-1/PlGF.
AUm: arteria umbilical; AUt: arterias uterinas; DHL: dehidrogenasa láctica; EG: edad gestacional; IP: índice de pulsatilidad; P/C: proteína/creatinina; PE: preeclampsia; PFE: peso fetal estimado; PFH: pruebas de función hepática; PFR: pruebas de función renal; PlGF: placental growth factor; sFlt-1: soluble fms-like tyrosine kinase-1; THE: trastorno hipertensivo del embarazo; US: ultrasonido.
La preeclampsia sigue siendo una enfermedad que genera grandes costos para los sistemas de salud, con una alta morbimortalidad materna y fetal. Su diagnóstico oportuno es la clave para disminuir sus complicaciones asociadas. La relación sFlt-1/PlGF ha demostrado tener una alta sensibilidad y especificidad para el diagnóstico de los trastornos hipertensivos del embarazo, por lo que se propone un algoritmo diagnóstico que incluye esta relación para la toma de decisiones.
FinanciaciónNinguna.
Conflictos de interesesNinguno.