Presentamos una serie de 49 casos de DIU-LNG (DIU Mirena®) sobre 25.166 consultas (0,19%). De ellos, en 12 casos apareció un quiste de ovario durante su seguimiento (24,48%).
DiseñoSe comparan con los otros casos sin quiste de ovario que corresponden al grupo control.
ResultadosCon quistes de ovario, la edad media fue de 41 años; la paridad media: 2; el IMC medio: 25,19, y los años de uso: 3,72. No hubo diferencias significativas con el grupo control excepto en la histerometría que fue mayor (p<0,001). Hubo diferencias significativas en antecedentes de quiste de ovario en 2 casos (16,66%) (p<0,01) en el grupo de quistes de ovario. La indicación más frecuente fue hipermenorreas anemizantes en el 58,33%. El efecto más importante en el sangrado fue su disminución en un 83,33%; hubo manchados en el 8,33% y amenorrea en el 8,33%.
ConclusionesEl volumen medio del quiste fue de 20,38cm3 (8,73-57,65). En el seguimiento ecográfico, el quiste desaparece en 6/10 casos (60%), 3 a los 3 meses (30%), 2 a los 6 meses (20%) y uno (10%) a los 18 meses. En un caso persistió más de 5 años. En los casos en que desaparece, no hay disminución progresiva del volumen del quiste.
We present a series of 49 patients with a levonorgestrel-releasing intrauterine device (LNG-IUD) among 25,166 consultations (0.19%). Of these, an ovarian cyst was found during follow-up in 12 patients (24.48%).
DesignWe compared these patients with patients without an ovarian cyst (control group).
ResultsIn patients with ovarian cysts, the mean age was 41 years, the mean parity was 2, the mean body mass index was 25.19, and the mean number of years of use was 3.72. There were no significant differences with the control group, except in hysterometry, which was higher in patients with an ovarian cyst (P<.001). There were significant differences in antecedents of ovarian cyst in 2 patients (16.66%) in the ovarian cyst group (P<.01). The most frequent indication for use of the LNG-IUD was hypermenorrheas with anemia in 58.33%. The most important effect on bleeding was its decrease in 83.33%; spottings occurred in 8.33% and amenorrhea in 8.33%.
ConclusionsThe mean cystic volume was 20.38cm3 (range: 8.73-57.65). In the sonographic follow-up, the cyst disappeared in six out of 10 patients (60%): at 3 months in three patients (30%), at 6 months in two patients (20%), and at 18 months in one patient (10%). In one patient, the cyst persisted for more than 5 years. In patients whose cysts disappeared, there was no progressive reduction in the volume of the cyst.
El dispositivo intrauterino liberador de levonorgestrel (DIU-LNG) es el DIU Mirena®, un dispositivo intrauterino de anticoncepción reversible1; la liberación de levonorgestrel (LNG) 20μg/día da atrofia endometrial, con lo cual mejora la menorragia o la hipermenorrea, puede producir amenorrea y protege contra la hiperplasia endometrial. Produce así un aumento de hemoglobina (Hb) y de ferritina sérica. Da menstruación más corta, ligera y menos dolorosa.
Tiene eficacia contraceptiva y sirve de tratamiento para la hemorragia uterina disfuncional. Puede utilizarse con miomas, también protege el endometrio con el tratamiento hormonal sustitutivo (THS) de la menopausia, incluso para la hiperplasia endometrial y neoplasia endometrial (como tratamiento conservador en el caso de mujer jóven con deseo de gestación)2. También serviría de protección del cáncer endometrial en el caso de mujeres obesas.
El DIU-LNG disminuye el sangrado y la dismenorrea con miomas. Sería tan recomendable para la endometriosis como los análogos de la hormona liberadora de las gonadotrofinas. Con adenomiosis, también disminuye la dismenorrea. Y con tamoxifeno (TMX) y DIU Mirena® no aparece afección endometrial.
El efecto anticonceptivo1 sería: por moco cervical más espeso; por inhibición de la motilidad y función del esperma intraútero y en la trompa de Falopio, con prevención de la fertilización; y prevención del crecimiento endometrial.
No se altera la mucina, la albúmina ni la inmunoglobulina G del moco cervical, el efecto en el moco no es un mecanismo de acción3 y no altera el transporte del huevo en la trompa.
En la función ovárica3 hay ciclos ovulatorios normales, ciclos anovulatorios con inhibición de la producción de estradiol (E2), hay anovulación con actividad folicular aumentada o hay ovulación con fase lútea inadecuada.
Se producen quistes de ovario funcionales en el 12% o 1,2/100 mujeres/año, es un efecto secundario característico de anticonceptivos con solo gestágenos4. Son asintomáticos, pueden dar molestias abdominales o dispareunia. Desaparecen espontáneamente en 2-3 meses (94%). No necesitan intervención, la laparoscopia no es necesaria salvo que haya rotura o torsión o si el quiste tiene un aumento grande y persistente.
Este aumento de riesgo relativo de quiste de ovario con el DIU Mirena® no tiene relación con la edad o el nivel de hormona estimulante del folículo, pero se correlaciona con la presencia de sangrados irregulares.
En este trabajo, presentamos una serie de DIU Mirena® y estudiamos los casos con quiste de ovario, comparándolos con los controles sin quiste de ovario, haciendo un seguimiento ecográfico de su evolución en el tiempo.
Material y métodosDesde el 27-4-2008 al 27-4- 2012, durante un periodo de 4 años, en la consulta de Ginecología del autor, en el Centro de Especialidades de Monteolivete, Valencia, hemos recogido todos los casos de DIU-LNG (DIU Mirena®), para estudiar aquéllos en los que durante su uso ha aparecido un quiste de ovario. Los restantes casos en los que no ha aparecido un quiste de ovario los consideramos el grupo control y comparamos ambos.
La serie consta de 49 casos, 12 casos con quiste de ovario y 37 sin quiste de ovario. Sobre un total de 25.166 visitas en ese periodo, los DIU Mirena® corresponden al 0,19%, y la incidencia de quistes de ovario y DIU Mirena® es del 24,48%.
Estudiamos: la edad, paridad, índice de masa corporal (IMC), edad a la menarquía, antecedentes médicos y quirúrgicos, fórmula menstrual, trastornos del ciclo, indicación para la inserción del DIU, histerometría, tipo de sangrado con el DIU, si es fumadora o si tiene depresión; en caso de retirada del DIU, el motivo; los casos de recambio y los años de uso.
En los casos de quiste de ovario, además, se ha hecho un seguimiento ecográfico programado a 3, 6 y 12 meses y más, para ver la evolución del quiste. Se indica en qué ovario aparece y sus características. Se calcula el volumen del quiste mediante la fórmula del volumen del elipsoide expresado en cm3 o ml. V=número pi×longitud×anchura×altura/6=0,523×l×a×alt.
En el análisis estadístico, los datos cuantitativos se expresan como rango, media y desviación estándar. Los datos cualitativos se expresan en porcentajes. La comparación de los datos de ambos grupos se hace mediante la prueba t de Student para las medias y la Chi-cuadrado para los porcentajes. La significación estadística se considera con una p<0,05.
ResultadosSobre 25.166 consultas, los DIU Mirena® son 49 casos (0,19%). De ellos, en 12 casos ha aparecido un quiste de ovario durante su seguimiento (24,48%). Los 37 casos restantes sin quiste de ovario se consideran el grupo control.
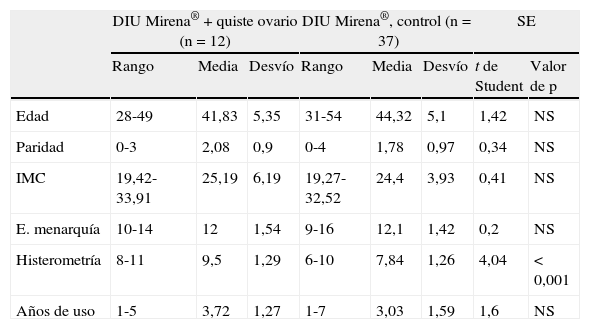
En la tabla 1 expresamos los datos cuantitativos de la serie: edad, paridad, IMC, edad a la menarquía, histerometría en la inserción y años de uso. Con quiste de ovario, la media de edad fue de 41 años; la paridad media: 2; el IMC medio: 25,19; la media de edad a la menarquía: 12 años; la histerometría media: 9,5cm. Y los años de uso, media de 3,72. No hubo diferencias significativas en ningún parámetro excepto en la histerometría, que en el grupo control es menor (p<0,001).
Datos cuantitativos
| DIU Mirena® + quiste ovario (n=12) | DIU Mirena®, control (n=37) | SE | ||||||
| Rango | Media | Desvío | Rango | Media | Desvío | t de Student | Valor de p | |
| Edad | 28-49 | 41,83 | 5,35 | 31-54 | 44,32 | 5,1 | 1,42 | NS |
| Paridad | 0-3 | 2,08 | 0,9 | 0-4 | 1,78 | 0,97 | 0,34 | NS |
| IMC | 19,42-33,91 | 25,19 | 6,19 | 19,27-32,52 | 24,4 | 3,93 | 0,41 | NS |
| E. menarquía | 10-14 | 12 | 1,54 | 9-16 | 12,1 | 1,42 | 0,2 | NS |
| Histerometría | 8-11 | 9,5 | 1,29 | 6-10 | 7,84 | 1,26 | 4,04 | <0,001 |
| Años de uso | 1-5 | 3,72 | 1,27 | 1-7 | 3,03 | 1,59 | 1,6 | NS |
IMC: índice de masa corporal; NS: no significativo; SE: significación estadística.
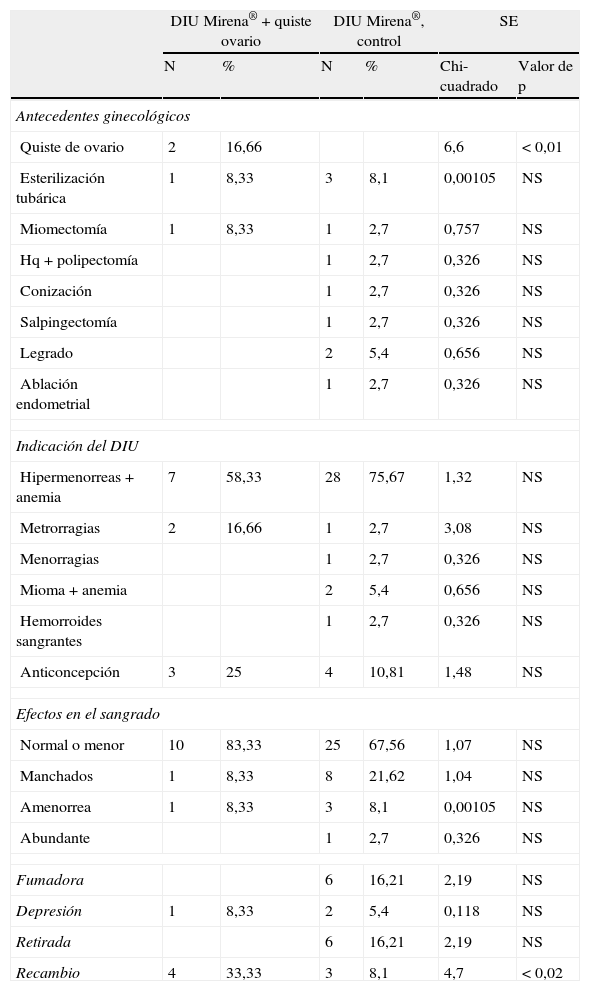
En la tabla 2 expresamos los datos cualitativos: los antecedentes ginecológicos, la indicación del DIU, los efectos en el sangrado, si es fumadora o tiene depresión, el motivo de retirada del DIU en su caso. Y si ha habido recambio. No hubo diferencias significativas en ningún parámetro, excepto en antecedentes de quiste de ovario, que ocurrió en 2 casos (16,66%) en el grupo con quistes de ovario (p<0,01). Y en recambio, en 4 casos en el grupo de quistes de ovario (33,33%) (p<0,02).
Datos cualitativos
| DIU Mirena® + quiste ovario | DIU Mirena®, control | SE | ||||
| N | % | N | % | Chi-cuadrado | Valor de p | |
| Antecedentes ginecológicos | ||||||
| Quiste de ovario | 2 | 16,66 | 6,6 | <0,01 | ||
| Esterilización tubárica | 1 | 8,33 | 3 | 8,1 | 0,00105 | NS |
| Miomectomía | 1 | 8,33 | 1 | 2,7 | 0,757 | NS |
| Hq+polipectomía | 1 | 2,7 | 0,326 | NS | ||
| Conización | 1 | 2,7 | 0,326 | NS | ||
| Salpingectomía | 1 | 2,7 | 0,326 | NS | ||
| Legrado | 2 | 5,4 | 0,656 | NS | ||
| Ablación endometrial | 1 | 2,7 | 0,326 | NS | ||
| Indicación del DIU | ||||||
| Hipermenorreas+anemia | 7 | 58,33 | 28 | 75,67 | 1,32 | NS |
| Metrorragias | 2 | 16,66 | 1 | 2,7 | 3,08 | NS |
| Menorragias | 1 | 2,7 | 0,326 | NS | ||
| Mioma+anemia | 2 | 5,4 | 0,656 | NS | ||
| Hemorroides sangrantes | 1 | 2,7 | 0,326 | NS | ||
| Anticoncepción | 3 | 25 | 4 | 10,81 | 1,48 | NS |
| Efectos en el sangrado | ||||||
| Normal o menor | 10 | 83,33 | 25 | 67,56 | 1,07 | NS |
| Manchados | 1 | 8,33 | 8 | 21,62 | 1,04 | NS |
| Amenorrea | 1 | 8,33 | 3 | 8,1 | 0,00105 | NS |
| Abundante | 1 | 2,7 | 0,326 | NS | ||
| Fumadora | 6 | 16,21 | 2,19 | NS | ||
| Depresión | 1 | 8,33 | 2 | 5,4 | 0,118 | NS |
| Retirada | 6 | 16,21 | 2,19 | NS | ||
| Recambio | 4 | 33,33 | 3 | 8,1 | 4,7 | <0,02 |
Hq: histeroscopia quirúrgica; NS: no significativo; SE: significación estadística.
Respecto a las indicaciones del DIU, las más importantes fueron: hipermenorreas anemizantes en el 58,33% en el grupo quistes de ovario, y en el 75,67% en el grupo control. Seguido de metrorragias en el 16,66% del grupo de quistes de ovario, y finalmente, como anticonceptivo en el 25% en el grupo quistes de ovario y en el 10,81% en el grupo control.
Respecto a los efectos en el sangrado con el DIU, tampoco hubo diferencias significativas entre ambos grupos. Fue normal o sangrado menor en el 83,33 y 67,56% respectivamente. Hubo manchados en el 8,33 y 21,62% respectivamente. Y amenorrea en el 8,33 y 8,10% respectivamente.
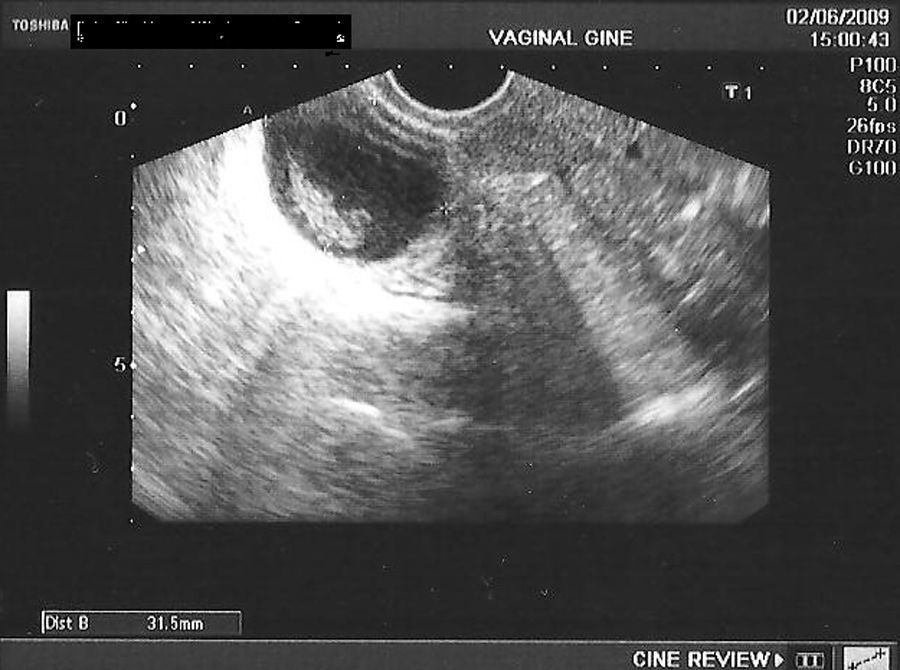
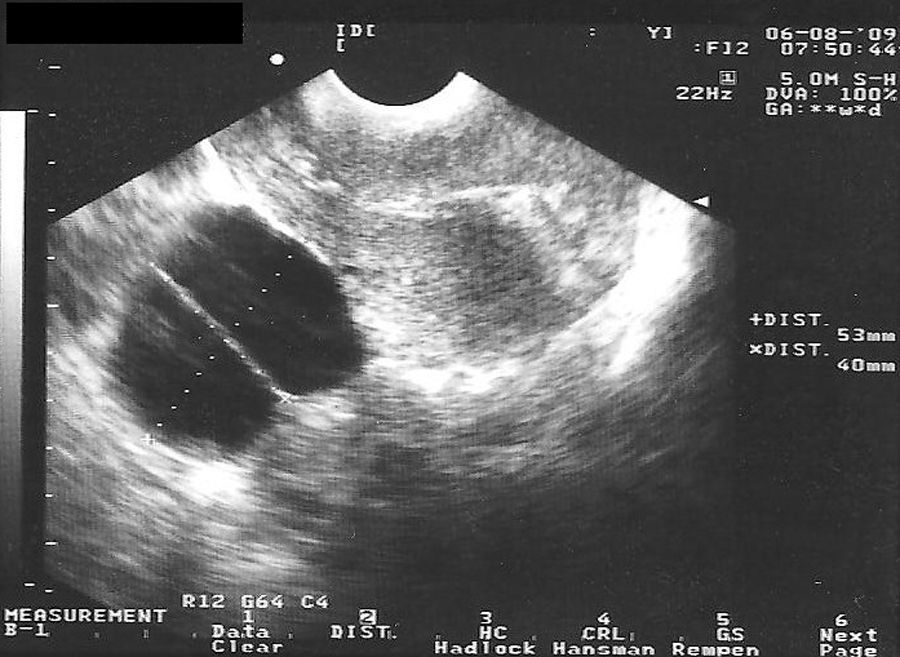
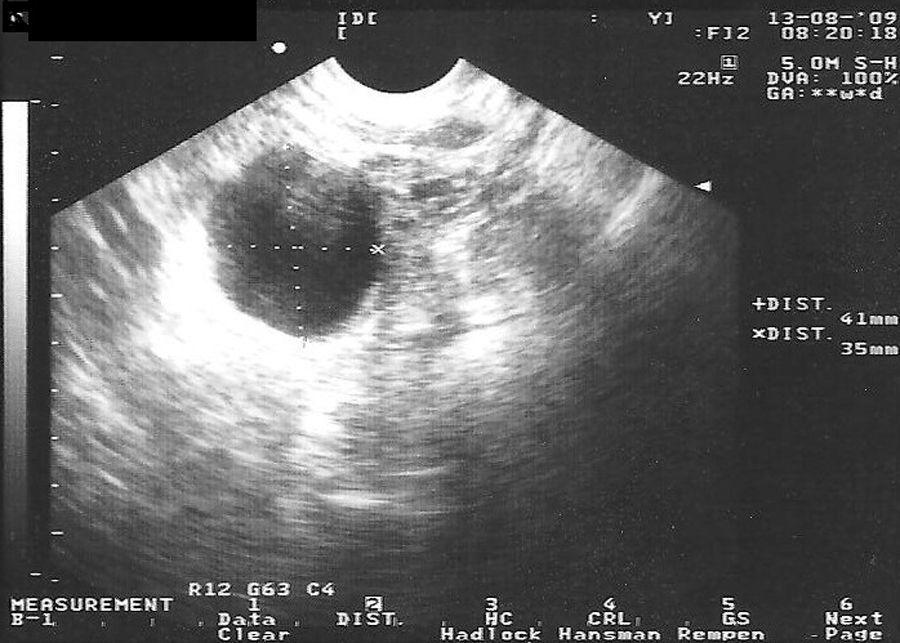
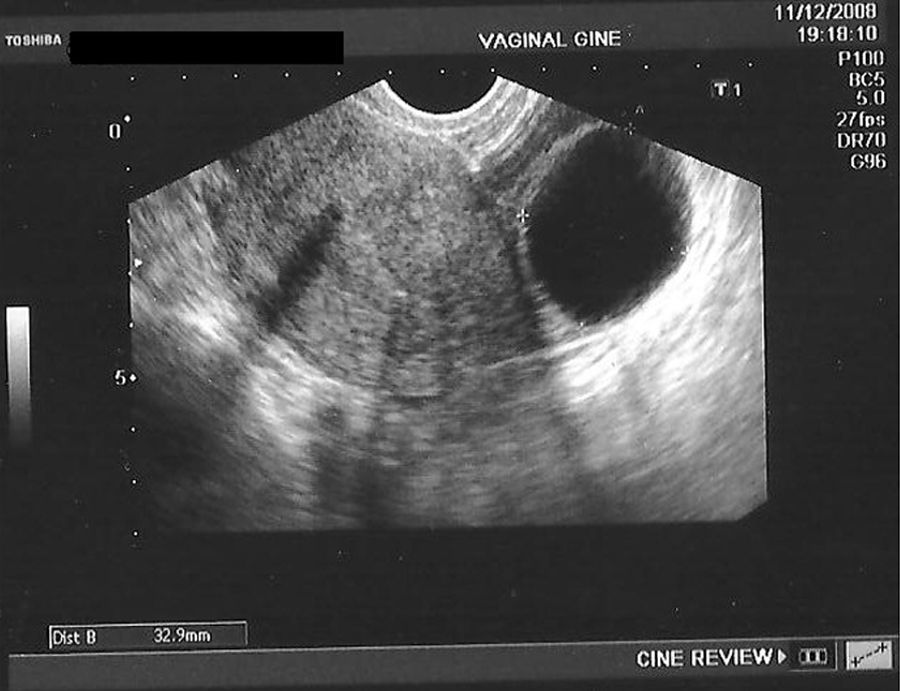
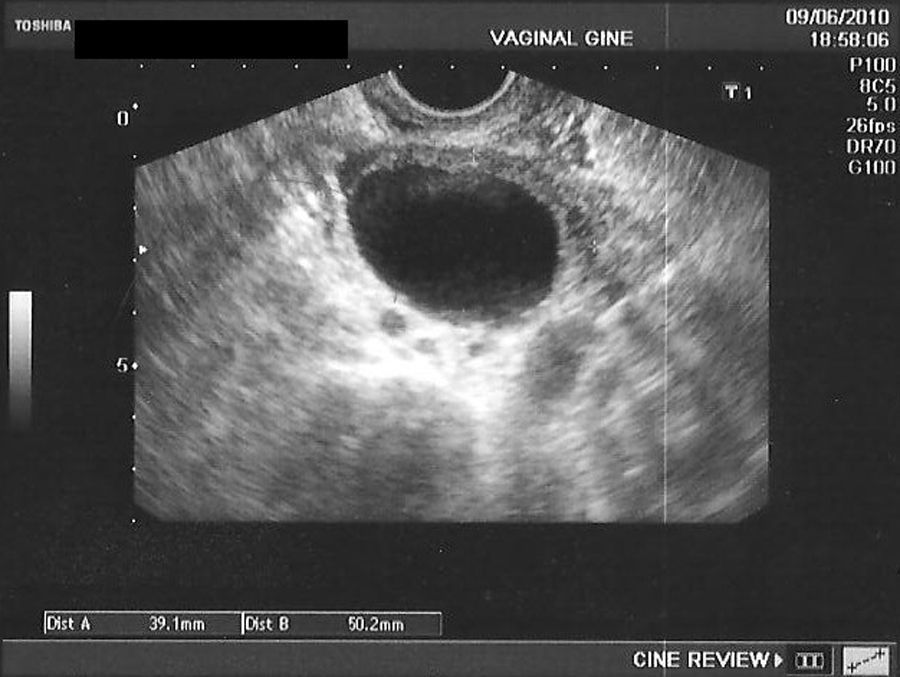
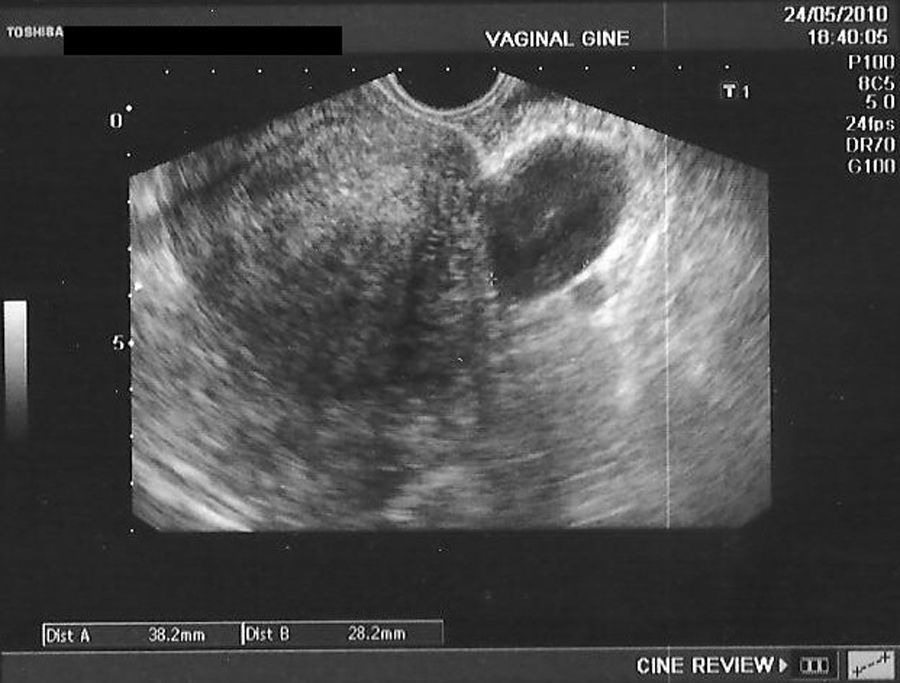
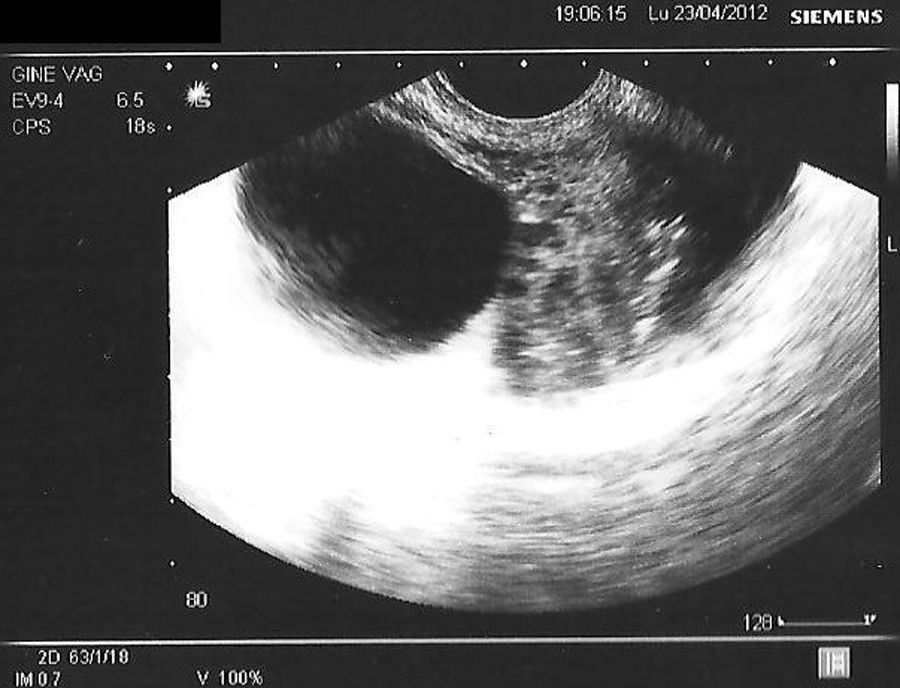
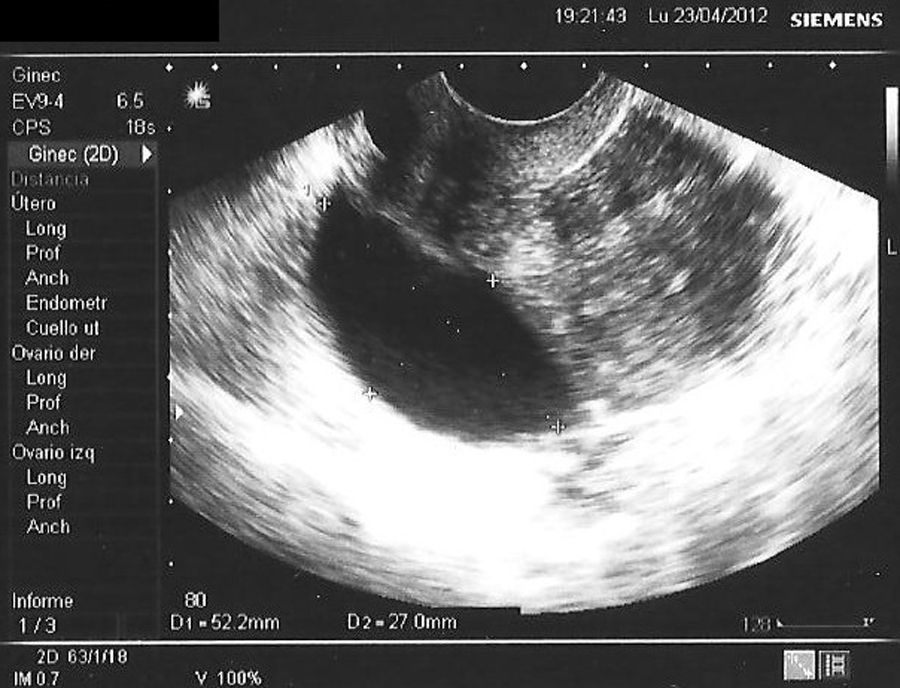
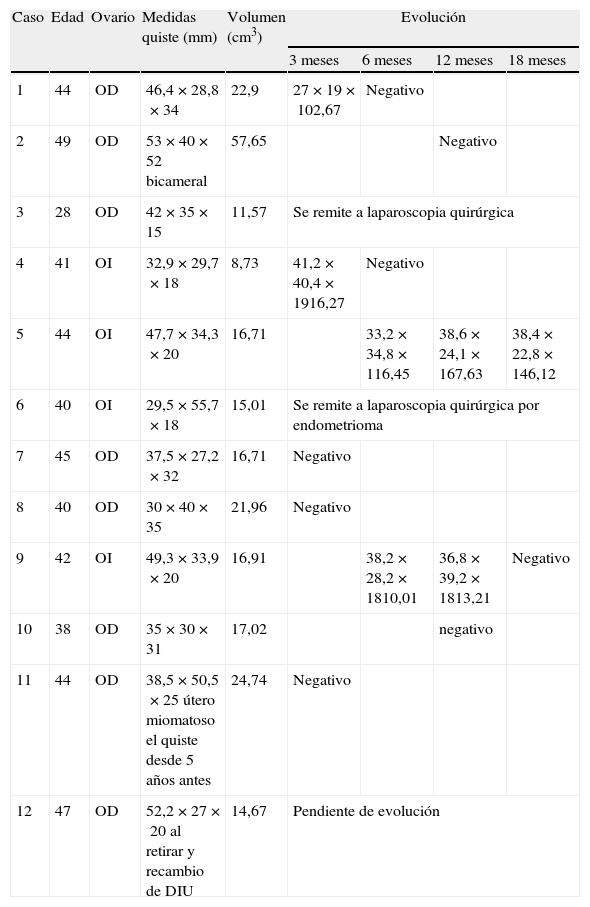
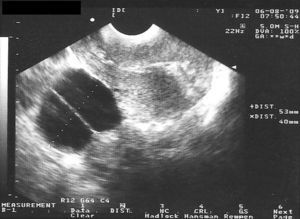
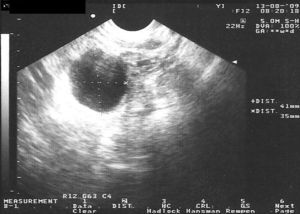
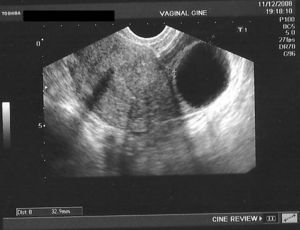
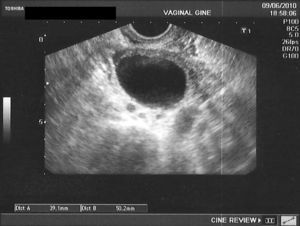
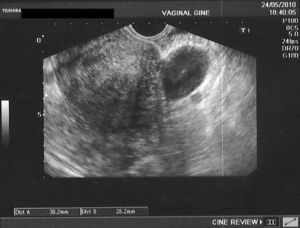
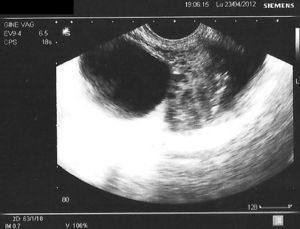
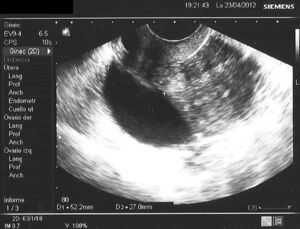
En la tabla 3 se presentan los casos de DIU+quiste de ovario (consideramos quiste a la formación mayor de 30mm). Se indica el ovario afecto, las medidas del quiste en mm, el volumen en cm3 y la evolución del seguimiento ecográfico a los 3, 6 y 12 meses.
DIU Mirena®+quistes de ovario. Seguimiento ecográfico
| Caso | Edad | Ovario | Medidas quiste (mm) | Volumen (cm3) | Evolución | |||
| 3 meses | 6 meses | 12 meses | 18 meses | |||||
| 1 | 44 | OD | 46,4×28,8×34 | 22,9 | 27×19×102,67 | Negativo | ||
| 2 | 49 | OD | 53×40×52 bicameral | 57,65 | Negativo | |||
| 3 | 28 | OD | 42×35×15 | 11,57 | Se remite a laparoscopia quirúrgica | |||
| 4 | 41 | OI | 32,9×29,7×18 | 8,73 | 41,2×40,4×1916,27 | Negativo | ||
| 5 | 44 | OI | 47,7×34,3×20 | 16,71 | 33,2×34,8×116,45 | 38,6×24,1×167,63 | 38,4×22,8×146,12 | |
| 6 | 40 | OI | 29,5×55,7×18 | 15,01 | Se remite a laparoscopia quirúrgica por endometrioma | |||
| 7 | 45 | OD | 37,5×27,2×32 | 16,71 | Negativo | |||
| 8 | 40 | OD | 30×40×35 | 21,96 | Negativo | |||
| 9 | 42 | OI | 49,3×33,9×20 | 16,91 | 38,2×28,2×1810,01 | 36,8×39,2×1813,21 | Negativo | |
| 10 | 38 | OD | 35×30×31 | 17,02 | negativo | |||
| 11 | 44 | OD | 38,5×50,5×25 útero miomatoso el quiste desde 5 años antes | 24,74 | Negativo | |||
| 12 | 47 | OD | 52,2×27×20 al retirar y recambio de DIU | 14,67 | Pendiente de evolución | |||
| Quiste ovario, volumen inicial | ||
| Rango | Media | Desvío |
| 8,73-57,65 | 20,38 | 12,58 |
Negativo: el quiste ha desaparecido; OD: ovario derecho; OI: ovario izquierdo.
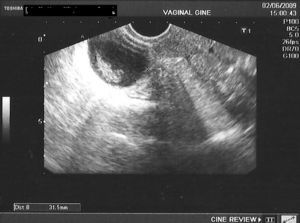
En las figuras 1–8 se presentan las imágenes más demostrativas.
El caso 3 se remitió para laparoscopia quirúrgica al ser un quiste que persistía 3 años. El caso 6 se remitió para laparoscopia quirúrgica por la sospecha de ser un quiste endometriósico (tenía antecedente de quistectomía y salpingectomía).
El caso 10 tenía un útero adenomiótico. El caso 11 presentaba un útero miomatoso y el quiste de ovario se mantenía desde 5 años antes.
En la evolución ecográfica de los quistes: a 3 meses, desaparecen 3 (30%); a 6 meses, 2 (20%) y uno persiste 18 meses (10%). En total desaparecen 6/10 (60%). No desaparece uno (10%), que persiste más de 18 meses. El otro caso restante, está pendiente de evolución, por recambio. En los casos estudiados con desaparición del quiste no hay un progresivo descenso del volumen del quiste.
Se ha producido el recambio del DIU en 4 casos (33,33%) a 4 y 5 años de uso. En ningún caso hubo que retirarlo.
En cambio, en el grupo control, 3 casos (3, 7 y 10) en la biopsia endometrial tenían: hiperplasia simple endometrial (+pólipo, caso 3), hipertrofia focal endometrial (caso 7) e hiperplasia endometrial sin atipia (caso 10), como se comprobaron y trataron por histeroscopia. En 11 casos se encontraron miomas intramurales (IM) o subserosos (SS) de pequeño tamaño. En total, 14 casos tenían miomas (37,83%). El caso 27 se remitió para histerectomía por útero miomatoso. El caso 28 presentaba también un mioma IM de 48×51mm con degeneración quística. El caso 32 tenía un mioma IM en fondo de 8cm. En el caso 36, antes de la inserción se encontró un quiste de ovario de 54,3×34,6×25mm. El caso 21 presentaba también un quiste de Bartolino derecho de 3cm.
Se produjo el recambio del DIU en 3 casos (8,10%) a 3, 4 y 5 años.
Durante el seguimiento hubo retiradas. El caso 31 se remitió para histerectomía vaginal por prolapso uterino iii. El caso 27 ya comentado, se remitió para histerectomía por útero miomatoso. Se retiró durante la intervención. El caso 9 se retiró a los 9 meses porque la paciente creía que no estaba en su sitio (no era cierto). Tenía el antecedente de otros 2 DIU Mirena® expulsados en su país. Otro caso, el 17, se retiró a los 3 meses por sangrado. El caso 36 lo expulsó en la defecación a los 10 días de la inserción. En el caso 24 se retiró a los 2 meses por enfermedad inflamatoria pélvica (EIP).
En otros 2 casos no se pudo retirar. El caso 11 a los 5 años al no ver los hilos, se remitió a histeroscopia y se le retiró. Y el caso 28 tampoco se veían los hilos y la paciente decidió mantenerlo.
En resumen, no encontramos diferencias significativas entre ambos grupos. Y en el grupo con quistes de ovario, estos son funcionales, foliculares, de volumen máximo 57,65cm3, y que en el seguimiento ecográfico no se ve una progresiva disminución de tamaño. Desaparecieron a los 3 meses, en el 30%, a los 6 meses en el 20% y en el 10% a los 18 meses. Un caso persistió más de 18 meses y también sabemos de otro caso con persistencia del quiste mayor de 5 años.
DiscusiónEn una serie de 335 mujeres de 25-40 años, de 1996-97 y estudiadas por ecografía transvaginal para ver los ovarios5, se encontraron lesiones anexiales en 26/335 (7,8%). Eran 22 quistes de ovario, un quiste de paraovario, 2 hidrosalpinx y un tumor sólido (quiste dermoide). La tasa de quistes de ovario, 22/335 fue del 6,6%. A los 3 meses, 18/22 (82%) habían desaparecido. Las lesiones ováricas en mujeres asintomáticas son frecuentes a esta edad, y en el 4/% de los casos desaparecen a los 3 meses. Si persisten, se deben hacer controles ecográficos o cirugía, según la paciente.
Al estudiar los quistes ováricos funcionales en las mujeres premenopáusicas y ginecológicamente sanas, en 24 meses, sobre 428 mujeres de 14-45 años6, por ecografía, se encontraron 29 casos con quistes de ovario mayores de 30mm. Se realiza exámen ecográfico cada 3 meses. Hay prevalencia baja, la mayoría se resuelven tras la regla. El 65% eran persistentes y se resuelven a los 3 meses. Los quistes de ovario son frecuentes en las mujeres sanas y fértiles y son autolimitados. Se resuelven independientemente del tratamiento contraceptivo hormonal oral. El DIU no influencia en la ocurrencia de quistes de ovario funcionales.
Al comparar los DIU, DIU-LNG y DIU de Cu7, con el DIU-LNG hay beneficios significativos, de importante repercusión médica y de salud pública, mejoran la calidad de vida de las usuarias, disminuye la menorragia y aumenta la Hb, tiene efecto en la dismenorrea, previene el embarazo ectópico y la EIP, y hay menos incidencia de vaginitis. Pero, puede haber quistes funcionales ováricos.
Con la contracepción oral de solo progestágenos, la minipíldora aumenta los quistes funcionales ováricos8. Sobre 46 mujeres de 24-39 años, 25 con minipíldora, hubo 12/21 quistes (57%). En 21 controles, 4/21 (19%) tenían quistes de ovario (p<0,025). Con la minipíldora es un método menos aceptable por los quistes y el dolor. Hay que suprimir la minipíldora y ver si desaparece el quiste.
En usuarias de implantes contraceptivos subdérmicos, con etonogestrel (Implanon®) o levonorgestrel (Jadelle®, Norplant®), comparadas con DIU9, los quistes de ovario en el primer año de uso son frecuentes y no son patológicos. Se estudiaron 344 mujeres a los 3 meses de los implantes o de TCu 380 A. Eran 116 casos de Implanon®, 123 casos de Jadelle® y Norplant® y 105 casos de DIU. Se hizo ecografía vaginal a los 3, 6 y 12 meses y se determinó E2 y Pg (progesterona). Los quistes de ovario mayores de 25mm, a los 3 meses fueron: 5,2, 1,3 y 1% respectivamente; a los 6 meses: 7,2, 8 y 2,1% respectivamente; y a los 12 meses: 26,7, 14,6 y 1,2% respectivamente. Con los implantes de gestágenos hay más quistes ováricos que con el DIU de Cu.
Si se comparan el DIU-LNG frente al DIU TCu (NovaT,TCu 200-220 o TCu 380)10, el DIU-LNG es comparable a la esterilización masculina o femenina. Ambos tipos de DIU son iguales en seguridad; tiempo de uso (5 años), aunque aún pueden durar 2 años más con eficacia y vuelta a la fertilidad tras retirarlo.
El DIU-LNG puede haber dificultad a la inserción más dolor y riesgo de perforación (no depende de la experiencia del médico). La eficacia no disminuye aún con posición inadecuada en el útero.
Una desventaja pueden ser los quistes de ovario funcionales. Al estudiar 15 mujeres con reglas normales y 7 mujeres con amenorrea, de edad media 35 años; con DIU-LNG 7 años11, y de controles 8 mujeres con DIU TCu 380 Ag, más de 7 años y media de edad 34 años. Con DIU-LNG, en las normales, hubo quistes foliculares en 6 (42%) con remisión; y en las amenorreicas hubo 5 quistes foliculares que desaparecieron en 45 días.
Nilsson et al.12, ya habían estudiado 20 mujeres con una edad media de 36 años, 8 con amenorrea y 12 con ciclos regulares; analizando E2, Pg y LNG. El 75% de los ciclos eran ovulatorios con el DIU, 5/8 (63%) con amenorrea y 7/12 (58%) con ciclo regular. El origen de la amenorrea es de naturaleza local. No había diferencias en la tasa de LNG en ambos grupos. EL LNG tiene efecto local en el endometrio, origina atrofia y amenorrea desde el primer mes de uso. La amenorrea no es un efecto adverso porque tras la retirada del DIU se recupera la fertilidad.
Pakarinen et al.13, comparan DIU-LNG intracervical y DIU-LNG fúndico, en el espesor endometrial, patrones de sangrado y persistencia de folículos ováricos. En canal cervical, 151 casos (con útero pequeño o nulíparas) y en fondo uterino 147 casos. De 18-43 años, media 31 años. Ecografía vaginal a 3, 6 y 12 meses. Los folículos ováricos fueron: a la inserción, 2/298 (0,7%); a los 3 meses, 18 (6,5%); a los 6 meses, 20 (7,7%), y a los 12 meses, 8 (3,2%). El número de folículos persistentes es bajo y se resuelven en 6-8 meses. Es mejor el DIU en el fondo que el cervical por LE, línea endometrial menor y menos días de sangrado.
Järvelä et al.14, estudian DIU-LNG en 27 mujeres fértiles, de 24-45 años (media: 32 años). Hubo quistes en 8/26, 31%; de 34,9-65,6mm, media 44,4mm. El DIU-LNG a veces inhibe la ovulación y produce disturbio en el sistema hipotálamo (HT)-hipófisis (HF)-ovario, altera el desarrollo folicular y la rotura con formación de quistes.
Inki et al.15, estudian 236 mujeres de 35-49 años, media 43 años, con DIU-LNG, con seguimiento de 12 meses, ecografía inicial y a 6 y 12 meses. Al inicio había 12/236 quistes de ovario (5,1%); a los 6 meses, 17/97 (17,5%), 13 con resolución espontánea. Y a los 12 meses, 17/79 (21,5%). Son quistes asintomáticos y con alta tasa de resolución (94%). No hay correlación del quiste y la edad, pero sí del quiste y del sangrado irregular.
Bahamondes et al.16, ven la prevalencia de quistes foliculares mayores de 25mm, en 100 mujeres con DIU Mirena®, 100 mujeres con implantes subdérmicos y 100 mujeres con DIU TCu 380 A, en 2000-2001. Las tasas de quistes ováricos fueron 19, 10 y 5% respectivamente. A los 15 días desaparecen 30/34, 88%. La mayoría desaparecen en 2 semanas y no hace falta intervención médica. Debe evitarse decir quiste, porque la paciente interpreta estructura anatómica que requiere tratamiento quirúrgico.
Con la ecografía vaginal se valora la posición del DIU Mirena® en la cavidad uterina. El extremo craneal y caudal de la rama vertical se ven como puntos hiperrefringentes. El depósito hormonal se ve como una sombra acústica dorsal17,18. Y también pueden verse los quistes funcionales del ovario.
Finalmente, de nuestro estudio, una serie de 49 casos de DIU Mirena®, 12 con quiste de ovario y 37 sin quiste, como controles. La frecuencia de DIU Mirena® es 0,19% y la incidencia de quiste de ovario y DIU Mirena® es del 24,48%. La edad media fue de 41 años, la paridad media de 2, la histerometría media de 9,5cm (p<0,001), y los años de uso de 3,72. En 2 casos (16,66%) ya tenían antecedentes de quiste de ovario (p<0,01). La indicación princeps es la hipermenorrea anemizante en un 58,33%. Hubo sangrado normal o menor en el 83,33% y amenorrea en el 8,33%.
En la evolución ecográfica de los quistes, a los 3 meses desaparecen el 30%, a los 6 meses el 20% y uno persiste a los 18 meses (10%). En total desaparecen 6/10 (60%), esta tasa es más baja que la referida en la literatura13,15. Sabemos de un caso con persistencia del quiste mayor de 5 años. Y no se ve una progresiva disminución de tamaño en el seguimiento ecográfico.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.