INTRODUCCIÓN
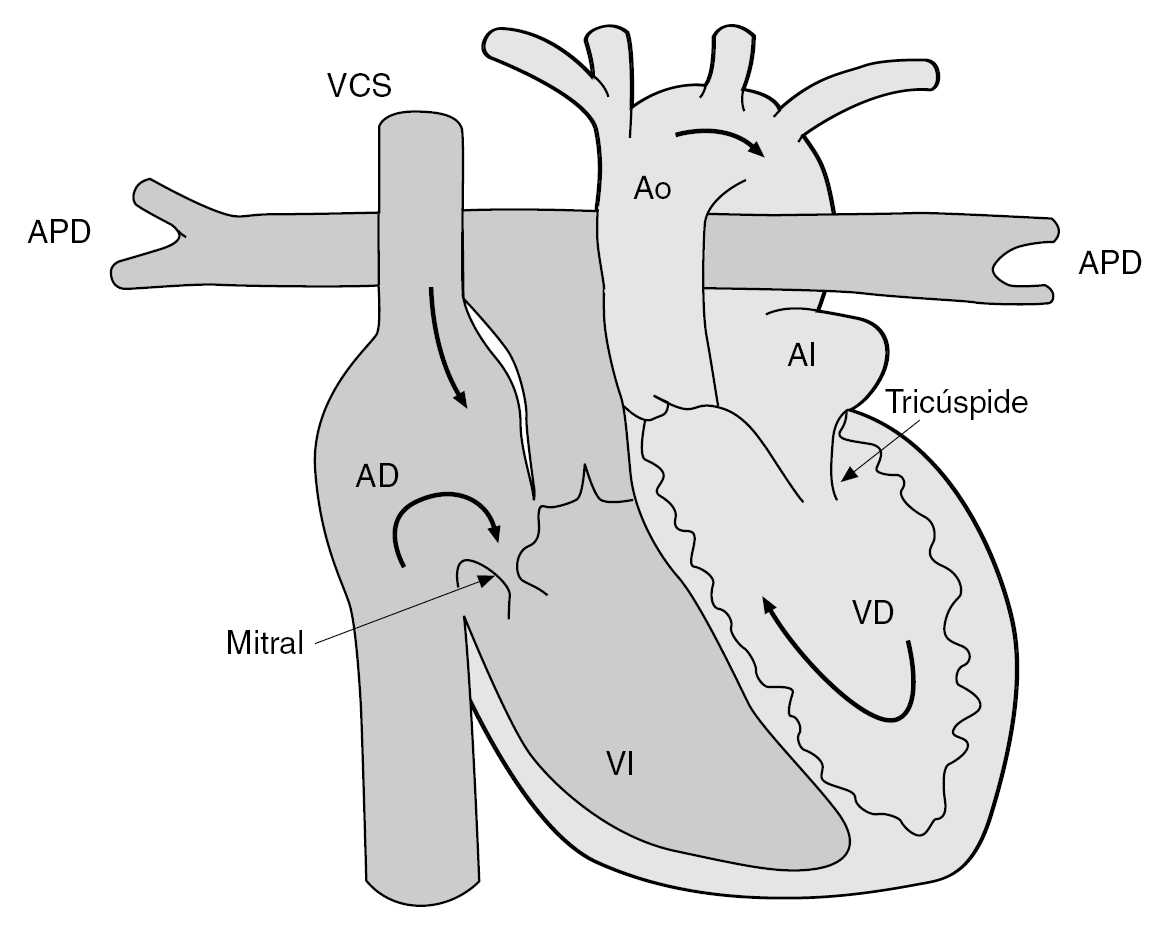
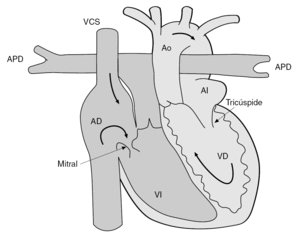
Las cardiopatías en el embarazo constituyen un importante problema, y son la primera causa de mortalidad materna de causa no obstétrica1. Su incidencia en gestantes se estima entre el 0,4 y el 2%1. Las cardiopatías congénitas (CC) en el hombre ocurren en alrededor del 8 de los recién nacidos vivos, por lo tanto, en la actualidad, con el descenso en la prevalencia de la fiebre reumática, la gran mayoría de las cardiopatías que complican el embarazo son CC. Del 80 al 90% de las CC están constituidas por: defectos septales ventriculares (CIV); defectos septales auriculares; estenosis pulmonar; tetralogía de Fallot y conducto arterial persistente; estenosis aórtica; transposición de grandes vasos, y coartación aórtica. Una CC infrecuente es la L-TGA (transposición de grandes arterias), que consiste en una doble discordancia atrioventricular y ventriculoarterial, por eso es conocida como transposición corregida genéticamente (fig. 1).
Fig. 1. Diagrama de transposición corregida de grandes vasos.
CASO CLÍNICO
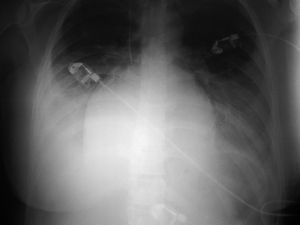
Se presenta el caso de una paciente originaria de Rumanía de 29 años de edad, sin antecedentes familiares de interés y como antecedentes personales 2 ingresos previos hospitalarios en su país de origen por neumonía, que es remitida en semana 26 de gestación por rotura prematura de membranas desde el Hospital Regional de Lanzarote a nuestra maternidad, al ser ésta de referencia. Como antecedentes ginecoobstétricos presenta una interrupción voluntaria del embarazo previa sin otros datos de interés. La gestación actual es de control ambulatorio de curso normal hasta su ingreso en Hospital de Lanzarote por amenaza de parto prematuro. Tras 2 días de ingreso en dicho hospital se produce amniorrexis espontánea, por lo que se decide su traslado al Hospital Materno-Infantil de Gran Canaria (HUMIC), en el que se le instaura tratamiento con antibioterapia, tocólisis con tractocile en perfusión continua intravenosa a 7,5 mg/ml y se inicia pauta de maduración pulmonar con betametasona intramuscular. A su llegada en nuestro hospital presenta situación estable, con buen estado general, constantes normales, con cifras de presión arterial de 110/60 mmHg, frecuencia cardíaca de 80 lat/min y se mantiene apirética con temperatura de 36,7 °C; desde el punto de vista obstétrico se objetiva una altura uterina que corresponde a amenorrea, genitales externos normales, cérvix con modificaciones con un test de Bishop de 8 (cérvix dilatado 2 cm, borrado y centrado), situación longitudinal con presentación cefálica, bolsa rota por la que fluye líquido claro no fétido, no refiere dinámica que tampoco se objetiva en registro cardiotocográfico (RCTG) ni clínicamente, sin aumento de la sensibilidad uterina. En la analítica al ingreso presenta leucocitosis franca de 20.900 103/ml con neutrofilia de un 90%, y el resto de parámetros dentro de límites normales, y a su ingreso se cursó urocultivo y exudados vaginal y rectal con resultado negativo. A su ingreso en HUMIC, ante el resultado analítico se retira tocólisis por sospecha de corioamnionitis subclínica y se completá la maduración pulmonar, se mantiene el tratamiento antibiótico (eritromicina) y reposo absoluto hospitalario. Se realiza nuevo control analítico y la leucocitosis permanece sin alteraciones significativas en el resto de éste, solicitándose PCR con resultado de 19,6 mg/dl. Se realiza ecografía que informa de gestación única en presentación cefálica, la biometría corresponde a placenta de inserción normal y oligoamnios total. A las 24 h de su ingreso en nuestro centro inicia trabajo de parto. Durante el período de dilatación cumple criterios de corioamnionitis, por lo que se instaura antibioterapia intraparto con cefazolina (1 g/6 h) y gentamicina (80 mg/8 h), y tras 6 h de estancia en paritorio se produce un parto eutócico de un recién nacido varón de 1.000 g con test de Apgar 3/8 que ingresa en la unidad de cuidados intensivos neonatales (UCIN). Tras el parto se produce retención de placenta y serealiza su extracción manual y posterior reposición de la volemia de forma masiva no controlada ,para mantener un control hemodinámico adecuado, así como la administración de occitócicos y prostaglandina F2α por cuadro de atonía uterina y metrorragia puerperal importante, que cede. En el puerperio inmediato presenta un cuadro de disnea importante que entra en insuficiencia respiratoria aguda con controles de saturación de oxígeno del 60-70%, por lo que requiere intubación y se decide, ante la sospecha de edema agudo de pulmón (EAP) en el contexto de proceso infeccioso, su traslado a unidad de medicina intensiva. Durante su estancia en dicha unidad precisa intubación y sedación con perfusión de catecolaminas para mantener el control hemodinámico. Se inicia antibioticoterapia con doxiciclina y meropemen. Se realiza una radiografía de tórax que informa de alteración en la imagen de la silueta cardíaca con corazón muy redondo y con signos de EAP (figs. 2 y 3). Se realiza electrocardiograma (ECG), en el que se objetiva ritmo sinusal con onda T () en cara inferior y T () en cara lateral alta. Dados estos hallazgos, se indica la realización de un ecocardiograma ante la sospecha de una miocardiopatía dilatada periparto, en el que se objetiva la presencia de una cardiopatía congénita (anomalía de salida de grandes vasos) con grave disfunción biventricular. Con dicha sospecha se suspenden catecolaminas y se inicia tratamiento con diuréticos y digoxina, y desde entonces la paciente presentó evolución muy favorable; se consiguió la extubación, y se mantuvieron saturaciones de oxígeno del 99%, sin presentar trabajo respiratorio, con función renal conservada y mejoría clínica, analítica y radiológica importantes, por lo que se traslada a nuestro de nuevo a nuestro servicio. Durante el puerperio la paciente se mantiene estable y asintomática, sin presentar signos de insuficiencia cardíaca ni respiratoria con tratamiento con digitálicos por vía oral, inhibidores de la enzima de conversión de la angiotensina y antiagregantes. Tras permanecer la paciente estable, se completa el estudio cardiológico mediante ecocardiografía transesofágica donde se confirma la existencia de L-TGA, sin otra anomalía asociada, con ventrículo en posición izquierda (VD) hipértrofico ligeramente dilatado con disfunción sistólica ligera y ventrículo en posición derecha (VI) con disfunción ligera, hipoquinesia de pared libre, insuficiencia mitral ligera, insuficiencia pulmonar ligera, aorta no competente, ausencia de insuficiencia tricuspídea. La paciente es dada de alta tras 8 días de ingreso hospitalario con tratamiento ambulatorio y con posteriores controles seriados en cardiología.
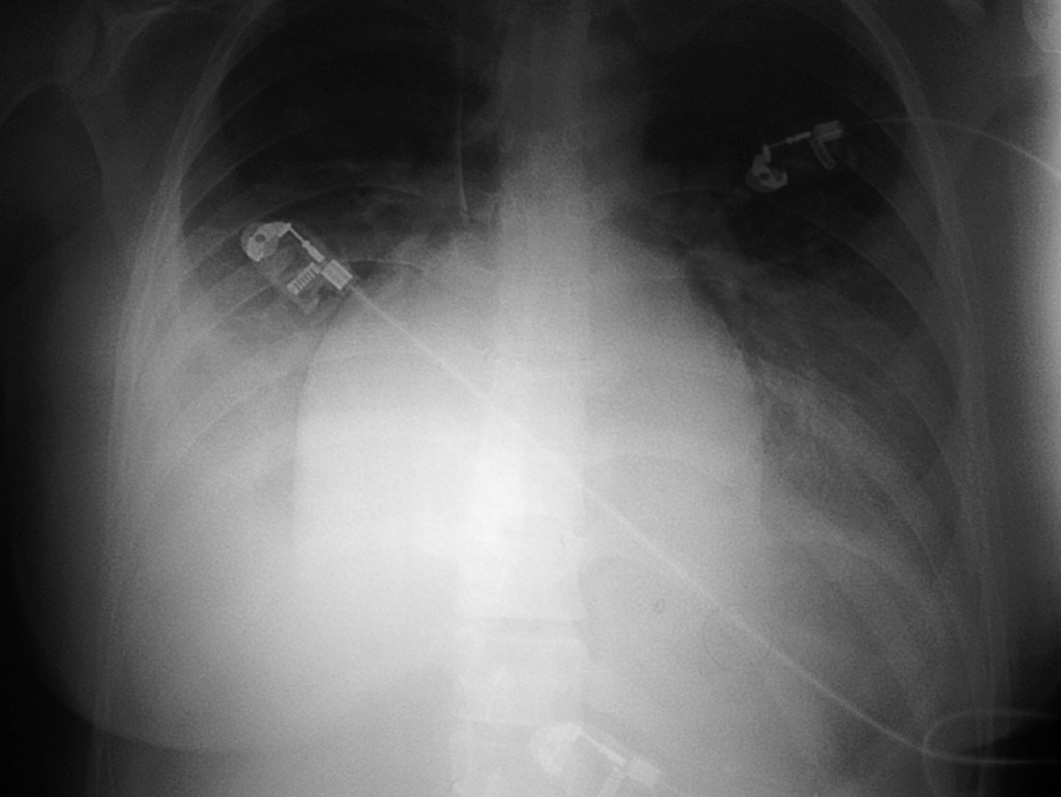
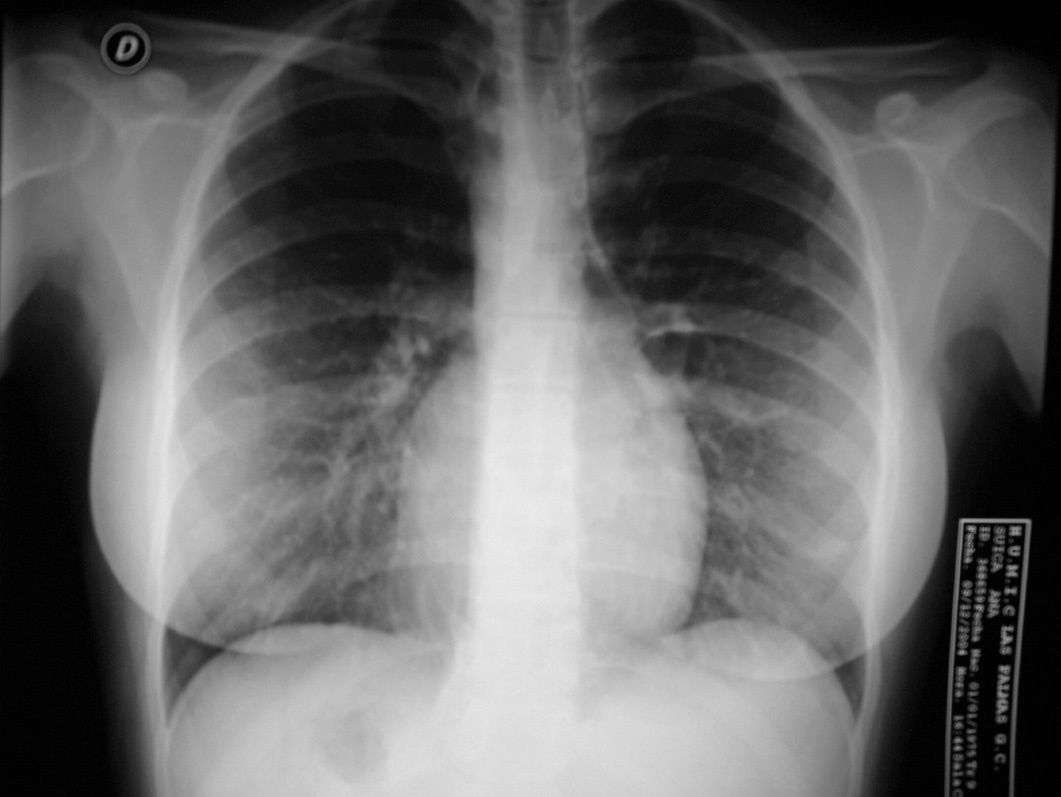
Fig. 2. Radiografía de tórax.
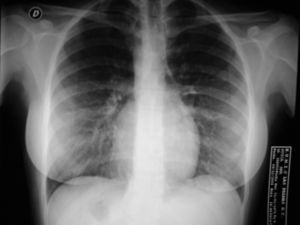
Fig. 3. Radiografía de tórax.
DISCUSIÓN
La L-TGA es una entidad especial, diferente a la transposición de grandes vasos; en la que se mantiene la total normalidad de los flujos sanguíneos, pero el ventrículo izquierdo (VI) tiene un miocardio, una estructura muscular y una válvula aurículoventricular morfológicamente propios del ventrículo derecho (VD), por lo tanto, el VD es el que se encuentra realizando las funciones del VI, enviando sangre a través de la aorta a todo el sistema; y el VD tienen un miocardio, una estructura muscular y una válvula auriculoventricular compatibles con la del VI, y en realidad es el VI el que está haciendo las veces del VD, y envía sangre al lecho pulmonar a través de la arteria pulmonar2. La función cardíaca se mantiene en esta condición, pero el problema es que pese a mantener un flujo sanguíneo normal, el VD y la válvula tricúspide terminan claudicando con el paso del tiempo. Asimismo, la L-TGV suele asociar otras anomalías como la enfermedad de Ebstein, la insuficiencia tricuspídea, la CIV o la estenosis pulmonar2.
Dentro de los cambios fisiológicos circulatorios de las gestantes, se encuentran el aumento de la volemia hasta en un 40% durante el tercer trimestre y del gasto cardíaco. Durante el trabajo de parto, el corazón está sometido a una carga hemodinámica adicional: el gasto cardíaco aumenta un 25% durante el primer período del parto, mientras que en el período expulsivo aumenta de un 50 a un 80%3; estos cambios pueden desencadenar el agravamiento de la patología cardíaca subyacente, como es el caso de CC no detectadas en el momento del nacimiento. La L-TGV, por lo que ya se ha comentado, es una de esas CC que puede no tener manifestaciones durante un largo período y descompensarse durante el embarazo o en el momento del parto. En el caso descrito, la paciente desconocía la existencia de dicha cardiopatía congénita, lo que produjo un manejo del balance hídrico inadecuado para una paciente con una cardiopatía de base. Se sabe que la redistribución vascular que se produce tras el momento del parto es el principal factor en el agravamiento de las pacientes con cardiopatías de base que se encuentran de parto; es fundamental un manejo preciso de los líquidos administrados a las parturientas, así como de la diuresis y las cifras de presión arterial de las pacientes4. Un balance hídrico inadecuado puede desencadenar en un EAP e incluso en un fallo cardíaco. En la tabla I se incluyen las causas más frecuentes de EAP en las gestantes5. Según Oyarzabal et al5, los defectos cardíacos estructurales o funcionales subyacentes son causa frecuente de EAP en la embarazada o parturienta; dentro de estas cardiopatías se encuentran el infarto agudo de miocardio o la miocardiopatía dilatada periparto4-6. Esta última patología es un tipo de fallo cardíaco que se desarrolla en el tercer trimestre o durante los primeros 6 meses posparto, ante la ausencia previa de signos de disfunción ventricular o enfermedad cardíaca4. Sin embargo, las enfermedades cardíacas están muchas veces infradiagnosticadas durante el embarazo, ya que apenas se usan modalidades de diagnóstico como el ecocardiograma. Según los mismos autores, otra causa importante de EAP es la sobrecarga hídrica iatrogénica, que se produce en los casos de reposición excesiva de volumen en los casos de metrorragias puerperales5. En el caso descrito, se produjo una pérdida hemática importante que necesitó reposición de la volemia de forma enérgica, hecho que junto con una cardiopatía existente de base desencadenó el EAP. Según refieren Plasencia et al4,7, el momento y la vía del parto en las pacientes con cardiopatías se deben planificar para dar cierta facilidad a una adecuada intervención. En cuanto al momento del parto es importante recordar que con las contracciones entran en la circulación 300-500 ml de sangre; este aumento del volumen sanguíneo, junto con el incremento de la presión arterial y la frecuencia cardíaca que se producen durante el parto, condicionan una importante elevación del gasto cardíaco, aumentando hasta en un 80% sobre los valores basales, pudiendo llegar a 9 l/min4. Plasencia et al7 y Barber et al8, describen que durante el manejo de las pacientes cardiópatas en trabajo de parto se debe intentar mantener un ambiente de tranquilidad y sedación, la postura ideal que debe adoptar la parturienta es el decúbito lateral izquierdo, y está indicada la utilización de anestesia epidural4,7,8. En cuanto a este punto, la mayoría de los autores coinciden en su oportunidad9-11, aunque para ello se debe realizar un estricto balance de líquidos durante todo el control de dilatación. Basándonos en este hecho, es fundamental no olvidar que debe realizarse un control estricto del balance hídrico de las parturientas cardiópatas; con un control exhaustivo de diuresis y constantes de forma horaria, así como un control continuo de la saturación de oxígeno4,8. Plasencia et al7 resaltan la importancia de la aparición durante el parto de signos de insuficiencia cardíaca, hipotensión y arritmia, y la oportunidad de su detección precoz4,8. En cuanto a la oxitocina, se ha especulado si su uso en las pacientes cardiópatas podría causar un aumento severo en la resistencia vascular pulmonar11 y debe evitarse hasta donde sea posible, pero en cualquier caso se debe individualizar su uso, aunque en ningún caso se contraindica, y son preferible dosis tope hasta 8 mU/min, pero los derivados de la ergotamina, por su efecto vasoconstrictor tienen una contraindicación absoluta8. La profilaxis de endocarditis bacteriana se debe llevar a cabo con ampicilina 2 g intravenosos (i.v.) y gentamicina 80 mg i.v. Ha de evitarse la sobrecarga cardíaca que representa el período de expulsivo, y se realiza su abreviamiento con un parto instrumental. Se debe evitar el sangrado excesivo y la depleción de volumen8,10,11. Puede estar indicada la realización de un alumbramiento dirigido y, en todo caso, se realizará masaje uterino enérgico tras el alumbramiento8. En general, se acepta que, salvo pocas excepciones, el parto vaginal con la abreviación del período expulsivo mediante fórceps es preferible en las parturientas con enfermedad cardíaca4. La elección de la vía del parto debe realizarse únicamente bajo criterios obstétricos, la anestesia epidural se ha utilizado con éxito en el caso de ser necesario realizar una cesárea. El puerperio y el postoperatorio, en el caso de una cesárea, son los momentos más conflictivos para estas pacientes, debido al incremento que el posparto produce en el gasto cardíaco y al estado de hipercoagulabilidad existente. Se debe realizar un control hemodinámico exhaustivo con monitorización continua de las constantes vitales (presión arterial, presión venosa central, pulso y oxigenación), control del sangrado y de la diuresis durante el período de puerperio inmediato4. En la tabla II se resumen las indicaciones de la Sociedad Española de Cardiología para el manejo de las parturientas1. En la bibliografía actual hay pocas referencias a L-TGV y su manejo durante el parto y embarazo, y la mayoría de las referencias son hacia pacientes con TGV o D-TGV corregida de forma quirúrgica mediante técnicas de switching como la Mustard12,13. Schabel et al14 describen un caso de L-TGV diagnosticada a las 20 semanas de gestación por un cuadro de taquicardia paroxística supraventricular; dicha gestante fue inducida a las 40 semanas, y tuvo un parto vaginal exitoso con anestesia epidural y donde se realizó monitorización continua de presión arterial, de saturación de oxígeno y electrocardiográfica. Frenkel et al15 describen otro caso de L-TGV con parto de un recién nacido sano. Pero, en cualquier caso, las referencias acerca de esta patología son escasas en la bibliografía actual. Tras el parto, el retorno venoso se incrementa debido a la falta de compresión de la cava inferior y al paso de sangre adicional proveniente del útero contraído, determinando un aumento de la precarga. Debido a esto, las pacientes de alto riesgo suelen desarrollar edema pulmonar en este período, por lo que es necesaria la monitorización de la función cardíaca, incluso con el uso de un catéter de Swan-Ganz. En pacientes con disfunción ventricular izquierda persistente está contraindicado un nuevo embarazo. Dados los riesgos tromboembólicos de los anticonceptivos orales, debe considerarse la esterilización permanente en estas pacientes.
Aceptado para su publicación el 16 de febrero de 2005.