La hiperplasia endometrial es una proliferación de glándulas endometriales de tamaño y forma irregular, con aumento de la razón glándula/estroma, que se desarrolla a consecuencia de una excesiva exposición a los estrógenos, sin que exista oposición a su efecto proliferativo, o bien por la presencia de factores genéticos.
Se presenta el caso de una paciente de 18 años con diagnóstico de hiperplasia endometrial atípica, en quien, en vista de que era nulípara y adolescente, se implementó tratamiento con goserelina y desogestrel, evidenciándose mejoría a los 10 meses de tratamiento.
Endometrial hyperplasia is a proliferation of endometrial glands of irregular size and shape, with an increase in the gland/stroma ratio, which develops as a result of excessive estrogen exposure, with no opposition to its proliferative effect, or due to the presence of genetic factors.
This article presents the case of an 18-year-old patient with a diagnosis of atypical endometrial hyperplasia who, because she was nulliparous and an adolescent, was treated with goserelin and desogestrel, which produced an improvement at 10 months of treatment.
La hiperplasia endometrial es una proliferación de glándulas endometriales de tamaño y forma irregular, con un aumento de la razón glándula/estroma, que se desarrolla a consecuencia de una excesiva exposición a los estrógenos, sin que exista oposición a su efecto proliferativo, tal y como ocurre en los ciclos anovulatorios, cuando se administran en terapia exógena, con aumento de su producción en entidades clínicas como tumores ováricos funcionantes de células de la granulosa o síndrome de ovario poliquístico1.
Los factores genéticos también están implicados en el desarrollo de la hiperplasia endometrial y los adenocarcinomas. Es así como la inactivación del gen supresor de tumores phosphatase and tensin homolog deleted on chromosome 10 (PTEN), el cual codifica una fosfatasa, facilita la remoción de grupos fosfatos de moléculas Akt y m-TOR cinasas, que se encuentran en la vía intracelular de la fosfoinositol 3-cinasa (PI3K). La actividad de PTEN produce una detención del ciclo celular y la apoptosis, así como la inhibición de la motilidad celular. Por lo tanto, con la pérdida de su expresión, las células ingresan en el ciclo celular y generan una excesiva población celular. Se ha demostrado que esta deleción es un evento temprano en la carcinogénesis endometrial que favorece además que las células se vuelvan más sensibles a la estimulación estrogénica2,3.
La International Society of Gynecological Pathologist y el comité de tumores endometriales de la OMS (3) deciden adoptar la clasificación de hiperplasia simple, compleja y atípica, con base en la apariencia, aglomeración y la presencia de atipia en el epitelio glandular, como originalmente fue definida por Kurman et al.
La hiperplasia simple es una lesión proliferativa que se caracteriza por cambios arquitectónicos en las glándulas de diversos tamaños, con mínimos cambios en la complejidad y densidad glandular y abundante estroma. La hiperplasia endometrial compleja es también una lesión proliferativa, en la cual se exhibe un incremento en el número y tamaño de las glándulas endometriales, que lucen apiñadas de forma irregular y con mínimo estroma interpuesto2,4.
La presencia de atipia celular es el factor pronóstico más importante para la progresión a carcinoma endometrial. Según estudios recientes el 23% de las pacientes con hiperplasias atípicas desarrollan adenocarcinoma de endometrio en un promedio de 4 años posterior al diagnóstico de la lesión precursora, mientras que solo el 2% de lesiones sin atipia progresan en un período estimado de 13,4 años3.
Caso clínicoSe presenta el caso de una adolescente de 18 años quien consulta en enero del 2011 por presentar hipermetrorragia de 6 meses de evolución sin concomitantes. Antecedentes personales: niega patológicos. Antecedentes ginecoobstétricos: menarquia a los 13 años, ciclos menstruales irregulares de 2 años de evolución iniciando hipermetrorragia en julio del 2011; sexarquia a los 16 años, gestas 0. Niega uso de ACO y realización de PAP. Antecedentes familiares: niega patológicos.
Al examen físico: buenas condiciones generales, sin signos de hirsutismo, cardiopulmonar, normal. Mamas simétricas sin nódulos. Abdomen blando depresible no doloroso, sin tumoraciones ni megalias; genitales normoconfigurados, vagina sin lesiones, cuello oce puntiforme. Exocérvix sin atipias. Tacto: útero regular de consistencia normal. Anexos no palpables. Resto del examen sin alteración.
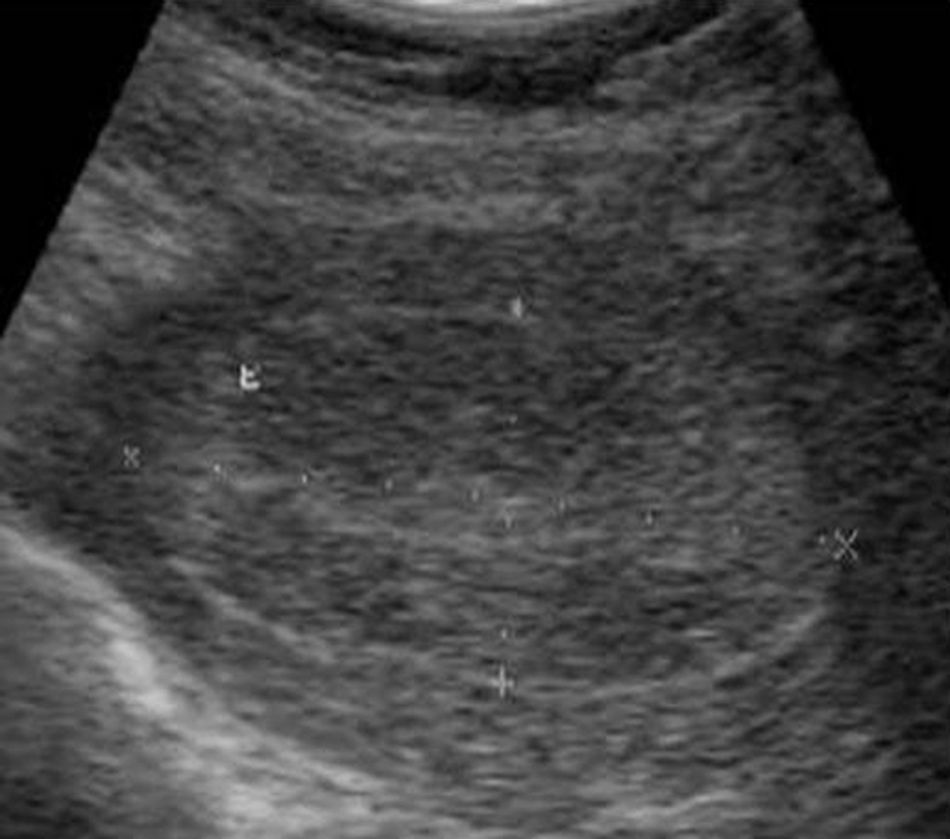
EvoluciónEnero de 2011. Se realiza ecosonograma pélvico que reporta útero de contornos regulares, miometrio homogéneo, engrosamiento endometrial de 21,5mm. (fig. 1), no acorde con ciclo menstrual. Ovarios sin alteración. Se planifica legrado biópsico que reporta hiperplasia endometrial atípica.
Febrero de 2011. Inicia tratamiento con goserelina 3,6mg, mensual por 4 ciclos, revalorada ecográficamente a la 3.era dosis, evidenciándose endometrio de 1,3cm.
Junio de 2011. Inicia tratamiento con desogestrel 0,75 mcg VO, continuo por 6 meses.
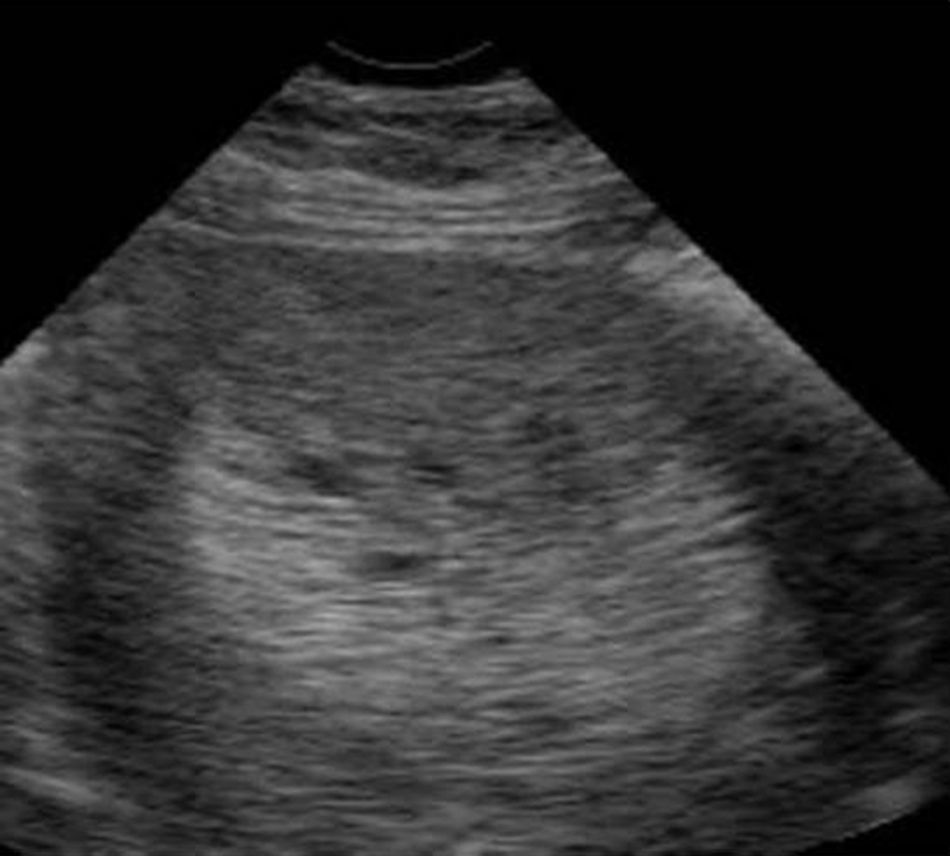
Diciembre de 2011. Control ecográfico que reporta útero piriforme de contorno regular, miometrio homogéneo, endometrio lineal. Ovarios sin alteración (fig. 2).
Enero de 2012. Biopsia endometrial que reporta endometrio proliferativo, sin evidencia de atipias celulares. Se plantea estudio genético.
ConclusiónLa hiperplasia atípica de endometrio se encuentra altamente relacionada con cáncer de endometrio.
Las pacientes con hiperplasia simple o compleja sin atipia pueden ser tratadas clínicamente, pues el riesgo de progreso para cáncer de endometrio es bajo, del 1 al 3%, mientras que las pacientes con hiperplasia atípica tienen riesgo elevado variando del 8 al 29%4,5.
La terapia de elección en la hiperplasia atípica es la histerectomía, sin embargo puede realizarse tratamiento médico en pacientes con alto riesgo quirúrgico o pacientes nulíparas con deseo de fertilidad. Uno de los más interesantes avances en el tratamiento de muchos es la capacidad de reversión de las respuestas hiperplásicas de cambios con el uso de progestágenos. La AMP y los derivados sintéticos de las progestágenas AM, 17-alfa-hidroxiprogesterona, son eficaces oralmente y pueden revertir la mayoría de las lesiones hiperplásicas. Es un tratamiento prolongado y requiere periódicas biopsias para confirmar la resolución de la lesión. Presentó la regularización del ciclo menstrual o entraron en amenorrea. La persistencia de sangrado anormal causado a estas mujeres a reconsiderar y aceptar el tratamiento quirúrgico3,5.
La hiperplasia endometrial es una entidad poco frecuente en adolescentes, enpacientes delgadas y sin relación con ovarios poliquísticos, tal como la paciente presentada, en las que hay que considerar el factor genético. Es importante señalar que el tratamiento conservador puede llevarse a cabo en pacientes nulíparas que desean preservar la fertilidad. A pesar de ser una entidad con alto potencial de adenocarcinoma, un adecuado seguimiento de la paciente permite controlar la enfermedad endometrial.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.