En la enfermedad renal crónica (ERC) la retención de fósforo por el riñón se inicia desde fases precoces de la enfermedad (FG < 60 ml/min); la acumulación de fósforo en sangre y otros tejidos es el mecanismo que pone en marcha el exceso de producción de PTH por las glándulas paratiroides. El hiperparatiroidismo secundario es el origen de importantes alteraciones óseas, pero hoy se sabe que además puede dar lugar a calcificaciones vasculares que aumentan la mortalidad cardiovascular ya de por sí elevada en estos pacientes1. En la ERC se admite que la hiperfosfatemia mantenida que presentan estos enfermos está relacionada con un incremento de la mortalidad en esta población1. La hiperfosfatemia no controlada puede ser el origen de la calcif icación de las paredes de vasos sanguíneos, válvulas cardíacas y otros tejidos blandos. El incremento del producto calcio-fósforo2-5 puede ser un estímulo que causa que las células musculares lisas de la pared arterial, en especial las alojadas en la capa media, se transformen en una célula procalcificante. Más concretamente, se ha demostrado que el exceso de fósforo es en sí mismo un estímulo lo suficientemente eficaz para que dicha célula muscular lisa inicie la síntesis de proteínas que promueven la aparición de las calcificaciones6. De ahí la importancia de utilizar estrategias para evitar la hiperfosforemia desde fases precoces de la enfermedad.
En el tratamiento de la hiperfosfatemia asociada a la ERC se pueden emplear las siguientes estrategias terapéuticas: dieta pobre en fósforo, mejoría en el esquema de diálisis (aumentando su frecuencia, por ejemplo) y tratamiento con quelantes (captores) de fósforo. Con respecto a las primeras 2 alternativas, es muy difícil que los pacientes sigan la dieta estricta y el aumento de la frecuencia de la diálisis7, aunque ha demostrado ser más eficaz que la pauta habitual, no es aplicable en todos los centros ni en todos los enfermos que lo requieren. Los quelantes de fósforo, clásicamente, se han agrupado en compuestos portadores de calcio (acetato cálcico o carbonato cálcico) y los que no lo tienen (hidróxido de aluminio y sevelamer). A este arsenal terapéutico se ha añadido un nuevo quelante sin calcio, el carbonato de lantano, que proporciona una eficacia quelante alta sin el riesgo de elevar la calcemia. El lantano es un elemento químico de peso atómico de 138,9 Da, perteneciente al grupo de las tierras raras y de número atómico 57. Se encuentran trazas de él en el agua y ciertos alimentos, así como en la composición del cuerpo humano8,9. En medicina se usa como material de relleno para el tratamiento de las caries dentales.
Mecanismo de acción, farmacocinética y farmacodinamia del carbonato de lantanoEl carbonato de lantano es una sal quelante de fósforo que no contiene calcio y posee un mecanismo de acción diferente del de sevelamer, quelante poliamínico sintético sin calcio.
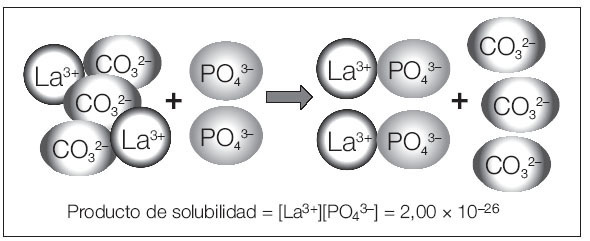
Tras su ingesta durante las principales comidas del día, se produce en la luz intestinal una sustitución del ion carbonato por el ion fosfato (procedente de los alimentos), de tal manera que se forma fosfato de lantano (sal insoluble) liberándose carbonato. De este modo, gran cantidad de fosfato se elimina por las heces, evitando su absorción en las vellosidades intestinales (fig. 1). A diferencia del sevelamer, el mecanismo de quelación es específico para el ion fosfato, ya que la sal de carbonato de lantano no interfiere con la absorción de vitaminas liposolubles (A, D, E, K), ni ácido fólico ni grasas procedentes de la dieta. El mecanismo de acción quelante de sevelamer es semejante al de otros polímeros sintéticos, como las resinas de intercambio iónico, empleadas en el tratamiento de la hipercolesterolemia. Éstas actúan secuestrando los ácidos biliares, impiden su reabsorción y reducen así el colesterol de las lipoproteínas de baja densidad.
Figura 1. Mecanismo de acción quelante de fósforo del carbonato de lantano en la luz intestinal.
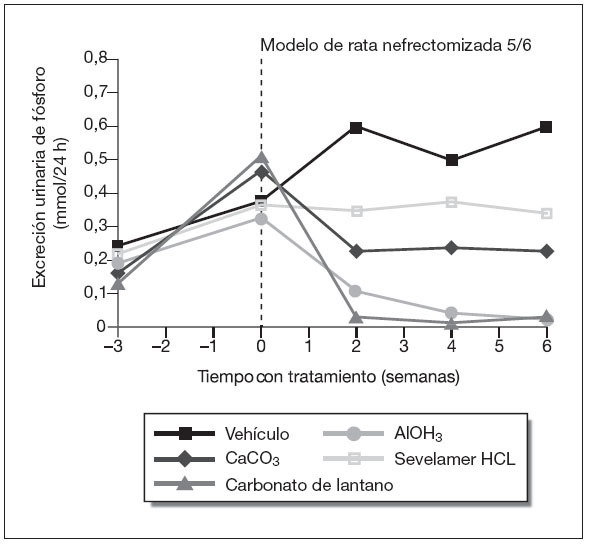
En estudios in vitro se ha demostrado que el carbonato de lantano liga el fosfato de una manera tan potente como el hidróxido de aluminio, en un valor de pH clínicamente relevante (entre 3 y 7). En un estudio preclínico con un modelo de ratas nefrectomizadas (nefrectomía 5/6), el carbonato de lantano mostró una mayor potencia quelante del fosfato de la dieta que el carbonato cálcico o el sevelamer. El estudio se llevó a cabo durante 6 semanas10. La potencia quelante fue establecida en función de la cantidad de fósforo urinario detectado. En la figura 2 se puede observar que la potencia quelante del carbonato de lantano es semejante a la del hidróxido de aluminio, y casi 4 veces la del sevelamer. Se ha calculado que la constante de afinidad quelante de fosfato es 200 y 4 veces mayor para el carbonato de lantano que para el sevelamer a pH 3 y 7, respectivamente11,12.
Figura 2. Medida de la potencia quelante de fósforo de fármacos en función de la cantidad de fosfato excretada en orina. Modelo experimental de ratas 5/6 nefrectomizadas. Modificado de Hutchison10.
A diferencia del aluminio, el lantano presenta una absorción intestinal marginal; su biodisponibilidad en animales es del 0,0007 %. En humanos se ha notifica-do una biodisponibilidad del 0,00089 %13,14. Las trazas de este elemento se eliminan mayoritariamente por la bilis, y solamente un 0,0003 % de la dosis de 1 g/día se eliminaría en la orina13-15. Se ha constatado que la farmacocinética del lantano es similar en voluntarios sanos y en enfermos dializados, y por tanto independiente de la función renal del individuo. Tras varias semanas de tratamiento, se ha detectado una concentración plasmática máxima de sólo 1 ng/ml. En humanos no hay evidencia de que el lantano atraviese la barrera hematoencefálica14. Se han detectado trazas en el hueso, aunque también se ha comprobado su existencia en pacientes dializados no tratados con carbonato de lantano, lo cual se explicaría por el hecho de que en algunas ciudades europeas se han medido concentraciones relativamente altas de lantano en el agua corriente y las verduras. La mediana de lantano detectado en hueso es de 1,8 µg/g, tras un año de tratamiento. Las máximas concentraciones registradas tras 1 y 4 años de tratamiento fueron de 5,5 y 9 µg/g, respectivamente. Parece que el lantano podría mostrar un efecto semejante al de los bisfosfonatos en la arquitectura ósea, que mejora la enfermedad ósea adinámica al cabo de 1 año de tratamiento14-16.
Eficacia clínica y perfil de seguridadLos resultados de los ensayos clínicos realizados (11 de fase I y 10 de fases II y III) demuestran que el carbonato de lantano es un quelante de fósforo eficaz y con perfil de tolerancia adecuado. Aproximadamente el 70 % de los enfermos tratados con carbonato de lantano en monoterapia presentan un adecuado control de la fosfatemia al cabo de 4 semanas de iniciar el tratamiento, tras el ajuste de dosis17. Los resultados de los dos grandes ensayos de fase III, con brazo comparador con carbonato cálcico y otros quelantes18-20, donde se ha incluido a 800 y 1.359 pacientes, muestran igualmente un adecuado control de la fosfatemia a largo plazo (3 años). Hasta un 65,8 % de los enfermos tratados con carbonato de lantano presentan fosfatemias µ 5,58 mg/dl durante estos ensayos. Las concentraciones de PTH registradas en el grupo de tratamiento con carbonato de lantano se mantuvieron en el intervalo recomendado de 150-300 pg/ml. En cambio, en el grupo control, permanecieron por debajo a lo largo del ensayo (Finn20). En todos los ensayos los episodios de hipercalcemia fueron estadísticamente mayores en el grupo comparador, en que se notificó una media del 20,2 % de estos episodios18. Los episodios de hipercalcemia en los enfermos tratados con carbonato de lantano oscilan entre el 0,4 y el 4,3 % de los pacientes. Entre los eventos adversos más frecuentemente notificados19 figuran los de origen gastrointestinal, como náuseas (15 %), vómitos (13 %), diarrea (11 %) y dolor abdominal (4,5 %). En todos los ensayos comparativos publicados la frecuencia de estos eventos adversos fue similar en el grupo de tratamiento con lantano que en el grupo control. Sin embargo, y a diferencia de lo que ha ocurrido con el principal comparador de grupo, el sevelamer, no se han publicado hasta la fecha casos de perforación intestinal21.
Se ha publicado que la obstrucción y la perforación intestinales pueden ocurrir hasta en un 6,7 % de los pacientes tratados con sevelamer. Probablemente, estos efectos adversos tengan que ver con el propio mecanismo de acción de este fármaco, ya que cada comprimido de sevelamer experimenta una gran hidratación en la luz intestinal absorbiendo líquido y su volumen aumenta entre 6 y 8 veces. Tal expansión de volumen puede causar obstrucción intestinal, necrosis intestinal por deshidratación de la pared intestinal y perforación. No hay diferencias en la frecuencia de aparición de otros efectos adversos descritos con el carbonato de lantano con respecto a otros quelantes que contienen calcio o sevelamer. A diferencia del hidróxido de aluminio, no se ha descrito toxicidad ósea, hematológica ni neurológica con el empleo de carbonato de lantano. Se han publicado datos de un ensayo clínico de 6 años de duración que confirman estas evidencias22.
Posología, pauta de administración y contraindicacionesLos comprimidos de carbonato de lantano deben administrarse durante las principales comidas del día. Se trata de comprimidos masticables insípidos. No es preciso ingerirlos con líquidos, lo que en estos enfermos supone una gran ventaja, ya que de esta manera se favorece la restricción hídrica a la que deben estar sometidos. La dosis diaria media reconocida por la OMS es de 2.250 mg. Esto equivaldría a 3 comprimidos de 750 mg al día. El número de comprimidos diarios es inferior al que habitualmente se precisa con otros quelantes de fósforo, lo que podría redundar en un mejor cumplimiento terapéutico12. En la mayoría de los ensayos clínicos el tratamiento suele iniciarse con dosis menores y se procede a un ajuste de dosis en un período de 2 a 4 semanas, en virtud de las cifras de fosfatemia de cada individuo. Además de los comprimidos de 750 mg, existe una presentación de 500 mg y otra de 1.000 mg. Este fármaco está indicado para el tratamiento de la hiperfosfatemia, tanto en pacientes en hemodiálisis como en diálisis peritoneal. Como contraindicaciones se ha descrito la hipersensibilidad al carbonato de lantano o a alguno de los excipientes y la hipofosfatemia.
ConclusionesEl carbonato de lantano se presenta como un nuevo quelante de fósforo, de gran potencia, libre de calcio, con un perfil de seguridad adecuado. Por su eficacia quelante se recomienda su empleo en monoterapia. El hecho de administrar un menor número de comprimidos diarios en comparación con otros quelantes puede traducirse en un mejor cumplimiento terapéutico a largo plazo.
AgradecimientoQuiero manifestar mi agradecimiento por el estímulo para su publicación y la revisión de este manuscrito a la Dra. María Teresa Gonzalez-Álvarez y el Dr. Julen Ocharan-Corcuera.
Los autores no declaran conflictos de intereses.
Correspondencia: Dr. V.M. Navas-Serrano. Departamento Médico. Shire Pharmaceuticals Ibérica. Madrid. España. Correo electrónico: vnavas@shire.com
Recibido el 16-1-2008; aceptado para su publicación el 17-1-2008.