El síndrome de hipersensibilidad (SH) a fármacos es una reacción adversa de tipo B que se presenta como una enfermedad sistémica con fiebre, erupción cutánea e implica a uno o más órganos internos1. Este tipo de reacciones de naturaleza idiosincrásica es impredecible y su importancia radica más que en su incidencia, en su potencial morbi-mortalidad asociadas.
Uno de los síntomas más indicativos son las manifestaciones cutáneas, las cuales aparecen aproximadamente en el 85% de los pacientes.
La limitada gravedad inicial del SH asociada a una remisión mediante la aplicación de preparados por vía tópica no debe descartar el potencial desarrollo de complicaciones posteriores. Este síndrome se ha asociado mayoritariamente al tratamiento con sulfamidas2.
Se presenta un caso de un varón de 75 años con antecedentes de nocardiosis pulmonar e inmunosupresión por corticoides (prednisona 60mg al día) para una miastenia gravis que ingresa por sospecha de nocardiosis diseminada con afectación del sistema nervioso central.
El diagnóstico se confirmó por las pruebas de laboratorio de líquido cefalorraquídeo (ADA: 10,1 UI/L; células nucleadas: 20 cel/mm3; células polimorfonucleadas: 55%; células mononucleadas: 45%; proteínas: 182,2mg/dL y glucosa: 74mg/dL) y por el resultado de la resonancia magnética cerebral, en la que se observaron lesiones bilaterales en hemisferios cerebrales compatibles con abscesos (Nocardia spp.) y probable afectación ependimaria ventricular.
Se decidió instaurar tratamiento con trimetoprim-sulfametoxazol a dosis de 15mg/kg/día (trimetoprim) asociado a ceftriaxona 2g cada 12h3, observándose una buena evolución radiológica en la resonancia magnética craneal y cervical tras 10 días de tratamiento.
Doce días después de iniciar el tratamiento antibiótico el paciente presentó una erupción cutánea generalizada con prurito que remitió mediante la instauración de tratamiento tópico. Este cuadro fue orientado inicialmente como probable toxicodermia por trimetoprim-sulfametoxazol que posteriormente fue confirmado mediante una biopsia cutánea.
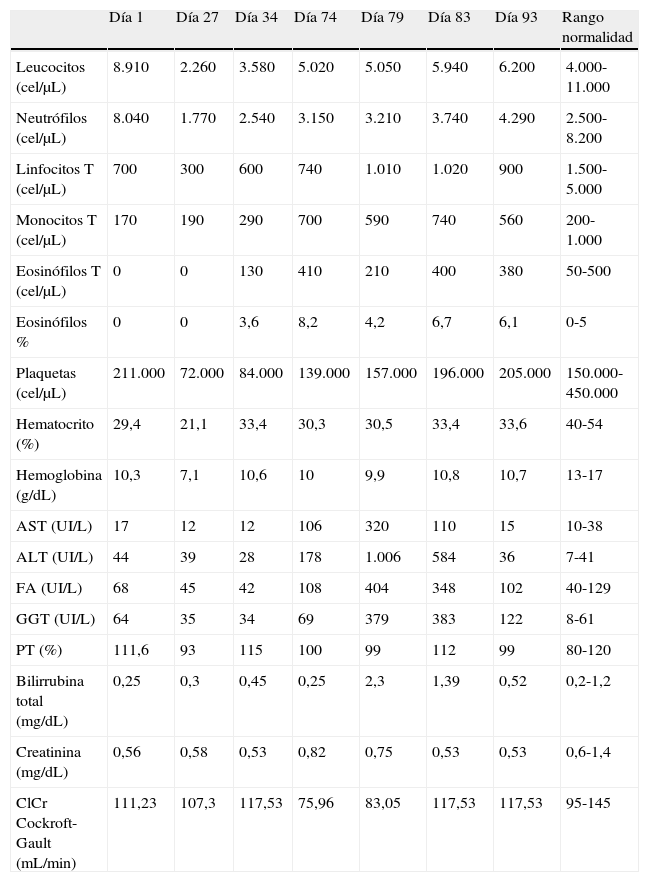
Veintisiete días después el paciente desarrolló una aplasia medular (tabla 1) y un síndrome confusional que se atribuyeron al antimicrobiano.
Evolución de los parámetros analíticos
| Día 1 | Día 27 | Día 34 | Día 74 | Día 79 | Día 83 | Día 93 | Rango normalidad | |
| Leucocitos (cel/μL) | 8.910 | 2.260 | 3.580 | 5.020 | 5.050 | 5.940 | 6.200 | 4.000-11.000 |
| Neutrófilos (cel/μL) | 8.040 | 1.770 | 2.540 | 3.150 | 3.210 | 3.740 | 4.290 | 2.500-8.200 |
| Linfocitos T (cel/μL) | 700 | 300 | 600 | 740 | 1.010 | 1.020 | 900 | 1.500-5.000 |
| Monocitos T (cel/μL) | 170 | 190 | 290 | 700 | 590 | 740 | 560 | 200-1.000 |
| Eosinófilos T (cel/μL) | 0 | 0 | 130 | 410 | 210 | 400 | 380 | 50-500 |
| Eosinófilos % | 0 | 0 | 3,6 | 8,2 | 4,2 | 6,7 | 6,1 | 0-5 |
| Plaquetas (cel/μL) | 211.000 | 72.000 | 84.000 | 139.000 | 157.000 | 196.000 | 205.000 | 150.000-450.000 |
| Hematocrito (%) | 29,4 | 21,1 | 33,4 | 30,3 | 30,5 | 33,4 | 33,6 | 40-54 |
| Hemoglobina (g/dL) | 10,3 | 7,1 | 10,6 | 10 | 9,9 | 10,8 | 10,7 | 13-17 |
| AST (UI/L) | 17 | 12 | 12 | 106 | 320 | 110 | 15 | 10-38 |
| ALT (UI/L) | 44 | 39 | 28 | 178 | 1.006 | 584 | 36 | 7-41 |
| FA (UI/L) | 68 | 45 | 42 | 108 | 404 | 348 | 102 | 40-129 |
| GGT (UI/L) | 64 | 35 | 34 | 69 | 379 | 383 | 122 | 8-61 |
| PT (%) | 111,6 | 93 | 115 | 100 | 99 | 112 | 99 | 80-120 |
| Bilirrubina total (mg/dL) | 0,25 | 0,3 | 0,45 | 0,25 | 2,3 | 1,39 | 0,52 | 0,2-1,2 |
| Creatinina (mg/dL) | 0,56 | 0,58 | 0,53 | 0,82 | 0,75 | 0,53 | 0,53 | 0,6-1,4 |
| ClCr Cockroft-Gault (mL/min) | 111,23 | 107,3 | 117,53 | 75,96 | 83,05 | 117,53 | 117,53 | 95-145 |
ALT: alanina aminotransferasa; AST: aspartato aminotransferasa; ClCr: aclaramiento de creatinina; FA: fosfatasa alcalina; GGT: gamma glutamil transpeptidasa; PT: tiempo de protrombina.
Se decidió sustituir el tratamiento con trimetoprim-sulfametoxazol por linezolid 600mg cada 12h.
Posteriormente, dada la recuperación gradual de los valores hematológicos y la ausencia de mejoría clínica con linezolid, se reintrodujo el tratamiento con trimetoprim-sulfametoxazol. Tras 40 días de la segunda pauta con este antibiótico (día 74) el paciente relató sensación nauseosa y mareo, asociados a vómitos de origen no alimentario ni bilioso. En la analítica correspondiente se observó una alteración hepática con eosinofilia relativa. En los días posteriores el paciente volvió a presentar diversos vómitos, esta vez de contenido bilioso.
Cinco días después (día 79) el paciente presentó una alteración del perfil hepático en forma de hepatitis aguda colestásica. La aplicación del algoritmo de Naranjo para la atribución del efecto adverso estableció el trimetoprim-sulfametoxazol como causa altamente probable de la hepatotoxicidad (puntuación de 9)4.
Se orientó como una hepatotoxicidad aguda farmacológica secundaria a trimetoprim-sulfametoxazol, por lo que se recomendó su retirada definitiva, manteniendo ceftriaxona en monoterapia.
Tras 4 días (día 83) el paciente experimentó una mejoría clínica y del perfil hepático (tabla 1).
Posteriormente el paciente evolucionó favorablemente completando tratamiento con ceftriaxona durante un año.
En este caso el paciente presentó inicialmente un episodio de toxicidad leve en forma de rash cutáneo asociado a trimetoprim-sulfametoxazol. Posteriormente el paciente presentó pancitopenia y afectación hepática, asociadas a este antibiótico de forma paralela a la afectación cutánea. No obstante, cada uno de estos efectos adversos se diagnosticaron de forma aislada y no como parte de un mismo cuadro de SH.
Este caso resalta la importancia de la identificación temprana y asociación del conjunto de síntomas al SH a un determinado fármaco, dada la potencial gravedad que puede llevar consigo este síndrome.