La malaria es potencialmente mortal y precisa un diagnóstico y un tratamiento urgentes. En zonas endémicas se está reduciendo su incidencia y mortalidad. La clínica es inespecífica, por lo que en malarias importadas es vital el antecedente de estancia en una zona malárica. La terapia de elección en Plasmodium falciparum son los tratamientos combinados con artemisininas, la cloroquina en la mayoría de los no P.falciparum y el artesunato intravenoso si existen criterios de gravedad.
Las infecciones humanas por protozoos intestinales son de distribución mundial, con una alta morbimortalidad global. Producen diarrea y a veces enfermedad invasiva, aunque la mayoría son asintomáticas. En nuestro medio, las poblaciones de mayor riesgo son los niños —incluyendo adoptados en el extranjero—, inmunodeprimidos, viajeros, inmigrantes y personas en contacto con animales o que practican sexo oral-anal. El examen microscópico diagnóstico tiene baja sensibilidad, mejorando con métodos de detección de antígenos o moleculares. Recientemente están apareciendo resistencias a los antiparasitarios.
Malaria is life threatening and requires urgent diagnosis and treatment. Incidence and mortality are being reduced in endemic areas. Clinical features are unspecific so in imported cases it is vital the history of staying in a malarious area. The first line treatments for Plasmodium falciparum are artemisinin combination therapies, chloroquine in most non-falciparum and intravenous artesunate if any severity criteria.
Human infections with intestinal protozoa are distributed worldwide with a high global morbid-mortality. They cause diarrhea and sometimes invasive disease, although most are asymptomatic. In our environment populations at higher risk are children, including adopted abroad, immune-suppressed, travelers, immigrants, people in contact with animals or who engage in oral-anal sex. Diagnostic microscopic examination has low sensitivity improving with antigen detection or molecular methods. Antiparasitic resistances are emerging lately.
La malaria en humanos es una infección producida por protozoos del género Plasmodium, que comprende 6 especies: Plasmodium falciparum, P. vivax, P. malariae, P. knowlesi, P. ovale wallikeri y P. ovale curtisi. Se transmite por la picadura de la hembra del mosquito Anopheles, aunque puede haber casos de transmisión vertical de madre embarazada a su hijo, por transfusiones de sangre, trasplante de órganos o al compartir jeringuillas.
Según estimaciones de la Organización Mundial de la Salud (OMS), en el año 2013 se produjeron 198 millones de casos de malaria sintomática en el mundo, la mayoría en África (82%), seguido del sudeste asiático (12%) y la región mediterránea oriental de la OMS (5%). Más del 90% son debidos a P.falciparum, que es la infección más grave y con mayor mortalidad. Se calculan unas 584.000 muertes al año, más del 90% en África, un 7% en el sudeste asiático y un 2% en la región mediterránea oriental. Un 78% de los fallecidos son niños menores de 5años1. P.vivax causa alrededor del 8% de los casos, la mayoría fuera de África, donde llega a representar hasta el 47%2.
Desde el año 2000 se desarrolla una campaña mundial contra la malaria financiada por un aumento de fondos sin precedentes. Se basa en una estrategia múltiple de control con mosquiteras impregnadas con insecticida, rociado residual domiciliario con insecticida, diagnóstico y tratamiento precoz de los casos de malaria con tratamientos combinados con artemisininas y profilaxis en el embarazo. Con esta estrategia se ha reducido la incidencia de malaria un 30% a nivel mundial desde el año 20001 y un 40% la infección por P. falciparum en África entre los años 2000 y 2015, especialmente gracias a la distribución de mosquiteras3. Se estima que la tasa de mortalidad ha disminuido en un 47% a nivel mundial entre 2000-2013 y en un 54% en África. Doce países con transmisión de malaria en el año 2000 no han informado de casos autóctonos en 20131. Los objetivos de desarrollo sostenible de la ONU plantean un nuevo impulso para poner fin a las epidemias del sida, la tuberculosis, la malaria y las enfermedades tropicales desatendidas para el año 20304.
Malaria importada en EspañaEn el año 2012 se comunicaron más de 5.000casos de malaria importada en la Unión Europea, el 63% de ellos en Francia y el Reino Unido5. En España se declararon ese año 484infecciones, de las que el 90% eran P. falciparum adquiridas en África, sobre todo en Guinea Ecuatorial y Nigeria. Del resto, 24 fueron P. vivax, la mitad de ellas de Pakistán, 11 P. ovale, 4 P. malariae y 3 mixtas. La mayoría fueron inmigrantes residentes en España que visitaron a su familia y amigos sin tomar profilaxis. También se aprecia un aumento progresivo en el número de casos desde el año 20086. A pesar de que en España es una enfermedad de declaración obligatoria7, sigue existiendo una infranotificación no cuantificada.
Manejo práctico de la malaria importadaRecientemente se han publicado unas completas recomendaciones para el diagnóstico microbiológico y el tratamiento de la malaria importada en España8,9, y la OMS ha actualizado en 2015 la Guía de tratamiento de la malaria10.
Sospecha clínicaLos signos y síntomas de la malaria son inespecíficos, pero los más frecuentes son: fiebre, cefalea, artromialgias, náuseas y vómitos. Puede acompañarse de dolor abdominal, diarrea, tos, astenia y, en casos graves, un rápido deterioro clínico con disnea, coma, crisis comiciales, ictericia, hemorragias, shock y finalmente la muerte si no se instaura un tratamiento precoz. Se puede confundir con múltiples infecciones víricas, intestinales, neurológicas, respiratorias o hepatitis. Además, los pacientes que han padecido malarias previas presentan cierta semiinmunidad que les protege frente a episodios graves, por lo que pueden permanecer asintomáticos y presentar infecciones submicroscópicas no detectables con las pruebas microbiológicas habituales11. Por eso, de cara al diagnóstico es muy importante confirmar el antecedente epidemiológico de haber permanecido en una zona con malaria al menos durante el último año. Más del 90% de las infecciones por P.falciparum importadas se manifiestan con clínica estando todavía en zona malárica o durante el primer mes después de la llegada. Sin embargo, en P.vivax, P.ovale y P.malariae, más del 45% pueden aparecer pasado el primer mes y hasta un año después de llegar12.
Las alteraciones analíticas más frecuentes también son inespecíficas e incluyen: trombocitopenia, anemia, elevación de LDH y bilirrubina. No suele producir leucocitosis, y si existe, sugiere una sobreinfección bacteriana. La esplenomegalia es frecuente en la exploración.
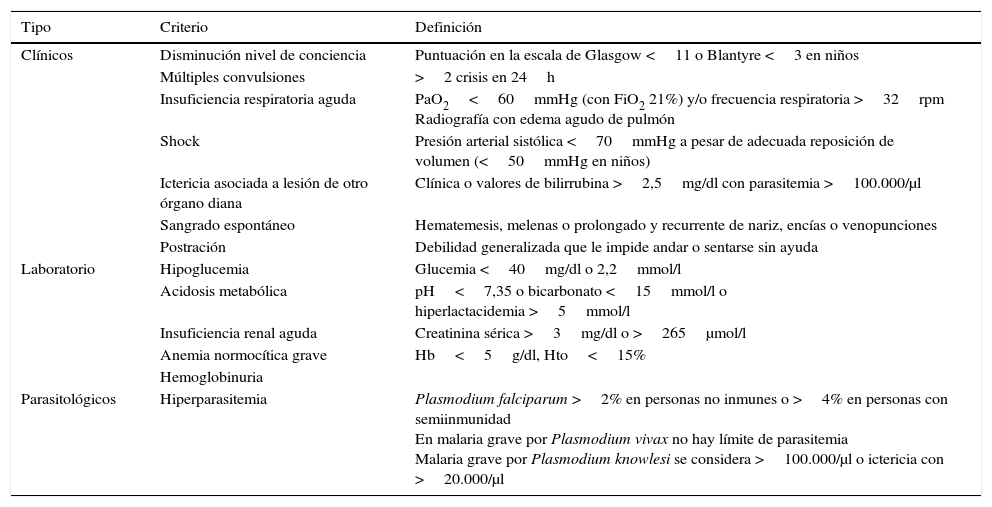
Malaria grave y complicadaP.falciparum produce la mayor parte de las malarias graves y muertes; con menos frecuencia P.vivax y P.knowlesi, que tiene el ciclo eritrocítico más corto de 24h. Excepcionalmente, P.ovale y P.malariae también puede producir complicaciones graves13. Los criterios de gravedad se resumen en la tabla 1, modificada para malarias importadas, y son similares a una sepsis con disfunción de múltiples órganos, aunque su fisiopatología es diferente14. En adultos es más frecuente la afectación renal, hepática o pulmonar. En niños, los casos graves se presentan más a menudo como malaria cerebral, anemia grave, hipoglucemia, acidosis o complicada con sobreinfecciones bacterianas. Otra complicación esporádica y grave es la rotura de bazo. Los grupos de especial riesgo para sufrir una malaria grave son las mujeres embarazadas15, los niños, los pacientes inmunodeprimidos (VIH con CD4 <350/μl16, hipoesplenismo) o los viajeros no semiinmunes. En malarias importadas, entre el 3,6 y el 23% presentan criterios de gravedad, y la mortalidad es mayor en viajeros no semiinmunes, llegando al 2-3%17.
Criterios de gravedad de la malaria importada
| Tipo | Criterio | Definición |
|---|---|---|
| Clínicos | Disminución nivel de conciencia | Puntuación en la escala de Glasgow <11 o Blantyre <3 en niños |
| Múltiples convulsiones | >2 crisis en 24h | |
| Insuficiencia respiratoria aguda | PaO2<60mmHg (con FiO2 21%) y/o frecuencia respiratoria >32rpm Radiografía con edema agudo de pulmón | |
| Shock | Presión arterial sistólica <70mmHg a pesar de adecuada reposición de volumen (<50mmHg en niños) | |
| Ictericia asociada a lesión de otro órgano diana | Clínica o valores de bilirrubina >2,5mg/dl con parasitemia >100.000/μl | |
| Sangrado espontáneo | Hematemesis, melenas o prolongado y recurrente de nariz, encías o venopunciones | |
| Postración | Debilidad generalizada que le impide andar o sentarse sin ayuda | |
| Laboratorio | Hipoglucemia | Glucemia <40mg/dl o 2,2mmol/l |
| Acidosis metabólica | pH<7,35 o bicarbonato <15mmol/l o hiperlactacidemia >5mmol/l | |
| Insuficiencia renal aguda | Creatinina sérica >3mg/dl o >265μmol/l | |
| Anemia normocítica grave | Hb<5g/dl, Hto<15% | |
| Hemoglobinuria | ||
| Parasitológicos | Hiperparasitemia | Plasmodium falciparum >2% en personas no inmunes o >4% en personas con semiinmunidad En malaria grave por Plasmodium vivax no hay límite de parasitemia Malaria grave por Plasmodium knowlesi se considera >100.000/μl o ictericia con >20.000/μl |
Ante cualquier paciente sintomático procedente de una zona endémica se debe sospechar una malaria importada, y siempre es imperativo realizar un diagnóstico urgente, idealmente en menos de 3-4h, tenga o no fiebre en ese momento8,18. En paralelo y según la clínica del paciente conviene realizar otras pruebas como hemocultivos, urocultivos, coprocultivos, punción lumbar o pruebas de imagen para descartar otros posibles focos de infección.
Las técnicas disponibles son: la gota gruesa y la extensión fina de sangre —ambas con tinción de Giemsa—, los test rápidos de detección de antígenos (TRD), la reacción en cadena de la polimerasa (PCR) convencional (multiplex) y la PCR a tiempo real. Si están disponibles cualquiera de ellas nos pueden permitir el diagnóstico urgente, pero si el resultado se retrasa se debe iniciar un tratamiento empírico cuando la sospecha de malaria es alta o el paciente está grave.
En la práctica clínica actual deben utilizarse siempre los TRD combinados con la gota gruesa. Aunque el gold standard o patrón de referencia diagnóstica sigue siendo la gota gruesa, no es una técnica fiable como prueba única si el laboratorio que la realiza no tiene experiencia suficiente en el diagnóstico de la enfermedad. La extensión fina es una técnica asequible, con la ventaja de que la puede realizar un hematólogo de guardia, pero es menos sensible y solo sirve para confirmar el diagnóstico en casos de malaria con parasitemias superiores a 1.500trofozoítos por microlitro. En ningún caso una extensión fina negativa puede descartar una malaria.
Los TRD actuales constan de un antígeno palúdico común (LDH parasitaria o aldolasa) junto a otro específico de P.falciparum (HRPf) y pueden realizarse a la cabecera del enfermo con un entrenamiento mínimo. Actualmente existen en el mercado kits con sensibilidad y especificidad similares a la gota gruesa en manos expertas para el diagnóstico de infecciones por P.falciparum y P.vivax. Presentan el inconveniente del precio y, en el caso del HRPf, pueden permanecer positivos hasta 3-4 semanas después de un tratamiento eficaz. La sensibilidad es menor en las infecciones por P.malariae y P.ovale, y por este motivo no se recomienda su uso como técnica diagnóstica única en pacientes procedentes de zonas endémicas donde circulen estas especies. La OMS publica periódicamente una evaluación de los diferentes TRD comercializados19. Si solo se dispone de microscopía, y persiste un alto índice de sospecha de malaria, se recomienda repetir la gota gruesa hasta 3 veces en 48-72 horas o valorar iniciar un tratamiento empírico.
La PCR multiplex es la técnica más sensible y permite confirmar con seguridad la especie de Plasmodium, diagnosticar malarias submicroscópicas, infecciones mixtas y por P.knowlesi, que morfológicamente es muy similar a P.malariae20. Si el paciente proviene del sudeste asiático, la microscopia se suele informar como infección por P.knowlesi/malariae hasta su confirmación por PCR. También se debe recordar que geográficamente es infrecuente encontrar P.vivax en el África subsahariana, excepto en Etiopía, Sudán del Sur y Madagascar, y que P.ovale no existe en América.
Las malarias submicroscópicas de todas las especies son muy frecuentes en países endémicos21 y pueden representar hasta un tercio de los casos importados si se realiza la PCR sistemáticamente. La mayoría son individuos semiinmunes asintomáticos, pero se ven también en viajeros que han recibido profilaxis y pueden producir clínica o alteraciones analíticas11. Todos deben recibir tratamiento, especialmente niños y mujeres embarazadas.
TratamientoLas recomendaciones de tratamiento para la malaria importada en España8 se especifican en la tabla 2, con algunas modificaciones recientes de la Guía para el tratamiento de la malaria de la OMS10.
Recomendaciones para el tratamiento de la malaria importada en España
| Malaria por Plasmodium falciparum o Plasmodium spp. sin criterios de gravedad | |||
|---|---|---|---|
| Población | Línea | Fármaco y dosis | Comentarios |
| Adultos | Primera línea | Dihidroartemisinina-piperaquina (Eurartesim® 40mg/320mg) <75kg, 3 comp./día×3 días (total 9 comp.) 75-100kg, 4 comp./día×3 días (total 12 comp.) Atovacuona-proguanilo (Malarone® 250mg/100mg) 4 comp./día×3 días (total 12 comp.) Arteméter-lumefantrina (Riamet® o Coartem® 20mg/120mg) 4 comp. a las 0, 8, 24, 36, 48 y 60h (total 24 comp.) | Tomar en ayunas Tomar con comida rica en grasa Tomar con comida rica en grasa |
| Segunda línea | Sulfato de quinina (comp. 300-325mg) 2 comp./8h+doxiciclina 100mg/12h×7 días (total 56 comp.) | Tomar con comida, un vaso grande de agua (200ml) y sin tumbarse al menos en una hora | |
| Embarazadas Primer trimestre | Primera línea | Sulfato de quinina (comp. 300-325mg) 2 comp./8h+clindamicina oral 450mg/8h×7días | |
| Embarazadas Segundo y tercer trimestre | Primera línea | Arteméter-lumefantrina (Riamet® o Coartem® 20mg/120mg) 4 comp. a las 0, 8, 24, 36, 48 y 60h | Tomar con comida rica en grasa |
| Segunda línea | Sulfato de quinina (comp 300-325mg) 2 comp./8h+clindamicina oral 450mg/8h×7días | ||
| Niños | Primera línea | Dihidroartemisinina-piperaquina <25kg: >2,5mg/kg (DHA) y 20mg/kg (PQ)/24h×3días >25kg: 2,25mg/kg (DHA) y 18mg/kg (PQ)/24h×3días Atovacuona-proguanilo 5-8kg: 2 comp. pediátricos/día×3días 9-10kg: 3 comp. pediátricos/día×3días 11-20kg: 1 comp. adulto/día×3días 21-30kg: 2 comp adulto/día×3días 31-40kg: 3 comp. adulto/día×3días >40kg: 4 comp. adulto/día×3días (igual que en adultos) Arteméter-lumefantrina 1 comp./dosis (<15kg; <3años) 2 comp./dosis (15-24kg; 3-8años) 3 comp./dosis (25-34kg; 9-14años) 4 comp./dosis (>34kg=adultos) En 6 dosis a las 0, 8, 24, 36, 48 y 60h | Coformulado en comprimidos de dihidroartemisinina-piperaquina (DHA/PQ) 20/160 o 40/320mg Comp. pediátrico: atovacuona 62,5mg; proguanilo 25mg Comp. adulto: 250mg atovacuona; 100mg proguanilo No recomendado en niños con menos de 5kg de peso Co-formulado en comprimidos de arteméter 20mg y lumefantrina 120mg. Existe una formulación pediátrica soluble. Administrar preferiblemente con comida grasa |
| Segunda línea | Sulfato de quinina 10mg sal/kg/8h + clindamicina 25-40mg/kg/día en 3-4 dosis×7días | Sulfato de quinina cápsulas de 300-325mg de sal | |
| Malaria por Plasmodium vivax, P. ovale, P. malariae o P. knowlesi sin criterios de gravedad | |||
|---|---|---|---|
| Se pueden utilizar las mismas recomendaciones que para la malaria por P. falciparum no complicado con estas diferencias: • En embarazadas no precisa añadir clindamicina al tratamiento con sulfato de quinina • En P. vivax y P. ovale añadir siempre primaquina si no hay contraindicación | |||
| Adultos | Primera línea | Cloroquina (Resochin® 250mg) o hidroxicloroquina (Dolquine® 200mg) 4 comp.+4 comp. a las 24h+2 comp. a las 48h (4+4+2=10 comp.) Si P. vivax: añadir siempre primaquinaa (Primaquine® 7,5mg base) 30mg base=4 comp./día×2sem. Si P. ovale: añadir siempre primaquinaa (Primaquine® 7,5mg base) 15mg base=2 comp./día×2sem. | P. vivax con alto nivel de resistencia a cloroquina en Papúa Nueva Guinea, Oceanía y zonas de Indonesia. En estos casos se tratará como P falciparum Bajo nivel de resistencia en algunas zonas de Etiopía, Madagascar, Centroamérica y Sudamérica donde es razonable usar cloroquina inicialmente. El resto se considera sensible a cloroquina. |
| Embarazo Todos los trimestres | Primera línea | Cloroquina (Resochin® 250mg) o hidroxicloroquina (Dolquine® 200mg) 4 comp.+4 comp. a las 24h+2 comp. a las 48h (4+4+2=10 comp.) | La primaquina está contraindicada en el embarazo por riesgo de anemia hemolítica. Para prevenir las recidivas se dará cloroquina oral, 2 comp. a la semana hasta el parto o final de lactancia |
| Embarazo Segundo y tercer trimestre | Segunda línea | Arteméter-Lumefantrina (Riamet® o Coartem® 20mg/120mg) 4 comp. a las 0, 8, 24, 36, 48 y 60h (total 24 comp.) | |
| Niños | Primera línea | 25mg/kg de cloroquina base repartida en 3 días (10mg/kg primera dosis seguida de 10mg/kg a las 24h y 5mg/kg a las 48h) Primaquinaa (Primaquine® 0,25 o 0,5mg/kg/día de base)×2 sem. | Cloroquina (Resochin® 250mg) 1comp.=155mg base No existe formulación pediátrica específica La primaquina está contraindicada en niños <6 meses y mujeres con lactancia de niños <6 meses |
| Malaria con criterios de gravedad | |||
|---|---|---|---|
| Adultos Embarazadas de cualquier trimestre | Primera línea | Artesunato i.v. 2,4mg/kg y repetir dosis a las 12h, 24h y cada 24h si es necesario hasta que se pueda iniciar el tratamiento oral. Se debe administrar un mínimo de 24h (3 dosis) | Siempre debe administrarse tratamiento secuencial tras la administración de artesunato o quinina i.v. con un ciclo completo de otro antimalárico (ver tratamiento de malaria no grave) |
| Adultos | Segunda línea | Quinina i.v. 20mg/kg dosis inicial a pasar en suero glucosado en 4h (dosis inicial de 10mg/kg si contraindicación), seguido de 10mg/kg en 4h cada 8h durante 7días, o hasta inicio del tratamiento oral. Se debe asociar doxiciclina i.v. 100mg/12h | |
| Embarazadas de cualquier trimestre | Segunda línea | Quinina i.v. 20mg/kg dosis inicial a pasar en suero glucosado en 4h, seguido de 10mg/kg en 4h cada 8h (máximo 1.800mg/día) asociado a clindamicina 10mg/kg/12h×7días | |
| Niños | Primera línea | Artesunato 2,4mg/kg (i.v o i.m) a las 0, 12, 24h, seguido de una dosis cada 24h hasta que sea posible pasar a vía oral. <20kg aumentar dosis de artesunato a 3mg/kg (i.v o i.m) | |
| Segunda línea | Quinina i.v. 10mg sal/kg/8h+clindamicina i.v. 25-40mg/kg/día en 3-4 dosis×7 días | ||
Medicación extranjera: Arteméter-lumefantrina, primaquina, artesunato i.v., quinina i.v.
La malaria es siempre una urgencia médica, y el retraso en el tratamiento es una de las principales causas de mortalidad17. Conviene tener acceso rápido al menos a las dosis iniciales de todos los antimaláricos recomendados, incluidos los medicamentos extranjeros. Como norma general se recomienda el ingreso del paciente, especialmente en infecciones por P.falciparum, aunque se puede realizar un tratamiento ambulatorio en centros con experiencia con criterios estrictos y un seguimiento adecuado22.
Tratamiento de malaria sin criterios de gravedadLos tratamientos disponibles poseen una eficacia superior al 90% y suelen ser bien tolerados. El tratamiento para P.falciparum se realiza por vía oral con combinaciones de 2 fármacos con diferente mecanismo de acción y vida media. Los recomendados a nivel mundial son los tratamientos combinados con artemisininas (TCA) durante 3días. El resto de especies de Plasmodium también son sensibles a los TCA, y se está planteando la posibilidad de unificar y simplificar el tratamiento de todos los Plasmodium con los TCA23. Un estudio reciente también ha demostrado las ventajas del TCA sobre la cloroquina en el tratamiento de P.knowlesi24. En el caso de que no sea posible identificar la especie de malaria, se debe tratar como si fuera P.falciparum, ya que es la más grave. En malarias importadas por P.falciparum se recomiendan los TCA o atovaquona-proguanilo, aunque este último no se debe usar en pacientes con hiperparasitemia10. Si el paciente ha tomado profilaxis de malaria, se debe tratar con un fármaco diferente.
En niños las medicaciones son las mismas que en adultos, ajustando la dosis al peso y sustituyendo la doxicilina por clindamicina en segunda línea. En las nuevas recomendaciones de la OMS se ha aumentado la dosis de dihidroartemisinina-piperaquina en niños con menos de 25kg, y se recomienda usar artemisininas también en niños que pesen menos de 5kg.
En el primer trimestre del embarazo, aunque cada vez hay más datos de seguridad sobre el uso de artemisininas, se sigue recomendando la combinación de quinina-clindamicina. En el segundo y tercer trimestres sería de elección artemeter-lumefantrina.
En malarias por Plasmodium no falciparum se sigue usando cloroquina, salvo en P.vivax de Papúa Nueva Guinea, Oceanía y zonas de Indonesia, donde presenta un alto nivel de resistencia a este fármaco, por lo que debe tratarse inicialmente como P.falciparum2. En P.vivax y P.ovale se debe añadir siempre primaquina como cura radical para eliminar los hipnozoítos hepáticos y evitar recidivas. La primaquina está contraindicada por riesgo de anemia hemolítica en el embarazo, en niños menores de 6 meses, madres con lactantes menores de 6 meses o en deficiencia grave de glucosa-6-fosfato deshidrogenasa (G6PDH), que se debe medir en sangre antes del tratamiento.
En infecciones mixtas se tratará como P.falciparum si incluye esta especie y con cloroquina si todas son sensibles, añadiendo primaquina si se identifica P.vivax o P.ovale.
Tratamiento de la malaria graveActualmente el artesunato intravenoso (i.v.) es el tratamiento de elección en la malaria grave en niños y adultos o cuando no se tolera la medicación vía oral. Aclara rápidamente la parasitemia y reduce la mortalidad un 25-40% comparado con la quinina i.v.10. La OMS ha introducido algunos cambios en el tratamiento con artesunato i.v. y recomienda aumentar la dosis —en malarias graves de niños con menos de 20kg— de 2,4 a 3mg/kg. Aunque su seguridad en el primer trimestre del embarazo no se ha establecido de manera firme, se considera que el beneficio demostrado compensa el riesgo potencial en el desarrollo del feto10.
En los últimos años se están describiendo casos de anemia hemolítica diferida a los 7-21días del tratamiento con artesunato i.v. hasta en un 27% de pacientes con malaria grave25. El beneficio clínico de este tratamiento parece compensar el riesgo de este efecto secundario. Se recomienda un seguimiento analítico semanal durante las primeras 4semanas, ya que algunos llegan a precisar transfusión sanguínea.
El tratamiento de soporte se debe realizar en una unidad de cuidados intensivos con las técnicas avanzadas y medicaciones indicadas según las complicaciones que presente el paciente. Se recomienda una cobertura antibiótica de amplio espectro y evitar la administración de un exceso de volumen por la gran facilidad de sufrir edema pulmonar por aumento de la permeabilidad vascular.
Resistencias a los antimaláricosA efectos prácticos, toda infección por P.falciparum se considera resistente a cloroquina, aunque mantiene la sensibilidad en América, al norte del canal de Panamá.
Actualmente se está vigilando e intentando frenar la expansión de resistencias a artemisininas detectadas en P.falciparum de Camboya, Laos, Myanmar, Tailandia y Vietnam. La resistencia está ligada a la mutación del gen K13 del parásito26, lo que supone un retraso de su aclaramiento en sangre, aunque de momento los TCA siguen siendo altamente eficaces en la zona. Por ahora no supone un problema en nuestro medio, ya que muy pocos pacientes provienen de esa región y contamos con medicaciones alternativas. En zonas fronterizas de estos mismos países asiáticos, P.falciparum también se considera resistente a mefloquina, dato importante de cara a la profilaxis.
Consejos al viajero. Prevención de la malariaAntes del viaje se debe realizar una consulta de consejos al viajero que incluye recomendaciones de seguridad, riesgos sanitarios, alimentación, vacunaciones o prevención de enfermedades transmitidas por picaduras de artrópodos, incluida la malaria. Para evitar contraer la malaria se recomienda la combinación de varias medidas personalizadas (A, B, C, D) según la salud previa del paciente, el destino y el tipo de viaje27:
- A.
Información del riesgo de malaria según la zona geográfica visitada, duración de la estancia, actividades realizadas o tipo de viaje. Se pueden consultar las zonas de riesgo y recomendaciones por países en documentos27 o páginas web (tabla 3).
Tabla 3.Páginas web con recomendaciones sobre malaria y viajes
http://www.cdc.gov/malaria/travelers/country_table/a.html
http://www.fitfortravel.nhs.uk/advice/malaria.aspx
http://www.msssi.gob.es/profesionales/saludPaises.do
http://www.who.int/malaria/travellers/es/
http://www.vacunasyviajes.es/vacunasyviajes/Malaria.html
http://www.viajarsano.com/home.html - B.
Prevención de la picadura del mosquito con repelentes (DEET con concentraciones superiores al 20% o icaridina), dormir bajo mosquitera con insecticida, vestimenta clara con mangas y pantalones largos y evitar el horario de mayor actividad del Anopheles al amanecer y al anochecer.
- C.
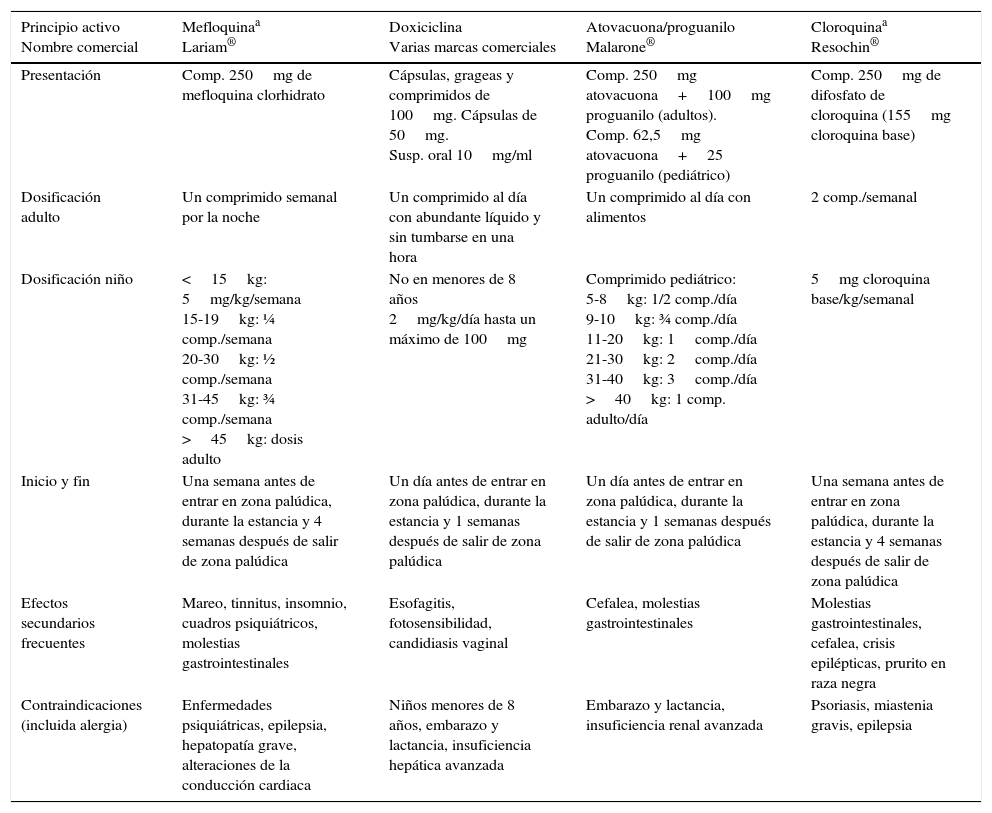
Quimioprofilaxis con fármacos sopesando beneficio-riesgo de efectos secundarios, alergias, enfermedades previas o coste económico. Se debe informar que es muy eficaz, pero nunca al 100%. Los más utilizados en adultos y niños se muestran en la tabla 4, con sus efectos secundarios más frecuentes y contraindicaciones.
Tabla 4.Fármacos recomendados para profilaxis de malaria en adultos y niños
Principio activo
Nombre comercialMefloquinaa
Lariam®Doxiciclina
Varias marcas comercialesAtovacuona/proguanilo
Malarone®Cloroquinaa
Resochin®Presentación Comp. 250mg de mefloquina clorhidrato Cápsulas, grageas y comprimidos de 100mg. Cápsulas de 50mg.
Susp. oral 10mg/mlComp. 250mg atovacuona+100mg proguanilo (adultos).
Comp. 62,5mg atovacuona+25 proguanilo (pediátrico)Comp. 250mg de difosfato de cloroquina (155mg cloroquina base) Dosificación adulto Un comprimido semanal por la noche Un comprimido al día con abundante líquido y sin tumbarse en una hora Un comprimido al día con alimentos 2 comp./semanal Dosificación niño <15kg: 5mg/kg/semana
15-19kg: ¼ comp./semana
20-30kg: ½ comp./semana
31-45kg: ¾ comp./semana
>45kg: dosis adultoNo en menores de 8 años
2mg/kg/día hasta un máximo de 100mgComprimido pediátrico:
5-8kg: 1/2 comp./día
9-10kg: ¾ comp./día
11-20kg: 1comp./día
21-30kg: 2comp./día
31-40kg: 3comp./día
>40kg: 1 comp. adulto/día5mg cloroquina base/kg/semanal Inicio y fin Una semana antes de entrar en zona palúdica, durante la estancia y 4 semanas después de salir de zona palúdica Un día antes de entrar en zona palúdica, durante la estancia y 1 semanas después de salir de zona palúdica Un día antes de entrar en zona palúdica, durante la estancia y 1 semanas después de salir de zona palúdica Una semana antes de entrar en zona palúdica, durante la estancia y 4 semanas después de salir de zona palúdica Efectos secundarios frecuentes Mareo, tinnitus, insomnio, cuadros psiquiátricos, molestias gastrointestinales Esofagitis, fotosensibilidad, candidiasis vaginal Cefalea, molestias gastrointestinales Molestias gastrointestinales, cefalea, crisis epilépticas, prurito en raza negra Contraindicaciones (incluida alergia) Enfermedades psiquiátricas, epilepsia, hepatopatía grave, alteraciones de la conducción cardiaca Niños menores de 8 años, embarazo y lactancia, insuficiencia hepática avanzada Embarazo y lactancia, insuficiencia renal avanzada Psoriasis, miastenia gravis, epilepsia - D.
Diagnóstico y tratamiento precoz acudiendo a un centro sanitario si se sospecha malaria.
En poblaciones especiales como largas estancias, inmunodeprimidos, embarazadas y lactantes, alergias o posibles interacciones medicamentosas, conviene remitir al paciente a un centro especializado. Actualmente no existen vacunas comercializadas frente a la malaria.
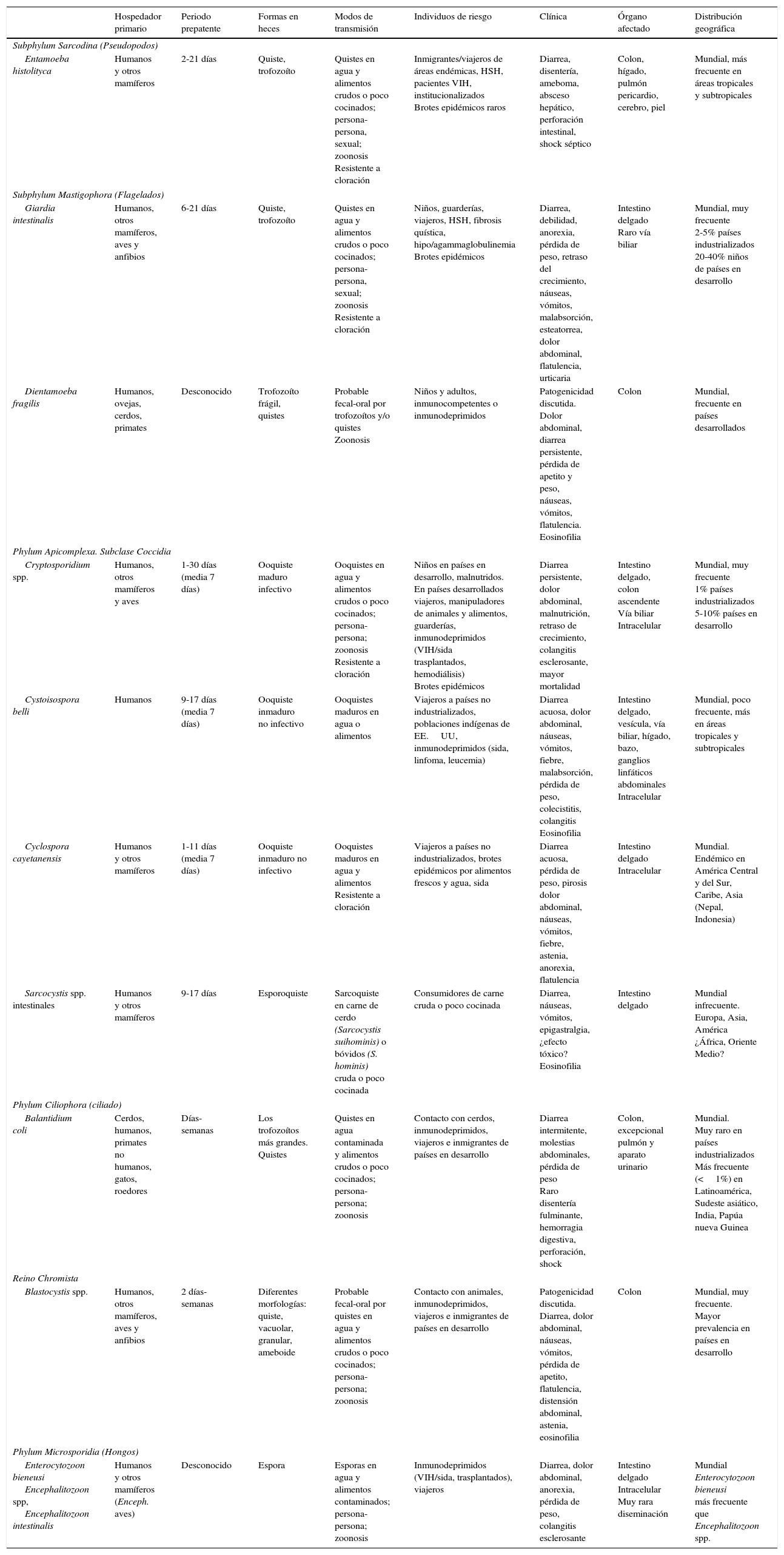
Protozoos intestinalesIntroducciónLas infecciones humanas por protozoos intestinales son de distribución mundial. En la tabla 5 se enumeran los patógenos más importantes con algunas de sus características. En el intestino humano también se pueden identificar múltiples protozoos no patógenos, como Entamoeba dispar, Entamoeba coli, Endolimax nana o Trichomonas hominis.
Características de los protozoos intestinales en humanos
| Hospedador primario | Periodo prepatente | Formas en heces | Modos de transmisión | Individuos de riesgo | Clínica | Órgano afectado | Distribución geográfica | |
|---|---|---|---|---|---|---|---|---|
| Subphylum Sarcodina (Pseudopodos) | ||||||||
| Entamoeba histolityca | Humanos y otros mamíferos | 2-21 días | Quiste, trofozoíto | Quistes en agua y alimentos crudos o poco cocinados; persona-persona, sexual; zoonosis Resistente a cloración | Inmigrantes/viajeros de áreas endémicas, HSH, pacientes VIH, institucionalizados Brotes epidémicos raros | Diarrea, disentería, ameboma, absceso hepático, perforación intestinal, shock séptico | Colon, hígado, pulmón pericardio, cerebro, piel | Mundial, más frecuente en áreas tropicales y subtropicales |
| Subphylum Mastigophora (Flagelados) | ||||||||
| Giardia intestinalis | Humanos, otros mamíferos, aves y anfibios | 6-21 días | Quiste, trofozoíto | Quistes en agua y alimentos crudos o poco cocinados; persona-persona, sexual; zoonosis Resistente a cloración | Niños, guarderías, viajeros, HSH, fibrosis quística, hipo/agammaglobulinemia Brotes epidémicos | Diarrea, debilidad, anorexia, pérdida de peso, retraso del crecimiento, náuseas, vómitos, malabsorción, esteatorrea, dolor abdominal, flatulencia, urticaria | Intestino delgado Raro vía biliar | Mundial, muy frecuente 2-5% países industrializados 20-40% niños de países en desarrollo |
| Dientamoeba fragilis | Humanos, ovejas, cerdos, primates | Desconocido | Trofozoíto frágil, quistes | Probable fecal-oral por trofozoítos y/o quistes Zoonosis | Niños y adultos, inmunocompetentes o inmunodeprimidos | Patogenicidad discutida. Dolor abdominal, diarrea persistente, pérdida de apetito y peso, náuseas, vómitos, flatulencia. Eosinofilia | Colon | Mundial, frecuente en países desarrollados |
| Phylum Apicomplexa. Subclase Coccidia | ||||||||
| Cryptosporidium spp. | Humanos, otros mamíferos y aves | 1-30 días (media 7 días) | Ooquiste maduro infectivo | Ooquistes en agua y alimentos crudos o poco cocinados; persona-persona; zoonosis Resistente a cloración | Niños en países en desarrollo, malnutridos. En países desarrollados viajeros, manipuladores de animales y alimentos, guarderías, inmunodeprimidos (VIH/sida trasplantados, hemodiálisis) Brotes epidémicos | Diarrea persistente, dolor abdominal, malnutrición, retraso de crecimiento, colangitis esclerosante, mayor mortalidad | Intestino delgado, colon ascendente Vía biliar Intracelular | Mundial, muy frecuente 1% países industrializados 5-10% países en desarrollo |
| Cystoisospora belli | Humanos | 9-17 días (media 7 días) | Ooquiste inmaduro no infectivo | Ooquistes maduros en agua o alimentos | Viajeros a países no industrializados, poblaciones indígenas de EE.UU, inmunodeprimidos (sida, linfoma, leucemia) | Diarrea acuosa, dolor abdominal, náuseas, vómitos, fiebre, malabsorción, pérdida de peso, colecistitis, colangitis Eosinofilia | Intestino delgado, vesícula, vía biliar, hígado, bazo, ganglios linfáticos abdominales Intracelular | Mundial, poco frecuente, más en áreas tropicales y subtropicales |
| Cyclospora cayetanensis | Humanos y otros mamíferos | 1-11 días (media 7 días) | Ooquiste inmaduro no infectivo | Ooquistes maduros en agua y alimentos Resistente a cloración | Viajeros a países no industrializados, brotes epidémicos por alimentos frescos y agua, sida | Diarrea acuosa, pérdida de peso, pirosis dolor abdominal, náuseas, vómitos, fiebre, astenia, anorexia, flatulencia | Intestino delgado Intracelular | Mundial. Endémico en América Central y del Sur, Caribe, Asia (Nepal, Indonesia) |
| Sarcocystis spp. intestinales | Humanos y otros mamíferos | 9-17 días | Esporoquiste | Sarcoquiste en carne de cerdo (Sarcocystis suihominis) o bóvidos (S. hominis) cruda o poco cocinada | Consumidores de carne cruda o poco cocinada | Diarrea, náuseas, vómitos, epigastralgia, ¿efecto tóxico? Eosinofilia | Intestino delgado | Mundial infrecuente. Europa, Asia, América ¿África, Oriente Medio? |
| Phylum Ciliophora (ciliado) | ||||||||
| Balantidium coli | Cerdos, humanos, primates no humanos, gatos, roedores | Días-semanas | Los trofozoítos más grandes. Quistes | Quistes en agua contaminada y alimentos crudos o poco cocinados; persona-persona; zoonosis | Contacto con cerdos, inmunodeprimidos, viajeros e inmigrantes de países en desarrollo | Diarrea intermitente, molestias abdominales, pérdida de peso Raro disentería fulminante, hemorragia digestiva, perforación, shock | Colon, excepcional pulmón y aparato urinario | Mundial. Muy raro en países industrializados Más frecuente (<1%) en Latinoamérica, Sudeste asiático, India, Papúa nueva Guinea |
| Reino Chromista | ||||||||
| Blastocystis spp. | Humanos, otros mamíferos, aves y anfibios | 2 días-semanas | Diferentes morfologías: quiste, vacuolar, granular, ameboide | Probable fecal-oral por quistes en agua y alimentos crudos o poco cocinados; persona-persona; zoonosis | Contacto con animales, inmunodeprimidos, viajeros e inmigrantes de países en desarrollo | Patogenicidad discutida. Diarrea, dolor abdominal, náuseas, vómitos, pérdida de apetito, flatulencia, distensión abdominal, astenia, eosinofilia | Colon | Mundial, muy frecuente. Mayor prevalencia en países en desarrollo |
| Phylum Microsporidia (Hongos) | ||||||||
| Enterocytozoon bieneusi Encephalitozoon spp, Encephalitozoon intestinalis | Humanos y otros mamíferos (Enceph. aves) | Desconocido | Espora | Esporas en agua y alimentos contaminados; persona-persona; zoonosis | Inmunodeprimidos (VIH/sida, trasplantados), viajeros | Diarrea, dolor abdominal, anorexia, pérdida de peso, colangitis esclerosante | Intestino delgado Intracelular Muy rara diseminación | Mundial Enterocytozoon bieneusi más frecuente que Encephalitozoon spp. |
HSH: hombres que tienen sexo con hombres; sida: síndrome de inmunodeficiencia humana adquirida; VIH virus de la inmunodeficiencia humana.
Los microsporidios se clasifican actualmente como hongos, y Blastocystis spp. no se considera como un protozoo estricto, incluyéndolo en el reino Chromista; sin embargo, permanecen dentro de esta revisión porque siguen compartiendo muchas características epidemiológicas y clínicas.
Todavía existen grandes lagunas en el conocimiento de los protozoos intestinales, pero los recientes estudios epidemiológicos, y el uso cada vez más frecuente de técnicas moleculares diagnósticas como la PCR, revelan un gran impacto sanitario global con una alta morbimortalidad no solo a nivel humano, sino también veterinario28,29. Se estima que Cryptosporidium spp. y Entamoeba histolytica causaron más de 155.000muertes y unos 10,6millones de años perdidos ajustados por discapacidad en el año 201030,31. En países de baja renta Cryptosporidium spp. afecta principalmente a niños, en los que justifica el 20% de las diarreas, provocando malnutrición, retraso del crecimiento y una mayor mortalidad, especialmente en menores de 2años, en los que es la segunda causa de diarrea moderada-grave detrás del rotavirus32.
Los protozoos intestinales más frecuentes a nivel mundial son Giardia intestinalis (también llamada Giardia lamblia o duodenalis), Cryptosporidium spp. y Entamoeba spp., que incluye E.histolytica, E.moshkovskii (produce colitis no invasiva) y la especie no patógena E.dispar, que son indistinguibles morfológicamente. En países de baja renta son los protozoos intestinales más frecuentes, y en EE.UU. son las 3 primeras causas de diarrea parasitaria. Junto con Dientamoeba fragilis, Blastocystis spp. y, en menor medida, Cyclospora cayetanensis son los protozoos más comunes en países desarrollados como el nuestro29.
Sin embargo, no existen datos fiables sobre su prevalencia en humanos, ni siquiera en países de renta alta. Esto se debe a varios factores, entre los que destaca que la mayoría de los humanos infectados por protozoos intestinales son portadores asintomáticos. En segundo lugar, muchos pacientes con clínica no acuden a una asistencia sanitaria porque sufren diarreas leves o autolimitadas. Finalmente, el diagnóstico de algunos protozoos requiere técnicas especiales que no se solicitan habitualmente y su sensibilidad suele ser baja33.
Su transmisión es fecal-oral, principalmente a través del agua o alimentos. Son microorganismos muy abundantes, ubicuos y la mayoría presentan formas quísticas o esporas muy resistentes en el medio ambiente. Se encuentran en aguas superficiales (ríos, lagos, manantiales, pozos, piscinas), agua potable, aguas residuales y alimentos contaminados por estas aguas, por abonos orgánicos o durante su manipulación. Los quistes de G.intestinalis, Cryptosporidium spp., Entamoeba spp. y C.cayetanensis son bastante resistentes a la cloración. Las esporas de los microsporidios y los quistes de G.intestinalis y Cryptosporidium spp. son muy pequeños (<30μm) y no se eliminan completamente con los filtros de potabilización habituales, por lo que podemos encontrarlos en aguas de consumo humano, incluso en países desarrollados29,34. Algunos protozoos también pueden transmitirse por contacto de persona a persona, por relación sexual anal-oral o como zoonosis por contacto con animales, incluidas las mascotas. Suelen tener una mayor prevalencia en países tropicales o subtropicales de baja renta, donde los sistemas de agua o saneamiento están menos desarrollados y el contacto con animales es más estrecho, especialmente en zonas rurales.
ClínicaLa mayoría de las infecciones son asintomáticas, aunque todas pueden producir clínica intestinal, principalmente diarrea aguda, que suele ser autolimitada por afectación del intestino delgado, del colon o de ambos. En ocasiones evolucionan a una diarrea prolongada o intermitente, a veces con sangre, como en la disentería por E.histolytica o Balantidium coli. Se puede acompañar de dolor abdominal, náuseas, vómitos, pirosis, tenesmo o flatulencia. En la práctica clínica resulta imposible realizar un diagnóstico etiológico solo por las características de la diarrea.
También pueden producir afectación sistémica con fiebre, malabsorción, retraso del crecimiento, mialgias, malestar general, astenia, anorexia y adelgazamiento. E.histolytica es invasiva y puede desencadenar una perforación de colon o producir abscesos hepáticos y en otros órganos.
El estado inmunitario y nutricional del paciente es muy importante de cara a las manifestaciones clínicas. Niños malnutridos o pacientes inmunodeprimidos sufren cuadros más prolongados, invasivos y con mayor morbimortalidad. En pacientes con VIH/sida, Cryptosporidium spp., C.cayetanensis, Cystoisospora belli o los microsporidios pueden producir diarreas fulminantes, adelgazamientos extremos o enfermedad invasiva, sobre todo de órganos abdominales.
Todavía se debate si Blastocystis spp. y D.fragilis producen enfermedad en humanos o son solo protozoos comensales. Aunque en la mayoría de los casos su aparición en heces no tiene significado clínico, cada vez hay más evidencia de que pueden ser patógenos y responder al tratamiento específico35,36. Algunos estudios parecen relacionarlos con el síndrome de colon irritable. Esta variedad clínica podría explicarse porque existen múltiples genotipos de Blastocystis spp. y D.fragilis con diferentes grados de virulencia para el ser humano. Esta diversidad genética, y probablemente de patogenicidad, también se está describiendo en otros protozoos como E.histolytica, G.intestinalis o Cryptosporidium spp., en lo que actualmente es un campo muy activo de investigación37,38.
Algunos protozoos también se están relacionando con manifestaciones extraintestinales como artritis reactivas, urticaria o astenia crónica. Finalmente, recordar que una vez erradicados del intestino humano pueden persistir la diarrea o las molestias abdominales por un déficit de lactasa secundario a atrofia de microvellosidades, diferentes grados de malabsorción o un síndrome de colon irritable postinfeccioso.
Los protozoos no suelen producir eosinofilia en sangre periférica como los helmintos; sin embargo, puede aparecer en el caso de D.fragilis, Sarcocystis spp., C.belli y Blastocystis spp.
Epidemiología en países industrializadosExisten diferencias en la epidemiología y morbimortalidad entre países de alta y baja renta. En países industrializados como el nuestro pueden ser importados o autóctonos. Aparecen como casos esporádicos o en brotes epidémicos y afectan especialmente a determinados pacientes de riesgo, en los que se recomienda la realización de pruebas diagnósticas específicas en caso de diarrea persistente o absceso hepático.
Protozoos importados- 1.
En la diarrea del viajero la etiología diagnosticada más común sigue siendo la bacteriana, seguida de protozoos y virus39. El protozoo más frecuente es G.intestinalis, sobre todo en visitantes de India, Tailandia, Nepal o Ghana. La amebiasis es más frecuente en viajeros procedentes de India, Indonesia, México y Tailandia40. Conviene recordar que en zonas endémicas de E.histolytica en América Central y Sudamérica, África, Sudeste asiático y el subcontinente indio, hasta el 80% de los infectados son portadores asintomáticos. C.cayetanensis se puede ver en brotes epidémicos de viajeros a Centroamérica, Caribe, Perú, Indonesia, Nepal y México41. En nuestro medio C.cayetanensis y E.histolytica prácticamente solo se aíslan en viajeros a zonas endémicas. La criptosporidiasis es poco frecuente en viajes.
- 2.
En niños adoptados o inmigrantes de países endémicos se recomienda un cribado de parásitos intestinales. Aunque la mayoría se encuentran asintomáticos, se aíslan con frecuencia G.intestinalis, Blastocystis spp., D.fragilis, Cryptosporidium spp. y E.histolytica42,43. Es un reflejo de la alta prevalencia en sus lugares de origen, donde además los niños suelen estar institucionalizados, lo que aumenta el riesgo.
- 3.
Los alimentos frescos importados pueden producir brotes epidémicos como los descritos en EE.UU. o Canadá por frambuesas, albahaca, cilantro o lechuga contaminados con C.cayetanensis44.
En países desarrollados son poco frecuentes los casos autóctonos de infección humana por C.cayetanensis o E.histolytica y excepcionales por B.coli, aunque es muy prevalente en cerdos.
- 1.
En España, Cryptosporidium spp. y G.intestinalis se detectan con más frecuencia en niños menores de 10años45. En países industrializados, la giardiasis es la segunda causa de diarrea en niños menores de 5años, después del rotavirus. Los que asisten a guarderías tienen un mayor riesgo de infección. Respecto a Cryptosporidium spp., se calcula que en EE.UU., y probablemente en nuestro medio, solo se diagnostica el 1% de los casos. Recientemente, la criptosporidiasis y la giardiasis se han incluido dentro de las enfermedades de declaración obligatoria en España con el fin de mejorar su notificación y control7. Sin embargo, no se incluye la amebiasis, de la que se han descrito algunos casos autóctonos en España46. En países desarrollados la especie no patógena E.dispar es 10 veces más prevalente que E.histolytica, y en países de baja renta la relación es aproximadamente 1:1, por lo que es importante contar con técnicas diagnósticas que las diferencien, como la detección de antígenos o la PCR.
- 2.
E.histolytica y G.intestinalis también pueden considerarse enfermedades de transmisión sexual y son más prevalentes en varones homosexuales o en prácticas sexuales que incluyan contacto oral-anal como factor de riesgo.
- 3.
Los pacientes inmunodeprimidos con infección por VIH/sida, trasplantados, tratados con quimioterapia o inmunosupresores, en hemodiálisis o con inmunodeficiencias congénitas son más susceptibles a presentar diarreas prolongadas y graves por protozoos intestinales. Cryptosporidium está presente en el 24% de los enfermos con diarrea y VIH a nivel mundial. La enfermedad grave por microsporidios y C.belli es casi exclusiva de pacientes inmunodeprimidos, y la giardiasis es más frecuente en individuos con déficit de inmunoglobulinas o fibrosis quística.
- 4.
La mayoría de estos protozoos son zoonosis y pueden transmitirse a través del contacto con animales, incluidas las mascotas domésticas. Por eso es muy importante la higiene en el contacto o manipulación de animales.
- 5.
Aunque la mayoría de los casos clínicos son esporádicos, Cryptosporidium spp., G.intestinalis y en menor medida C.cayetanensis producen brotes epidémicos por agua de consumo o de baño. También se han descrito brotes por E.histolytica en países en desarrollo. Estos 4 protozoos son los más resistentes a métodos de potabilización como la cloración.
El examen microscópico parasitológico (EMP) continúa siendo el pilar fundamental del diagnóstico de las protozoosis intestinales. A pesar del desarrollo reciente de diferentes técnicas de detección de antígenos y moleculares, el EMP es la única herramienta diagnóstica disponible hoy en día en la mayoría de los laboratorios de microbiología, aunque tiene una sensibilidad limitada y muy variable (20-90%) que depende del método de concentración utilizado y del número de muestras procesadas33. La estrategia tradicional de pedir 3 muestras separadas en el tiempo para completar el EMP se está revisando en algunos centros aplicando diferentes opciones, como el pooling de muestras, el procesamiento inicial de una sola muestra y pedir otras 2 si persisten los síntomas o la sustitución del EMP por métodos de PCR multiplex que presentan una sensibilidad incluso superior (hasta en un 14%) procesando una sola muestra en comparación con la microscopia de 3 muestras47. En ocasiones es preciso realizar técnicas invasivas para obtener una muestra diagnóstica, como la biopsia/aspirado duodenal y de colon o el aspirado de abscesos hepáticos.
Otro problema de la microscopia es que requiere personal de laboratorio bien formado para el diagnóstico morfológico, especialmente si no se realizan tinciones permanentes como el tricrómico, un procedimiento laborioso que habitualmente se utiliza solo en laboratorios de referencia de parasitología. Además, en los países de renta alta la menor prevalencia de protozoosis intestinales dificulta la formación del personal técnico de laboratorio, que paulatinamente va perdiendo la capacidad de reconocimiento morfológico33.
Detección de antígenosLa detección de antígenos mejora la sensibilidad diagnóstica, permite trabajar con muestras frescas sin conservantes y elimina el factor subjetivo de la microscopia. Es una técnica consolidada actualmente en el diagnóstico de la giardiasis y criptosporidiasis, aunque representa un coste añadido si se realiza como complemento de la microscopia. Para eliminar este problema, en algunos centros se aplican algoritmos que incluyen un cribado inicial con test antigénicos y el uso adicional de microscopia si existen factores de riesgo relacionados con otros protozoos intestinales para los que no existen test rápidos comerciales, como D.fragilis o algunos subtipos de Blastocystis. Actualmente existen varios test rápidos comerciales que detectan Giardia, Cryptosporidium y Entamoeba spp. o E.histolytica, por separado o en dispositivos combinados y utilizando diferentes técnicas (IFD, ELISA e ICT). Algunos de los test combinados disponibles se muestran en la tabla 6 con sensibilidades entre el 75 y el 99% según la técnica y el protozoo. De ellos, solo 2 detectan E.histolytica. El principal inconveniente de estos test es el precio y la necesidad de realizar también microscopia si se quieren descartar otras parasitosis, aunque podría ser una solución aceptable para sustituir la microscopia en el cribado inicial en centros sanitarios donde no se atienda regularmente a inmigrantes o viajeros.
Rentabilidad diagnóstica de los test rápidos combinados (Giardia-Cryptosporidium-Entamoeba)a
| Casa | Nombre | Test | Sensibilidad | Especificidad | Observaciones |
|---|---|---|---|---|---|
| Certest | CERTEST Crypto-Giardia Combo Card | ICT | >97%b | >99%b | Identifica Entamoeba spp. |
| Biopharma | RIDA®QUICK Cryptosporidium/Giardia/Entamoeba Combi | ICT | Cry 83%c Gia 92% Ent 85% | Cry 93%c Gia 99% Ent 87% | Identifica Entamoeba spp. |
| TechLab | TRI-COMBO PARASITE SCREEN | EIA | 97,8%d | 97,8%d | Identifica E. histolytica |
| Meridian | ImmunoCard STAT!® CGE | ICT | Cry 80%c Gia 92%c Ent 75%e | Cry 97%c Gia 99%c Ent 90%e | Identifica E. histolytica |
Por último, la serología sigue siendo importante como apoyo al diagnóstico de amebiasis, especialmente en viajeros.
Métodos molecularesEn los últimos años se han publicado numerosos estudios que analizan la prevalencia de las parasitosis intestinales con métodos moleculares muy sensibles. Actualmente se encuentran disponibles comercialmente algunos productos de PCR multiplex como el Luminex xTAG® Gastrointestinal Pathogen Panel (GPP), que permite detectar más de 15 microorganismos productores de diarrea, entre ellos G.intestinalis y E.histolytica39. Por otro lado, actualmente es posible también realizar análisis frente a múltiples patógenos directamente sobre muestras sin procesar con la nueva tecnología de microarrays (p.ej., Bio Fire Diagnostics Film Array), que incluye también otros parásitos menos comunes, como C.cayetanensis, un protozoo que puede identificarse gracias a que autofluoresce cuando se utiliza una luz ultravioleta a una longitud de onda determinada.
En algunos países europeos el cribado inicial de las muestras con PCR multiplex para Giardia y Cryptosporidium ha sustituido a la detección de antígenos y la microscopia como método diagnóstico inicial48. Este enfoque se irá imponiendo gradualmente según aparezcan nuevos kits comerciales más económicos, aunque es muy importante contar con laboratorios de referencia capaces de diagnosticar, mediante microscopia, serología y métodos moleculares, parásitos más raros o emergentes. Otro problema asociado al uso de técnicas moleculares es la imposibilidad de diagnosticar parasitosis no sospechadas clínicamente o no incluidas en panel comercial. Por todo ello es importante contar con una buena coordinación entre el laboratorio de microbiología y el clínico responsable del paciente48.
Prevención y controlEn el ámbito doméstico se recomienda mantener medidas de higiene muy eficaces, como el lavado de manos después de cuidar enfermos con diarrea, manipular objetos contaminados y animales o usar el servicio. Se debe extremar la limpieza de la ropa, el lavado de frutas y verduras frescas y consumir aguas potabilizadas adecuadamente. Las personas que trabajan en ambientes de alto riesgo como guarderías, residencias o manipuladores de alimentos deben tener especial cuidado con la higiene y no volver a trabajar hasta eliminar los protozoos. Niños o adultos con diarrea no deberían acudir a guarderías ni bañarse en piscinas o lugares de baño públicos. Se debe cuidar especialmente de las personas más susceptibles a las infecciones graves, como son los inmunodeprimidos, malnutridos o embarazadas. En las relaciones sexuales de riesgo con contacto oral-anal se recomiendan medidas de limpieza y protección. En hospitales se debe mantener una estricta higiene de heces o fómites y se recomienda aislamiento de contacto.
Desde el campo de la salud pública es esencial el control sanitario y la trazabilidad de toda la cadena alimentaria, desde el campo a la mesa. Se recomienda congelar las carnes o cocinarlas bien para evitar la sarcocistosis49 y otras infecciones. Las autoridades deben garantizar la potabilización del agua de consumo con la combinación de varios métodos de tratamiento químicos y físicos, así como una adecuada depuración de las aguas residuales y el tratamiento de los lodos. También se debe hacer un control de las aguas de baño, incluyendo piscinas, ríos o lagos29.
En los viajes, sobre todo a zonas menos desarrolladas, se debe seguir la máxima de comer alimentos bien cocinados, que se puedan pelar o, si no, evitarlos. La bebida debe ser embotellada y bien sellada, o infusiones con agua hervida.
Por último, se están investigando vacunas para los protozoos más patógenos, aunque no se esperan resultados a corto plazo.
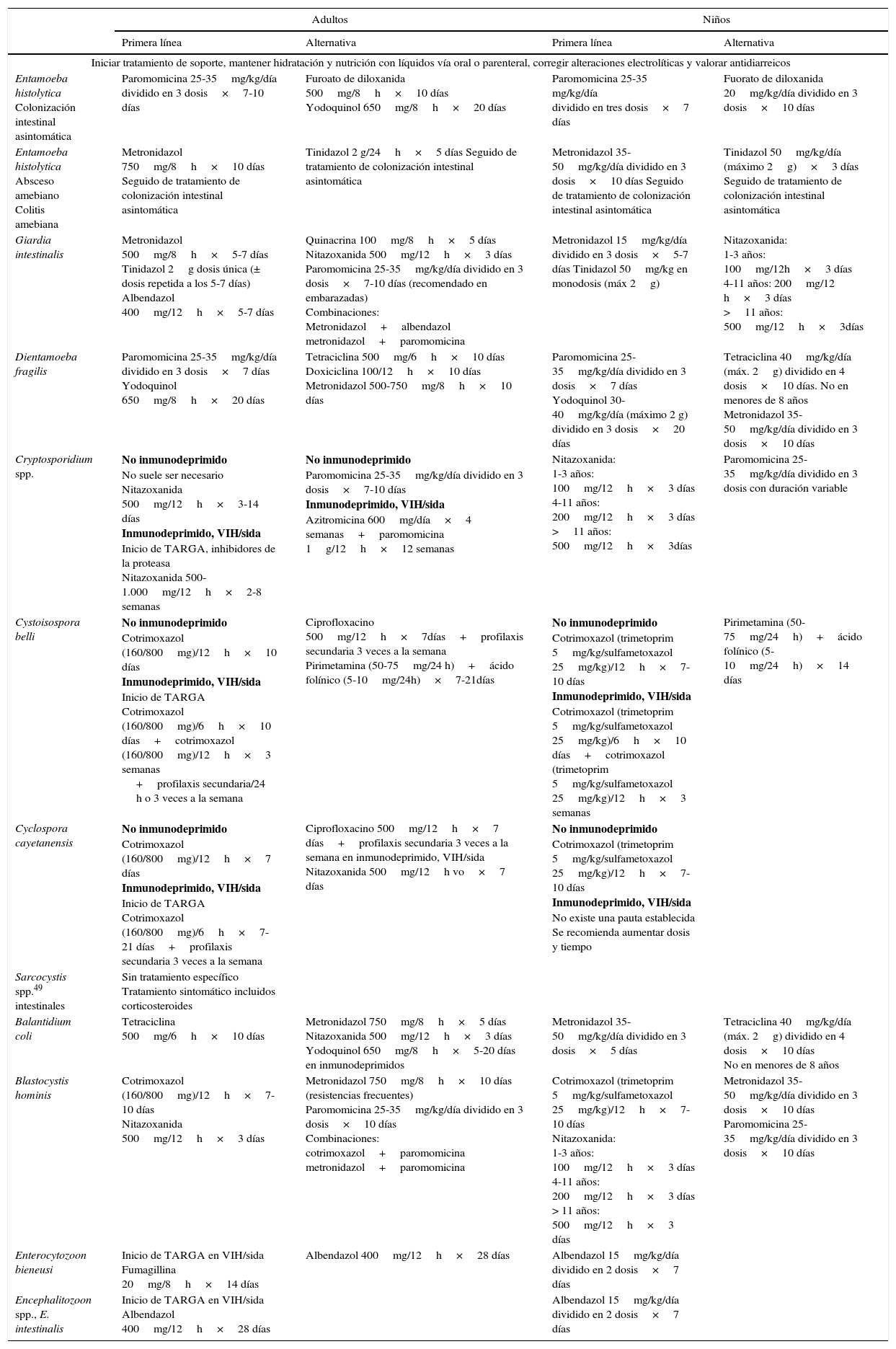
TratamientoLos tratamientos farmacológicos recomendados actualmente para los protozoos intestinales en niños y adultos se presentan en la tabla 7. El primer problema que surge es el criterio para iniciar un tratamiento, sobre todo en pacientes asintomáticos o con gérmenes de patogenicidad debatida, como D.fragilis o Blastocystis spp. En segundo lugar, la aparición cada vez más frecuente de resistencias a los tratamientos de primera línea como el metronidazol en G.intestinalis, sobre todo originarias de la India50, o Blastocystis spp35. Por último, existen pocos estudios de tratamiento para protozoos con diseños robustos y con un número suficiente de pacientes. En Cryptosporidium spp. y microsporidios, los tratamientos son poco eficaces o no claramente demostrados.
Tratamiento farmacológico de protozoos intestinales en adultos y niños
| Adultos | Niños | |||
|---|---|---|---|---|
| Primera línea | Alternativa | Primera línea | Alternativa | |
| Iniciar tratamiento de soporte, mantener hidratación y nutrición con líquidos vía oral o parenteral, corregir alteraciones electrolíticas y valorar antidiarreicos | ||||
| Entamoeba histolytica Colonización intestinal asintomática | Paromomicina 25-35mg/kg/día dividido en 3 dosis×7-10 días | Furoato de diloxanida 500mg/8h×10 días Yodoquinol 650mg/8h×20 días | Paromomicina 25-35 mg/kg/día dividido en tres dosis×7 días | Fuorato de diloxanida 20mg/kg/día dividido en 3 dosis×10 días |
| Entamoeba histolytica Absceso amebiano Colitis amebiana | Metronidazol 750mg/8h×10 días Seguido de tratamiento de colonización intestinal asintomática | Tinidazol 2 g/24h×5 días Seguido de tratamiento de colonización intestinal asintomática | Metronidazol 35-50mg/kg/día dividido en 3 dosis×10 días Seguido de tratamiento de colonización intestinal asintomática | Tinidazol 50mg/kg/día (máximo 2g)×3 días Seguido de tratamiento de colonización intestinal asintomática |
| Giardia intestinalis | Metronidazol 500mg/8h×5-7 días Tinidazol 2g dosis única (± dosis repetida a los 5-7 días) Albendazol 400mg/12h×5-7 días | Quinacrina 100mg/8h×5 días Nitazoxanida 500mg/12h×3 días Paromomicina 25-35mg/kg/día dividido en 3 dosis×7-10 días (recomendado en embarazadas) Combinaciones: Metronidazol+albendazol metronidazol+paromomicina | Metronidazol 15mg/kg/día dividido en 3 dosis×5-7 días Tinidazol 50mg/kg en monodosis (máx 2g) | Nitazoxanida: 1-3 años: 100mg/12h×3 días 4-11 años: 200mg/12 h×3 días >11 años: 500mg/12h×3días |
| Dientamoeba fragilis | Paromomicina 25-35mg/kg/día dividido en 3 dosis×7 días Yodoquinol 650mg/8h×20 días | Tetraciclina 500mg/6h×10 días Doxiciclina 100/12h×10 días Metronidazol 500-750mg/8h×10 días | Paromomicina 25-35mg/kg/día dividido en 3 dosis×7 días Yodoquinol 30-40mg/kg/día (máximo 2 g) dividido en 3 dosis×20 días | Tetraciclina 40mg/kg/día (máx. 2g) dividido en 4 dosis×10 días. No en menores de 8 años Metronidazol 35-50mg/kg/día dividido en 3 dosis×10 días |
| Cryptosporidium spp. | No inmunodeprimido No suele ser necesario Nitazoxanida 500mg/12h×3-14 días Inmunodeprimido, VIH/sida Inicio de TARGA, inhibidores de la proteasa Nitazoxanida 500-1.000mg/12h×2-8 semanas | No inmunodeprimido Paromomicina 25-35mg/kg/día dividido en 3 dosis×7-10 días Inmunodeprimido, VIH/sida Azitromicina 600mg/día×4 semanas+paromomicina 1g/12h×12 semanas | Nitazoxanida: 1-3 años: 100mg/12h×3 días 4-11 años: 200mg/12h×3 días >11 años: 500mg/12h×3días | Paromomicina 25-35mg/kg/día dividido en 3 dosis con duración variable |
| Cystoisospora belli | No inmunodeprimido Cotrimoxazol (160/800mg)/12h×10 días Inmunodeprimido, VIH/sida Inicio de TARGA Cotrimoxazol (160/800mg)/6h×10 días+cotrimoxazol (160/800mg)/12h×3 semanas +profilaxis secundaria/24 h o 3 veces a la semana | Ciprofloxacino 500mg/12h×7días+profilaxis secundaria 3 veces a la semana Pirimetamina (50-75mg/24 h)+ácido folínico (5-10mg/24h)×7-21días | No inmunodeprimido Cotrimoxazol (trimetoprim 5mg/kg/sulfametoxazol 25mg/kg)/12h×7-10 días Inmunodeprimido, VIH/sida Cotrimoxazol (trimetoprim 5mg/kg/sulfametoxazol 25mg/kg)/6h×10 días+cotrimoxazol (trimetoprim 5mg/kg/sulfametoxazol 25mg/kg)/12h×3 semanas | Pirimetamina (50-75mg/24h)+ácido folínico (5-10mg/24h)×14 días |
| Cyclospora cayetanensis | No inmunodeprimido Cotrimoxazol (160/800mg)/12h×7 días Inmunodeprimido, VIH/sida Inicio de TARGA Cotrimoxazol (160/800mg)/6h×7-21 días+profilaxis secundaria 3 veces a la semana | Ciprofloxacino 500mg/12h×7 días+profilaxis secundaria 3 veces a la semana en inmunodeprimido, VIH/sida Nitazoxanida 500mg/12h vo×7 días | No inmunodeprimido Cotrimoxazol (trimetoprim 5mg/kg/sulfametoxazol 25mg/kg)/12h×7-10 días Inmunodeprimido, VIH/sida No existe una pauta establecida Se recomienda aumentar dosis y tiempo | |
| Sarcocystis spp.49 intestinales | Sin tratamiento específico Tratamiento sintomático incluidos corticosteroides | |||
| Balantidium coli | Tetraciclina 500mg/6h×10 días | Metronidazol 750mg/8h×5 días Nitazoxanida 500mg/12h×3 días Yodoquinol 650mg/8h×5-20 días en inmunodeprimidos | Metronidazol 35-50mg/kg/día dividido en 3 dosis×5 días | Tetraciclina 40mg/kg/día (máx. 2g) dividido en 4 dosis×10 días No en menores de 8 años |
| Blastocystis hominis | Cotrimoxazol (160/800mg)/12h×7-10 días Nitazoxanida 500mg/12h×3 días | Metronidazol 750mg/8h×10 días (resistencias frecuentes) Paromomicina 25-35mg/kg/día dividido en 3 dosis×10 días Combinaciones: cotrimoxazol+paromomicina metronidazol+paromomicina | Cotrimoxazol (trimetoprim 5mg/kg/sulfametoxazol 25mg/kg)/12h×7-10 días Nitazoxanida: 1-3 años: 100mg/12h×3 días 4-11 años: 200mg/12h×3 días > 11 años: 500mg/12h×3 días | Metronidazol 35-50mg/kg/día dividido en 3 dosis×10 días Paromomicina 25-35mg/kg/día dividido en 3 dosis×10 días |
| Enterocytozoon bieneusi | Inicio de TARGA en VIH/sida Fumagillina 20mg/8h×14 días | Albendazol 400mg/12h×28 días | Albendazol 15mg/kg/día dividido en 2 dosis×7 días | |
| Encephalitozoon spp., E. intestinalis | Inicio de TARGA en VIH/sida Albendazol 400mg/12h×28 días | Albendazol 15mg/kg/día dividido en 2 dosis×7 días | ||
sida: síndrome de inmunodeficiencia humana adquirida; TARGA: tratamiento antirretroviral de gran actividad; VIH virus de la inmunodeficiencia humana.
Medicación extranjera: yodoquinol, quinacrina, fumagillina, nitazoxanida, furoato de diloxanida.
En nuestro medio todo paciente que presente síntomas relacionados con la infección debe recibir tratamiento. En el caso de D.fragilis o Blastocystis spp. también, si no existe otro germen que justifique la clínica35,36. Si presenta varios gérmenes patógenos en heces se deben tratar todos y cada uno de ellos al mismo tiempo o secuencialmente.
Actualmente no existen recomendaciones para el tratamiento de portadores asintomáticos en países de renta alta. Se debe valorar si existen factores de riesgo de enfermedad o la posibilidad de transmisión a otras personas, así como la eficacia y la toxicidad del tratamiento. Se debe ofrecer en:
- 1.
Riesgo de enfermedad invasiva por E.histolityca o B.coli.
- 2.
Pacientes inmunodeprimidos.
- 3.
Posibilidad de transmisión a pacientes inmunodeprimidos o colectivos como en el caso de guarderías, residencias o manipuladores de alimentos.
Los asintomáticos sin factores de riesgo no deberían recibir tratamiento ni en el caso de infecciones por D.fragilis, Blastocystis spp.
En pacientes inmunodeprimidos con VIH/sida es imprescindible iniciar precozmente el tratamiento con antirretrovirales (TARGA), especialmente en protozoos con tratamientos subóptimos como Cryptosporidium spp. y microsporidios. La mejoría de la inmunodepresión, por sí sola, supone en muchos casos la curación de la infección.
Siempre se debe instaurar un tratamiento de soporte manteniendo una buena hidratación vía oral o intravenosa, una adecuada nutrición y corregir los trastornos electrolíticos. Mantener la lactancia en el caso de los bebés es beneficioso porque aporta inmunoglobulinas IgA protectoras, nutrientes e hidratación.
Si el paciente mantiene una clínica gastrointestinal prolongada a pesar del tratamiento o presenta una recurrencia de los síntomas, puede deberse a varios factores:
- 1.
Resistencia a los fármacos pautados. Si se sospecha esta resistencia se puede ofrecer otro fármaco de una familia diferente, la misma medicación aumentando la dosis y/o duración o bien una combinación de 2 o más fármacos. La elección dependerá de la disponibilidad de los medicamentos, sus efectos secundarios y la situación clínica del paciente. En estos protozoos no es posible realizar pruebas de sensibilidad a los antibióticos de forma rutinaria.
- 2.
Inmunodepresión del paciente que reduce la posibilidad de curación como en VIH/sida, trasplantados o con tratamientos inmunosupresores. En la giardiasis conviene investigar si existe un déficit de inmunoglobulinas o fibrosis quística.
- 3.
Enfermedad intestinal no infecciosa. Algunos protozoos como Giardia pueden producir un déficit de lactasa en más del 20% de los pacientes que puede durar varios meses. En este caso se recomienda eliminar la leche de la dieta. También se puede prolongar la clínica por un síndrome de colon irritable postinfeccioso sin presencia del protozoo en el intestino. Solo precisa tratamiento sintomático.
- 4.
Reinfección que solo es posible si mantiene contacto con un foco infeccioso.
No existe consenso en recomendar un control microbiológico en heces después del tratamiento si desaparece la clínica. En nuestro medio parece razonable hacerlo en los grupos de riesgo citados anteriormente para detectar portadores asintomáticos.
En el absceso hepático por E.histolytica se recomienda el drenaje percutáneo con control radiológico cuando es mayor de 5cm, afecta al lóbulo hepático izquierdo o no responde al tratamiento farmacológico en 5-7días. También se puede añadir cloroquina al tratamiento y cobertura antibiótica de amplio espectro por la posibilidad de sobreinfección bacteriana. La cirugía se reserva para el caso de perforación colónica, que también puede suceder en la balantidiasis, o en abscesos amebianos complicados.
FinanciaciónEste artículo no ha precisado financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.