Ignatzschineria es una bacteria de reciente descripción que en raras ocasiones se ha asociado a infección en humanos. Presentamos el primer caso en España de sepsis por Ignatzschineria indica.
Se trata de un varón de 44 años, indigente, con historia de alcoholismo crónico, que acudió a urgencias de nuestro hospital por intenso dolor en las piernas y fiebre de 38,6°C. En la exploración presentaba ulceraciones superficiales sobre región tibial anterior de la pierna derecha, piel macerada con zonas necróticas y celulitis con pérdida de continuidad en surco interdigital entre el tercer y cuarto dedo del pie izquierdo, en el que se observó presencia de larvas. En la analítica destacaba leucocitosis de 16.400×109/l y PCR de 65mg/l. Una radiografía y un eco-doppler del miembro inferior derecho descartaron osteomielitis y trombosis venosa. Tras extraer hemocultivos y cultivos de exudados, ingresa con tratamiento con amoxicilina-clavulánico intravenoso y corticoide por el importante edema asociado.
Al tercer día se observó crecimiento de bacilos gramnegativos en una botella aerobia de hemocultivo. A las 24h crecieron en agar sangre colonias oxidasa y catalasa positivas. La identificación con tarjeta ID-GN del sistema Vitek®2 (bioMérieux) fue Acinetobacter lwoffii/Moraxella spp. Ante la duda entre las características fenotípicas y el resultado obtenido se envió la cepa al hospital de referencia para confirmación por espectrometría de masas, Bruker Microflex® LT MALDI-TOF MS (Bruker Daltonics), con el software Bruker Biotyper® 3.1 (Bruker Daltonics) y la base de datos Biotyper library v6.0 (6.903 entradas), identificándose como Ignatzschineria indica. Se confirmó por secuenciación del ARNr16S mediante ABI PRISM® 3130xl Genetic Analyzer (Applied Biosystems), usando las bases de datos leBIBIQBPP y GenBank (NCBI). En el exudado de las lesiones cutáneas se aisló Alcaligenes faecalis y Proteus hauseri, confirmados también por MALDI-TOF. No se detectó Ignatzschineria indica en los cultivos de exudados. La sensibilidad se realizó con la tarjeta AST/243. El aislado fue sensible a ampicilina (≤2μg/ml), amoxicilina/clavulánico (≤2μg/ml), cefotaxima (≤1μg/ml), ciprofloxacino (≤0,25μg/ml), gentamicina (≤1μg/ml), imipenem (≤0,25μg/ml), trimetoprim/sulfametoxazol (1/19μg/ml). Se mantuvo el tratamiento con amoxicilina-clavulánico durante 10 días, con buena evolución.
El género Ignatzschineria pertenece al grupo de las gammaproteobacterias. Fue descrito por primera vez en 2001 por Tóth et al.6,7 como Schineria en honor al entomólogo Ignatz Rudolph Schiner (1813-1873) que describió la mosca Wohlfahrtia magnifica en 1862. En 2007 se renombra Ignatzschineria. Existen 3 especies reconocidas: I. indica, I. larvae e I. ureiclastica. Las 3 se han aislado de la mosca Wohlfahrtia magnifica y se asocian a miasis o parasitación por larvas de mosca en animales y de forma excepcional en seres humanos. Estos microorganismos son bacilos gramnegativos aerobios no fermentadores de glucosa, no formadores de esporas, no hemolíticos, oxidasa, ureasa y catalasa positivos. Se han aislado en la porción anterior del tracto digestivo de las larvas.
Hasta septiembre de 2017 se publicaron en PubMed 6 casos de bacteriemias por Ignatzschineria spp. (tabla 1). Todos mencionan heridas mal cuidadas con presencia de larvas como fuente probable de bacteriemia: 3 casos en Francia (Maurin et al.4, 2007; Roudiere et al.5, 2007, y Le Brun et al.2, 2015); 2 en Estados Unidos (Barker et al.3, 2014) y uno en los Países Bajos (Heddema et al.1, 2016). Los casos descritos tratados con beta-lactámicos evolucionaron favorablemente, salvo un paciente que fue hallado inconsciente y que fue éxitus (Le Brun et al.2, 2015). En 2 pacientes no se comenta la evolución (Barker et al.3, 2014). Las cepas fueron sensibles a beta-lactámicos, quinolonas y aminoglucósidos, con variabilidad de los antibióticos testados, ya que no hay un antibiograma estandarizado, ni puntos de corte.
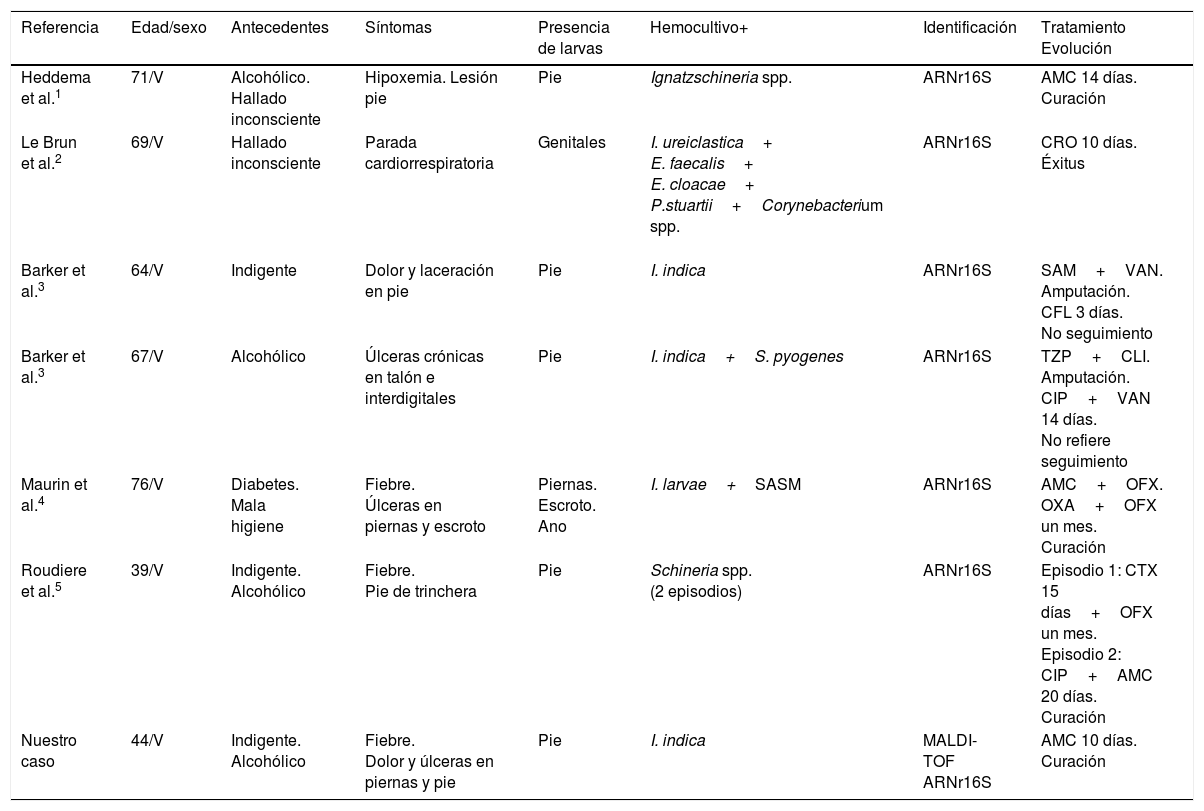
Casos descritos de sepsis por Ignatzschineria spp
| Referencia | Edad/sexo | Antecedentes | Síntomas | Presencia de larvas | Hemocultivo+ | Identificación | Tratamiento Evolución |
|---|---|---|---|---|---|---|---|
| Heddema et al.1 | 71/V | Alcohólico. Hallado inconsciente | Hipoxemia. Lesión pie | Pie | Ignatzschineria spp. | ARNr16S | AMC 14 días. Curación |
| Le Brun et al.2 | 69/V | Hallado inconsciente | Parada cardiorrespiratoria | Genitales | I. ureiclastica+ E. faecalis+ E. cloacae+ P.stuartii+Corynebacterium spp. | ARNr16S | CRO 10 días. Éxitus |
| Barker et al.3 | 64/V | Indigente | Dolor y laceración en pie | Pie | I. indica | ARNr16S | SAM+VAN. Amputación. CFL 3 días. No seguimiento |
| Barker et al.3 | 67/V | Alcohólico | Úlceras crónicas en talón e interdigitales | Pie | I. indica+S. pyogenes | ARNr16S | TZP+CLI. Amputación. CIP+VAN 14 días. No refiere seguimiento |
| Maurin et al.4 | 76/V | Diabetes. Mala higiene | Fiebre. Úlceras en piernas y escroto | Piernas. Escroto. Ano | I. larvae+SASM | ARNr16S | AMC+OFX. OXA+OFX un mes. Curación |
| Roudiere et al.5 | 39/V | Indigente. Alcohólico | Fiebre. Pie de trinchera | Pie | Schineria spp. (2 episodios) | ARNr16S | Episodio 1: CTX 15 días+OFX un mes. Episodio 2: CIP+AMC 20 días. Curación |
| Nuestro caso | 44/V | Indigente. Alcohólico | Fiebre. Dolor y úlceras en piernas y pie | Pie | I. indica | MALDI-TOF ARNr16S | AMC 10 días. Curación |
AMC: amoxicilina/clavulánico: CFL: cefalexina; CIP: ciprofloxacino; CLI: clindamicina; CRO: ceftriaxona; CTX: cefotaxima; OFX: ofloxacino; OXA: oxacilina; SAM: ampicilina-sulbactam; SASM: Staphylococcus aureus sensible a la meticilina; TZP: piperacilina-tazobactam; V: varón; VAN: vancomicina.
El nuestro es el primer caso descrito en España y el primero identificado mediante MALDI-TOF, ya que el único caso en el que se comenta su realización, no se llegó a ninguna identificación concluyente (Heddema et al.1, 2016). Destacamos la dificultad para su identificación por los métodos microbiológicos habituales, por lo que se debe tener en cuenta el aislamiento de bacilos gramnegativos en hemocultivos en pacientes con miasis y malas condiciones sociales (alcoholismo crónico, déficit de higiene, indigencia) que podrían pertenecen al género Ignatzschineria. Ante un paciente con cualquiera de los factores de riesgo citados se precisa la identificación por espectrometría de masas MALDI-TOF o amplificación y secuenciación del ARNr16S.