Introducción
En la década de los años ochenta del siglo xx se describió la relación entre la infección por el virus del papiloma humano (VPH) y el cáncer de cuello uterino 1. A mediados de los años noventa del siglo pasado, se estableció que la causa del cáncer cervical de células escamosas es el VPH 2,3, y más recientemente se señalaron los genotipos del VPH que están relacionados con los carcinomas de células escamosas 4.
Los VPH infectan selectivamente el epitelio de la piel y las mucosas. Estas infecciones pueden ser asintomáticas, pueden producir lesiones benignas, como las verrugas vulgares, o asociarse a diversas neoplasias, benignas o malignas.
Los VPH pertenecen al género Papilomavirus de la familia Popavaviridae. Son virus sin cubierta de 55 nm de diámetro, con cápsides icosaédricas, y con un genoma de ADN circular bicatenario de 7.900 pares de bases. La organización del genoma de todos los VPH es similar, consta de una región temprana (E, de early), una región tardía (L, de late) y una región larga de control (LCR, long control region). El gen L1 codifica la proteína principal de la cápside y el gen L2, una proteína secundaria. Otras proteínas codificadas por los genes del virus son las proteínas E1 y E2 que regulan la replicación del ADN viral y la propia expresión de los genes, y las proteínas E6 y E7 que interfieren con las proteínas celulares supresoras de tumores.
Los VPH son específicos de especie y no se propagan en cultivos de tejidos ni en animales de experimentación. Por otro lado, se han asociado genotipos concretos a manifestaciones clínicas específicas. Estos virus se clasifican por su localización en cutáneos o mucosos; o por su riesgo oncogénico en bajo, medio o alto grado. En la actualidad, se han identificado más de 100 genotipos del VPH, de los cuales 40 genotipos pueden infectar al ser humano por vía sexual mediante contacto directo con lesiones infectadas.
Virus del papiloma humano y cérvix (cuello uterino)
Existen 2 enfermedades cervicales relacionadas con el VPH: los condilomas acuminados y el cáncer de cuello uterino (también llamado cáncer de cérvix o cervical). Dentro de los cánceres de cuello uterino, los carcinomas de células escamosas comprenden entre el 85 y el 90% de éstos, mientras que el resto son adenocarcinomas. Si el cáncer tiene características de ambos tipos se conoce como carcinoma mixto.
Casi el 100% de los carcinomas escamosos contienen el ADN de VPH 2. El 87% de éstos es causado por 7 genotipos del VPH 5-7, y los más frecuentes son los genotipos de alto riesgo oncogénico 16, 18 y 31 3. La infección por el VPH genotipo 18 está asociado al carcinoma escamoso cervical y la infección por el genotipo 16 al adenocarcinoma cervical. Asimismo, la infección por este genotipo (VPH-16) se asocia con un aumento en el riesgo de desarrollar un cáncer invasivo.
Previo a la aparición de cáncer, el VPH causa alteraciones celulares muy superficiales, sin invasión, cuyos hallazgos citológicos se denominan lesiones escamosas intraepiteliales (SIL, por sus siglas en inglés squamous intraepithelial lesion) y los hallazgos histológicos, neoplasia intraepitelial cervical (CIN, por sus siglas en inglés cervical intraepithelial neoplasia). Las anormalidades celulares preneoplásicas observadas en el extendido citológico se catalogan de manera binaria como lesiones intraepiteliales escamosas de alto o bajo grado, mientras que la neoplasia intraepitelial se clasifica por sus 3 grados progresivos de displasia (CIN 1: leve, CIN 2: moderada y CIN 3: intensa). Estas lesiones pueden curar o progresar a cáncer. No se conoce con exactitud el mecanismo por el cual unas veces las lesiones desaparecen y otras avanzan. No obstante, la mayoría de mujeres negativas al virus de la inmunodeficiencia humana (VIH) se recuperan sin tratamiento dentro de los 6-12 meses de la infección sin más consecuencias para su salud. No se sabe por qué algunas mujeres con la infección por el VPH presentan cambios celulares precancerosos o incluso cáncer. Aunque muchas mujeres desarrollan inmunidad natural contra diferentes tipos del VPH, todavía no se sabe bien cuál es el papel que desarrolla esta inmunidad.
En la mujer, el cáncer de cuello uterino es la segunda causa de muerte por cáncer en el mundo después del cáncer de mama. En 1993, el cáncer de cérvix fue la neoplasia más frecuente entre las mujeres con sida. Desde entonces los Centers for Diseases Control and Prevention (http://www.cdc.gov/) estadounidenses añadieron el cáncer invasivo de cuello uterino como criterio definitorio de sida, y la displasia de alto grado dentro de la categoría B 8.
Factores de riesgo relacionados con el desarrollo de SIL/CIN
En los primeros años de la epidemia del VIH se describió una alta prevalencia de infección por el VPH entre las pacientes VIH+*9. Estudios observacionales demostraron una relación entre la coinfección VIH/VPH y la aparición de CIN 10,11. En la actualidad, las mujeres VIH+ tienen una mayor prevalencia de CIN, respecto a las mujeres VIH (7 frente a 1%) 10. Esta mayor prevalencia de CIN se ha relacionado con una alta prevalencia de la infección por el VPH por los genotipos de alto riesgo oncogénico 16 y 18, y con una mayor carga viral de VPH en la misma lesión.
La incidencia de SIL de alto grado (HSIL) en mujeres VIH+ está en relación con su estado inmunitario, es decir, con las cifras de CD4. En mujeres VIH+ con una citología basal normal y ausencia de infección por el VPH (VPH ADN negativo), se ha estimado una incidencia de SIL a los 2 años del 9% con cifras de CD4 < 500 × μl (incidencia que no varía con cifras menores de 200 CD4 × μl) y del 4% con cifras de CD4 > 500 × μl (incidencia similar a la encontrada en mujeres VIH) 12. Asimismo, las mujeres VIH+ respecto a las mujeres VIH cursan con una progresión más rápida a HSIL una vez diagnosticadas de una alteración citológica cervical 13.
Además de la propia infección por el VPH y de la persistencia de esta infección (probablemente como resultado del contacto sexual sin protección), otros factores de riesgo también han sido relacionados con el desarrollo de SIL/CIN 10,11,14:
La inmunodepresión: secundaria al VIH con cifras de linfocitos CD4 inferiores a 200 × μl, o secundaria a un transplante, o a cualquier proceso que pueda debilitar el sistema inmunitario.
La promiscuidad: de las propias pacientes o bien de sus parejas sexuales.
El tabaquismo: las mujeres fumadoras tienen casi el doble de probabilidades de desarrollar cáncer cervical que las no fumadoras.
La edad: el riesgo de cáncer de cuello uterino aumenta en los últimos años de la adolescencia y a partir de los 35 años de edad, aunque se puede presentar a cualquier edad.
La iniciación en la vida sexual a edad temprana: tener relaciones sexuales antes de los 18 años de edad aumenta el riesgo de enfermedad cervical.
La alta paridad: a mayor número de hijos mayor riesgo.
El uso de anticonceptivos orales durante largo tiempo.
Pruebas diagnósticas/pruebas de cribado de enfermedad cervical
Citología
No hay duda de que la citología convencional (prueba de Papanicolaou) es la prueba de cribado (screening) que ha contribuido de manera espectacular a la reducción de la incidencia y mortalidad por cáncer cervical.
El resultado de la citología es la primera información de que dispone el clínico sobre la posible enfermedad cervical. Esta prueba de cribado basada en los cambios citopatológicos no es la prueba diagnóstica de referencia para determinar la infección por el VPH. Aunque la citología es una prueba diagnóstica barata, presenta una serie de limitaciones, como son la importante variabilidad interobservador 15, una sensibilidad baja 16,17 y una serie de anomalías de significado incierto (ASCUS, células escamosas atípicas de significado indeterminado) que incluso citopatólogos expertos son incapaces de clasificar como alteraciones reactivas o lesiones premalignas 18,19.
La citología en medio líquido es más cara que la citología convencional, pero tiene la ventaja de permitir completar el diagnóstico mediante técnicas complementarias con una única muestra.
Histología (biopsia)
La información anatomopatológica, obtenida de biopsia dirigida por colposcopia y tinción con acético al 3%, es el método de referencia de la enfermedad cervical. En todos los casos en que se diagnostique una citología patológica o anormal, la información citológica se tendría que complementar con la información histopatológica (biopsia).
Técnicas moleculares
En la actualidad disponemos de 3 pruebas diagnósticas basadas en técnicas moleculares: la captura híbrida, la reacción en cadena de la polimerasa (PCR) y la PCR a tiempo real.
La captura híbrida es una prueba de cribado que permite detectar la presencia del VPH de alto y/o bajo grado oncogénico, pero no identifica el tipo de VPH. Esta prueba de cribado está aprobada por la Food and Drug Administration estadounidense.
En un trabajo reciente de nuestro grupo 20, realizado en mujeres VIH+ no tratadas previamente con tratamiento antirretroviral de gran actividad (TARGA), se estudió la prevalencia de infección cervical por el VPH mediante captura híbrida de segunda generación y mediante los cambios citológicos/histológicos indicativos de infección por el VPH. La prevalencia de infección por el VPH basada en la captura híbrida fue del 49%, y la prevalencia de infección por genotipos de alto riesgo oncogénico del 46%, mientras que la prevalencia basada en los cambios citológicos/histológicos indicativos de infección por el VPH fue del 36%. La sensibilidad, especificidad y los valores predictivos positivo y negativo de la captura híbrida respecto a los cambios citológicos/histológicos indicativos de infección por el VPH fue del 78, 69, 61 y 83%, respectivamente.
La PCR es otra prueba de laboratorio utilizada para la identificación del VPH. Es una técnica muy sensible que informa del genotipo de VPH. La PCR a tiempo real permite cuantificar la carga viral en la lesión.
Prevención/tratamiento
En la actualidad, el mejor tratamiento de la infección por el VPH es la prevención. Por tanto, el control ginecológico periódico, especialmente en la población de mujeres VIH+, es muy importante. Es esencial como parte del examen ginecológico practicar una inspección externa y la biopsia de toda lesión sospechosa, ya que la neoplasia vulvar intraepitelial también es más prevalente entre las mujeres VIH+21.
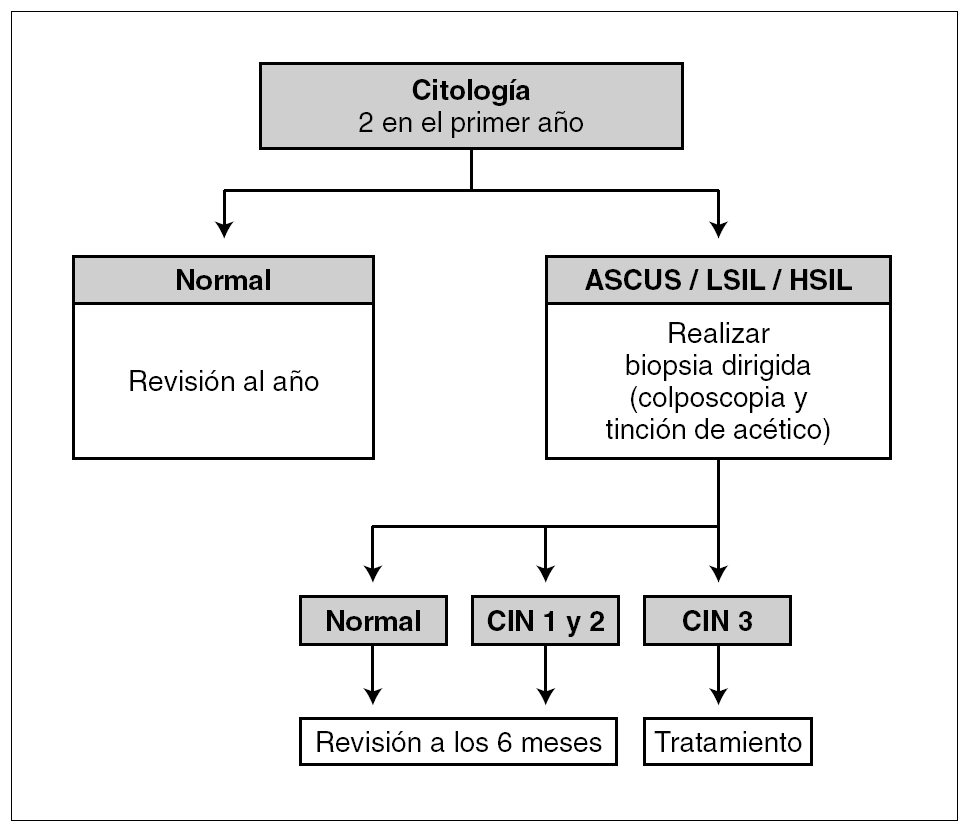
A toda mujer VIH+ se le debería practicar una citología cada 6 meses en el primer año del diagnóstico de la infección por el VIH y, si es normal, una cada año. Si la citología es anormal (ASCUS, LSIL o HSIL), se debería practicar una colposcopia y biopsia de las lesiones. El uso combinado de la citología cervical y las técnicas moleculares en una población de riesgo, como es la infectada por el VIH, puede ayudar a aumentar la eficacia del cribado de la enfermedad cervical por el VPH.
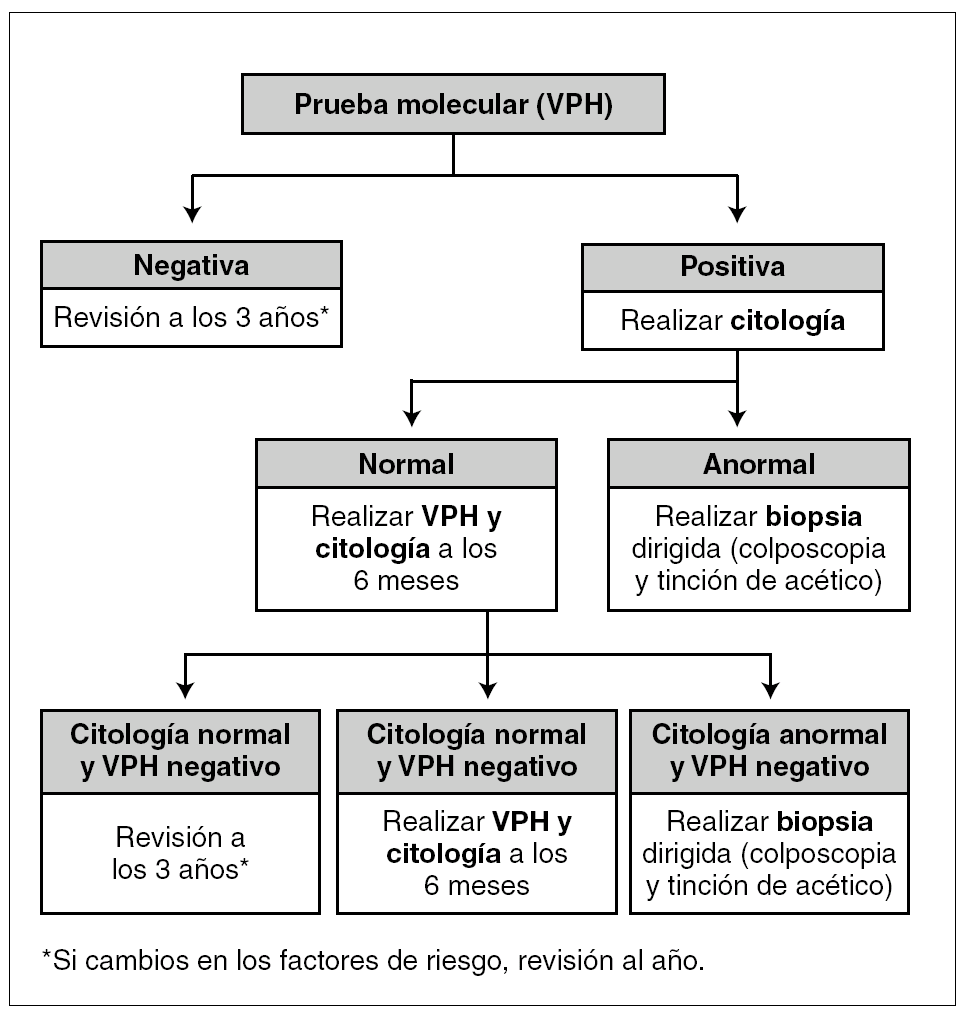
En la figura 1 se presenta el algoritmo de exploración ginecológica basado en los resultados de la citología cervical, y en la figura 2 la propuesta de algoritmo basado en la disponibilidad de pruebas moleculares para la detección del VPH.
Figura 1. Algoritmo de exploración ginecológica para mujeres VIH + cuando sólo se dispone de la prueba diagnóstica de citología convencional (prueba de Papanicolaou). ASCUS: células escamosas atípicas de significado indeterminado; CIN: neoplasia intraepitelial cervical (cervical intraepithelial neoplasia); HSIL: incidencia de SIL de alto grado; LSIL: incidencia de SIL de bajo grado; SIL: lesiones escamosas intraepiteliales (squamous intraepithelial lesion).
Figura 2. Algoritmo de exploración ginecológica para mujeres infectadas por el virus de la inmunodeficiencia humana positivo cuando se dispone pruebas moleculares de detección del virus del papiloma humano (VPH) y de citología convencional (prueba de Papanicolaou).
El uso de las técnicas moleculares debería estar recomendado en los casos siguientes: a) en pacientes infectadas por el VIH con citología cervical negativa, pero con historia clínica de riesgo para adquirir la infección por el VPH; b) en los casos donde el resultado citológico sea un ASCUS, y c) en el control posconización.
El tratamiento de las HSIL y del carcinoma in situ es la conización cervical. La conización cervical es una intervención quirúrgica que consiste en la extirpación de una parte del cuello del útero en forma de cono, cuya finalidad puede ser tanto diagnóstica como terapéutica. Este tratamiento suele ser menos eficaz y presenta una mayor recurrencia entre las mujeres VIH+ respecto a las mujeres VIH. Es probable que los márgenes de resección puedan estar infectados por el VPH 22,23. Por otro lado, la neoplasia vulvar intraepitelial debe tratarse, ya que el riesgo de progresión a neoplasia invasiva no es despreciable 21.
Virus del papiloma humano y ano
Al igual que en el cérvix, el VPH está relacionado con 2 enfermedades anales: los condilomas acuminados y el cáncer de células escamosas de ano.
Si bien la evolución natural de la infección anal, genital y oral por el VPH en pacientes VIH+ todavía no se ha establecido claramente, es probable que el modelo evolutivo clásico (infección-displasia progresiva-carcinoma invasivo) aceptado para cérvix, se corresponda con los cambios clinicopatológicos que se han descrito en los últimos años en la mucosa anogenital y oral de estos pacientes. Como ejemplo, y en el caso específico de la displasia anal, existen coincidencias anatómicas con la displasia cervical que podrían justificar un comportamiento biológico similar. Así, la mayoría de casos de displasia anal se inicia en la zona de epitelio transicional en el canal anal (situada entre el epitelio escamoso poliestratificado del ano, y el epitelio columnar del recto), similar al epitelio transicional del cérvix 24.
Los hallazgos citológicos se denominan lesiones escamosas intraepiteliales anales (ASIL, por sus siglas en inglés anal squamous intraepithelial lesion) y los hallazgos histológicos, neoplasia intraepitelial anal (AIN, por sus siglas en inglés anal intraepithelial neoplasia). Aunque recientemente se ha intentado diferenciar diversos subtipos de displasia anal en pacientes VIH (bowenoide, verrucosa, eritroplásica, leucoplásica), basándose en una clasificación clínico-patológica, ésta todavía no ha tenido una repercusión práctica 25.
Factores de riesgo relacionados con el desarrollo de ASIL/AIN
Los varones homosexuales VIH+ y las mujeres VIH+ (principalmente si éstas presentan una citología cervical anormal) tienen un mayor riesgo de infección anal por el VPH, y un mayor riesgo de presentar ASIL y cáncer respecto a la población VIH 4,26,27. También se ha descrito anormalidades en la citología anal en el grupo de heterosexuales VIH+*28 y en el de pacientes usuarios de drogas por vía parenteral sin historia de sexo anal receptivo 29. La evolución y pronóstico de los carcinomas epidermoides anales en pacientes VIH es peor que la de pacientes similares seronegativos 30.
Entre los factores de riesgo descritos para una citología anal anormal (ASCUS, LSIL, HSIL), encontramos 27:
La detección de la infección por el VPH, especialmente en el cérvix en el caso de mujeres.
La inmunodepresión secundaria al VIH con cifras de linfocitos CD4 bajas.
Carga viral de VIH elevada.
Historia de sexo anal receptivo.
La promiscuidad (elevado número de parejas sexuales).
Antecedentes de otras infecciones de transmisión sexual como condilomas anales, sífilis o hepatitis.
En un trabajo de nuestro grupo llevado a cabo en el año 2005 en una cohorte de pacientes varones VIH+*31, la prevalencia de infección anal por el VPH fue del 78%, y no se observaron grandes diferencias entre los pacientes homosexuales y heterosexuales, 83 y 68%, respectivamente. Merece la pena destacar que el número medio de genotipos de VPH que infectaban fue de 3, y que los genotipos más prevalentes fueron el 16, 18, 33 y 39. En cambio, en este mismo grupo de pacientes los resultados citológicos fueron patológicos en un 43% de los pacientes (ASCUS: 13%, LSIL: 19%, HSIL: 11%), y tampoco se observaron diferencias considerables entre el colectivo de homosexuales (48%) y el de heterosexuales (32%). Un 25% de pacientes estaba infectado por el VPH, pero no presentaba alteraciones citológicas.
Prevención/tratamiento
Tal como se ha comentado, el mejor tratamiento de la infección por el VPH es la prevención. Por ello, en la actualidad sería conveniente practicar una citología anal a todo paciente infectado por el VIH, bien para prevenir el cáncer anal o bien para conocer la historia natural de los ASIL. Si esta citología resulta patológica, se debería proceder a practicar una colposcopia anal de alta resolución con biopsia de las lesiones identificadas mediante la tinción de ácido acético al 3%. Es preciso conocer la relación citológico/biopsia anal, dado que en ocasiones el grado de la lesión es mayor en la biopsia 32.
El tratamiento de las displasias anales de bajo grado: ASCUS y LSIL consiste en un control estrecho, por lo que se aconseja repetir la citología y colposcopia anal a los 6 meses 32. La displasia anal de alto grado (HSIL o AIN 2-3) debe tratarse con cirugía. Aunque recientemente se ha referido la utilidad de los rayos infrarrojos, las recidivas de las AIN 2-3 son frecuentes, posiblemente como consecuencia de su particularidad de ser una lesión multifocal. En algunos casos, se han ensayado opciones no quirúrgicas para tratar la displasia anal in situ, incluido el uso tópico de imiquimod al 5% en crema o 5-FU. Si bien el tratamiento ha sido exitoso en algunos casos, el riesgo de invasividad inherente a estas lesiones arroja dudas acerca del uso extensivo de estos tratamientos 33,34.
Virus del papiloma humano y pene
La infección por el VPH está relacionada con los condilomas acuminados y el cáncer escamoso de pene. A diferencia del cérvix, la historia natural de la infección por el VPH en el pene y su relación con el cáncer de pene no es bien conocida.
Las alteraciones histológicas causadas por el VPH se denominan neoplasia intraepitelial peneal (PIN, por sus siglas en inglés penile intraepithelial neoplasia).
No hay mucha información sobre la prevalencia de la infección por el VPH en el pene. Un trabajo de nuestro grupo en pacientes VIH+ señaló que el 36% de la población estudiada estaba infectada por el VPH, sin que se observara diferencias entre pacientes homosexuales (38%) y heterosexuales (32%) 31.
El VPH puede localizarse en el surco coronal, el glande y el cuerpo, y en menor proporción en la uretra. Esta infección es la causa de los condilomas acuminados, lesiones papulares de apariencia blanda, en ocasiones múltiples, localizadas a menudo en partes secas, como el cuerpo del pene. También la infección por el VPH puede causar lesiones exofíticas de apariencia vascular y de coliflor. En otras ocasiones la infección es subclínica, asintomática y sólo la tinción con ácido acético y la penescopia pondrán en evidencia zonas sospechosas de enfermedad, susceptibles de que se realice una biopsia.
El cáncer escamoso de pene es una enfermedad poco frecuente 35, relacionada con los genotipos VPH 16 y 18. A diferencia de otros procesos oncológicos, el pronóstico de este cáncer es más favorable en los pacientes VPH + que en los pacientes VPH- 36.
Factores de riesgo relacionados con la infección por el virus del papiloma humano en pene
La infección por el VPH en pene se asocia habitualmente con la infección concomitante por el VPH en otras localizaciones, como el ano o la cavidad oral 31, o el cuello uterino o la vagina de la pareja.
La infección por el VPH comporta un riesgo de desarrollar cáncer de pene 4. De hecho, el VPH se encuentra en el 50-60% del total de estos cánceres 36.
Prevención/tratamiento
Al igual que todas las enfermedades causadas por el VPH, el mejor tratamiento es la prevención. El riesgo de la infección peneal por el VPH es menor con el uso del preservativo y en pacientes circuncidados 37.
El tratamiento de los condilomas puede ser diverso y varía dependiendo de la localización, del tamaño de la lesión, de la tolerancia del paciente, de la experiencia del clínico y de la accesibilidad a los tratamientos. Entre los tratamientos tópicos se utiliza el imiquimod, el podofilino y el ácido tricloroacético. La cirugía, la crioterapia o el láser también constituyen alternativas terapéuticas.
Virus del papiloma humano y cavidad oral
La infección en la cavidad oral por el VPH en pacientes VIH+ es relativamente frecuente. Aunque generalmente esta infección suele ser asintomática, la infección por el VPH está relacionada con los condilomas acuminados y los cánceres escamosos de la cavidad oral (amígdala palatina, lengua).
La información sobre la prevalencia de la infección por el VPH en la cavidad oral en nuestro medio es escasa. Recientemente, nuestro grupo encontró que casi un tercio (30%) de la población masculina VIH+ está infectada por el VPH en la cavidad oral, siendo la prevalencia entre homosexuales de un 33%, y de un 23% entre heterosexuales 31.
Probablemente el desarrollo de enfermedad oral como consecuencia de la infección por el VPH suele ocurrir tras un período largo desde el momento de la infección. La mayoría de papilomas se localiza en la mucosa labial, también se pueden localizar en la mucosa bucal, la lengua, el paladar blando y la encía. Normalmente, en la cavidad oral, la expresión clínica de la infección por VPH es reflejo del genotipo causal. Los genotipos 1, 2 y 7 son los más frecuentes en la cavidad oral, y el factor etiológico de las verrugas comunes cutáneas. Los genotipos 13 y 32, descritos únicamente en esta localización, son la causa de la hiperplasia focal epitelial o enfermedad de Heck. El genotipo 16 es otro VPH prevalente en la cavidad oral, al igual que en el aparato genital. Los genotipos de alto riesgo oncogénico 16 y 18 están presentes en un 20% de los cánceres de cabeza y cuello, y en un 50% de los cánceres de amígdala palatina 38.
Hasta la actualidad, en los pacientes VIH+ no se ha descrito un aumento de los cánceres de cabeza y cuello, pero la mayor esperanza de vida conseguida con el tratamiento TARGA puede cambiar su incidencia y prevalencia.
Factores de riesgo relacionados con la infección por el VPH en la cavidad oral
La infección por el VPH en la cavidad oral está asociada a comportamientos sexuales como la homosexualidad, el sexo oral no protegido y la historia de enfermedad de transmisión sexual. La infección concomitante por el VPH en pene también es un factor de riesgo para la infección por el VPH en cavidad oral 31. Todo ello indica que el VPH puede transmitirse a la cavidad oral por contacto sexual. La cavidad oral puede actuar como un reservorio de la infección y como origen de la transmisión a todas las áreas del cuerpo con células escamosas de la pareja receptiva.
Prevención/tratamiento
El mejor tratamiento es la prevención y evitar los factores de riesgo relacionados con la infección por el VPH en la cavidad oral.
VIH/TARGA, inmunidad y VPH
La inmunodepresión por el VIH produce un mayor grado de replicación del VPH, una mayor carga viral del VPH y un aumento de las lesiones epiteliales de alto y bajo grado. Opuestamente, el TARGA aumenta las cifras de los CD4, y favorece la reconstitución del estado inmunológico. Sin embargo, parece que la reconstitución del estado inmunológico tiene un pobre efecto en la inmunidad específica contra el VPH, es decir, la regresión de las displasias de alto grado causada por la infección por el VPH y la progresión hacia cáncer parecen no estar asociadas con el estado inmunitario. Sirva de ejemplos: los pacientes VIH presentan muy frecuentemente verrugas vulgares (entre el 2,9 y 27% de las lesiones cutáneas), que con frecuencia son extensas, recalcitrantes y con gran dificultad terapéutica, a pesar de la reconstitución inmunológica 39. O, el TARGA ha contribuido a la disminución de la prevalencia de enfermedades oportunistas de la cavidad oral como la leucoplasia y la candidiasis en pacientes VIH+; en cambio, estos pacientes tienen una mayor incidencia de condilomas en la cavidad oral 40.
Una vez que la displasia de alto grado se desarrolla, otros factores, como los cambios cromosómicos que provocan las proteínas E6 y E7 del VPH, desempeñan el papel más importante en la progresión hacia el cáncer. El impacto del tratamiento TARGA, con la consecuente mejora del sistema inmunitario, en la historia natural de la infección cervical por el VPH no es concluyente: algunos estudios describen un beneficio franco y otros no 41,42. Las discrepancias observadas entre los diferentes estudios pueden explicarse parcialmente por diferencias metodológicas en el diseño de los estudios, por los criterios usados para evaluar el efecto del TARGA, y por la adherencia al TARGA 42. Tampoco se ha observado que un buen control del VIH con el TARGA tenga un efecto beneficioso (regresión) en la displasia anal, al menos en el primer año de tratamiento. Asimismo, algunos estudios en pacientes homosexuales describen que se mantiene una alta prevalencia de CIN a pesar del TARGA 43.
Es posible que el pobre efecto sobre las lesiones epiteliales se deba a que las lesiones alcanzan "un punto genético de no retorno", es decir, incluso con un estado inmunitario recuperado, éste ya no es capaz de erradicar la lesión 44. Si el TARGA y la recuperación del sistema inmunitario pueden tener algún efecto beneficioso, éste se produciría en las etapas iniciales de la displasia, ya que una vez desarrollada una displasia de alto grado las lesiones no regresan después de iniciar el tratamiento.
Todo ello hace necesario realizar estudios longitudinales que aclaren el papel que desempeña el TARGA/sistema inmunitario en la coinfección por el VPH. Además, la disponibilidad de este tratamiento es reciente (apenas una década), por lo que conviene evaluar el efecto del TARGA a más largo plazo.
Virus del papiloma humano, prevención y preservativo
Como se ha comentado repetidamente en este escrito, el mejor tratamiento es la prevención.
El contagio heterosexual del VIH con sexo no protegido es la primera causa de transmisión en España, y, probablemente, también sea ésta la causa en el VPH. Es importante la educación sexual de la población adolescente, para que tenga una mayor conciencia del riesgo de infección por ambos virus VIH/VPH y lo que puede comportar unas relaciones sexuales sin medidas protectivas. Otras 2 medidas efectivas para prevenir la infección por el VPH son la disminución del número de parejas sexuales y aumentar la edad del primer coito.
La infección por el VPH afecta a las partes del cuerpo relacionadas con la actividad sexual, por lo que a priori se puede pensar que la utilización de preservativos en las relaciones sexuales (vaginales, anales y orales) puede contribuir a la prevención de la infección. Es conocido que el preservativo previene otras enfermedades de transmisión sexual, como son el VIH, el herpes tipo 2, la sífilis, la gonorrea, la clamidia y el tricomona 45. Aunque no está bien dilucidado cuál es el papel que desempeña el preservativo en la prevención de la infección por el VPH 46-48 por falta de estudios prospectivos, la utilización de preservativo se ha asociado con la eliminación del VPH de bajo riesgo 49; con una menor incidencia de condilomas genitales 50; con una menor incidencia de displasia de alto grado y cáncer de cérvix 50; con un mayor porcentaje de regresión de la infección cervical y de CIN 51; con una disminución de la persistencia del VPH 50, y con un mayor porcentaje de regresión de la infección peneal en parejas de mujeres con CIN 48.
Según datos del propio Ministerio de Sanidad, en España el cáncer de cérvix supone en torno al 5% de las enfermedades indicadoras de sida en los últimos años, bastante más elevada que en otros países europeos de nuestro entorno (cifras del 2%), lo que refleja el fallo de los mecanismos de prevención de una enfermedad que es curable en sus etapas más iniciales.
En nuestra sociedad ha primado más llevar a cabo campañas de prevención secundaria (cribado de enfermedad cervical con la citología) que de prevención primaria (uso del preservativo). Las razones de esta situación errónea pueden ser complejas: la infección por el VPH es asintomática, la frecuente pero incorrecta opinión de que el preservativo no reduce la transmisión, la ignorancia de la etiología venérea de los cánceres relacionados con el VPH y la creencia de que las vacunas "resolverán el problema" 52.
Virus del papiloma humano y vacuna
La propia historia en el conocimiento del VPH, su importancia en los cánceres escamosos y las implicaciones sociales que conlleva esta infección, motivaron la investigación de una vacuna profiláctica del VPH 5-7.
Hoy día se están desarrollando 2 vacunas en 2 laboratorios diferentes. Una vacuna se obtiene a partir de la proteína L1 de los genotipos 6, 11, 16 y 18, y la otra de los genotipos 16 y 18. Ambas vacunas inducen la aparición de anticuerpos neutralizantes, previenen la infección y consecuentemente las lesiones citológicas relacionadas 7.
El desarrollo clínico de las vacunas se ha llevado a cabo en mujeres, como profilaxis de la infección cervical por el VPH. Actualmente, estas vacunas están en fase de registro, fase previa a la autorización para su comercialización. En paralelo, se están realizando ensayos clínicos para evaluar la eficacia de la vacuna profiláctica en varones heterosexuales y en un subgrupo de varones homosexuales VIH. La utilidad de la vacuna en la población inmunocompetente proporcionará conocimiento para su desarrollo en pacientes inmunodeprimidos, como son los VIH+.
Si la vacuna demuestra ser efectiva, en un futuro no muy lejano, la prevención de los procesos asociados a la infección por el VPH en localizaciones tan diversas y tan frecuentes en la población VIH+ como la vulva, la vagina, el ano, el pene y la orofaringe será una realidad. La prevención de estas enfermedades contribuirá de forma notoria a la disminución de su prevalencia, con el consiguiente beneficio social.
Conclusiones
La infección por el VPH está relacionada con los carcinomas de células escamosas. Unos 40 genotipos pueden infectar al ser humano por vía sexual a través de contacto directo con lesiones infectadas, por eso la infección por el VPH afecta principalmente a las partes del cuerpo relacionadas con la actividad sexual.
En una población de riesgo como es la infectada por el VIH, el cribado rutinario de infección por el VPH en cérvix, pene, ano y cavidad oral, en combinación con la citología/histología y las técnicas moleculares, puede ayudar a aumentar la eficacia en el tratamiento de los cánceres relacionados con el VPH.
El TARGA ha contribuido a la disminución de la prevalencia de diversas enfermedades oportunistas. En cambio, no se conoce muy bien cuál es el impacto del TARGA, y la consecuente mejora del sistema inmunitario, en la historia natural de la infección por el VPH y su evolución a cáncer.
En la actualidad, ante la falta de un tratamiento específico y efectivo contra el VPH, y a la espera de que la vacuna demuestre su efectividad, el mejor tratamiento es la prevención y evitar los factores de riesgo.
Correspondencia: Dr. G. Sirera.
Hospital Universitari Germans Trias i Pujol.
Avda. Del Canyet, s/n. 08916 Badalona. Barcelona. España.
Correo electrónico: gsirera@ns.hugtip.scs.es