Un porcentaje variable de muestras analizadas por el equipo cobas 4800 pueden dar un resultado invalidado por inhibición de la PCR o erróneo al no extraerse el ADN correctamente con el test cobas 4800 CT/NG.
MétodoValoración de un protocolo de agitación y dilución de la muestra original (exudado u orina) en un total de 116 muestras. Para analizar la sensibilidad de este método, 100 muestras (exudados y orinas) con resultado conocido fueron retestadas.
ResultadosUn 98,3% (114/116) de las muestras se resolvieron con este protocolo con un 100% de concordancia al consultar con datos clínicos, tinción de Gram y otras muestras analizadas en paralelo del mismo paciente.
DiscusiónLos datos indican que no hay pérdida de sensibilidad con este protocolo, por lo que los usuarios de esta plataforma podrían usarlo sin necesidad de métodos alternativos.
A variable percentage of samples analysed using the Cobas 4800 assay can give an invalid result by PCR inhibition or erroneous due to incorrect DNA extraction with the Cobas 4800 CT/NG test.
MethodAn analysis was performed using the vortex agitation and dilution protocol on the original sample (swab or urine) for a total of 116 samples. In order to analyse the sensitivity of this method, 100 samples (swabs and urine) with known results were retested.
ResultsA total of 98.3% (114/116) of the samples analysed were resolved with this protocol with 100% agreement after reviewing clinical data, Gram stain, and other samples analysed in parallel from the same patient.
DiscussionThe data indicate no loss of sensitivity with this protocol; thus Cobas 4800 users could use this method without the need for alternative methods.
Las técnicas basadas en la amplificación de ácidos nucleicos se encuentran entre las técnicas de elección para la detección de Chlamydia trachomatis (C. trachomatis) y cada vez son más utilizadas para la detección de Neisseria gonorrhoeae (N. gonorrhoeae). La nueva generación de técnicas basadas en la amplificación de ácidos nucleicos, como por ejemplo la plataforma cobas 4800 (Roche Diagnostics GmbH, Mannheim, Alemania) instalada en nuestro laboratorio en 20101, incluye secuencias genéticas para detectar la nueva variante de C. trachomatis2,3 y, por otro lado, para reducir los falsos negativos y reacciones cruzadas con especies comensales de Neisseria spp.4,5. Además han mejorado la sensibilidad diagnóstica y han permitido la valoración individual de casos con resultado discordante con el cultivo tradicional.
Estudios previos en esta plataforma correlacionaron pacientes con gonorrea y PCR invalidada por errores de pipeteo con la muestra original debido a la secreción mucopurulenta causada por la infección con N. gonorrhoeae6. En cuanto al tipo de muestras, exudados rectales y faríngeos (muestras no validadas en cobas 4800) pueden contener componentes que inhiban la PCR7, los exudados cervicales pueden interferir a causa del moco cervical o, por otro lado, una alta carga de leucocitos en muestras (1×105) y hematíes tanto en orinas como en exudados8–10.
La resolución de estas muestras no valorables (definidas como error durante la extracción y procesado de la muestra o inhibición de la PCR) es importante en infecciones asintomáticas que frecuentemente pasan desapercibidas y sin tratamiento, provocando un riesgo potencial tanto para el propio paciente como a nivel epidemiológico11–13. En este estudio valoramos un método sencillo y fiable para resolver en esta plataforma este tipo de muestras sin necesidad de técnicas alternativas.
Material y métodosColección de muestrasEste análisis se realizó desde el 1 de noviembre de 2013 hasta el 30 de abril de 2014. Se recepcionaron un total de 4.224 muestras de un centro de infecciones de trasmisión sexual para la detección de C. trachomatis y N. gonorrhoeae en la plataforma cobas 4800. La mayoría (64%) provenían de pacientes sintomáticos, incluían tanto exudados (endocervicales [31,4%], rectales [15,5%] y faríngeos [5,3%]) como orinas (47,8%). Estas muestras se recogían en cobas PCR media Female swab sample kit o en cobas PCR media Urine Sample kit (Roche Diagnostics GmbH, Mannheim, Alemania), respectivamente, siguiendo las recomendaciones del fabricante y se conservaron a temperatura ambiente (máximo 3 días) hasta ser procesadas y a −80°C hasta 30 días en el caso de ser retestadas.
Protocolo de resolución de resultados no valorables de la muestra originalEl protocolo de resolución utilizado, dependiente del tipo de muestra, fue:
- -
En el caso de exudados, agitación intensa con vortex de 30seg de la muestra original, una alícuota de 1mL se añadió a un nuevo tubo estéril de cobas PCR Female swab sample kit que contenía 4,3mL de tampón (≤40% [v/v hidrocloruro de guanidina Tris-HCl]).
- -
En el caso de orina, agitación intensa con vortex de 30seg de la muestra original, una alícuota de 3mL (volumen mínimo para procesar estas muestras) se añadió a un nuevo tubo estéril de cobas PCR media Urine Sample.
Tras esta dilución, se reanalizaron por el equipo cobas 4800 sin otra desviación del protocolo especificado por el fabricante. Se consideraron que las muestras fueron resueltas si se obtuvo un resultado válido del equipo cobas 4800.
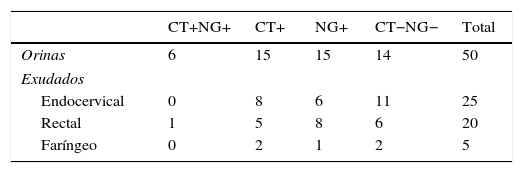
Validación del protocolo de resolución de muestras no valorables a partir de muestra originalSe realizó una validación de este protocolo con 100 muestras con resultado válido y conocido del equipo cobas 4800 con datos clínicos de cada paciente. Se seleccionó una representación significativa de cada tipo de muestra incluida en este estudio, así como de rango de ciclos de amplificación (rango entre 25-39 ciclos). Estas muestras se describen en la tabla 1.
Estas muestras fueron analizadas por el test cobas 4800 CT/NG antes y después de la dilución de la muestra original.
Análisis estadísticoEl análisis estadístico de este estudio se realizó con el programa SPSS Statistics v22 (SPSS Inc., Chicago, IL, EE. UU.). Las variables continuas se expresaron como mediana (Q1-Q3) y las variables categóricas como números (porcentaje).
Aspectos éticosEste estudio ha sido diseñado siguiendo la declaración de Helsinki y aprobado por el comité de Ética del Hospital Universitario de Valme.
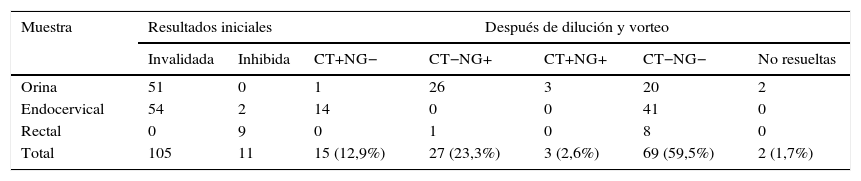
ResultadosDe las 4.224 muestras analizadas, 116 (2,7%) tuvieron un resultado no valorable, de las que, tras ser reanalizadas con el método descrito, se obtuvo un resultado valorable en 114 (98,3%): 69 muestras negativas, 15 positivas para C. trachomatis, 27 positivas para N. gonorrhoeae y 3 positivas para ambos microorganismos. Dos orinas, correspondiente a 2 pacientes varones sintomáticos con sospecha de gonococia y tinción de Gram positiva, no pudieron resolverse tras dilución de la muestra original y posterior retestado. Estos datos se resumen en la tabla 2.
Resultados obtenidos con cobas 4800: resultados invalidados o inhibidos antes y después del protocolo de dilución
| Muestra | Resultados iniciales | Después de dilución y vorteo | |||||
|---|---|---|---|---|---|---|---|
| Invalidada | Inhibida | CT+NG− | CT−NG+ | CT+NG+ | CT−NG− | No resueltas | |
| Orina | 51 | 0 | 1 | 26 | 3 | 20 | 2 |
| Endocervical | 54 | 2 | 14 | 0 | 0 | 41 | 0 |
| Rectal | 0 | 9 | 0 | 1 | 0 | 8 | 0 |
| Total | 105 | 11 | 15 (12,9%) | 27 (23,3%) | 3 (2,6%) | 69 (59,5%) | 2 (1,7%) |
Con objeto de confirmar los resultados obtenidos, se revisaron los datos clínicos de estos pacientes: muestras positivas para C. trachomatis correspondían a pacientes sintomáticos (12/15, 80%) o seguimientos de contacto con sospecha de infección. Las positivas para N. gonorrhoeae correspondían a pacientes sintomáticos con cultivo de N. gonorrhoeae positivo y/o tinción de Gram positiva, mientras que las positivas para ambos microorganismos procedían de pacientes sintomáticos con sospecha de infección, con otras muestras (exudados rectales) positivas para ambos organismos.
Las muestras que resultaron negativas (41 exudados cervicales, 20 orinas y 8 exudados rectales) correspondieron a 22 pacientes varones y 47 mujeres. La mayoría eran pacientes control sin sospecha de infección con otras determinaciones también negativas. El resto (pacientes sintomáticos) presentaban infección no gonocócica, infección por virus herpes simplex 2 y condiloma, respectivamente. El resto se trataba de pacientes en seguimiento de contacto o control postratamiento, tenían otras muestras de distintas localizaciones con resultado negativo para ambos, clamidia y gonococo.
Las 100 muestras analizadas para la validación de este protocolo obtuvieron una concordancia del 100% con respecto a los resultados previos por el equipo cobas 4800. El valor medio del ciclo umbral (Ct) al que amplificaban las muestras positivas antes y tras la dilución fueron los siguientes: positivas para C. trachomatis presentaban una mediana de Ct de 32,2 ciclos (rango de 24,1-38,2 ciclos), que tras dilución ascendía a 33,5 ciclos. Para las positivas para N. gonorrhoeae, la mediana de Ct sin dilución fue de 27,6 (rango de 23,5-39,3 ciclos), y tras dilución fue de 30,4 ciclos.
DiscusiónNuestro laboratorio, centro de referencia del centro de infecciones de trasmisión sexual, tiene un porcentaje de muestras positivas para C. trachomatis y N. gonorrhoeae del 10,3% y del 5% (datos internos de 2013), donde, un 2-5% de las muestras analizadas dieron lugar a un resultado no válido.
En esta plataforma hay pocos estudios sobre resolución de este tipo de muestras, entre los que destaca Miller et al.6 que empleaba Sputasol (1,4% dithiothreitol; Oxoid Ltd., Basingstoke, Reino Unido) para reanalizar este tipo de muestras con buenos resultados, u otros estudios que plantean la necesidad de métodos alternativos para la resolución de este tipo de muestras14.
En este estudio es de destacar que tras el reanálisis de muestras con resultado no valorable, el 39,5% dio un resultado positivo. De estas, un 66,7% fueron positivas para N. gonorrhoeae en su mayoría en muestras de orina de pacientes varones que dieron un resultado «failed». Los valores Ct presentaban una mediana de 27,8 ciclos en estas muestras; indican un nivel de carga bacteriana alto. Probablemente este resultado se deba a un exceso de sedimentos o leucocitos en la orina.
Una de las limitaciones de este estudio es el limitado número de muestras con baja cantidad de ADN bacteriano testadas, especialmente aquellas con un valor Ct≥38 ciclos, en donde la dilución de estas muestras podría dar lugar a un falso negativo. A pesar de ello, nuestros datos indican que solo entre un 7-10% de las muestras analizadas presentaban un Ct superior a este valor cuyo resultado se podría valorar junto a la clínica, cultivo de Gram o confirmación por otro test. En la bibliografía hay pocos estudios que avalen un resultado N. gonorrhoeae positivo con en esta plataforma15. Otra limitación del estudio es el uso de muestras no validadas en la plataforma cobas 4800 (exudados rectales y faríngeos), pero analizadas e incluidas en estudios previos7. Por otro lado, el número de muestras inhibidas es bajo, por lo que sería necesario un mayor número de este tipo de muestras para confirmar la sensibilidad del protocolo de dilución.
Por ello, este método fácil, sensible y que no requiere de métodos alternativos o uso de otros reactivos, permitiría a aquellos usuarios del equipo cobas 4800 resolver con garantías aquellas orinas y exudados mucopurulentos y, por consiguiente, reducir el número de muestras no amplificables con el consiguiente ahorro de tiempo, recursos por parte del laboratorio y de una nueva toma de muestra.
Conflicto de interesesNinguno que declarar.