Este artículo de formación ofrece los conceptos básicos en los tratamientos de depuración renal continua. Se muestra un diagrama del tamaño de las moléculas que suelen estar implicadas en estos tratamientos. Desde esta visión, se puede entender mejor por qué determinadas sustancias necesitan un tipo concreto de proceso físico para ser eliminadas. A partir del conocimiento de estos procesos, se clasifican las terapias a programar en cada máquina. Se ofrecen esquemas sencillos elaborados con trazos simples, representando el filtro, las membranas o las moléculas que se explican.
Es necesario entender también cada parte del circuito, independientemente de la casa comercial que lo fabrique. Por esta razón se muestra un circuito general, elaborado también con trazos simples. Por último, se especifican algunos de los problemas que puede presentar este manejo para la enfermera de UCI.
This training article provides the basic concepts in continuous renal purification treatments. A diagram of the size of the molecules that are usually involved in these treatments is shown. This allows a better understanding of why certain substances need a specific type of physical process to be removed. From the knowledge of these processes, the therapies to be programmed in each machine can be classified. Simple line diagrams are provided, representing the filter, the membranes, and the molecules, which are explained.
It is also necessary to understand each part of the circuit, regardless of the distribution company. For this reason, a general circuit is shown, also drawn using simple lines. Finally, some of the management problems that can present for the ICU nurse are specified.
En las Unidades de Cuidados Intensivos (UCI), el uso de terapias de tratamiento sustitutivo tiene una elevada incidencia y se detecta un aumento de la mortalidad de los pacientes en fracaso renal agudo hasta en un 50% sobre aquellos que no las necesitan1. Habitualmente, los pacientes críticos presentan una labilidad hemodinámica que impide el uso de las técnicas intermitentes utilizadas en pacientes crónicos. Esto hace que estos pacientes requieran técnicas continuas prolongadas en el tiempo, que no modifiquen su medio interno de manera brusca1,2.
La aplicación de estas terapias conlleva un control exhaustivo del funcionamiento del catéter, de la permeabilidad del circuito, de la programación del monitor, de los valores de los iones y de los efectos secundarios del desequilibrio de estos.
Dependiendo de la gestión de recursos de cada centro, los monitores de tratamientos continuos son parcial o totalmente responsabilidad de la enfermera de UCI3,4. Dada la complejidad de estos pacientes y la suma de cargas de trabajo asociados a su atención, las enfermeras deben tener suficiente conocimiento y seguridad en los puntos clave de este tratamiento.
ObjetivoEl objetivo de este trabajo es proporcionar la información esencial para una correcta instauración, mantenimiento y evaluación de las terapias de tratamiento sustitutivo continuo a los pacientes con fracaso renal agudo en la UCI.
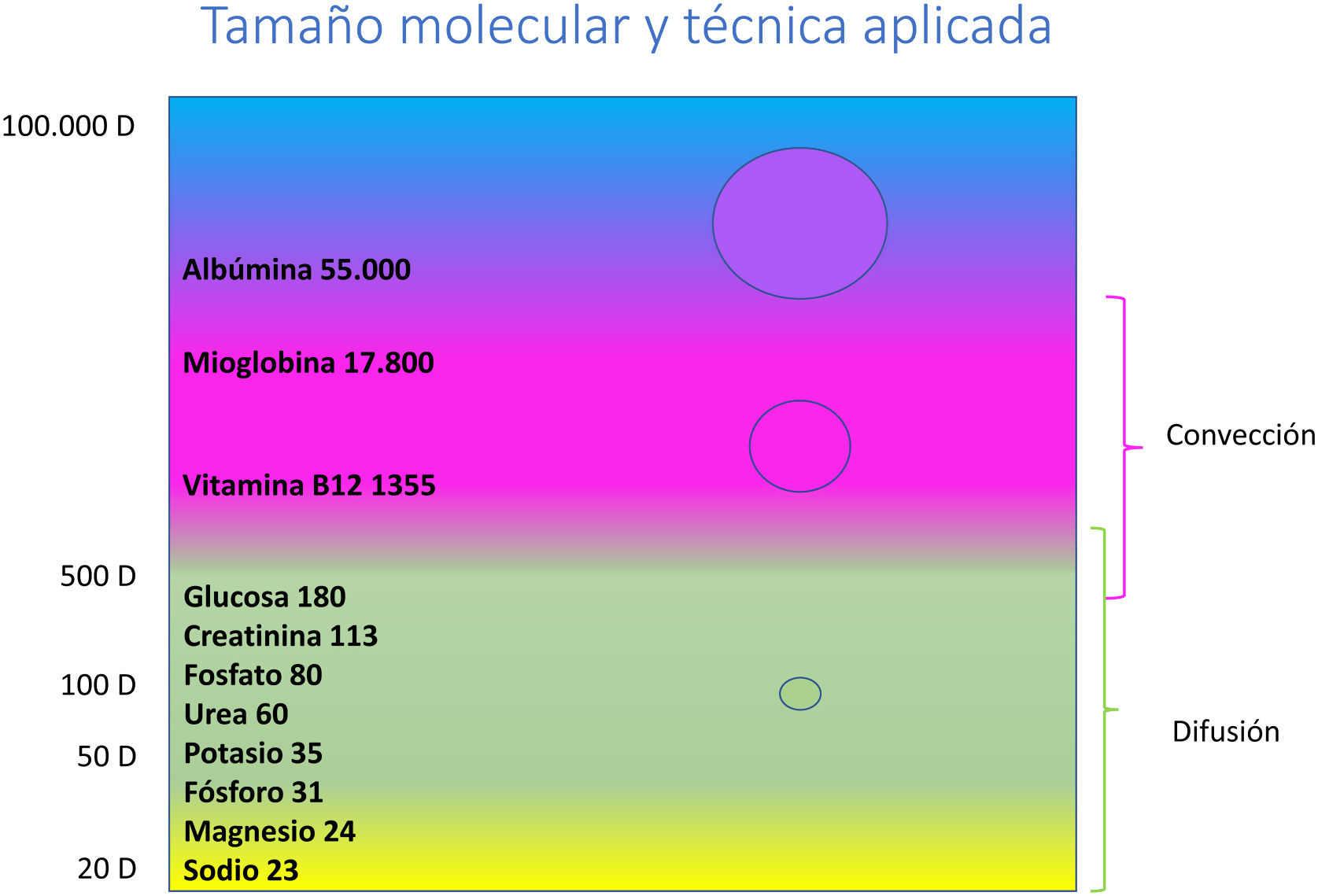
La física de solutosLos procesos físicos que esencialmente tienen lugar en los filtros de los circuitos son los que se explicarán a continuación. Todos ellos están relacionados con la pérdida de volumen de agua plasmática o bien con la pérdida de sustancias de bajo o medio peso molecular. Este parámetro es fundamental porque es un determinante mayor del filtrado de la molécula a través de la membrana semipermeable de los filtros que se utilizan5. El tamaño de las moléculas se relaciona también con el tipo de técnica depurativa a elegir (fig. 1).
Los procesos de depuraciónAnte una membrana semipermeable interpuesta entre dos cámaras, existen distintos procesos de depuración en función de la concentración de solutos, del volumen de agua, e incluso de las características propias de la membrana.
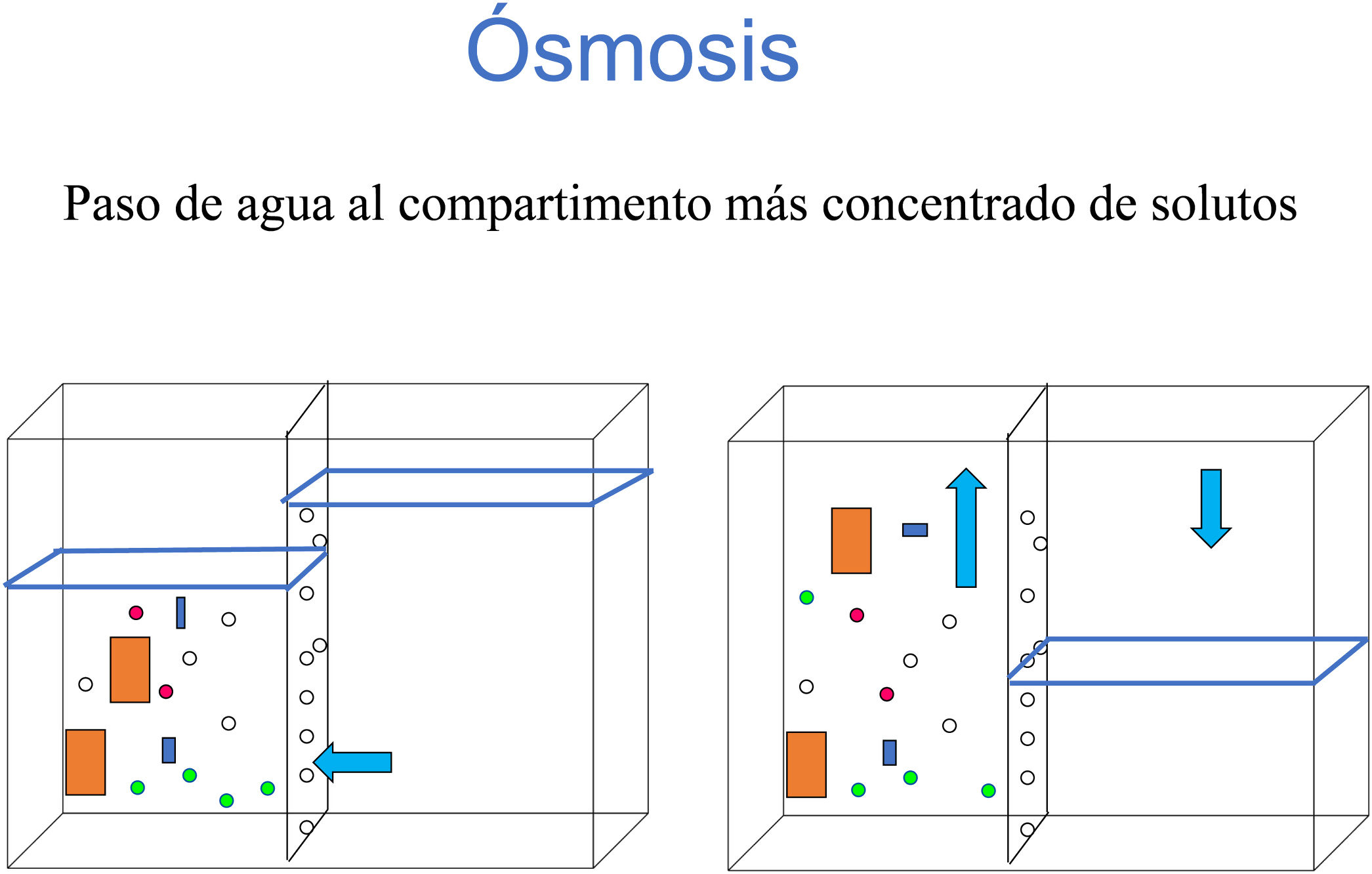
ÓsmosisLa ósmosis es el movimiento de agua a través de una membrana semipermeable que consigue bajar la concentración de solutos en el compartimento hacia el que se desplaza (fig. 2). Este desplazamiento siempre se produce desde el compartimento menos concentrado al más concentrado de solutos.
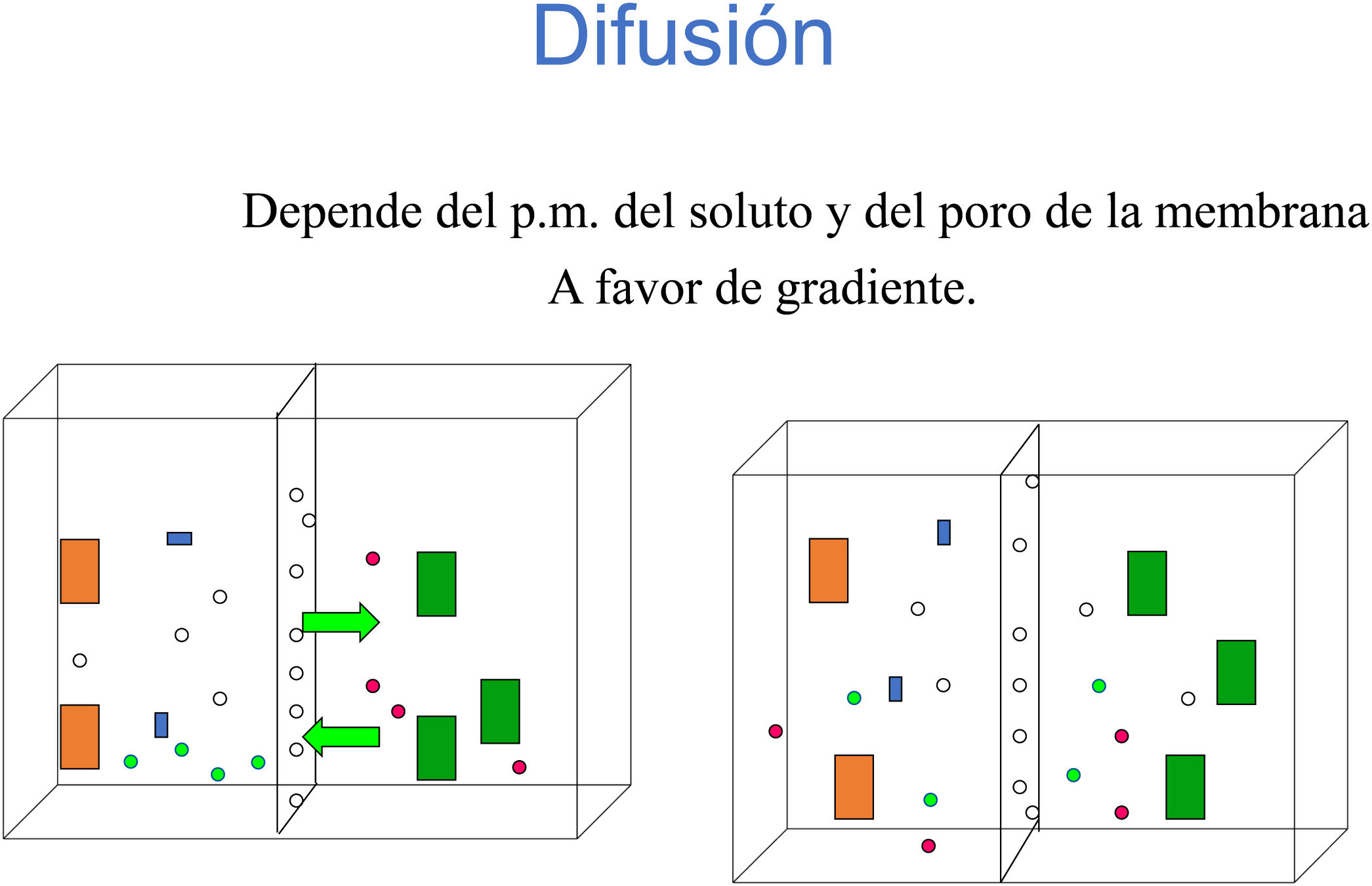
DifusiónEl proceso difusivo es aquel por el cual dos compartimentos, separados por una membrana semipermeable, pueden intercambiar solutos6. Estos solutos, pueden pasar de forma bidireccional si tienen un tamaño menor que el poro de la membrana y el sentido que tomarán será del compartimento de mayor concentración al de menor. En la figura 3 se observa que las moléculas pequeñas que tenían más concentración en el compartimento de la izquierda han pasado a la derecha y viceversa. De esta manera, si se les da tiempo, podrán igualarse las concentraciones de ambos compartimentos.
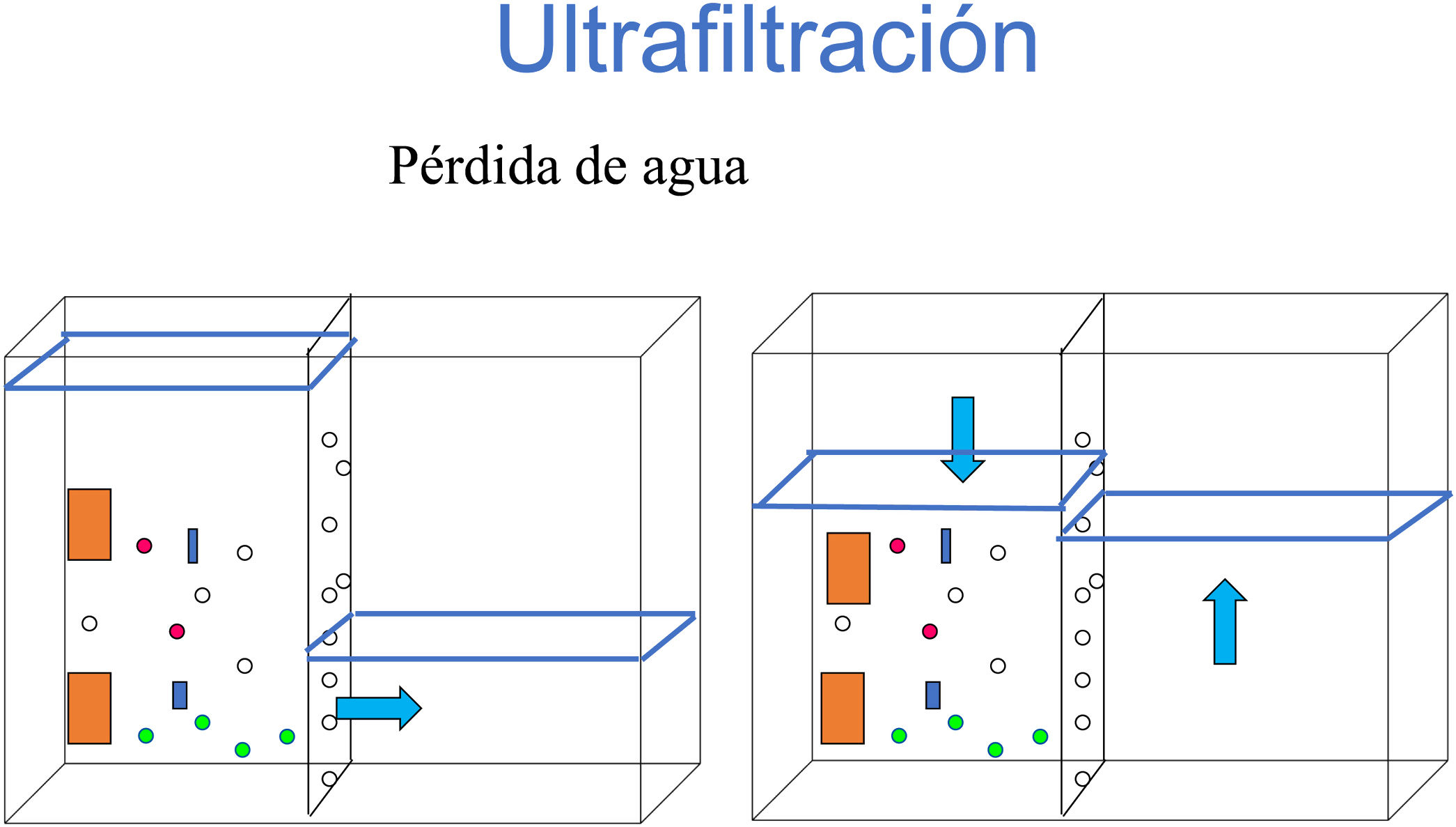
UltrafiltraciónSe entiende por ultrafiltración la pérdida de agua de una solución concentrada de solutos. Se puede relacionar con una ósmosis inversa.
Mediante este proceso, el compartimento que cede agua quedará más concentrado de solutos, tal como podemos ver en la figura 4.
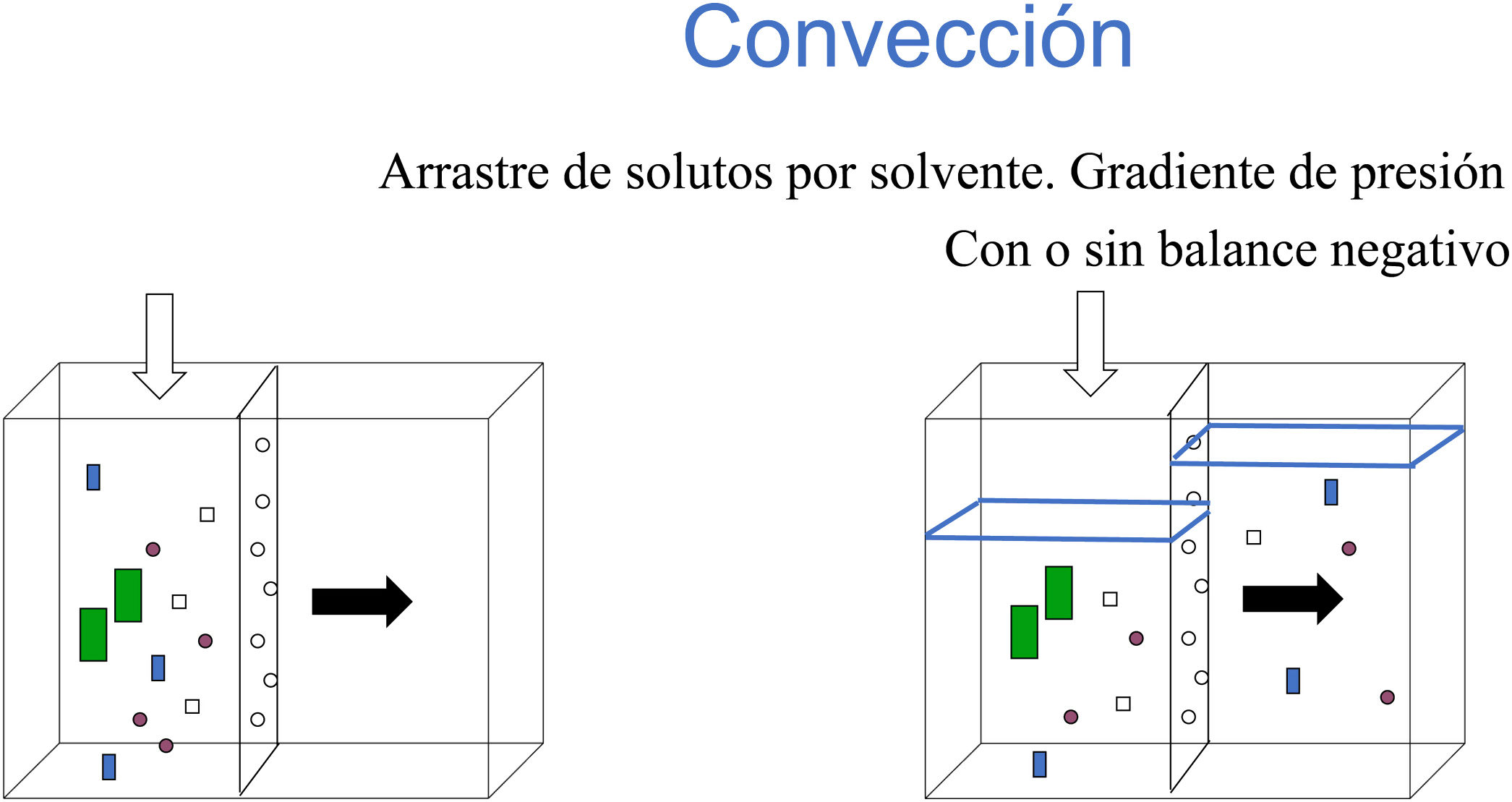
ConvecciónSe entiende por convección aquel proceso por el cual, generándose un gradiente de presión, pueden filtrarse ciertas moléculas a través de la membrana, acompañadas por el agua del ultrafiltrado (figura 5).
Por el hecho de haber aumentado la presión en el compartimento inicial, algunas moléculas de tamaño mayor que no pasaban por difusión lo harán ahora por convección. En el esquema inicial de tamaño molecular, este tipo de moléculas se clasifican dentro de moléculasmedianas7.
En el caso de las técnicas depurativas, la presión necesaria para lograr este proceso se ejerce con la entrada de líquido al compartimento hemático (llamado líquido de reposición). De esta manera se puede equilibrar la pérdida de volumen. Como consecuencia del aumento de presión en el compartimento sanguíneo y favorecer el paso de agua y solutos por la membrana, aumenta la presión transmembrana8. Cuanta mayor dosis convectiva se utilice (ml/kg/h), mayor será la presión transmembrana que indique el monitor. La evolución de este ítem será útil en la evaluación de la permeabilidad del filtro.
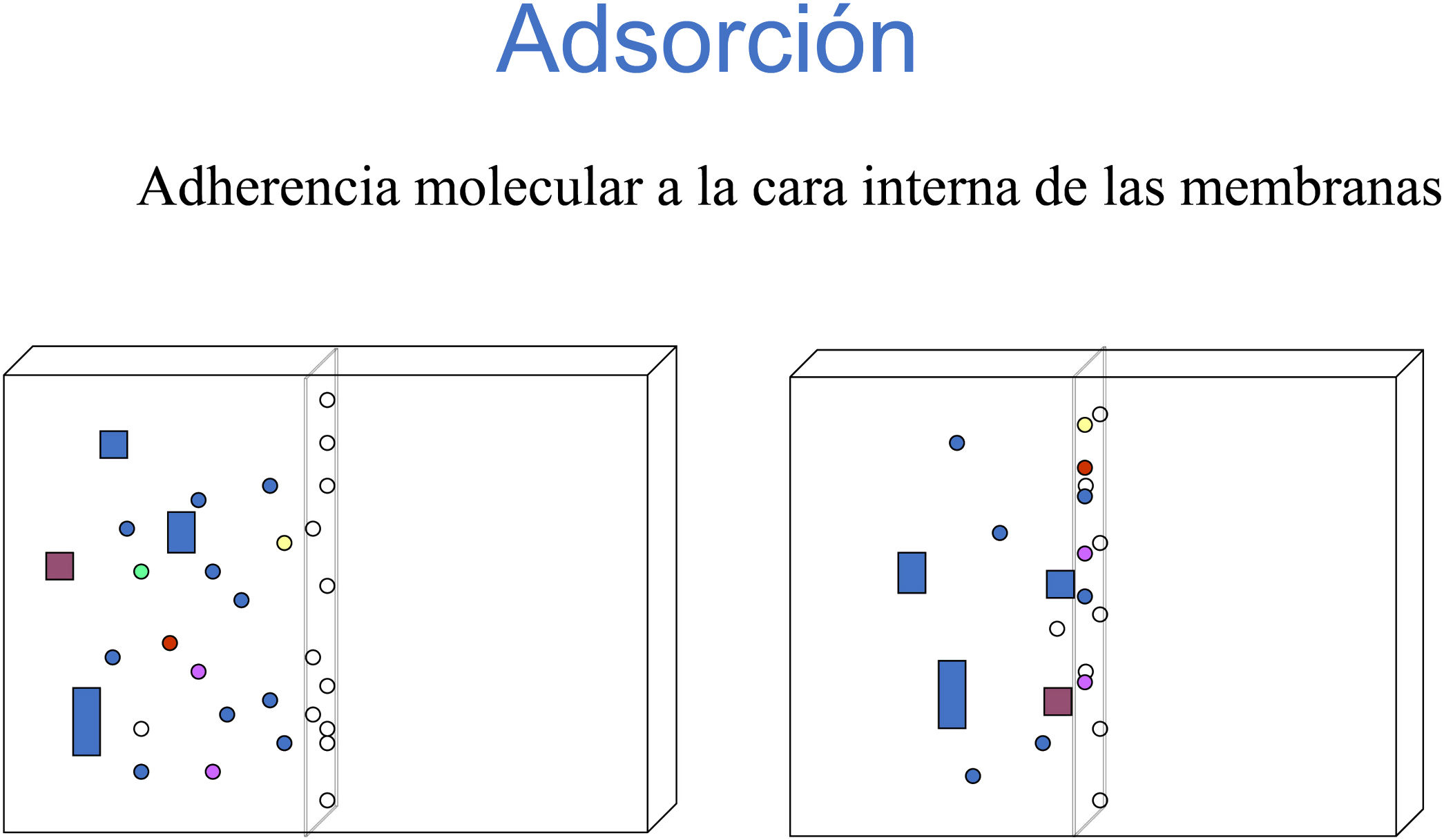
AdsorciónEn ocasiones, determinadas moléculas no se detectan en el líquido que se desecha y tampoco en la sangre ya depurada. Estas moléculas han quedado adheridas a la cara interna de la membrana del filtro por la cual tienen cierta afinidad. Este proceso se conoce como adsorción (figura 6). No todas las membranas ni todas las moléculas tienen el mismo comportamiento en este sentido. Los factores de los que depende este proceso son principalmente la permeabilidad de la membrana, el tamaño molecular del soluto, la naturaleza de la membrana y su carga eléctrica9. Un dato importante es que la adsorción se satura con el tiempo, perdiendo importancia cuanto más tiempo se utiliza el mismo filtro. En la actualidad existen membranas especialmente diseñadas para poder eliminar una determinada sustancia adhiriéndola en su superficie.
Todos estos procesos explicados hasta ahora sobre la depuración de solutos, no se producen de la misma manera en todos los tipos de membranas. No todas tienen las mismas condiciones: coeficiente de ultrafiltrado, coeficiente de cribado, tamaño y número de poros, hidrofilia, etc.10. No es el objetivo de este capítulo explicar estos conceptos, pero está claro que el equipo asistencial debe conocer el material del que dispone en su servicio y utilizarlo de forma adecuada.
Terapias programables en un monitor de técnicas continuasTeniendo en cuenta las posibilidades que existen para eliminar agua y solutos, se puede programar el monitor de diversas formas para obtener los resultados deseados. Las abreviaturas de los tratamientos han sido consensuadas a nivel internacional11.
Slow continuous ultrafiltration (SCUF)La conocida como slow continuous ultrafiltration es aquella terapia que busca como objetivo la pérdida de volumen en el lecho vascular del paciente. Precisa de un filtro a través del cual pase la sangre y una salida de líquido que constituirá el balance negativo (efluente). No utiliza líquidos de tratamiento como sí lo hacen el resto de las terapias (figura 7).
Si el paciente está bien nutrido y la presión oncótica del lecho vascular atrae el agua del tercer espacio, el edema de extremidades, si existiera, bajará. También de esta manera, un paciente que tiene líquido en algún órgano vital como puede ser el pulmón, se verá beneficiado de esta terapia.
Para ayudar a controlar cuánta agua se puede retirar del lecho vascular, algunos monitores, tanto de diálisis convencional como de tratamientos continuos, disponen de control de hematocrito. Si la volemia del paciente va bajando y no hay buen rellenado vascular (refilling) proveniente del tercer espacio, el hematocrito subirá. A este hecho, además, le acompañarán signos evidentes de hipotensión y habrá que disminuir el objetivo de la pérdida hídrica12.
En ocasiones puede parecer que la velocidad de la bomba hemática pueda estar relacionada con la hipotensión del paciente. Esto solo podría tener lugar en el momento del inicio de la terapia, relacionado con la salida del volumen de sangre hasta completar el circuito hemático del monitor. Si se comprueba una hipotensión, tras algún tiempo de tratamiento, hay que pensar que está relacionado con la tolerancia o no a la disminución de la volemia y no con la velocidad de la bomba hemática. Por tanto, cuando el circuito está instaurado y el tratamiento sigue su curso, no se debe bajar la bomba hemática como primer recurso para remontar una hipotensión en el paciente.
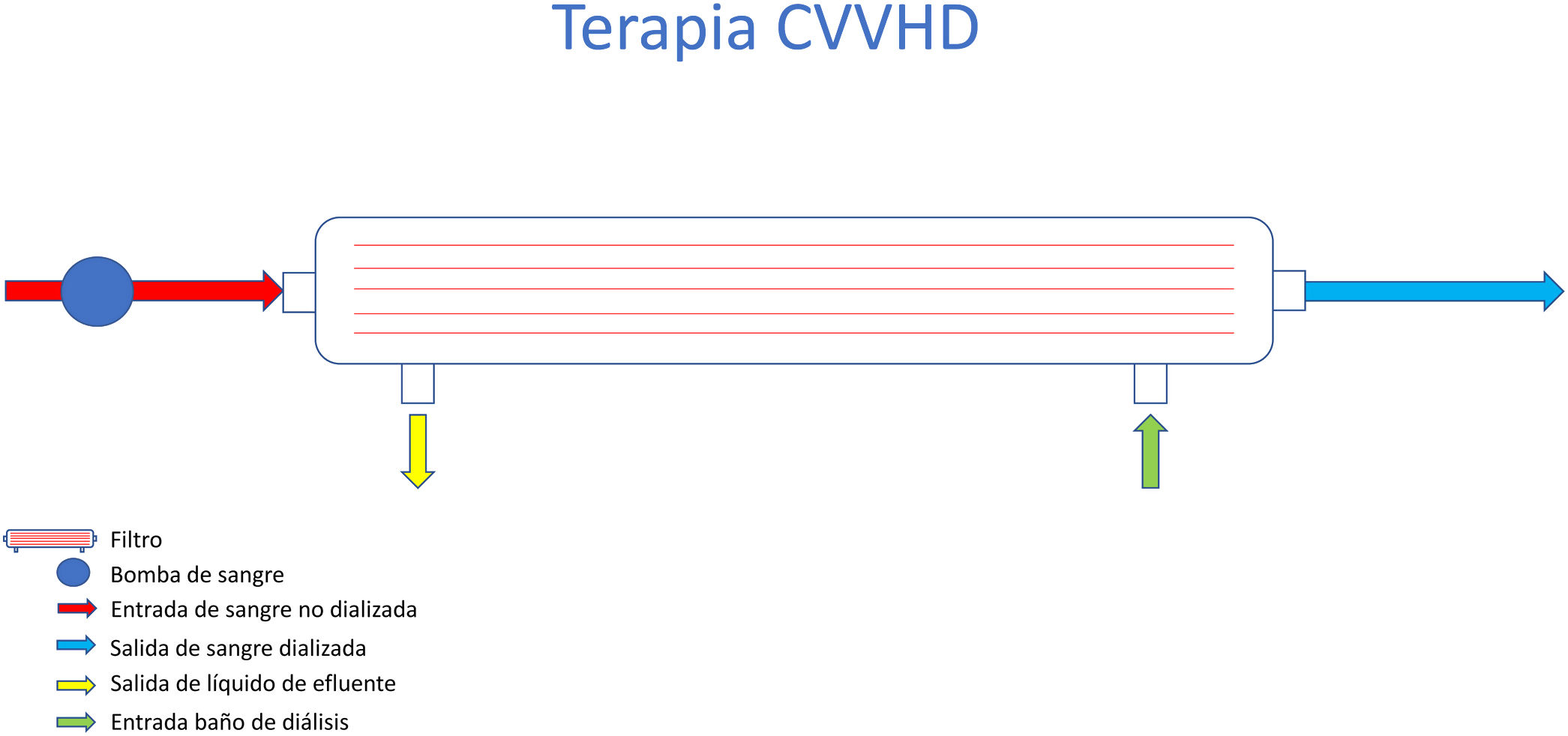
Hemodiálisis veno-venosa continua (CVVHD)La terapia continua veno-venosa que utiliza baño de diálisis, se denomina hemodiálisis y se fundamenta en un mecanismo difusivo, gracias a un gradiente de concentración (figura 8).
El objetivo de esta terapia es eliminar, esencialmente, moléculas pequeñas como puede ser la urea, la creatinina o el potasio.
Es esencial que el baño de diálisis que se utilice contenga los iones necesarios que se quieran mantener y la ausencia de aquellos que se quieran eliminar. Esto implica que el baño esté equilibrado a nivel de pH, bicarbonato, sodio, magnesio, cloro, fósforo, calcio, potasio y glucosa, esencialmente. Es recomendable que, si alguno de estos iones se descompensa durante el tratamiento, sea repuesto al organismo por una vía parenteral externa. No se recomienda utilizar ampollas de iones comercializados añadidas directamente a las bolsas de tratamiento para suplir este disbalance. La estabilidad de los iones añadidos en las bolsas no puede garantizarse fuera del laboratorio en el que se han llegado a comercializar. En este sentido, el potasio en su forma de cloruro potásico es la molécula más estable. El resto de los iones, sobre todo los divalentes, tienden a formar agregados que se deben controlar cuidadosamente13. De la misma manera, las dos partes que forman la bolsa de tratamiento no deben mezclarse hasta el momento de ser utilizadas, para minimizar este tipo de problemas asociados.
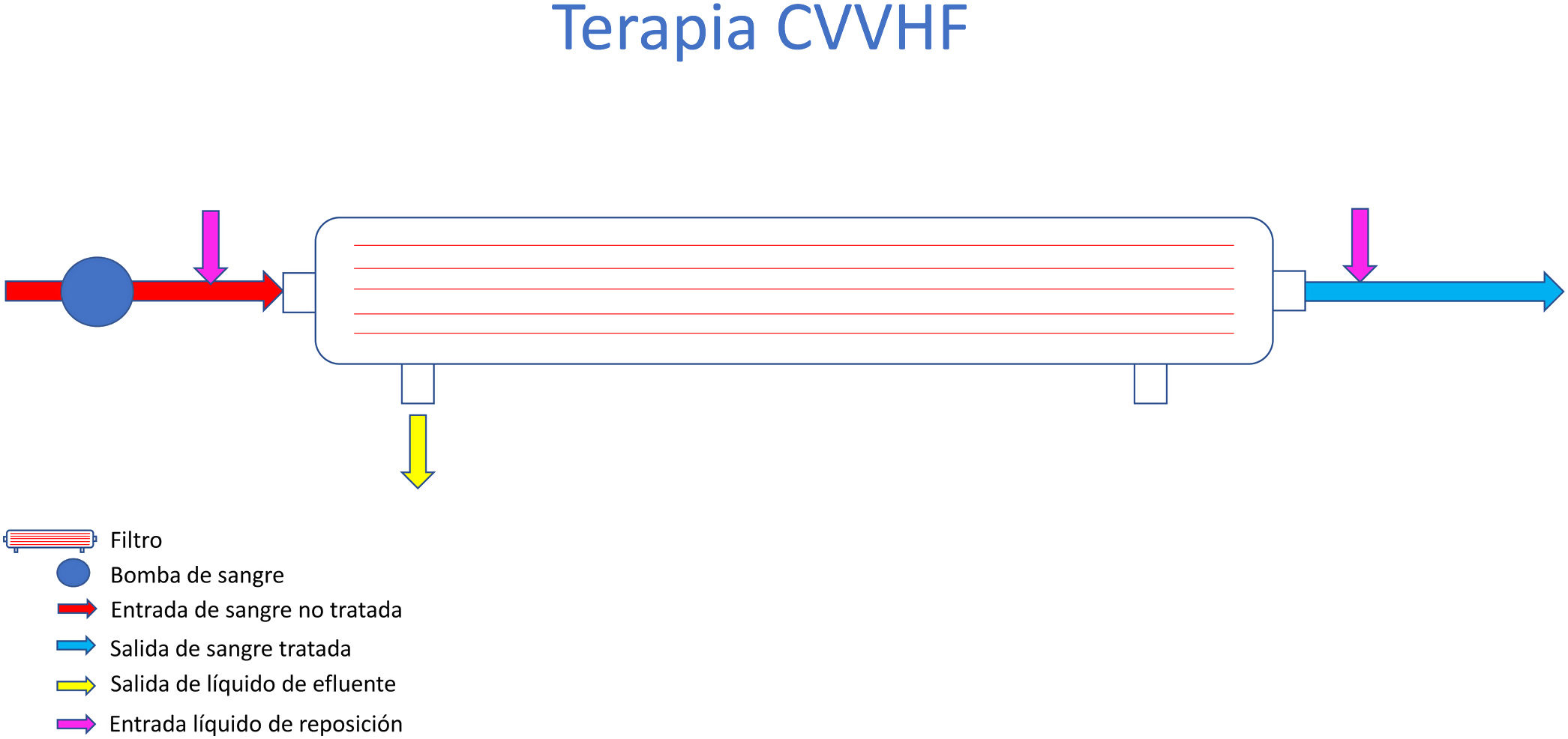
Hemofiltración veno-venosa continua (CVVHF)La terapia continua veno-venosa que utiliza líquido de reposición para realizar el tratamiento, se denomina hemofiltración y se fundamenta en un mecanismo convectivo, gracias a un gradiente de presión. Esta terapia tiene la finalidad de aumentar la presión en el lado plasmático del filtro o disminuirla en el otro lado con el objetivo de que fluya el agua del primer compartimento al segundo. Este proceso puede comportar una gran pérdida de líquido que arrastra solutos, lo cual obliga a realizar una reposición. Como se puede ver en la figura 9, la entrada de este líquido de reposición tiene lugar en el compartimento hemático y puede ser en prefiltro y/o posfiltro. En este tipo de terapias es preciso ajustar muy bien la velocidad de la bomba de sangre a la dosis convectiva deseada (ml/kg/h). La fracción de filtración14 no debe superar un valor del 20-25%. Esto es fundamental en los procesos en que la anticoagulación del sistema no puede llevarse a cabo con citrato.
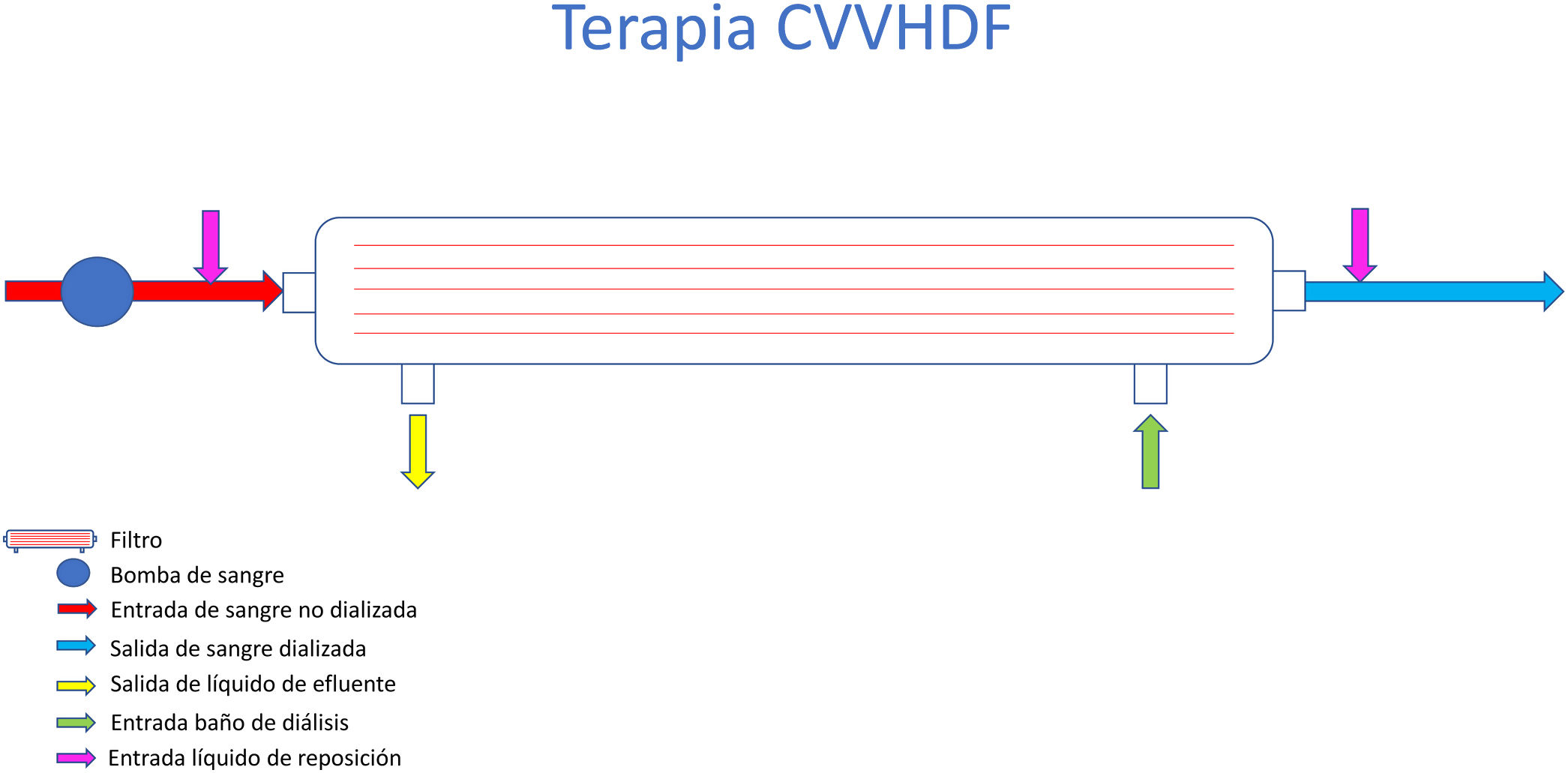
Hemodiafiltración veno-venosa continua (CVVHDF)En algunos casos es preciso combinar la terapia difusiva (gradiente de concentración) con la convectiva (gradiente de presión). Entonces, se programa la hemodiafiltración. Por tanto, se pondrá baño de diálisis en el filtro y también líquido de reposición (fig. 10). Algunos monitores tienen tres bombas de líquidos y otros dos. Esto condiciona que se pueda poner baño de diálisis y además la reposición en modalidad pre y/o posfiltro.
Como en el caso de la hemofiltración, si no se utiliza citrato, hay que calcular la fracción de filtración para programar la bomba hemática adecuadamente, ya que la exposición de la sangre a la membrana supone un riesgo elevado de coagulación.
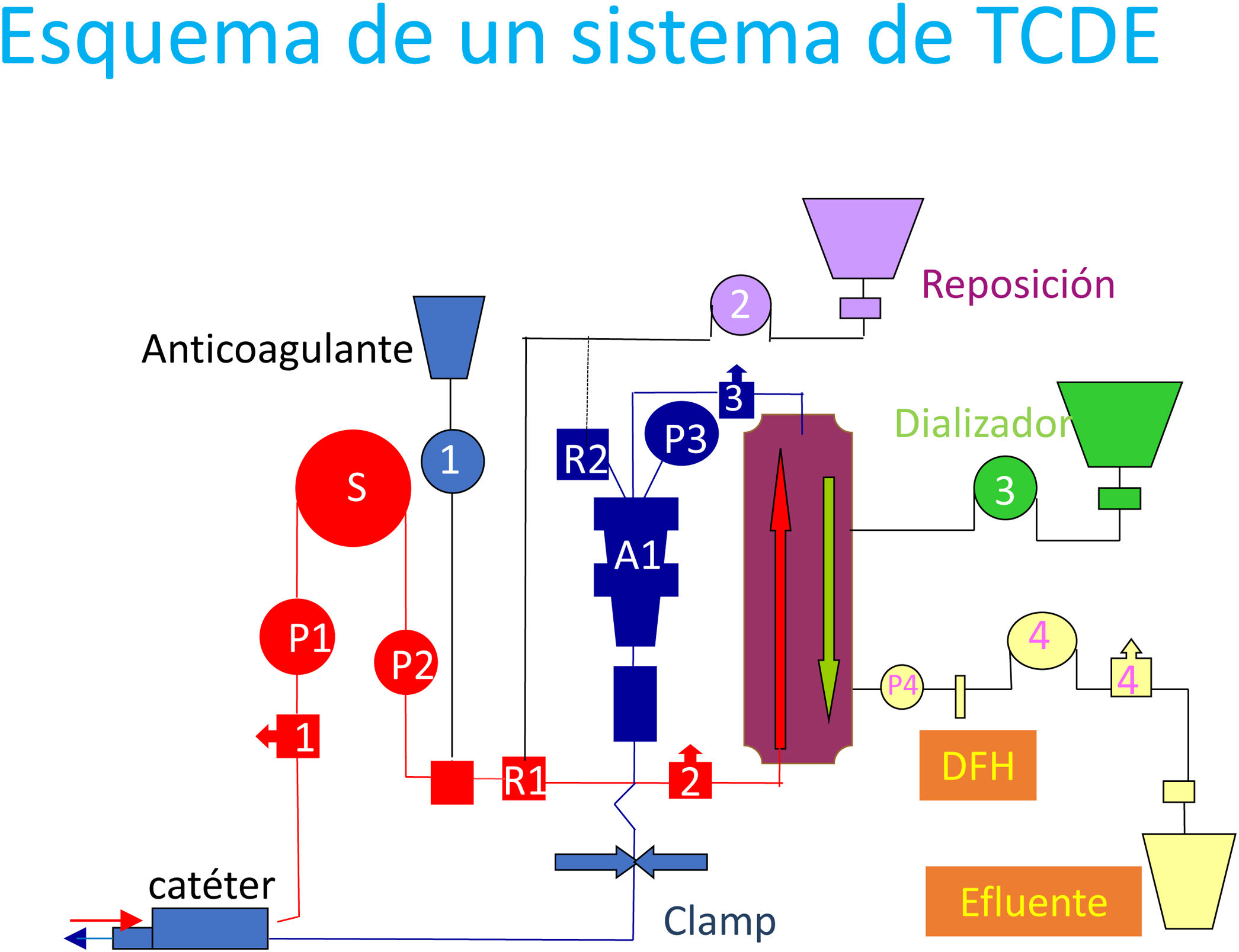
Composición de las diferentes líneas de un set de técnicas continuasPara poder iniciar una terapia depurativa a un paciente agudo en una UCI, es preciso canalizar una vía central e implantar un catéter de calibre suficiente para obtener el flujo de sangre necesario. En el caso de adultos, suele utilizarse un catéter específico de doble luz de unos 12 a 14 French, preferiblemente en vena yugular derecha o en la vena femoral. Es necesario calcular el flujo que puede darnos cada tramo del catéter, utilizando una jeringa de 20 cc y aspirando de forma rápida y continua de forma que, si en menos de seis segundos la jeringa se llena, podemos asegurar, como mínimo, el flujo de 200ml/minuto de esa luz. Una vez realizado el test de flujo, se sutura el catéter a piel y se sella con una solución apropiada para ello4. Tras la implantación y cuidado del catéter, hay que disponer de un set completo que canalice esa sangre del paciente y sea capaz de depurarla. El conocimiento de este set es el objetivo de este apartado (figura 11).
Un set completo podrá trabajar con cualquiera de las técnicas continuas de depuración extracorpórea enumeradas en los apartados anteriores. Debe contener diferentes líneas con algunas partes fundamentales para el buen funcionamiento de todo el sistema. La enfermera encargada de la puesta en marcha y el mantenimiento de estos equipos debe conocer cada una de las líneas e interpretar su buen funcionamiento15.
Línea hemáticaLa línea del set que se encarga de conducir la sangre desde el catéter hasta el filtro se representa en un tramo rojo en la figura 11 (línea aferente). Esta parte contiene los siguientes elementos: toma de muestras, sensor de presión P1, bomba de sangre (S), sensor de presión P2, línea de entrada de bomba de jeringa (frecuentemente usada para anticoagulación con heparina) y entrada de líquido de reposición prefiltro (R1). El sensor P1 indicará esencialmente la resistencia que ofrece el catéter a la activación de la bomba de sangre. El sensor P2 indicará la resistencia del filtro al paso de sangre por los capilares.
Una vez pasado el filtro, la línea hemática que retorna al paciente (línea eferente) se representa en color azul en la figura 11 y ha de contener los siguientes elementos: sensor de presión P3, toma de muestras, cazaburbujas, entrada de líquido de reposición posfiltro (R2), sensor de nivel de aire (A1) y clamp. Normalmente, el sensor de nivel de aire se encuentra situado en el tramo medio del cazaburbujas. Si se activa este sensor, el sistema activa el clamp de forma automática, de manera que una embolia gaseosa nunca llegará a producirse si el sistema se maneja correctamente. Es esencial controlar el nivel del cazaburbujas para minimizar la activación de este sensor. Se aconseja, así mismo, disminuir el contacto aire-sangre en el cazaburbujas para evitar con ello la procoagulación del sistema en este punto. El sensor de presión P3 orienta sobre la resistencia al paso de sangre hacia la línea de retorno y el catéter.
Línea de baño de diálisisEl tramo de fungible que conduce el líquido desde la bolsa hasta la entrada a la carcasa del filtro para hacer la difusión se representa en color verde en la figura 11. Tan solo contiene una bomba infusora y la conexión a la bolsa de líquido de tratamiento. Cada bolsa descansa sobre una báscula que controla su peso continuamente. Es muy importante comprobar (previo a la conexión a paciente) el calibrado de las básculas para no incurrir en errores en el balance.
Trabajar con líquidos de tratamiento que están a temperatura ambiente y además tener unos 200ml de sangre fuera del organismo, implica disminución de la temperatura corporal de los pacientes. Opcionalmente algunos monitores incorporan sistemas de calentamiento de estos líquidos que contribuyen a minimizar la hipotermia generada en estos tratamientos. De igual manera, en algunos casos, también es posible tener sistemas que calienten las líneas de sangre del circuito extracorpóreo. El control de la temperatura corporal del paciente es fundamental en estas terapias.
Línea de líquido de reposiciónEsta línea, que logrará el efecto convectivo, está representada en color violeta en la figura 11 y puede entrar en prefiltro o posfiltro. Algunos monitores pueden ofrecer las dos entradas de forma simultánea cuando está activada la bomba de diálisis.
Estas líneas, como la anterior, solo contienen conexión a bolsa de tratamiento y bomba infusora, así como las básculas correspondientes. Así mismo, carecen de sensor de presión específico.
Línea de líquido del efluenteEsta es la línea más compleja de las que llevan líquidos. A parte de la bomba y de la toma de muestras, tiene un sensor de presión previo a la bomba que representamos como P4 (figura 11). También contiene otro sensor llamado de fuga hemática. Es importante saber que, si algún capilar del filtro se fisura por algún motivo, este sensor será el que avise de esta eventualidad, captando un cambio de color en el líquido de desecho y alertando de la conveniencia de retornar la sangre al paciente.
La bomba del efluente se autoprograma con la suma de todos los líquidos de tratamiento más el balance deseado para el paciente. Si por ejemplo ponemos 1000 de diálisis y 800 de reposición con un balance deseado de -100, la bomba del efluente trabajará a 1900ml/h. Toda la programación del tratamiento siempre será dinámica, puesto que el paciente agudo es muy cambiante y requiere que se adapte el monitor a su situación concreta16.
Situaciones de alarma en los circuitos de técnicas continuas. Cuidados enfermerosEn la implantación y mantenimiento de los circuitos descritos en el apartado anterior, existen medidas de seguridad que ayudan en el manejo y optimización de estos tratamientos.
Es necesario conocer las alarmas que indican los eventos más importantes y actuar en consecuencia, para que el tratamiento sea efectivo y minimizar los riesgos asociados.
Todas las casas comerciales introducen una clasificación dentro de los monitores en la que se incluyen diferentes niveles de alarma. Se describirán aquí estos niveles que, según el monitor pueden recibir distintos nombres, pero que, en general, podrán clasificarse en: «alarmas de aviso», alarmas de «precaución», alarmas de «mal funcionamiento del equipo» y alarmas de «advertencia». Es usual que se clasifiquen por importancia y se dé un tono acústico y un color de aviso diferente según el grado de importancia de dichos eventos (color verde, color ámbar o color rojo).
Si se diera el caso de que confluyen a la vez varias alarmas en el sistema, el monitor priorizará la de más importancia, señalando esta en la pantalla principal y requiriendo su resolución inmediata. Solucionada esta, aparecerá la de un valor inferior y así sucesivamente.
Se enumerarán aquí alguno de estos casos, por orden de menor a mayor importancia, ofreciendo la actuación oportuna en cada caso.
Alarmas de aviso. El paciente no corre peligro, no se detiene ninguna bomba, ni de líquidos ni de sangre. Este podría ser el caso de avisos relacionados con el mantenimiento del monitor o bien que el set que se puso en su día requiere cambio por exceso de tiempo de funcionamiento. El tratamiento pues, no se detiene y el operador ha de optar por una decisión que solo depende de él. Este tipo de avisos pueden repetirse durante el tratamiento, dependiendo del tipo de monitor y del evento en sí.
Alarmas de precaución. En este caso sigue activa la bomba de sangre (eventualmente y, según el monitor, también la de jeringa), pero se detienen el resto de las bombas de líquidos, que son las que realizan el tratamiento pautado en el sistema. Este sería un ejemplo claro en la finalización de una bolsa de líquidos que se ha de cambiar por una nueva o bien la bolsa del efluente que debemos vaciar. El operador intervendrá directamente sobre el tratamiento, ya que está detenido. No existe riesgo de coagulación del sistema porque no se ha detenido la bomba hemática.
Este tipo de actuaciones que requieren parar las bombas de líquidos, podrán elegirse (si no se ha activado aún la alarma oportuna) accediendo a la opción «cambio de bolsas». Esta opción detiene todo el tratamiento y deja funcionando la bomba hemática. De esta forma, se podrá vaciar la bolsa del efluente o poner bolsas de tratamiento nuevas. Es una buena opción en situaciones de aislamiento del paciente, si la bolsa ya estaba a punto de activar una alarma.
Alarmas de mal funcionamiento. Este tipo de alarmas se provocan cuando de algún modo el monitor no puede asegurar un tratamiento óptimo. Puede darse el caso de errores en el balance de líquidos por afectación de las balanzas o bien problemas mecánicos en los rotores de bombas. Estas incidencias son muy ocasionales, pues los monitores realizan un diagnóstico previo que asegura la funcionalidad de todo el equipo. No obstante, es preciso saber que cuando ocurre alguna eventualidad de este tipo, es necesario retornar la sangre al paciente y elegir otro monitor para reiniciar la terapia hasta que técnicamente se resuelva el problema que generó la alarma.
Alarmas de advertencia. Estas son las alarmas que requieren intervención inmediata porque el riesgo de pérdida hemática es muy alto, ya que generan la detención de la bomba de sangre. Esto supone que tenemos poco tiempo para solucionarlas por estar relacionadas con la coagulación de todo el sistema extracorpóreo. Debido a la importancia de este tipo de alarmas, describiremos algunas de ellas más detenidamente y su potencial solución:
1. Aire en sangre. Como hemos de recordar, el detector de aire en la línea hemática está situado en la zona próxima al caza venoso y genera activación del clamp que asegura la protección del paciente frente a una embolia gaseosa. La intervención en este caso está relacionada con la subida del nivel del caza y el ajuste del nivel de sangre por encima del detector de aire. Algunos monitores disponen de dispositivos que ayudan a realizar esta función.
2. No se detecta retorno. El sensor que activa esta alarma es P3, situado generalmente en el caza venoso. Si la sangre va a poca velocidad o bien el catéter genera poca resistencia en este tramo, puede haber una presión de retorno muy cercana a cero que el monitor no es capaz de diferenciar de una eventual desconexión de esa línea. Por esta razón, la actuación ha de estar dirigida a aumentar la presión en este punto. En algunos casos es preciso aumentar la velocidad de la bomba de sangre, pero siempre ha de valorarse de forma interdisciplinar ya que no en todos los tratamientos es aconsejable hacerlo así, sobre todo en el caso de anticoagulción con citrato.
3. No se detecta entrada. Tiene el mismo origen que la alarma anterior, pero en este caso relacionada con P1. Si es muy cercana a cero, el monitor avisa que no se puede distinguir de una eventual desconexión y requiere generar mayor presión negativa. La resolución pasa por aumentar el flujo de sangre. Igualmente, no debe realizarse esta acción sin estar seguros de que es la única solución y si esta es compatible con el tratamiento del paciente.
4. Presión P1 excesivamente negativa. El sensor que nos avisa de esto se sitúa antes de la bomba de sangre y detecta que hay un problema de flujo en ese punto. La actuación que requiere es revisar el catéter en esa rama y la línea que sigue hasta la bomba hemática. Puede haberse pinzado la línea, puede hacer pared el catéter en el vaso o puede haber algún coágulo en ese tramo. Todos ellos son factores que pueden afectar al flujo de sangre según esté programada la bomba hemática. En este caso, es preciso revisar la línea de sangre antes de la bomba y asegurar su correcta posición, alineación con el catéter, etc. Al mismo tiempo, es posible rotar el catéter para liberarlo de la pared del vaso.
5. Presión transmembrana fuera de rango. Esta alarma, junto con «presión prefiltro alta», son ejemplos de advertencias sobre la posible coagulación del filtro que requieren intervención directa sobre la valoración de coágulos en el sistema y la necesidad del retorno de sangre al paciente. Hay que puntualizar aquí que los problemas en el catéter o en el caza venoso, de no ser solucionados a tiempo, pueden provocar la activación de esta alarma sin que el filtro esté coagulado. La presión detectada por el sensor de retorno es captada retrógradamente por el sensor prefiltro.
Después de ver todo el conjunto de actuaciones que se requieren en estos tratamientos, podemos afirmar que si la enfermera de UCI está preparada para el montaje, mantenimiento e interpretación de cada una de las incidencias que se produzca durante el tratamiento del paciente portador de este tipo de técnicas, su seguridad será mayor y no cabe duda que evolucionará mejor17–19.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.