Las terapias depurativas renales en situaciones agudas son de uso habitual en las unidades de cuidados intensivos (UCI). Los principios utilizados para la sustitución de la función renal son: la convección, difusión y adsorción. La adsorción ha sido descrita como un principio efectivo para depurar sustancias tóxicas en la sangre mediante el uso de membranas y sorbentes añadidos a circuitos extracorpóreos. El control de los mediadores proinflamatorios («tormenta de citoquinas») en el paciente séptico o de las toxinas urémicas unidas a proteínas están en investigación mediante estas técnicas depurativas adsortivas. La capacidad de estas terapias de eliminar endotoxinas y citoquinas en pacientes con o sin lesión renal aguda, las convierten en medidas complementarias para tener en cuenta en el soporte vital de los pacientes críticos. Actualmente, se han desarrollado las siguientes terapias adsortivas: MARS, Cytosorb®, CPFA, OXIRIS® y Seraph®. Las enfermeras de cuidados críticos son las encargadas de implementar, vigilar y controlar todo el proceso depurativo, por lo que su formación y conocimientos son fundamentales para el éxito de estas terapias.
Renal depurative therapies in acute situations are commonly used in intensive care units (ICU). The principles used for the replacement of renal function are convection, diffusion, and adsorption. Adsorption has been described as an effective principle for removing toxic substances from the blood using membranes and sorbents added to extracorporeal circuits. The regulation of pro-inflammatory mediators (“cytokine storm”) in the septic patient or protein-bound uraemic toxins is under investigation using these adsorptive depurative techniques. The potential of these therapies to eliminate endotoxins and cytokines in patients with or without acute kidney injury make them complementary interventions to be considered in the life support of critically ill patients. Currently, the following adsorptive therapies have been developed: MARS, Cytosorb®, CPFA, OXIRIS® and Seraph®. Critical care nurses are responsible for starting, monitoring, and managing the complete purification procedure, so their training and knowledge are essential for the success of these therapies.
La probabilidad de sufrir una lesión renal aguda (LRA) es muy variable y tiene una prevalencia del 7-18% en pacientes ingresados en hospitalización y hasta el 50% de los pacientes ingresados en cuidados intensivos1,2. Esta probabilidad se ve incrementada por las distintas comorbilidades del paciente, principalmente la edad, la hipertensión arterial y la diabetes3. Otro de los factores que influyen a la hora de desarrollar episodios de LRA son la sepsis, las intoxicaciones y la tormenta inflamatoria4,5. Una vez establecido cualquier proceso patológico, el retraso en la detección y en la aplicación de medidas puede desembocar en una mayor mortalidad, mayores secuelas y aumento de la estancia hospitalaria6.
Una de las circunstancias que se ha observado como factores predisponentes en el deterioro de los pacientes críticos es la presencia de sustancias en el torrente sanguíneo que se convierten en nocivas para el organismo, como pueden ser las toxinas urémicas unidas a proteínas o una respuesta proinflamatoria desproporcionada denominada tormenta de citoquinas7–9. Ambas sustancias se convierten en agresores a tejidos y órganos que provocan un empeoramiento del paciente crítico10,11.
Una estrategia utilizada para eliminar estos agresores ha sido la prescripción de flujos altos en las terapias depurativas superiores a los valores comunes de 20-35 mL/kg/h en los pacientes sépticos4,12–14. El objetivo de esta técnica estudiada como hemofiltración de alto flujo (HFHV) es la retirada de los mediadores inflamatorios de pequeño y mediano tamaño (5-60 kDa), aumentando la convección y añadiendo las propiedades adsortivas de las membranas15. La técnica se puede realizar, de manera continua o de manera intermitente, en forma de «pulsos» con flujos de 50-70 mL/kg/h durante 24 h o 100-120 mL/kg/h durante cortos periodos de cuatro a ocho horas, respectivamente16. Estudios como el IVOIRE de Joannes-Boyau et al. incrementaron los flujos hasta 70 mL/kg/h sin encontrar diferencias significativas respecto a la mortalidad a los 28 días17. Actualmente no existe evidencia de que sea beneficioso, y además conlleva el riesgo de provocar un dialitrauma relacionado con sustancias de pequeño tamaño, como los iones18,19.
Otro método para eliminar o modular la respuesta inflamatoria ha sido desarrollar las técnicas adsortivas. La adsorción es un fenómeno físico y químico por el cual un sólido o líquido atrae y retiene en su superficie gases, vapores, líquidos o sustancias disueltas. Este proceso puede ser utilizado para fijar en la superficie de las membranas de los circuitos extracorpóreos sustancias que no pueden ser eliminadas por su tamaño (mayor que los poros de las membranas disponibles), como pueden ser las toxinas urémicas fijadas a proteínas o las citoquinas20. Otro planteamiento utilizado ha sido la adición a sistemas extracorpóreos de filtros con capacidades adsortivas, que son capaces de eliminar sustancias fijadas a proteínas mediante la presencia de sistemas con alta disponibilidad de albúmina21. En aquellas sustancias que van liberadas en el plasma se han desarrollado técnicas con la presencia de plasmafiltros específicos previos a los cartuchos adsortivos. Estos cartuchos tienen la propiedad de provocar una detoxificación por adsorción13. Otros sorbentes, como la resina, han sido eficaces para facilitar la eliminación de sustancias, por ejemplo, de tóxicos biliares en el fallo hepático22,23.
Elemento de especial interés en las técnicas adsortivas es la afinidad de las propias membranas, en los circuitos extracorpóreos, por determinadas sustancias. De manera general, las cualidades de las membranas deben ser: una alta biocompatibilidad, durabilidad, amplia superficie, alta permeabilidad a solutos y a líquidos y bajo precio. Los polímeros se han constituido como elementos adecuados a estos objetivos20. Los más utilizados han sido el polimetacrilato de metilo, poliacrilonitrilo y polietilamina24,25. De manera específica para las técnicas adsortivas, son elementos de interés la afinidad, la carga eléctrica y que el tamaño del poro de la membrana sean los adecuados para las sustancias que pueden quedar adsorbidas en la propia superficie de la membrana4,24,26. Actualmente se siguen desarrollando estudios para encontrar qué materiales son los más adecuados para potenciar las capacidades adsortivas de las membranas, con elementos que atraigan las distintas moleculas20,27. Uno de los elementos incorporados a las membranas ha sido la polimixina B, que ha demostrado beneficios en el tratamiento de pacientes sépticos como una menor mortalidad a 28 días del grupo intervención. La polimixina B se ha añadido a las membranas debido a que es un péptido que destruye la membrana de las bacterias gramnegativas15,19. La adsorción de sustancias por los circuitos extracorpóreos se convierte por tanto en un reto de la investigación.
IndicacionesLas indicaciones de las terapias adsortivas son de dos tipos: de causa no renal y de causa renal.
Dentro de las indicaciones no renales está la eliminación del torrente sanguíneo de la mayor cantidad de mediadores que puedan inducir respuestas inflamatorias desadaptativas, modulando la tormenta inflamatoria. Esta cascada inflamatoria genera reacciones adversas potenciadas por el propio sistema inmune que se asocia a daños en distintos órganos del cuerpo. Los principales responsables de esta situación son altas concentraciones de citoquinas en el torrente sanguíneo15. Las citoquinas que más se han estudiado que influyen en estas respuestas desadaptativas son: linfoquinas (producidas por los linfocitos), monokinas (producidas por los monocitos), quimiocinas (producidas por células activas químicamente), interleucinas (IL)(producidas por leucocitos) y el factor de necrosis tumoral α (TNF-α)8.
Durante la pandemia de COVID-19, la necesidad de controlar las citoquinas se ha visto reforzada ante los hallazgos de distintos estudios, en los que pacientes críticos con esta enfermedad desarrollaban respuestas proinflamatorias desproporcionadas28. Las terapias adsortivas se han comprobado como unas técnicas depurativas que posibilitan la retirada de estos mediadores proinflamatorios del torrente sanguíneo27,29. Ante el desconocimiento de cómo actuar ante esta nueva enfermedad, se tuvieron que adaptar recomendaciones de expertos30,31. Ronco et al. recomendaba la posibilidad de utilizar las membranas y sus capacidades adsortivas para controlar y eliminar esta respuesta inflamatoria desproporcionada30. En estudios previos se tenía la constancia de que las terapias adsortivas y la retirada de citoquinas provocaban los siguientes beneficios: disminución de la dosis de catecolaminas, descenso de los niveles de procalcitonina y del ácido láctico, descenso en los valores de la escala Sequential Organ Failure Assessment Score (SOFA), aumento de la presión arterial media y un descenso de los niveles plasmáticos de las siguientes IL: IL-1, IL-4, IL-6 e IL-1010,19,30,32.
Por su parte, dentro de las indicaciones renales, las terapias adsortivas están centradas como la convección y la difusión, en eliminar los productos de desecho metabólicos. La adsorción dentro de esta indicación se utiliza también en la eliminación de toxinas urémicas unidas a proteínas que son difíciles de eliminar por convección y difusión9,24,33. Además, en esta indicación, se han utilizado membranas con alta capacidad adsortiva para la disminución de la sintomatología de los síndromes urémicos11.
Por todo lo expresado anteriormente, es necesario para el personal de cuidados críticos conocer los principios fisicoquímicos y las indicaciones de las técnicas adsortivas utilizadas en las unidades de cuidados intensivos (UCI).
ObjetivoDescribir las distintas técnicas adsortivas y su utilidad en el contexto del paciente crítico.
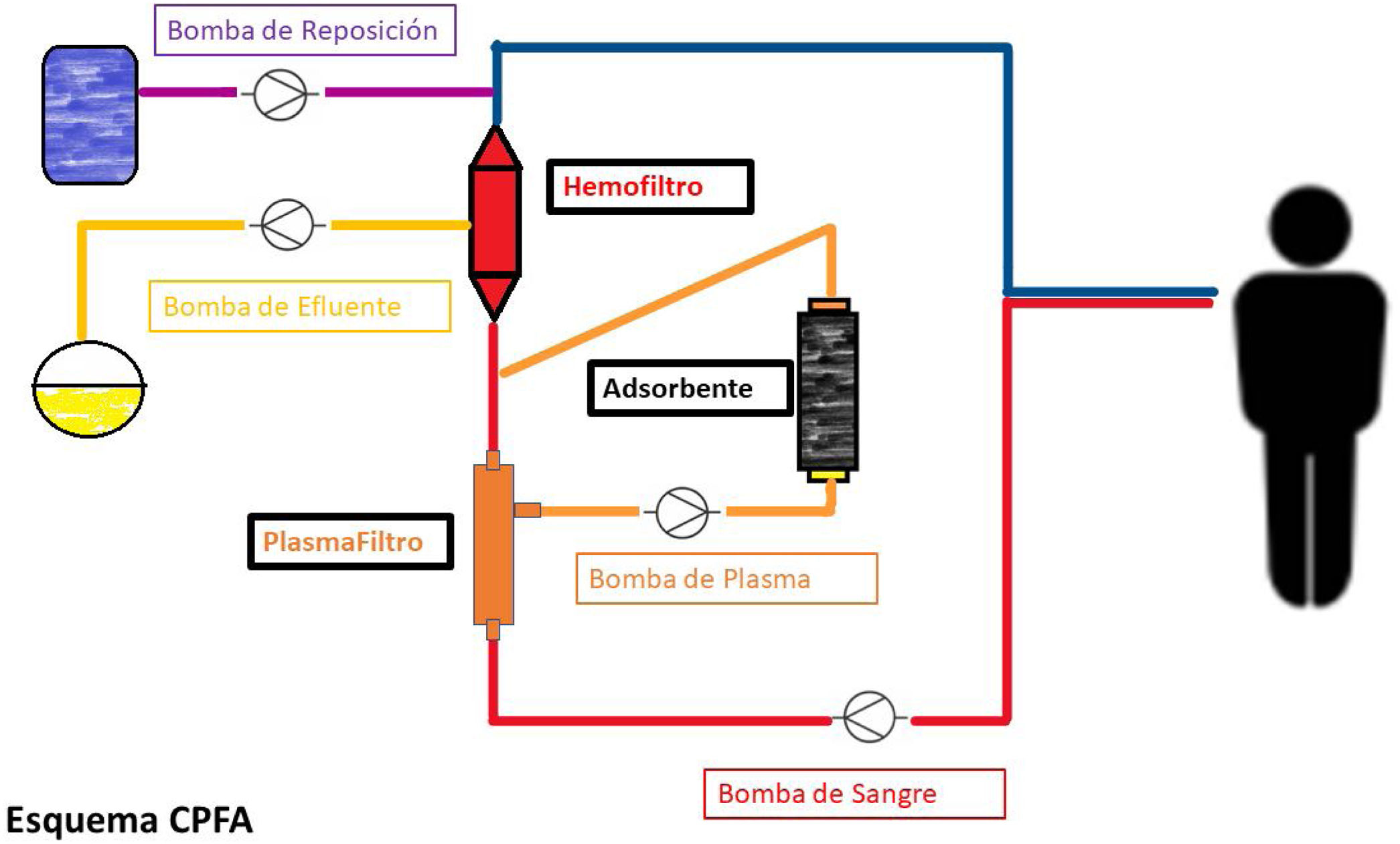
TécnicasFiltración y adsorción de plasma acoplado (CPFA)Esta terapia, denominada en inglés como coupled plasma filtration-adsorption (CPFA), utiliza la filtración de plasma acoplado a adsorbente combinada simultáneamente con hemofiltración. CPFA fue desarrollada con el objetivo de crear un método no selectivo para eliminar mediadores inflamatorios a través de un circuito extracorpóreo que incorporaba un plasmafiltro y un cartucho de resina como adsorbente34. El sistema cuenta con una línea principal y una vía accesoria adsortiva, por donde pasa únicamente plasma para ser detoxificado. CPFA brinda la oportunidad de asociar otras técnicas depurativas donde además se pueda controlar el volumen y la eliminación de pequeñas moléculas a través del ultrafiltrado35. Algunos autores han reportado su uso también en casos de rabdomiólisis36, en pacientes quemados con sepsis y LRA37 y como soporte hasta la recuperación de la función hepática basal con o sin transplante38. La indicación más extendida de esta técnica es durante los procesos sépticos y el síndrome de respuesta inflamatoria sistémica (SIRS)34–36,38.
En el estudio de Livigni et al., a pesar de no tener datos concluyentes al tratar con CPFA a pacientes sépticos, se observó una reducción en la mortalidad en el subgrupo con un mayor volumen de plasma tratado > 0,18 mL/kg/día, odds ratio [OR]: 0,36, intervalo de confianza [IC] 95% [0,13-0,99], p = 0,03334. Para prolongar la duración del circuito en CPFA es preciso incorporar anticoagulación34,35,37,38.
Como se muestra en la figura 1, la sangre pasa primero por un plasmafiltro que separa una parte del plasma. Esta parte del plasma pasará al cartucho de resina adsorbente, uniéndose al resto de la sangre, para seguir un proceso de hemofiltración. Un aspecto importante de esta técnica es el ritmo de la bomba de plasma, que debe estar entre el 10-22% de la bomba de sangre del circuito principal38.
Sistema de recirculación de adsorbente molecular (MARS)El sistema MARS (molecular adsorbent recirculating system) ha sido utilizado para dializar la albúmina. Esta proteína transporta diversas sustancias tóxicas asociadas al fallo hepático. Además de depurar la albúmina, se realiza también depuración de otras moléculas no ligadas a proteínas22,39. En este grupo se encuentran: amoniaco, creatinina y urea. En las sustancias ligadas a proteínas se hallan: ácidos biliares, bilirrubina total e indirecta, ácidos grasos de cadena corta o media y mediadores inflamatorios (IL-6, TNF-α)39,40. Esta técnica depurativa ha sido utilizada principalmente como medida de soporte en el fallo hepático agudo y crónico reagudizado23,39,40.
Especial atención debe ponerse durante esta técnica en los episodios de sangrado, ya que durante la técnica MARS se han observado episodios de alteración de los factores de coagulación. Este hecho es importante de vigilar por las enfermeras de UCI, minimizando la anticoagulación23. Una contraindicación absoluta es la presencia de coagulación intravascular diseminada.
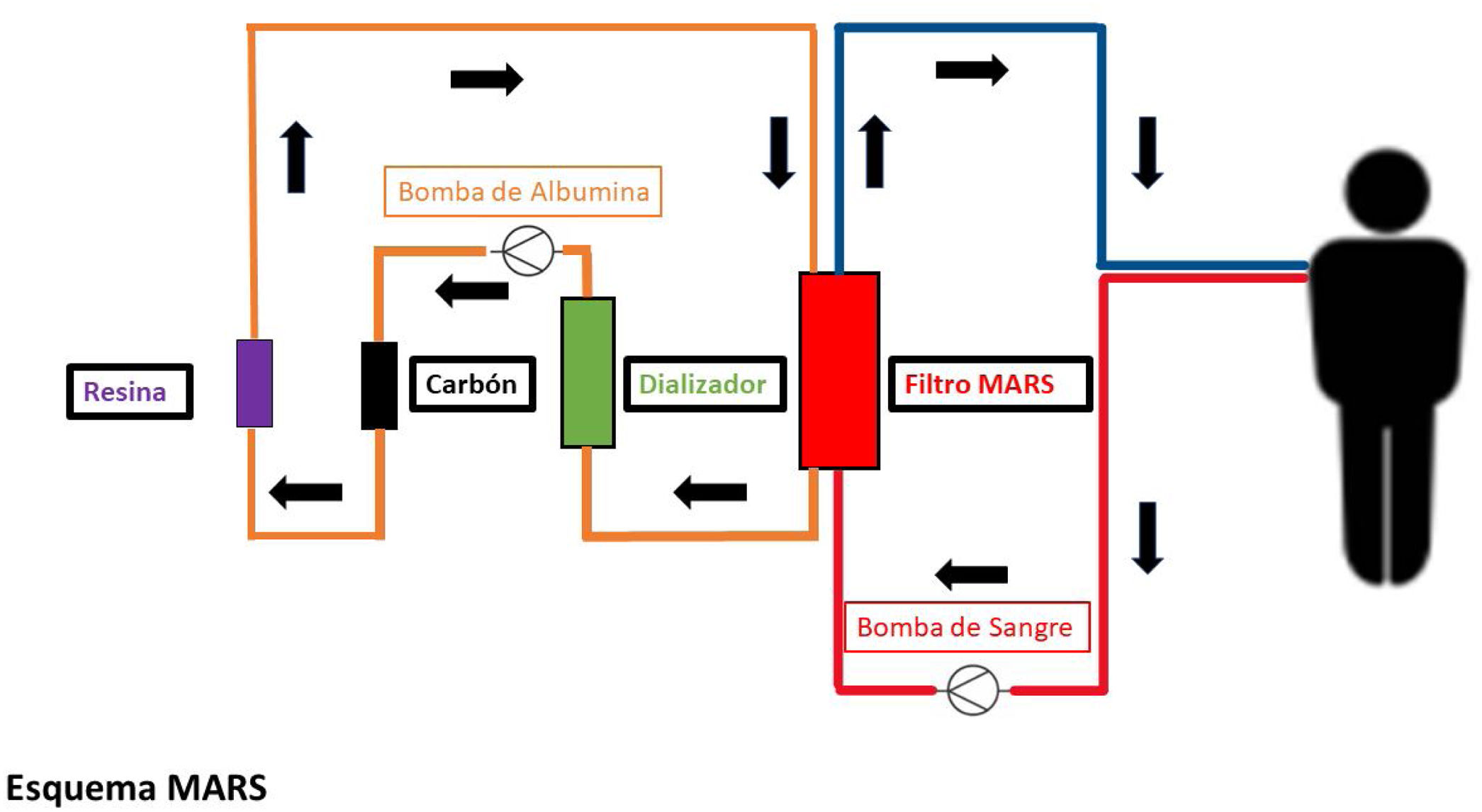
Las sustancias del metabolismo hepático se eliminan mediante una técnica de diálisis con albúmina. El procedimiento consiste en la adición a un sistema extracorpóreo de un sistema que contrapone albúmina entre el 10%-25% a un ritmo variable entre 150-250 mL/min22. El tiempo de duración de esta terapia es entre cuatro a ocho horas. El sistema MARS está compuesto por tres compartimentos diferenciados (fig. 2):
- •
Compartimento 1 (sanguíneo): el circuito extracorpóreo conecta el paciente mediante un catéter de doble luz a un filtro de dializador de alto flujo, y a través de este se pone en contacto la sangre con la albúmina y se produce el intercambio de toxinas.
- •
Compartimento 2 (dialítico): la albúmina del circuito transporta las toxinas hasta un dializador de bajo flujo, donde se eliminarán mediante difusión las sustancias de pequeño tamaño porque entran en contacto con un líquido de diálisis.
- •
Compartimento 3 (adsortivo): la albúmina posteriormente pasa por una columna de carbón activado y, posteriormente, por una de resina, donde se regenera y vuelve al filtro para continuar recaptando toxinas.
Los compartimentos 2 y 3 forman un circuito cerrado de aproximadamente entre 500-600 mL de albúmina (concentración de albúmina variable), que desarrolla el proceso depurativo adsortivo y difusivo.
Los resultados de distintos estudios lo han verificado como una medida de soporte segura y factible23,41. La coagulación de los filtros ha sido el mayor inconveniente de este tipo de terapias. Gilg et al. han usado anticoagulación regional con citrato al aplicar esta técnica sin presentar mayores complicaciones42. Estos autores hallaron en pacientes con fallo hepático poshepatectomía una mortalidad a 60 y 90 días, menor de la esperada al aplicar MARS42.
Cytosorb®Esta técnica adsortiva es denominada por la marca comercial de la membrana. Esta membrana compuesta por perlas de poliestireno divinilbenceno es biocompatible y hemocompatible con una baja resistencia al flujo sanguíneo y altamente porosa20. La membrana tiene una alta afinidad con sustancias hidrofóbicas de hasta 55 Kd, rango que ocupan la mayoría de las citoquinas43. La eliminación de las citoquinas es concentración dependiente, a mayor concentración mayor rapidez en la adsorción20,44. En estudios in vitro, se ha constatado que este sistema no adsorbe endotoxinas45. La técnica consiste en la incorporación de un filtro adsortivo de 300 mL a una terapia extracorpórea como pueden ser la hemodiafiltración39,44,46 o ECMO47. A pesar de este hecho debe ser considerado como una terapia autónoma de las anteriores.
Desarrollado como un sistema de hemopurificación, sus mayores experiencias están centradas en la retirada del torrente sanguíneo de citoquinas para el control del shock séptico y el síndrome de respuesta inflamatoria desadaptativa19,47. La retirada de las citoquinas contribuye al descenso de las necesidades de catecolaminas8. Paul et al. encontraron una mayor supervivencia en los pacientes sépticos a los que se les aplicó esta técnica de manera precoz (primeras 24 h de ingreso en UCI)48. Mehta et al. observó estos mismos hallazgos, pero determinando su inicio precoz en un período anterior a las 48 h de ingreso en UCI49.
Este filtro al adaptarse a otros sistemas extracorpóreos se utiliza en línea, con lo cual no precisa de una bomba de sangre específica50. La recomendación actual es que el ritmo de la bomba sea superior a 150 mL/minuto47. Los distintos estudios recomiendan la anticoagulación para mantener la funcionalidad de la membrana. Si el sistema en el cual se acopla ya posee una anticoagulación no es preciso una específica. Si no fuera así, debe plantearse la anticoagulación47.
Sus principales indicaciones son aquellas subsidiarias de una modulación de la respuesta inflamatoria, como por ejemplo: síndrome de respuesta inflamatoria sistémica (SIRS), shock séptico, politraumatismos, rabdomiólisis, grandes quemados y pancreatitis severas19,44,47,48,51.
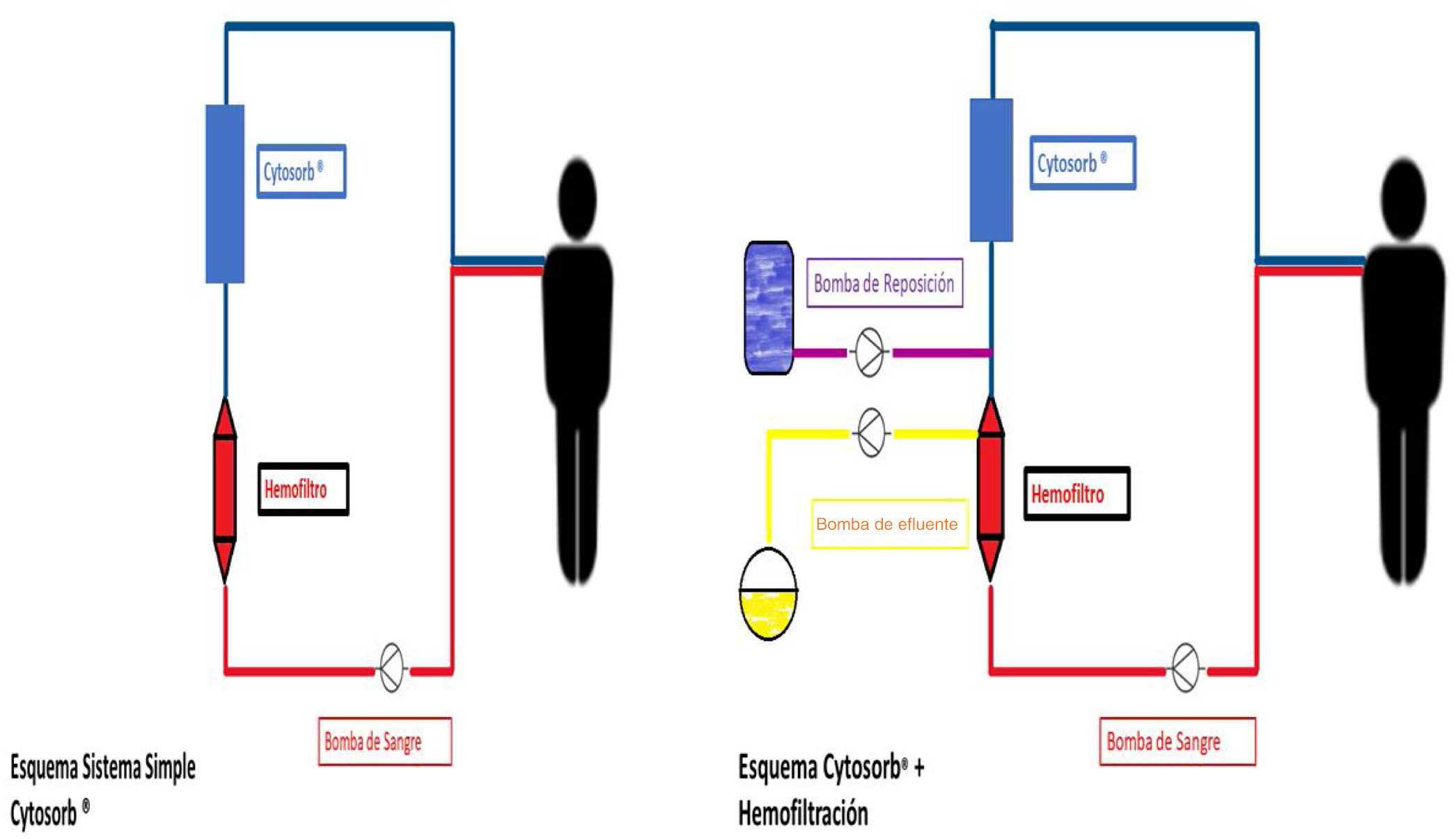
En la figura 3 se muestra el sistema Cytosorb® en dos presentaciones posibles. En la primera, un sistema simple donde el circuito extracorpóreo traslada en un único lineal la sangre pasando por un hemofiltro y posteriormente, por el filtro Cytosorb® para adsorber las sustancias tóxicas. En el segundo esquema podemos observar cómo a un sistema de hemofiltración se le acopla en la línea de retorno, un filtro Cytosorb® para atrapar las sustancias no eliminables por medio del ultrafiltrado. Schädler et al. observaron una eliminación entre el 5-18% de niveles sanguíneos de IL-6 al aplicar la técnica durante seis horas al día durante siete días, recomendando la técnica cuando los niveles de IL-6 son elevados debido a que la adsorción de la membrana es concentración dependiente51.
Oxiris®La terapia adsortiva Oxiris® se constituye como un desarrollo de la membrana AN69 que estaba compuesta por acrilonitrilo y metalil sulfonato de sodio52, y a la que se le ha añadido polietilenimina cargada positivamente para adsorber endotoxinas cargadas negativamente53 e incorporando heparina en su membrana interna20. Este filtro combina las terapias de hemofiltración, con las propiedades de eliminación de mediadores inflamatorios, citoquinas y endotoxinas45. Broman et al. observaron en pacientes sépticos con fallo renal tratados con terapia depurativa continua renal con Oxiris®, una disminución significativa de los niveles sanguíneos de TNF-α, IL-6, IL-8 y IFNγ (interferón)53. Esta reducción fue significativa al comparar dos grupos, uno con terapia estándar y otro, con Oxiris®. Esta terapia repercutió en una menor dosis de noradrenalina en el grupo intervención a partir de las cuatro horas de tratamiento y se prolongó las 24 h siguientes53. En este mismo sentido, Tan et al. reportan una disminución de medidas de soporte tras utilizar el filtro Oxiris® en un paciente séptico54. Wei et al. reportan un caso clínico de sepsis abdominal que se benefició de esta terapia como medida de soporte con buenos resultados, consiguiendo la estabilización en 80 h25; sin embargo, se precisan más estudios multicéntricos y aleatorizados para poder generar evidencias clínicas55. Por otra parte, Malard et al. observaron una capacidad adsortiva de hasta el 68% de endotoxinas y más de un 90% de citoquinas en estudios in vitro a los 120 min de inicio de la terapia45. Actualmente, los expertos determinan que la población diana de esta terapia deben ser los pacientes sépticos con fallo renal5.
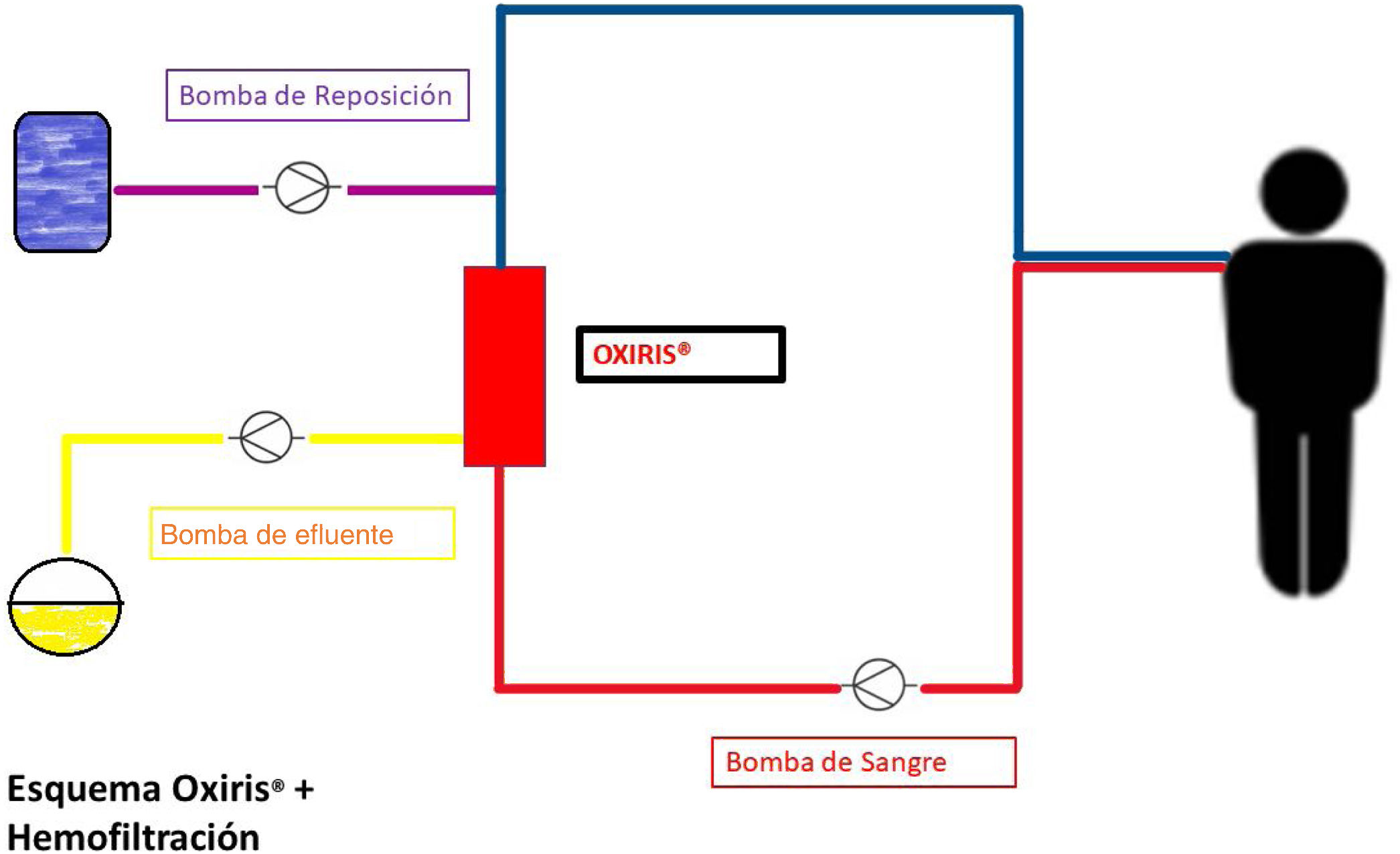
En la figura 4 podemos observar el montaje del sistema Oxiris®, en este caso es preciso destacar que el hemofiltro y la membrana adsortiva son la misma, una única membrana con dos funciones que lleva a cabo procesos difusivos, convectivos y adsortivos.
Esta terapia también ha sido incluida en las posibles recomendaciones para luchar contra la pandemia COVID-1930,31. Los primeros estudios indican un comportamiento similar a otras entidades infecciosas, con un descenso de valores sanguíneo de IL-6 y buenos resultados a corto plazo27.
Seraph100®La membrana Seraph100® es un filtro específico para la reducción de microorganismos en el torrente sanguíneo durante septicemias y que ha sido probado ante bacterias, virus, hongos, parásitos y toxinas.
Este filtro está formado por perlas de polietileno recubiertas de heparina. Debido a que múltiples microorganismos utilizan los glicosaminoglicanos para unirse a las células y tejidos, la apariencia de la heparina similar al heparán sulfato permite captar esos microorganismos10. Este filtro se monta en línea con otros circuitos extracorpóreos y puede ser utilizado como terapia única o complementaria56. El descenso de microorganismos se ha observado significativo en períodos de terapia de 240 min57.
Además se ha observado in vitro que su utilización no elimina significativamente los antibióticos y drogas que se utilizan en los pacientes sépticos58, exceptuando a los aminoglucósidos para los que sí se observó una reducción de niveles plasmáticos del 20% en la medición de los primeros cinco minutos59. Otros estudios han encontrado capacidad adsortiva eficaz frente a: S. aureus, S. marcescens, A. baumannii, E. faecalis, E. coli, CMV, C. albicans60.
Actualmente, a pesar de no haber sido desarrollado para tratar el COVID-19, algunos casos clínicos han observado la disminución de la carga viral61–63. Kelly et al. presentaron su uso en dos casos clínicos con unos resultados de disminución de la necesidad de soporte respiratorio tras aplicar esta terapia64. Más estudios son precisos para indicar sus usos clínicos e indicaciones62.
Cuidados de las técnicas adsortivasLas terapias adsortivas son cada vez más habituales en las UCI, por lo que la actuación de las enfermeras es de vital importancia. Las enfermeras de UCI son responsables del inicio, mantenimiento y finalización de las terapias extracorporeas65. Su formación en este tipo de técnicas mejoran los resultados asistenciales66.
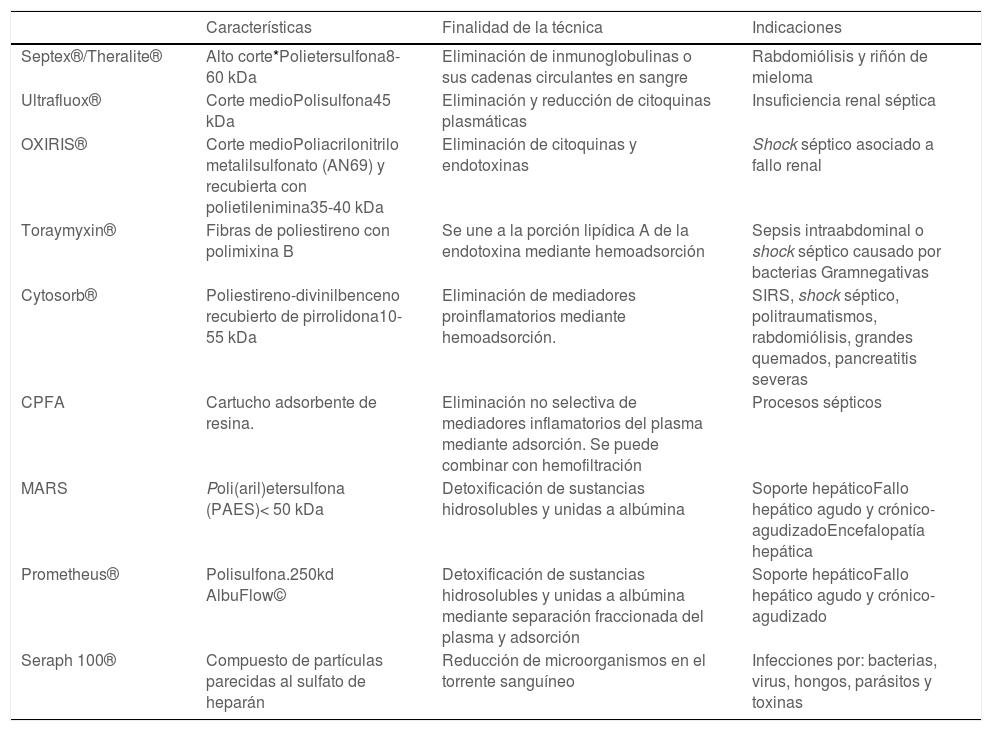
Antes de iniciar este tipo de terapias es preciso conocer los objetivos, características y la duración del tratamiento (tabla 1). Si el sistema de adsorción tiene vías accesorias o se añaden membranas a otros sistemas, es necesario comprobar el purgado de todos los sistemas y compartimentos, corroborando su adecuada conexión. Es de especial interés que las bombas de plasma en el caso que las hubiera nunca superen los porcentajes relacionados con la bomba de sangre. Los flujos de bomba de sangre deben estar ajustados a cada una de las distintas terapias adsortivas.
Tipo de membranas adsortivas
| Características | Finalidad de la técnica | Indicaciones | |
|---|---|---|---|
| Septex®/Theralite® | Alto corte*Polietersulfona8-60 kDa | Eliminación de inmunoglobulinas o sus cadenas circulantes en sangre | Rabdomiólisis y riñón de mieloma |
| Ultrafluox® | Corte medioPolisulfona45 kDa | Eliminación y reducción de citoquinas plasmáticas | Insuficiencia renal séptica |
| OXIRIS® | Corte medioPoliacrilonitrilo metalilsulfonato (AN69) y recubierta con polietilenimina35-40 kDa | Eliminación de citoquinas y endotoxinas | Shock séptico asociado a fallo renal |
| Toraymyxin® | Fibras de poliestireno con polimixina B | Se une a la porción lipídica A de la endotoxina mediante hemoadsorción | Sepsis intraabdominal o shock séptico causado por bacterias Gramnegativas |
| Cytosorb® | Poliestireno-divinilbenceno recubierto de pirrolidona10-55 kDa | Eliminación de mediadores proinflamatorios mediante hemoadsorción. | SIRS, shock séptico, politraumatismos, rabdomiólisis, grandes quemados, pancreatitis severas |
| CPFA | Cartucho adsorbente de resina. | Eliminación no selectiva de mediadores inflamatorios del plasma mediante adsorción. Se puede combinar con hemofiltración | Procesos sépticos |
| MARS | Poli(aril)etersulfona (PAES)< 50 kDa | Detoxificación de sustancias hidrosolubles y unidas a albúmina | Soporte hepáticoFallo hepático agudo y crónico-agudizadoEncefalopatía hepática |
| Prometheus® | Polisulfona.250kd AlbuFlow© | Detoxificación de sustancias hidrosolubles y unidas a albúmina mediante separación fraccionada del plasma y adsorción | Soporte hepáticoFallo hepático agudo y crónico-agudizado |
| Seraph 100® | Compuesto de partículas parecidas al sulfato de heparán | Reducción de microorganismos en el torrente sanguíneo | Infecciones por: bacterias, virus, hongos, parásitos y toxinas |
kDa: miles de daltons; CPFA: coupled plasma filtration-adsorption; MARS: molecular adsorbent recirculating system; SPAD: single-step albumin dialysis.
Se debe vigilar el estado general del paciente, sobre todo aquellos signos derivados de una mayor superficie de recorrido de la volemia sanguínea: la frecuencia cardíaca, la temperatura y la tensión arterial. La disminución de los mediadores inflamatorios mediante las técnicas adsortivas tiene como consecuencia la disminución de la necesidad de soporte inotrópico5,25,44. Las enfermeras de la UCI deben tener un control estricto de las complicaciones derivadas de la terapia, tanto en la detección como en la prevención.
Si la etiología para el uso de técnicas adsortivas ha sido un fenómeno séptico, poder valorar la técnica mediante el uso de pruebas complementarias es una herramienta útil10.
Uno de los principales problemas de estas técnicas adsortivas es la unión a la membrana de las propias sustancias y del conglomerado formado por los tóxicos. El concepto de saturación del filtro debe estar presente durante el desarrollo de estas técnicas. Es frecuente el incremento progresivo de las presiones del sistema67. Otra señal de alarma es la presión extremadamente negativa de la línea del efluente en los sistemas que cuentan con hemofiltración. Esto indica que los poros del filtro están siendo obstruidos por las sustancias presentes en la sangre.
ConclusiónLas terapias adsortivas están en continuo desarrollo y actualmente se están llevando a cabo más estudios para evaluar sus indicaciones y recomendaciones específicas. La adsorción se observa como un mecanismo útil a la hora de evitar respuestas desadaptativas durante los episodios de shock. El shock séptico actualmente es la recomendación más consistente de este tipo de terapias.
El papel de las enfermeras de críticos es de vital importancia en el manejo de estas terapias. Deben de tener una especialización en el uso de estas medidas de soporte; además de mantener una actualización constante para reconocer sus indicaciones y cuidados. Una base sólida de conocimientos tanto de los principios fisicoquímicos de las terapias adsortivas como del manejo del monitor se convierten en elementos fundamentales para implementar unos cuidados de calidad.
FinanciaciónEste artículo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.