Formación
Monitorización del paciente en ventilación mecánica
Monitoring of patients on mechanical ventilation
P. Bazan1
E. Paz2
M. Subirana3
Diplomadas en Enfermería
1 Servicio de Medicina Intensiva. Hospital de la Comunidad. Mar del Plata. Argentina
2 Servicio de Cuidados Intensivos de Cirugía Cardíaca. Hospital de Sant Pau. Barcelona. España
3 Servicio de Medicina Intensiva. Hospital de Sant Pau. Barcelona. España.
Correspondencia:
Mireia Subirana
Servicio de Medicina Intensiva
Hospital de Sant Pau
Avda. Sant Antoni Mº Claret, 167
08025 Barcelona
E-mail: msubirana@hsp.santpau.es
RESUMEN
Las manifestaciones de un paciente en insuficiencia respiratoria aguda reflejan el nivel de dependencia, los cuidados que necesita y el soporte ventilatorio mecánico que precisa. Los objetivos de la ventilación mecánica (VM) son corregir la hipoventilación, mejorar la oxigenación y el transporte de oxígeno, y disminuir el trabajo respiratorio. Los cuidados de enfermería que requiere un paciente conectado a VM varían en función de su estado y del modo de ventilación empleado. Cuando una enfermera responsable de un paciente en VM establece un plan de cuidados, identifica los objetivos útiles como instrumento de medida para evaluar constantemente las intervenciones. La monitorización del soporte ventilatorio se incluye dentro de las intervenciones y se encamina a constatar que los objetivos se consiguen. En este artículo se revisan los ítems que nos permiten la monitorización del paciente ventilado desglosada en monitorización general y monitorización respiratoria.
PALABRAS CLAVE
Cuidados respiratorios. Monitorización. Monitorización respiratoria. Ventilación mecánica.
SUMMARY
The clinical situation of a patient with acute respiratoy failure, indicates the level of care and mechanical ventilatory support required. The aims of mechanical ventilation are to correct hypoventilation, improve oxygenation and oxigen transport and reduce the work of breathing. Nursing care of patients under mechanical ventilation varies according to their state and the ventilation mode. When establishing a care plan, nurses identify the objectives, which will be useful to measure the interventions. These interventions include aspects related to monitoring and indicate whether or not the objectives are met. In this article the items that allow monitoring of a patient under mechanical ventilation grouped into general monitoring and respiratory monitoring are reviewed.
KEY WORDS
Respiratory care. Monitoring. Respiratory monitoring. Mechanical ventilation.
INTRODUCCION
Los procesos patológicos que pueden producir fallo respiratorio o ventilatorio ponen de manifiesto signos y síntomas relacionados con la hipoxemia. Signos como la taquipnea, el aumento del trabajo respiratorio, la utilización de músculos accesorios, taquicardia, coloración de la piel y síntomas como la disnea son útiles para el reconocimiento de un episodio agudo. Frecuentemente, si el cuadro agudo evoluciona, se acompañan de cambios en la conducta, objetivándose agitación psicomotriz, agresividad, datos que orientan hacia un estado creciente de hipoxemia. En el paciente crónico los cambios en la conducta que pueden observarse son debidos a la hipercapnia, apareciendo somnolencia, bajo nivel de autoestima y rechazo a la participación activa de su autocuidado. En ocasiones las terapias medicamentosas (broncodilatadores, corticoides, antibióticos, etc.), las no medicamentosas (oxigenoterapia, fisioterapia y mantener la vía aérea superior permeable y bien hidratada), y el soporte integral que ejerce el equipo de enfermería, pueden llegar a estabilizar la función respiratoria e iniciar una mejoría a corto plazo. Otras veces, el deterioro de la función respiratoria, con alteración en la gasometría, incremento del trabajo respiratorio, también de la frecuencia, la disnea y los ruidos agregados en la auscultación de los campos pulmonares y vías respiratorias superiores, presencia de aleteo nasal, dificultad en la expresión verbal por compromiso respiratorio, y la progresiva alteración del estado de conciencia, lleva a requerirse la aplicación de la ventilación mecánica (VM), para cumplir el objetivo interdisciplinario de promover una ventilación cómoda y eficaz, mantener las vías aéreas permeables, suministrar un adecuado flujo y restablecer el intercambio efectivo de gases (1-4).
Los objetivos de la VM son corregir la hipoventilación, mejorar la oxigenación, y el transporte de oxígeno, disminuir el trabajo respiratorio procurando descanso y reacondicionamiento muscular, además del confort del paciente, es decir, de minimizar la disincronia. La magnitud de las manifestaciones refleja el nivel de dependencia de la persona, los cuidados que necesita y permiten ajustar el soporte ventilatorio mecánico a sus necesidades. Cuando una enfermera responsable de un paciente en VM establece un plan de cuidados, identifica los objetivos, los cuales serán útiles como instrumento de medida para evaluar constantemente las intervenciones siendo factor de motivación. La monitorización del soporte ventilatorio se incluye dentro de las intervenciones y se encamina a constatar que los objetivos se consiguen. En este artículo se revisan los ítems que nos permiten la monitorización del paciente ventilado desglosada en monitorización general y monitorización respiratoria en la que se valoran los parámetros respiratorios, el intercambio de gases, la mecánica pulmonar y la sincronía paciente-ventilador (tabla 1) (5-7).
Tabla 1 Monitorización del paciente en ventilación mecánica | |||
| Monitorización general | |||
| * Estado neurológico | |||
| * Estado respiratorio | |||
| * Estado cardiovascular | |||
| * Estado renal | |||
| * Estado gastrointestinal | |||
| Monitorización respiratoria | |||
| Parámetros respiratorios | Intercambio de gases | Mecánica pulmonar | Sincronía paciente-ventilador |
| * FIO2 | * Gasometría arterial | * Trabajo respiratorio | |
| * Frecuencia | * Pulsioximetría | * Compliancia | |
| * Espirometría | * Capnografía | * Resistencias | |
| * Humedad y temperatura | * SvO2 | * Presión de oclusión | |
| * Espacio muerto | * Curvas de flujo y presión | ||
| * Permeabilidad | |||
| * Presión | |||
| * Relación I/E | |||
| * Sensibilidad | |||
| * Alarmas | |||
MONITORIZACION GENERAL DEL PACIENTE VENTILADO
La monitorización general del paciente en ventilación mecánica engloba la valoración del estado neurológico, respiratorio, cardiovascular, renal y gastrointestinal (3,4,8-10).
Dentro del estado neurológico del paciente se incluye la valoración del nivel de conciencia, estado mental, nivel de ansiedad, la presencia de dolor, así como la interpretación de cuál es el estado del paciente en relación al ventilador, si está el paciente respirando cómodamente o al contrario está luchando con el ventilador. En este apartado es importante establecer una comunicación no verbal efectiva para conocer las necesidades del paciente, siempre que su estado de conciencia lo permita.
A nivel respiratorio se debe registrar la frecuencia respiratoria (f) y el patrón respiratorio observando la simetría del movimiento torácico y realizar una auscultación bilateral de los sonidos respiratorios, con la finalidad de detectar si existe evidencia de sonidos adventicios. Para asegurar la permeabilidad de la vía aérea y la adecuada ventilación, además de humidificar y calentar el gas inspirado para evitar la deshidratación del epitelio pulmonar y favorecer la movilización de las secreciones, puede ser necesaria, de forma regular, una adecuada higiene traqueobronquial y fisioterapia respiratoria. Otro aspecto que se detalla ampliamente en el apartado de monitorización de parámetros respiratorios es el control de las presiones en la vía aérea. El empleo de la presión positiva en la vía aérea, incrementa el riesgo de barotrauma y neumotórax, por ello es importante el control de las presiones en la vía aérea, ya que permite asegurar la permeabilidad de la vía aérea y detectar la presencia de fugas. La movilización y los cambios de posición minimizan el acumulo de secreciones, proporcionan una mejor distribución de la ventilación y de la perfusión y previenen el deterioro de la integridad cutánea. También se debe valorar la coloración de piel y mucosas y la temperatura corporal. Finalmente dentro de este apartado se destaca la importancia de la radiografía de tórax en la monitorización del paciente en VM, siempre es más útil si se compara con otras previas, ya que es lo que permite detectar cambios de las alteraciones pulmonares.
Dentro del estado cardiovascular, se valoran la frecuencia cardíaca, sonidos cardíacos, pulsos periféricos, presión arterial, distensión yugular, presencia de edema periférico y oliguria. Se debe tener en cuenta que la presión arterial media puede disminuir durante la ventilación mecánica, de forma especial con el empleo de presión positiva al final de la espiración (PEEP), ya que la presión torácica positiva disminuye el retorno venoso. La monitorización de la presión capilar pulmonar (PCP) permite una aproximación a la presión en aurícula izquierda, refleja la presión hidrostática pulmonar como causa del edema pulmonar y puede ser usada como guía del volumen sanguíneo, de la precarga y del funcionamiento del corazón izquierdo. Cuando un paciente esta en VM, la PCP se debe medir al final de la fase espiratoria del ciclo respiratorio, ya que es lo más cercano a la capacidad residual funcional (CRF). Cuando se emplea PEEP la PCP no refleja la presión de aurícula izquierda. Dentro del apartado de presiones hemodinámicas destacar que se debe monitorizar cuidadosamente la medida del gasto cardíaco, ya que el retorno venoso (precarga), se dificulta con la ventilación a presión positiva.
El estado de la función renal va a determinar el balance de líquidos y de electrolitos. En función del estado del paciente, es importante el control de peso diario, así como el control de entradas y salidas. El mantenimiento de la hidratación y del volumen sanguíneo es esencial en el paciente en VM para evitar la reducción del retorno venoso en presencia de presión positiva intratorácica. La monitorización cuidadosa de la humidificación del gas suministrado por el ventilador impide las pérdidas insensibles por el pulmón.
En la valoración del estado gastrointestinal, el empleo de la SNG, además de ser útil en caso de distensión, permite la monitorización de la secreción gástrica con la finalidad de evitar el sangrado, ya que las úlceras de estrés se asocian a menudo a la VM. El estado nutricional del paciente afecta a la función pulmonar de varias maneras. Los centros respiratorios en el cerebro están influenciados por los índices metabólicos. Las condiciones que reducen el índice metabólico reducen a su vez el estímulo central, y al revés, cuando el índice metabólico está incrementado se produce un incremento de la respuesta ventilatoria. Cuando las demandas energéticas son superiores a los aportes, se produce fatiga y debilidad de los músculos respiratorios (en especial del diafragma y de los intercostales) y esto puede predisponer a un fallo respiratorio. La capacidad vital disminuye progresivamente en el estado catabólico. Una disminución de la resistencia respiratoria se asocia a una disminución de la tensión arterial de oxígeno. Desde el punto de vista nutricional, el objetivo del tratamiento del paciente con insuficiencia respiratoria aguda (IRA) es inducir un estado anabólico. Para ello, es necesario realizar una valoración nutricional al inicio de la IRA, para instaurar el soporte nutricional adecuado que cubra las necesidades individuales del paciente. Para favorecer el tránsito intestinal y prevenir la retención gástrica y su posible regurgitación, siempre que no esté contraindicado, el paciente debe permanecer con el cabezal de la cama incorporado unos 45º.
MONITORIZACION RESPIRATORIA DURANTE LA VM
La monitorización respiratoria supone la monitorización de los parámetros ventilatorios, el seguimiento del intercambio gaseoso y el análisis de la mecánica pulmonar. Requiere además el seguimiento de la patología pulmonar y la prevención y corrección de las posibles complicaciones derivadas de la VM. El estado de la vía aérea superior, la hidratación, permeabilidad y la cantidad y calidad de secreciones, y las posturas de confort o antiálgicas que adopte la persona pueden dar información de su estado pulmonar.
Monitorización de los parámetros ventilatorios
La tecnología de nuevos ventiladores mecánicos nos permite la posibilidad de adquirir información continua, fiable, y de cuantificar el estado funcional respiratorio, siendo ésta una ayuda para el cuidado y el seguimiento de la persona y su patología. Para la monitorización tenemos en cuenta los parámetros que se detallan a continuación y en un posible orden, aunque muchos de ellos se valoran simultanea y dinámicamente (5,8,11-13).
* Fracción inspirada de oxígeno. La fracción inspirada de oxígeno (FIO2) suministrada por el ventilador debe ser comprobada periódicamente para asegurar cuál es la FIO2 que recibe el paciente. Se debe administrar la FIO2 más baja que proporcione una adecuada oxigenación arterial.
* La frecuencia respiratoria (f), parámetro sensible e inespecífico, es el número de ciclos ventilatorios en un minuto, siendo lo normal de 12 a 20 respiraciones por minuto. Se divide en dos fases: inspiratoria y espiratoria; entre ellas existen dos períodos sin modificación de volumen, la pausa inspiratoria y la pausa espiratoria. Los datos que nos brinda la frecuencia respiratoria en relación al tiempo son, el tiempo inspiratorio, que incluye la pausa inspiratoria, el tiempo espiratorio, que incluye a su vez la pausa espiratoria, y la duración del ciclo completo o tiempo total. Monitorizar la frecuencia respiratoria en una persona en VM es importante, especialmente en los modos ventilatorios de sustitución parcial, se debe contabilizar durante un minuto y compararla con la f ajustada. Algunos ventiladores monitorizan de forma separada los ciclos programados y los ciclos respiratorios espontáneos.
* Espirometría: La señal para valorar el funcionamiento del ventilador es el flujo. Su medida se obtiene indirectamente, en algunos ventiladores es el volumen minuto (V.E) y en otros el volumen corriente. Existen equipos que monitorizan volúmenes espontáneos y programados por separado, cuando se emplean técnicas de sustitución parcial. El V.E y el volumen circulante (VT) pueden ser monitorizados directamente de la vía aérea con un espirómetro. Una disminución en el V.E espirado puede indicar fugas en el sistema.
* Humedad y temperatura. Para evitar la deshidratación del epitelio pulmonar y favorecer la movilización de las secreciones el gas inspirado debe ser humidificado y calentado. La humidificación absoluta que han de proporcionar los sistemas de humidificación es de 25 a 35 mg de agua por litro de ventilación; la mayoría de los intercambiadores de calor y humedad (ICH) se adecúan a estos valores. El centro de control de enfermedades de Atlanta aconseja no cambiar los circuitos cuando se utilicen ICH. Cuando se utilizan humidificadores de agua caliente, estudios recientes han demostrado que si no se cambian los circuitos del respirador de forma sistemática, no aumenta la frecuencia de neumonía asociada al ventilador. Cuando utilizamos humidificadores de agua caliente se debe monitorizar la temperatura del gas inspirado y sus alarmas correspondientes, límite superior: 37 ºC y límite inferior: 30 ºC (14-18).
* Medida del espacio muerto. La medición del espacio muerto es útil para valorar que parte de la ventilación interviene en el intercambio de gases. El rango de normalidad del espacio muerto (VD/VT) es entre un 25 a un 40% del VT y aumenta en aquellas patologías que está disminuida la perfusión pulmonar (embolismo pulmonar, hipertensión pulmonar). El espacio muerto se calcula fácilmente a partir del CO2 espirado y de la PaCO2 (tabla 2). En el momento de programar el VT o V.E, en el ventilador se debe tener en cuenta el tipo de ventilador empleado, hay ventiladores que detectan el volumen de gas que permanece en las tubuladuras e incrementan la misma cantidad en el volumen programado; al contrario, hay ventiladores que no contabilizan este volumen (19-20).
| Tabla 2Ecuación clínica del espacio muerto |
| VD/VT = PaCO2 PECO2/PaCO2 |
* Permeabilidad de la vía aérea. Uno de los objetivos del cuidado de la vía aérea es prevenir la obstrucción a través de la aspiración de secreciones y la correcta humidificación. Monitorizar la permeabilidad de la vía aérea comprende la valoración de la calidad y cantidad de secreciones, esto implica el manejo y control de las mismas mediante la auscultación, la vibropercusión y la aspiración. Recordaremos ligeramente lo más importante de estas técnicas.
Para valorar el flujo de aire en el sistema respiratorio del paciente, se auscultan los pulmones e identifican los sonidos respiratorios normales y anormales. La auscultación pulmonar ayuda a detectar la presencia anormal de líquido o moco además de vías aéreas obstruidas. De este modo, puede determinar también el estado de los alveolos y la pleura circundante. Los sonidos respiratorios anormales adventicios básicamente son: crepitantes, roncus, sibilancias y roce pleural (9,21-22).
La vibración y percusión son procedimientos que se llevan a cabo preferiblemente de forma secuencial mientras el paciente se encuentra en la posición de drenaje postural iniciada para el segmento afectado. En ocasiones pueden efectuarse en forma independiente. La percusión, que es más efectiva como tratamiento de las atelectasias y la retención de secreciones, los estudios indican que la velocidad y la fuerza de la percusión no son tan importantes como el ritmo. Algunos investigadores creen que la oxigenación alveolar aumenta durante la percusión y después de ésta. No debemos olvidar las contraindicaciones de esta técnica, entre las que se incluyen la fractura costal, angina inestable, arritmias, hemoptisis, metástasis neoplásicas en costillas, o vértebras, heridas abiertas, broncoespasmo, edema pulmonar. La vibración ayuda a movilizar y desplazar las secreciones hacia la parte superior del árbol bronquial y a espectorarlas de las vías aéreas. Ambos procedimientos se utilizan con precaución en personas con inestabilidad hemodinámica, recuento bajo de plaquetas, corticoterapia, broncoespasmo, neumotórax, tuberculosis o embolia pulmonar (2,4).
Antes de realizar la aspiración de secreciones el paciente debe ser hiperoxigenado (100% de O2 durante más de 30 segundos), hiperventilado (aumentando la f y el V.E o el VT) e hiperinsuflado (utilización del suspiro). Se puede instilar solución fisiológica (SSF) con la finalidad de diluir y movilizar las secreciones, y una vez finalizada la aspiración se mantiene la hiperoxigenación durante más de un minuto. Lerga et al (23) demostraron que la instilación de SSF disminuye los valores de PaO2 sin que se observe un aumento en la cantidad de secreciones. En relación a la metodología para realizar las maniobras de hiperinsuflación e hiperoxigenación, existe controversia. Hay estudios que demuestran que es mejor realizar la hiperinsuflación e hiperoxigenación con el ventilador en lugar de llevarlo a cabo con el ambú, ya que con el ambú se tiene dificultad para administrar el VT, es difícil mantener la FiO2 y la PEEP programada si éste no tiene válvula. Sin embargo, Herce A et al (24), en un estudio realizado en 172 maniobras de aspiración en pacientes postoperados sin lesión pulmonar, comprobaron que el empleo correcto del ambú para hiperinsuflar e hiperoxigenar cuando se comparaba con la hiperinsuflación e hiperoxigenación realizada con un ventilador mecánico tenía las mismas repercusiones en la oxigenación y en la hemodinámica de los pacientes.
El sistema cerrado de aspiración de secreciones puede ser muy útil en pacientes con microorganismos potencialmente contaminantes. Sin embargo, existen estudios que demuestran que pueden producir caídas intermitentes en la presión de la vía aérea en especial cuando la persona está ventilada en volumen control y con flujos bajos, la importancia clínica de esto no está clara (1,3,8). Con la utilización de tubos que permiten la aspiración de secreciones subglóticas y manteniendo la presión de neumotaponamiento superior a 20 cmH2O, Rello et al (25) demostraron una disminución de la incidencia de neumonías asociadas al ventilador de 40% vs el 8% en personas en ventilación mecánica durante los primeros ocho días de su ingreso en UCI.
* Presión en la vía aérea. En los ventiladores ciclados a volumen, una vez se ha ajustado el V.E, la presión en la vía aérea permanece relativamente constante. Un incremento en la presión representa un incremento en la presión necesaria para administrar el volumen programado en el pulmón del paciente. Un incremento el la resistencia de la vía aérea o una disminución de la compliancia pulmonar producen un aumento de presión. Un cúmulo de secreciones, las secreciones densas, broncoespasmos, atelectasias, neumonías con consolidación y el edema pulmonar son ejemplos que pueden producir un aumento de la lectura de presión. La presencia de fugas en el circuito o alrededor del tubo endotraqueal (TET), o una mejora en las condiciones del paciente provocan una disminución de la presión. Es importante el control de la presión el neumotaponamiento cada ocho horas, ya que la presión realizada por el neumotaponamiento sobre las paredes de la traquea es una de las causas más frecuentes de lesión postintubación. Su valor no debe exceder los 25 mmHg de la presión de perfusión capilar de la traquea, y mantenerse entre 18 y 20 mmHg al final de la espiración. Existen tubos que cuando la presión es superior a 25 cmH2O se desinfla el neumotaponamiento y otros que se adaptan al diámetro de la tráquea con la finalidad de evitar lesiones (26,27).
La programación de presión positiva al final de la espiración (PEEP), permite mantener una presión positiva que evita el colapso alveolar al final de la espiración, hecho que repercute en una mejora de la oxigenación al aumentar la CRF.
* Relación inspiración/espiración (I/E). La relación I/E habitual es 1:2 ó 1:3. Los cambios en la relación afectan a la relación ventilación/perfusión (V/Q).
* Sensibilidad o trigger, es uno de los parámetros más importantes, ya que permite al ventilador reconocer el esfuerzo inspiratorio del paciente e iniciar una insuflación. Pueden ser de presión o de flujo (28-29).
* Sistema de alarmas. El concepto de alarma puede definirse como aquel mecanismo que permite alertar la aparición de un suceso, en función de unos límites ajustados por el operador. La importancia de su control reside en el hecho de que de su adecuado funcionamiento depende la seguridad del paciente en VM. Las alarmas nunca deben ser desactivadas (30).
Intercambio de gases
* Gasometría arterial. Para determinar la eficacia de la VM lo más adecuado es tener en cuenta la medición y análisis de la presión parcial de oxígeno en sangre (PaO2). Esta medición se puede realizar cada vez que se realicen cambios en los parámetros del respirador, por la presencia de cambios clínicos en la persona, para seguir su evolución o bien después de procesos de aspiración que interrumpen la integridad del sistema. Es habitual ver que se espere 20 o 30 minutos para realizar gasometría arterial. Estudios recientes demuestran que en el 87% de pacientes con neumonía los cambios más importantes en la PaO2 se producen dentro de los primeros cinco minutos de haber modificado la FiO2, actualmente se aconseja realizar la gasometría arterial diez minutos después de haber realizado modificaciones en los parámetros del ventilador (31).
La PaO2, la SaO2, y el contenido arterial de oxígeno (CaO2), se correlacionan con la FiO2 y con la PEEP. El pH y la PaCO2 se correlacionan con la ventilación minuto.
La hipoventilación, las alteraciones de la relación V/Q y el shunt pulmonar son los motivos fisiopatológicos que comportan un descenso de la PaO2. La hipoventilación mostrará un aumento de la PaCO2 y un descenso de la PaO2, en las alteraciones de la relación V/Q, sucede lo mismo pero si el paciente puede aumentar su V.E sólo se observa hipoxemia. El shunt mostrará hipoxemia y poca respuesta a la administración de oxígeno.
Existen varios índices que permiten cuantificar la capacidad del pulmón para difundir oxígeno, los más utilizados son la diferencia alveoloarterial de oxígeno (A-aPO2), el cociente arterioalveolar de oxígeno (PaO2/ PAO2), y el cociente entre la presión arterial de oxígeno y la fracción inspirada de oxígeno (PaO2/FiO2). La PaO2/FiO2 a pesar de que no tiene en cuenta los cambios de CO2, es la más fácil de aplicar además de ser el índice que se utiliza como uno de los criterios de lesión pulmonar aguda (PaO2/FiO2 < 300) y de SDRA. (PaO2/FiO2<200) (32-35).
* Pulsioximetría. Desde la década de los años setenta la pulsioximetría ha sido uno de los avances más importantes en la monitorización no invasiva de los pacientes críticos. Es un método espectrofotométrico y asume que sólo la sangre arterial pulsátil genera el cambio de absorción de la luz que capta el fotodetector. El pulsioxímetro facilita el manejo de la FiO2 y orienta sobre los cambios que se producen en el paciente. Cuando el sensor está situado en el lóbulo de la oreja, la respuesta a los cambios de FiO2 son más rápidos que si el sensor es digital. Para asegurar la precisión de la lectura se debe verificar que la intensidad de la señal sea adecuada y que la forma de la onda sea repetible. La limitación fisiológica es que sólo es útil para la detección de hipoxia, pero no permite estimar valores altos de PaO2 debido a la curva de disociación de la hemoglobina. Entre las limitaciones técnicas se incluyen todos aquellos factores que interfieran en la detección del pulso o de la cianosis (36,37).
* Capnografía. La capnografía permite medir y monitorizar la concentración de CO2 en el aire espirado (Pet CO2), su empleo es muy útil para analizar la eficacia de la ventilación. La mejor expresión de la ventilación adecuada se obtiene al conseguir niveles imperceptibles de CO2 durante la inspiración y valores elevados, próximos a los de la presión arterial de CO2 al final de la espiración. Los análisis de la diferencia entre la PaCO2 y el valor medio de Pet CO2 junto con el volumen minuto proporciona información sobre la producción de CO2 y permite calcular la relación entre VT y el espacio muerto. La capnografía es más una técnica cualitativa que cuantitativa, ya que la morfología del capnograma en muchas situaciones clínicas da más información que la medida aislada de la Pet CO2(38,39).
SvO2. La saturación venosa mixta expresa la interacción entre la demanda tisular y el aporte de oxígeno. La monitorización continua se realiza con un catéter de fibra óptica colocado en arteria pulmonar. La fiabilidad depende del flujo sanguíneo, el hematocrito o de la distancia de la punta del catéter a la pared vascular (33).
Mecánica pulmonar
* Trabajo respiratorio. El trabajo respiratorio (WOB) se define como el trabajo necesario para vencer las resistencias que ofrece el pulmón y la pared torácica durante la respiración. La medida del WOB sirve para optimizar la VM durante la fase de desconexión y permite detectar el motivo por el cual ciertos pacientes presentan dificultades para ser extubados después de períodos prolongados de ventilación artificial. También permite conocer las características funcionales de los ventiladores y evaluar los efectos terapéuticos de ciertos medicamentos (40).
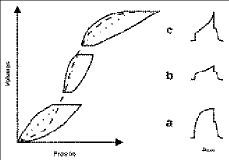
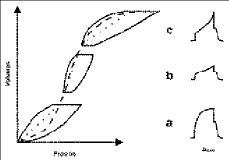
* La compliancia se define como la capacidad de expansión del parénquima pulmonar y de la caja torácica. Se utiliza para valorar la gravedad de la afectación parenquimatosa. El cociente entre el cambio de volumen y la diferencia de presión entre la presión de pausa inspiratoria y la de final de espiración permite calcular la compliancia total del sistema respiratorio. Este valor puede no ser lineal por los aumentos de volumen y en el bucle presión-volumen mostrar la presencia de inflexiones que puede sugerir reclutamiento, orienta del nivel óptimo de PEEP (Fig. 1a) o sobredistensión (Fig. 1c), lo que permite ajustar el VT a la mecánica pulmonar del paciente. Algunos ventiladores realizan la monitorización de la compliancia en forma automática. Estas determinaciones muestran una buena correlación con las realizadas en condiciones estáticas, sólo que no tiene en cuenta la presencia de auto-PEEP (33,40,41).
Figura 1. Representación de un bucle presión-volumen y registro de presión en vía aérea (Paw) en función del tiempo, en tres fases del bucle: a) reclutamiento, b) relación lineal y c) sobredistensión.
Figura 2.Registros de flujo y de presión en vía aérea (Paw). De izquierda a derecha curva de flujo cuadrada, sinusoidal, acelerada y decelerada.
* Resistencias. La resistencia inspiratoria es otra variable fácil de monitorizar durante la VM. Durante la insuflación pasiva a flujo constante se monitoriza la presión pico en vía aérea y la presión de pausa inspiratoria, la diferencia entre ambas se divide por el flujo y se obtiene el valor de la resistencia inspiratoria. La resistencia al flujo es de dos tipos, la causada por el tejido pulmonar y la causada por la vía aérea. Aproximadamente el 80% del total de las resistencias pulmonares son debidas a la resistencia de la vía aérea de gran calibre junto con la que ofrece la vía aérea artificial. La medición de la resistencia pulmonar es útil en la valoración de la respuesta del paciente al tratamiento con broncodilatadores y para monitorizar la evolución del paciente (33,40).
* Presión de oclusión. La presión negativa generada por la contracción de los músculos inspiratorios durante la respiración normal se consume en disipar las resistencias del sistema respiratorio, la presión restante es la que genera el flujo inspiratorio. La medida de la presión con la vía aérea ocluida a los 100 ms de iniciarse la inspiración (P0.1) se relaciona directamente con la descarga del centro respiratorio. Algunos ventiladores realizan de forma automática la medida de la P0.1, ya que es un buen indicador de la evolución de la IRA, de la capacidad del paciente en recuperar la respiración espontanea o del grado de hiperinsuflación dinámica que padece (33,40).
* Curvas de flujo y de presión en vía aérea. La VM implica la entrega de flujo y presión a la vía aérea del paciente con objeto de obtener cambios en el volumen del pulmón, para asegurar una ventilación óptima se requiere la adecuada vigilancia y monitorización del flujo, presión y volumen. La curva de flujo tiene dos partes diferenciadas, la inspiratoria y la espiratoria. La curva de flujo inspiratorio representa la magnitud, duración y patrón de flujo entregado por el ventilador. Existen cuatro tipos de curvas de flujo inspiratorio (Fig. 2). La espiración, al igual que en ventilación espontanea, es pasiva en VM, por lo que la magnitud, duración y patrón de flujo espiratorio vendrá definida por la compliancia y resistencia del circuito y de la vía aérea del paciente. Durante la VM la monitorización de la presión en la vía aérea (Paw), ofrece información muy detallada de la mecánica pulmonar y sirve para activar las alarmas de sobrepresión y desconexión. Las presiones de mayor interés del ciclo respiratorio son la presión pico (Pmax), la presión media (MAP), la presión meseta (Ppl) y la PEEP. La Pmax es la presión que se genera al final de la inspiración y está influida por el diámetro del tubo endotraqueal, la presencia de secreciones en la vía aérea, la magnitud del flujo y la presión de retracción elástica-estática del sistema respiratorio. La Pmax ha sido utilizada como índice para valorar el riesgo de barotrauma, pero actualmente se desestima porque no brinda información de la presión alveolar. Cuando se interrumpe el flujo en el respirador se produce una caída de la Paw debido a la redistribución del volumen en las unidades pulmonares, la presión sigue disminuyendo durante la pausa inspiratoria. La presión medida al final de una pausa inspiratoria de tres segundos es la Ppl y refleja la presión estática del sistema respiratorio. La figura 3 muestra el cambio en la Pmax y en la Ppl de la vía aérea respecto a la línea de base cuando aumenta la resistencia, la magnitud del flujo o disminuye la compliancia del sistema para un mismo VT. La presión media de la vía aérea que calculan de forma automática algunos ventiladores es la más importante, ya que es la responsable de los cambios que el ventilador produce en el intercambio de gases, en las alteraciones hemodinámicas y en la producción de barotrauma. Para detectar la presencia de auto-PEEP, presión positiva al final de la espiración intrínseca del paciente, es preciso realizar una pausa espiratoria de tres segundos (33,40,42).
Figura 3.Registro de presión en vía aérea, presión pico (1) y presión meseta (2) para un mismo VT: a) situación basal, b) resistencias aumentadas, c) aumento de flujo, y d) disminución de la compliancia.
Sincronía paciente-ventilador
La interacción paciente-ventilador puede verse alterada por diferentes factores. A nivel del paciente los factores que interfieren en la sincronía son los relacionados con el centro respiratorio, la mecánica pulmonar y la presencia de hiperinsuflación pulmonar dinámica. A nivel del ventilador, en primer lugar es fundamental el control del aparato para verificar su correcto funcionamiento, prevenir desperfectos y mantener una ventilación cómoda y segura. Los factores que afectan la sincronía paciente-ventilador, relacionados con el ventilador, son el trigger (sensibilidad), el flujo, el VT, la presión inspiratoria y las resistencias del ventilador. En este control se tendrá en cuenta la revisión diaria de los parámetros programados en el respirador, la respuesta del paciente al tipo de ventilación y los niveles de alarmas (43,44).
Para finalizar, destacar el hecho de que las enfermeras de las UCIs dedicamos una gran parte de tiempo a la monitorización del paciente. Esta observación sumamente exhaustiva es muy importante, ya que constituye uno de los componentes del cuidado. La completa integración de la información que recibimos a través de la monitorización, junto con la información obtenida al valorar al paciente de forma holística, permiten ofrecer una atención de enfermería de alta calidad.
AGRADECIMIENTO
Al Dr. Salvador Benito por su inestimable ayuda y soporte.
BIBLIOGRAFIA
1. Gauntlett Beare P, Nyers JL, eds. Valoración de enfermería del aparato respiratorio. En: Principios y prácticas de la enfermería médicoquirurgica. Madrid: Mosby-Doyma libros; 1995. p. 477-97.
2. D''Angelo HH, Chapman M, Schilling JA. Evaluación respiratoria. En: Manual de cuidados respiratorios. Barcelona: Doyma; 1991. p. 26-48.
3. Martin S, Canobbio MM, Vargo E, Fyfe M, eds. Aparato Respiratorio. En: Normas para el cuidado de pacientes. Proceso de enfermería diagnósticos y resultados. Barcelona: Doyma; 1991. p. 245-312.
4. Oto I, Arqué M, Barrachina L. Observación y valoración del paciente con problemas de oxigenación. En: Enfermería Médico-Quirúrgica II, Necesidad de oxigenación. Barcelona: Salvat Editores; 1990. p. 29-40.
5. Slutsky A. ACCP Consensus conference on mechanical ventilation. Chest 1993;104:1833-59.
6. Stewart T, Slutsky A. Mechanical ventilation: a shifting philosophy. Current Opinion in Critical Care 1995;1:49-56.
7. Kéronac S, Pepin J, Ducharme F, Duquette A, Major F. Propuestas para la práctica enfermera. En: El pensamiento enfermero. Barcelona: Masson SA; 1996. p. 75-98.
8. Dolan JT, ed. Therapeutic modalities in the treatment of the patient with acute respiratory dysfunction. En: Critical Care Nurnsing. Clinical management through the nursing process. Philadelphia, F.A: Davis Company; 1990. p. 611-37.
9. Kirton CA. Valoración de los sonidos respiratorios. Nursing; 1997. p. 36-7.
10. Gauntlett Beare P, Nyers JL, eds. Actuaciones de enfermería frecuentes en las alteraciones respiratorias. En: Principios y prácticas de la enfermería médicoquirurgica. Madrid: Mosby-Doyma libros; 1995. p. 499-546.
11. American Association for Respiratory Care. Consensus statement on the essentials of a mechanical ventilators - 1992. Respir Care 1992;37:1000-8.
12. Branson RD, Chatburn RL. Technical description and classification of modes of ventilator operation. Respir Care 1992;37: 1026-44.
13. Jubran A, Tobin MJ. Monitoring during mechanical ventilation. Recent advances in mechanical ventilation. Clinics in Chest Medicine 1996;17:453-73.
14. Shelly MP. Inspired gas conditioning. Respir Care 1992;37: 1070-80.
15. Shelly MP, Lloyd GM, Park GR. A review of the mechanisms and methods of humidification of inspired gases. Intensive Care Med 1988;14:1-9.
16. American Association for Respiratory Care. Clinical practice guideline. Humidification during Mechanical Ventilation. Respir Care 1992;37:1000-8.
17. Dreyfuss D., Djedaïni K, Weber P, Brun P, Lanore JJ, Rahmani J, et al. Prospective study of nosocomial pneumonia and of patients and circuit colonization during mechanical ventilation with circuit changes every 48h versus no changes. Am Rev Respir Dis 1991;143:738-43.
18. Dreyfuss D, Djedaïni K, Gros I, Mier L, Le Bourdelles G, Cohen Y, et al. Mechanical ventilation with heated humidifiers or heat and moisture exchangers: effects on patient colonization and incidence of nosocomial pneumonia. Am J Respir Care Med 1995;151:986-92.
19. Shapiro BA, Peruzzi WT, Templin RK. Evaluación de la ventilación espacio muerto. En: Manejo clínico de los gases sanguíneos. Buenos Aires, Argentina: Editorial Médica Panamericana; 1996. p. 98-104.
20. Subirana M. Mantenimiento y control de los ventiladores mecánicos. En: Net A, Benito S, eds. Ventilación mecánica. Barcelona: Springer-Verlag Ibérica; 1998. p. 333-43.
21. Poser des sondes respiratoires. En: Soins respiratoires. París, France: Vigot; 1981. p. 28-75.
22. Kathleen Soneki Waring. Mantenimiento de las vías aéreas. En: Cuidados Intensivos en Enfermería Nursing photobook. Barcelona: Doyma; 1986. p. 28-43.
23. Lerga A, Zapata MA, Herce A, Martínez A, Margall MA, Asiaín MC. Aspiración de secreciones: estudio de los efectos de la instilación de suero fisiológico. Enferm Intensiva 1997;8: 129-37.
24. Herce A, Lerga A, Martínez A, Zapata MA, Asiaín MC. Aspiración endotraqueal: respirador versus resucitador manual como método de hiperoxigenación e hiperinsuflación. Enferm Intensiva 1999;10:99-109.
25. Rello J, Sonora R, Jubert P, Artigas A, Rue M, Valles J. Pneumonia in intubated patients: role of respiratory airway care. Am J Respir Crit Care Med 1996;154:111-5.
26. Lawin P, Morr-Strahmann U. Intubación prolongada y traqueostomía. En: Cuidados Intensivos 3ª ed. Barcelona, Salvat; 1986. p. 231-45.
27. Subirana M, Jover C, Font A. Cuidados respiratorios del paciente crítico. En: Net A, Benito S, eds. Ventilación mecánica. Barcelona: Springer-Verlag Ibérica; 1998. p. 55-69.
28. Sassoon CSH. Mechanical ventilator desing and function: The trigger variable. Respir Care 1992;37:1056-69.
29. Polese G, Massara A, Poggi R, Brandolese R, Brandi G, Rossi A. Flow-triggering reduces inspiratory effort during weaning from mechanical ventilation. Intensive Care Med 1995;21: 682-6.
30. MacIntyre NR, Day S. Essentials for ventilator-alarm systems. Respir Care 1992;37:1108-12.
31. Solis R, Anselmi C, Lavietes M. Rate of decay or increment of PaO2 following a change in supplemental oxygen in mechanically ventilated patients with diffuse pneumonia. Chest 1993; 103:554-6.
32. Benito S. Monitoring of mechanical ventilation. En: Fraçois Lemaire, Ed. Mechanical Ventilation. Paris: Masson; 1991. p. 159-69.
33. Lemaire F, Bak E, Bento S. Monitorización respiratoria durante la ventilación mecánica. En: Net A, Benito S, eds. Ventilación mecánica. Barcelona: Springer-Verlag Ibérica; 1998. p. 281-92.
34. Shapiro BA, Peruzzi WT, Templin RK. Oxigenación arterial. En: Manejo clínico de los gases sanguíneos. Buenos Aires, Argentina: Editorial Médica Panamericana; 1996. p. 28-48.
35. Artigas A, Bernard GR, Carlet J, Dreyfuss D, Gattinoni L, Hudson L, Lamy M, Marini JJ, Matthay MA, Pinsky R, Spragg R, Suter PM, and the Consensus Committee. The America-european Consensus Conference on ARDS, Part 2. Am J Respur Crit Care Med 1998;157:1332-47.
36. Jubran A, Tobin MJ. Monitoring gas exchange during mechanical ventilation. En: Tobin JM, ed. Principles and Practice of mechanical ventilation. New York: McGraw Hill; 1994. p. 919-43.
37. Ralston AC, Webb Rk, Runciman WB. Potencial errors in pulse oximetry. I. Pulse oximeter evaluation. Anaesthesia 1991; 46:202-6.
38. Boysen PG. The technique of capnography. J Crit Illness 1989;4:53-9.
39. Hess D. Capnometry and capnography: technical aspects, prhysiologic aspects and clinical applications. Respir Care 1990;35:557-76.
40. Tobin MJ, Van de Graaff. Monitoring of lung mechanics and work of breathing. En: Tobin JM, ed. Principles and Practice of mechanical ventilation. New York: McGraw Hill; 1994. p. 967-1004.
41. Benito S. La mecánica pulmonar en el tratamiento ventilatorio. En: Net A, Benito S, eds. Ventilación mecánica. Barcelona: Springer-Verlag Ibérica; 1998. p. 216-25.
42. Macintyre NR. Análisis gráfico de las curvas de flujo la presión y el volumen durante la ventilación mecánica. Madrid: Johnson & Johnson.
43. Ranieri VM, Mascia L, Giuliani R. Patient-ventilator interaction: Physiology or the triggering function. En: JL Vincent, Ed. Yearbook of Intensive Care and Emergency Medicine. Berlin: Springer; 1995. p. 115-26.
44. Dick CR, Sassoon C. Patient-ventilator interactions. Clinics in Chest Medicine 1996;17:423-38.