INTRODUCCIÓN
El hospital de Navarra es el centro sanitario de referencia de la comunidad foral de Navarra para la patología neuroquirúrgica.
El manejo de los traumatismos craneoencefálicos graves (TCEG) en general y de los que presentan una hipertensión intracraneal (HIC) en particular, es uno de los desafíos más importantes en el manejo del paciente neurocrítico1.
Se entiende como TCEG el paciente con una puntuación en la escala de coma de Glasgow (anexo 1) < 8 puntos posreanimación, o deterioro neurológico en la fase aguda. Se considera, a efectos de este protocolo, como «fase aguda» la primera semana después del accidente. Como primera semana se considera el tiempo trascurrido desde el accidente (hora 0 hasta las 168 h de éste)1.
La mortalidad, aproximadamente del 50%2, y la morbilidad del paciente con un TCEG están asociadas de forma altamente significativa al aumento de la presión intracraneal (PIC) en la fase aguda del traumatismo, lo que demuestra que la HIC es el indicador que mejor define el pronóstico de estos pacientes3.
El compartimiento intracraneal contiene un volumen más o menos constante, que está constituido por 3 elementos importantes: cerebro (80%), líquido cefalorraquídeo (LCR) (10%) y sangre (10%). A medida que la masa intracraneal aumenta, se produce un desplazamiento del LCR seguido por el compartimiento cerebral vascular como mecanismo de compensación para mantener una PIC dentro de los límites normales (Principio de Monroe-Kelly)2-5.
La PIC se expresa normalmente en mmHg. Se acepta que en posición decúbito lateral o supino normalmente es < 20 mmHg. En los pacientes que tengan una craniectomía descompresiva ósea > 5 cm, el umbral debe bajar a 15 mmHg1.
La monitorización de la PIC permite calcular la presión de perfusión cerebral (PPC), que es una relación matemática diferencial de la presión arterial media (PAM) y la PIC. Así, el tratamiento del TCEG se debe dirigir no sólo a controlar la PIC sino en especial a restaurar una PPC adecuada (PPC >= 60)1.
Existen diversas técnicas o cuidados de enfermería, necesarios y habituales en estos enfermos, que aun realizándolos correctamente, pueden provocar un aumento de la PIC6-8, como son: el aseo diario, los cambios posturales, la aspiración de secreciones (AS), etc.
Diversos autores recomiendan la creación de nuevos protocolos para minimizar las complicaciones derivadas de la técnica de AS, como la hipoxemia, la hipercapnia y el aumento de la PIC con la consiguiente disminución de la PPC7,9,10.
En nuestra unidad, se viene observando que la PIC aumenta con la AS, y en algunos casos llega a sobrepasar los límites normales, por lo que se precisa tratamiento para disminuirla.
Las recomendaciones publicadas por las guías de práctica clínica de la Brain Trauma Fundation11 incluyen como medidas de primer nivel para el tratamiento de la HIC la utilización de bloqueadores neuromusculares.
Por todo esto, se planteó si los relajantes musculares (RNM) podrían utilizarse como medida preventiva de HIC ante la aspiración de secreciones; y este fue el objetivo de nuestro estudio.
MATERIAL Y MÉTODOS
Se recogieron datos sobre pacientes ingresados en la unidad de cuidados intensivos (UCI) del Hospital de Navarra durante el año 2004. El tamaño de la muestra fue de 13 pacientes, de los cuales 9 eran varones y 4 mujeres, con edades comprendidas entre los 15 y los 72 años. Tenían una valoración neurológica ( 8 puntos en la escala de Glasgow y, por lo tanto, precisaron intubación orotraqueal y conexión a ventilación mecánica. Estaban sedoanalgesiados para una puntuación de 6 en la escala de Ramsay (anexo 2). Llevaban canalizada una arteria para monitorización (monitor: Fujitsu computers®. Siemens SC 8000) de la presión arterial (catéter arterial: Leader-Cath Vyon®, set de presión arterial: Casa Edwars®) y portaban un catéter de PIC intraparenquimatosa (catéter de PIC: Codman® MicroSensor Skull Boltkit Metal. Codman a Johnson a Johnson Company. Monitor de PIC: ICP Express Codman) y, por lo tanto, podíamos obtener valores sobre su PPC.
El criterio de inclusión de pacientes en el estudio fue: todo el que lleve catéter de PIC intraparenquimatoso y que se encuentre dentro de las primeras 36 h poscolocación. Según las guías de tratamiento de la Brain Trauma Fundation1,3,11, la monitorización de la PIC está indicada en:
1. TCE grave (TCEG) + tomografía computarizada (TC) craneal anormal al ingreso.
2. TCEG + TC craneal normal + 2 o más de las siguientes características al ingreso:
Edad mayor de 40 años.
Respuesta motora anormal uni o bilateral.
Presión arterial sistólica (PAS) < 90 mmHg.
3. La monitorización no está indicada como rutina en pacientes con TCE leve-moderado, aunque queda en manos del clínico la decisión en pacientes con lesiones ocupantes de espacio (LOE).
Los criterios de exclusión fueron:
Embarazo.
Edad < 14 años.
Relajación muscular en perfusión continúa.
Que se precise de otra aspiración endotraqueal durante el intervalo de 2 h entre ambas aspiraciones del estudio.
El manejo del paciente durante la recogida de datos se encaminó a no realizar manipulaciones innecesarias que lleven a un aumento de la PIC por causas no relacionadas con la AS. Por tanto, el paciente tuvo la cabecera elevada 30°, la cabeza alineada con el cuerpo, en posición neutra, para evitar su rotación y flexión para no obstruir el retorno venoso a las yugulares, así como evitar la flexión extrema de la cadera y, en caso de cirugía descompresiva, no realizar presión sobre la zona craniectomizada1,12-14. Tanto la recogida de datos como las actividades que incluyen la manipulación del paciente, las realizaron 2 enfermeras de la unidad (siempre una de ellas componente del grupo investigador), así se limitaban variaciones en el seguimiento del protocolo.
Con estas medidas se pretendió no introducir sesgos y asegurar que la única causa de elevación de la PIC durante la AS sea la propia aspiración.
La metodología del ensayo consistió en considerar a cada individuo como caso y control al mismo tiempo, practicándole 2 AS, separadas 2 h una de otra; una de ellas previa prefusión en bolo del RNM y otra sin él. La administración del RNM en la primera o segunda aspiración se realizó de forma aleatoria. Cuando en la primera AS se administró el relajante, se dejó un período de blanqueo que se corroboró mediante train of four (TOF) (anexo 3), que debía dar un valor de 4/4 para asegurarnos que no hubiera acción del RNM. En ambos casos el paciente estaba correctamente sedoanalgesiado.
Los agentes utilizados para la sedoanalgesia fueron: Diprivan® y cloruro mórfico o midazolam y cloruro mórfico, que al anular los estímulos nocioceptivos permiten conseguir una adecuada protección cerebral, y ayudan en la prevención y tratamiento de la HIC15.
El RNM que se utilizó fue el besilato de cisatracurio (Nimbes®) ya que se utiliza bajo criterio médico en este tipo de pacientes y cumple las características del bloqueador neuromuscular ideal.
El RNM ideal debería ser de inicio rápido, duración intermedia y predecible para uso en perfusión continua, no presentar efectos cardiovasculares ni en el sistema nervioso autónomo deletéreos, no producir liberación de histamina, metabolismo independiente de función renal o hepática y tener metabolitos inactivos16,17.
Según las recomendaciones del laboratorio GlaxoSmithKline, S.A.18 y de los intensivistas consultados, la dosis de besilato de cisatracurio que se usó fue de 20 mg; dosis con la que se consiguió en un tiempo de 5 min una respuesta de 0/4 en el TOF (relajación muscular completa, que produjo la parálisis del diafragma, previno la tos, el hipo y los movimientos respiratorios).
La recogida de datos se llevó a cabo durante los turnos de tarde y noche, ya que es en este momento cuando las condiciones son óptimas por haber menor acúmulo de actividades en torno al paciente.
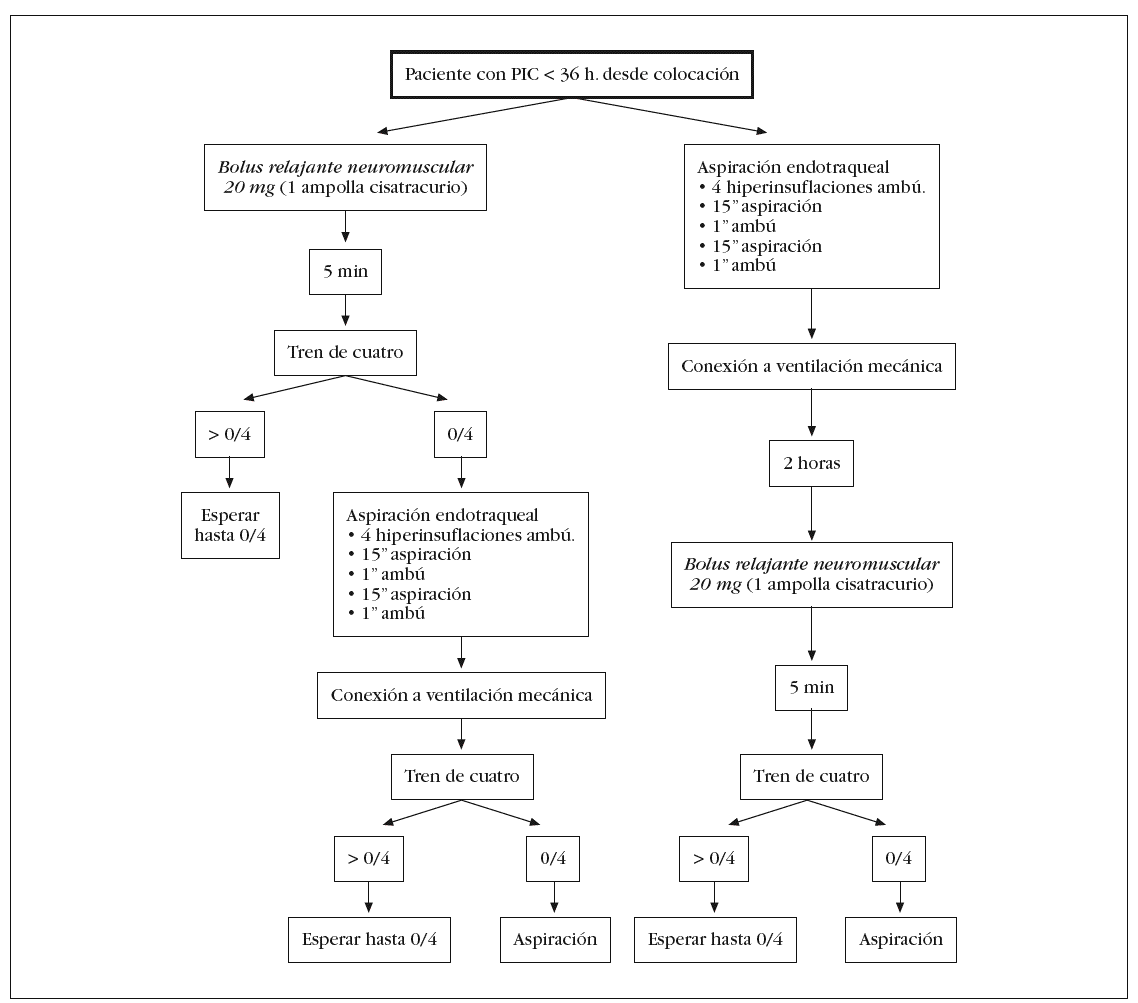
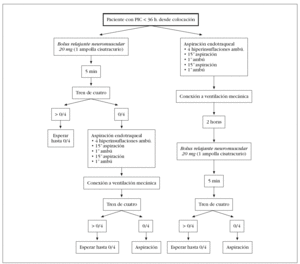
En este momento se puede proceder a la AS siguiendo el siguiente protocolo (fig. 1):
Figura 1.
Selección de sonda de aspiración de tamaño adecuado: la sonda no debe ser más grande que la mitad del diámetro del tubo endotraqueal19-21. En el estudio se utilizaron sondas PharmaPlast® del calibre 14 Fr para tubos endotraqueales < 8 mm y de 18 Fr para tubos de diámetro > 8 mm.
Ajuste de aparato de aspiración (Vacutrán®) a 120-150 mmHg.
Hiperoxigenar al paciente con bolsa resucitadora (Resucitador Ambú® Mark III y bolsa completa de 1.500 ml) conectada a O2 de pared a 15 l para conseguir FiO2 al 100% mediante 4 respiraciones hiperinsufladas. Esto lo realizó una segunda persona que nos ayudó en la técnica para poder presionar el Ambú® con las 2 manos19-21. Se tuvo en cuenta si el paciente tenía un valor de presión positiva al final de la espiración (PEEP) > 5 cmH2O prefijado en el ventilador, en cuyo caso se colocó una válvula que realiza esta función en el Ambú®.
Introducir la sonda hasta que se encuentre resistencia, luego retirarla 1 cm19. Aplicar aspiraciones intermitentes mediante la válvula de la sonda. Rotar la sonda lentamente a medida que se retira. El paso completo de aspiración puede realizarse de manera segura por un período de hasta 15 s sin incurrir en serias caídas de la oxigenación. Cada oclusión intermitente de la válvula no durará más de 5 s, a continuación se ventilará al paciente durante 1 min19 (12 respiraciones hiperinsufladas) y se volverá a introducir la sonda, para posteriormente volver a ventilar al paciente durante 1 min antes de proceder a la reconexión al ventilador20,21.
Durante este proceso se recogieron los siguientes datos: PIC, PAM reconexión al ventilador. También se recogieron valores séricos de sodio, temperatura, datos relacionados con los parámetros prefijados en el ventilador (FiO2, volumen minuto, frecuencia respiratoria, PEEP) así como datos gasométricos (Ph, paO2, paCO2).
El análisis estadístico del estudio se llevó a cabo con la comparación de medias para datos apareados mediante las pruebas t de student o test de Wilcoxon, según la variable siga o no una distribución normal. El paquete informático que se utilizó fue el SPSS 11.0. El nivel de significación estadística aceptado fue del 5%.
Dilemas éticos
La realización de este trabajo (se trata de un ensayo clínico en seres humanos) podría plantear dilemas éticos como también sucede en la práctica asistencial. Así, tras obtener la aprobación del Comité Ético del Hospital de Navarra y cumplir los criterios éticos de la Declaración de Helsinki de 1975 (enmendada en 2000)22, se elaboró un documento de consentimiento informado que se entregó a un familiar responsable, junto con una detallada explicación oral a cargo del investigador que realizaría el posterior ensayo.
Así, una vez firmada la autorización/negación de este documento, el paciente ingresaba, o no, de manera voluntaria en el estudio.
RESULTADOS
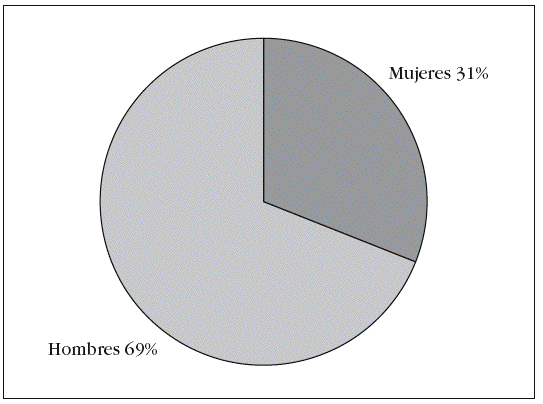
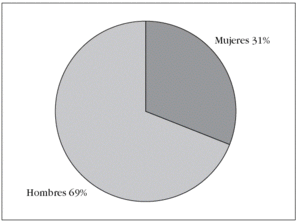
Se estudiaron 13 pacientes con una edad media de 42,46 años y una desviación estándar (DE) de 21,65, de los cuales el 69% eran varones (edad media, 46,44 años; DE = 22,19) y el 31% mujeres (edad media, 33,5 años; DE = 20,21) (fig. 2).
Figura 2. Distribución por sexos.
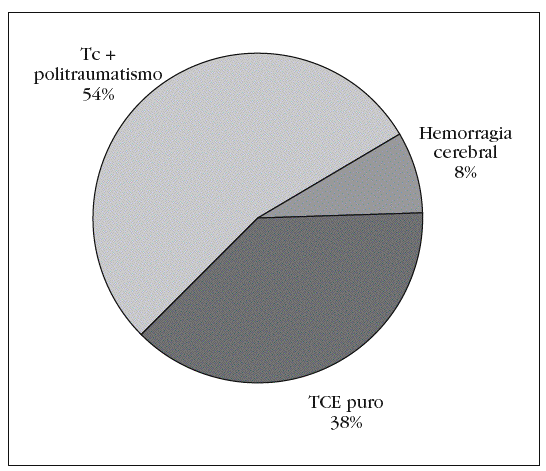
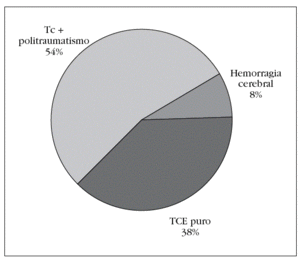
Figura 3. Distribución por diagnósticos.
Los pacientes se clasificaron en 3 grupos según fueran TCE puro: grupo I; TCE + politraumatismo: grupo II, y hemorragia cerebral: grupo III. Atendiendo a esta clasificación, el 38% de los pacientes pertenecieron al grupo I el 54% al grupo II y el 8% al grupo III (fig. 3).
El 77% de los pacientes se sometió a cirugía descompresiva, mientras que el 23% restante no la pre cisó.
En el 54% de los casos se utilizaron inotrópicos para mantener la PPC; el inotrópico de elección fue la noradrenalina en todos los casos. El 46% restante no requirió inotrópicos.
Para alcanzar un Ramsay de 6 puntos se utilizó, en un 38% de los casos, la combinación de midazolam + cloruro mórfico, en un 31% propofol + cloruro mórfico y en el mismo porcentaje únicamente propofol.
El valor del sodio en los pacientes de nuestro estudio se encontraba entre 135 y 148 mEq/l.
El rango de temperatura registrado fue 35,7 a 38,2 °C.
Fallecieron durante su estancia en UCI 2 pacientes (15%).
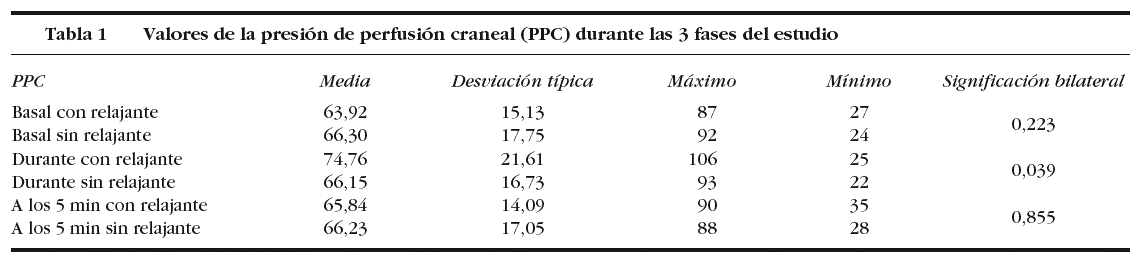
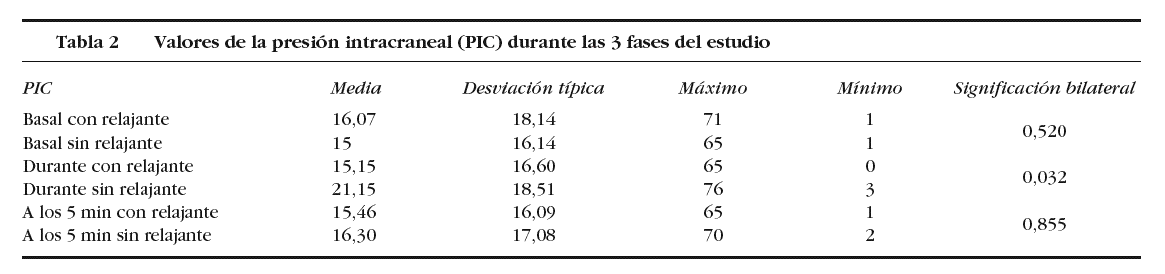
Las características descriptivas de la muestra según los valores que adopta la PIC y la PPC se adjuntan en las tablas 1 y 2.
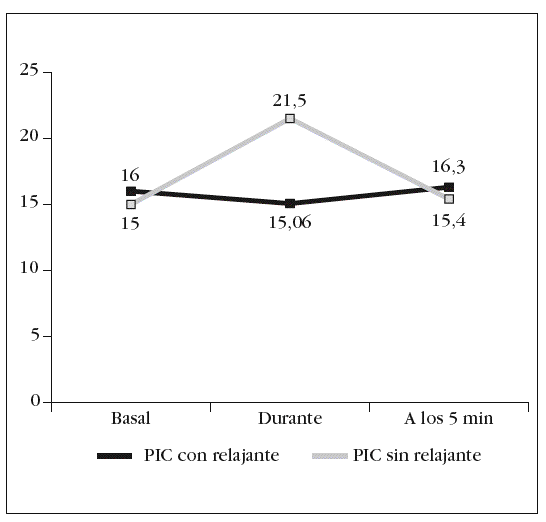
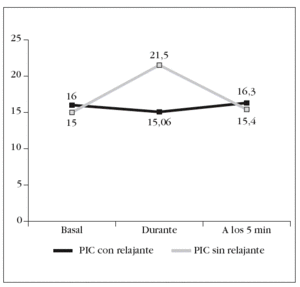
Al comparar los valores de la PIC durante la AS, con administración de RNM y sin ella, se han obtenido valores estadísticamente significativos (p = 0,032) (fig. 4).
Figura 4. Variación de la presión intracraneal (PIC) durante las 3 fases del estudio.
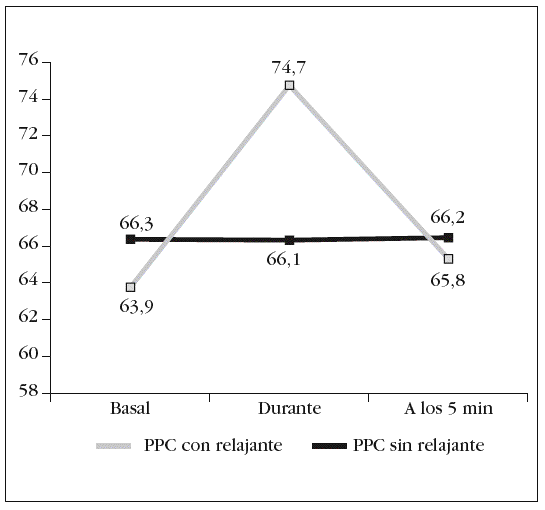
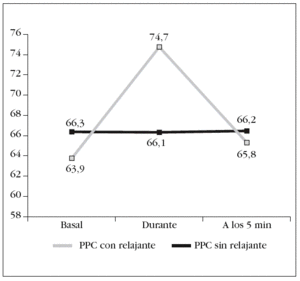
Figura 5. Variación de la presión de perfusión cerebral (PPC) durante las 3 fases del estudio.
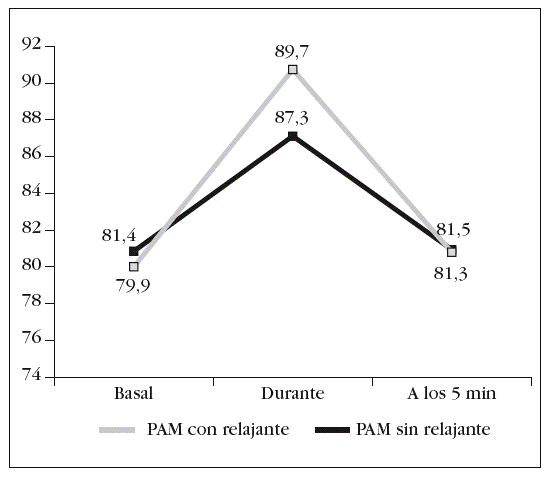
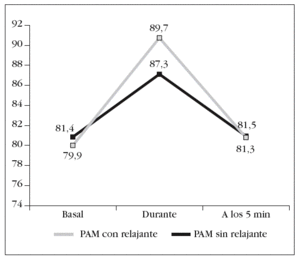
Figura 6. Variación de la presión arterial media (PAM) durante las 3 fases del estudio.
Asimismo, fue durante la AS cuando la PPC alcanzó diferencias significativas (p = 0,039) al comparar las AS con RNM con las que se efectuaron sin él (fig. 5).
Por el contrario, no se hallaron diferencias estadísticamente significativas en los valores de PAM en ninguna de las fases del proceso de AS (fig. 6).
Al comparar las PIC basales y las obtenidas 5 min después de la reconexión al ventilador, no se encontró significación estadística entre el grupo con RNM y sin él (p = 0,520 y p = 0,286, respectivamente).
Al igual que ocurrió con la PIC, las diferencias de PPC basales y 5 min después de la reconexión al ventilador tampoco fueron estadísticamente significativas cuando se administró el RNM (p = 0,223 y p = 0,855, respectivamente).
En cuanto a los valores gasométricos referidos a la paO2 hubo diferencias estadísticamente significativas (p = 0,030) al comparar las cifras basales y a los 5 min cuando se utilizó RNM; no se encontró significación estadística cuando éste no se utilizó (p = 0,064).
No se obtuvo significación estadística en los va lores de paCO2 en ninguna de las fases del proceso de AS.
DISCUSIÓN
La supervisión y el control de la PIC y la PPC dentro de los límites normales, es un objetivo inmediato en el cuidado de los pacientes con lesión traumática o hemorrágica severa del cerebro, para prevenir el daño cerebral isquémico secundario a estas le siones23.
Distintos autores confirman la relación existente entre diversas actividades de enfermería, entre ellas la AS y variaciones en la hemodinámica sistémica y cerebral. Así Arribas et al8, mostraban elevaciones de la PIC durante la AS y una recuperación de los valores basales de ésta < 5 min.
Vivanco et al7 también reflejan las elevaciones durante la higiene corporal y los cambios posturales del paciente, además de durante la AS, al igual que el trabajo publicado previamente por Rising24. Los resultados obtenidos por Murillo y Castellano9 contradicen los estudios anteriores y afirman que durante la AS los pacientes no experimentaron un aumento de la PIC.
Gemma et al25 reflejan una elevación de la PIC durante la AS de 2 mmHg por encima del valor potencialmente patológico en pacientes bien sedados y de 13 mmHg en pacientes con sedación insuficiente. En los pacientes correctamente sedados observaron un aumento de la PPC durante la AS, mientras que en los que no recibieron sedación suficiente la PPC disminuyó, aunque nunca por debajo del límite normal, resultado similar al obtenido por Brucia J et al26.
En nuestro trabajo también se evidencia un incremento de los valores de PIC, que alcanza rangos patológicos (PIC media = 21,15 mmHg) en los pacientes que aún estando bien sedoanalgesiados no habían recibido RNM para la AS. Sin embargo, en estos pacientes la PPC no presenta apenas modificaciones y semantiene dentro de las cifras terapéuticamente aceptadas debido a un aumento de la TAM. Cuando nuestros pacientes recibieron el bolo de cisatracurio, la PIC no aumentó respecto de su valor basal y se mantuvo en una media de 15 mmHg durante la AS, mientras que La PPC subió una media de 11 mmHg.
Durante la aplicación de la técnica la PAM subió tanto en los pacientes relajados como en los que no lo fueron, y era más evidente en los primeros (fig. 6).
Si se compara nuestro estudio con el de Kerr et al27, se obtienen resultados similares a pesar de que los catéteres utilizados para la monitorización de la PIC fueron distintos y el RNM que utilizaron fue el vecuronio. Mientras que en su estudio, el 20% de los casos no habían recuperado los valores basales trascurridos 10 min desde la AS, en nuestro trabajo el 100% de los pacientes retornaron a ellos a los 5 min de finalizar el proceso.
En relación con las cifras gasométricas, se obtuvieron valores más bajos de paO2 cuando se había utilizado el RNM; sin embargo, se puede encontrar la justificación en que los parámetros del ventilador habían variado en algunos casos, y se administraron concentraciones más bajas de oxígeno (disminución de FiO2).
CONCLUSIONES
Por lo expuesto hasta ahora, se puede concluir que la AS es un estímulo suficientemente importante como para causar una elevación de la PIC que alcance valores patológicos. Además, la sedoanalgesia adecuada de los pacientes, pese a ser imprescindible, no es suficiente para evitar episodios de HIC.
El bloqueo neuromuscular se ha mostrado como una técnica eficaz de prevención de episodios de HIC ante una técnica de enfermería como la AS, y además mejora la PPC durante la ejecución de ésta.
La presencia de estudios que advierten acerca de los efectos secundarios del uso continuado de RNM (polineuropatía, alargamiento de conexión a ventilación mecánica, incremento de las complicaciones pulmonares, etc.) además de la imposibilidad de realizar un examen neurológico completo bajo el efecto del relajante27,28, nos hacen ser cautos a la hora de plantear estandarizar este procedimiento debido a la falta de evidencia científica sobre sus resultados a largo plazo.
La investigación acerca de técnicas de AS eficaces pero inocuas para este tipo de pacientes es un reto para el futuro de la enfermería intensiva. Además, la variabilidad existente entre instituciones sobre el manejo y control de la HIC deben seguir motivando la investigación de las medidas que, conocidas o no, sean a la postre las más beneficiosas para nuestros pacientes.
AGRADECIMIENTOS
Agradecemos la colaboración desinteresada del Dr. José Roldán Ramírez (médico adjunto de la UCI del Hospital de Navarra) por la ayuda técnica prestada.