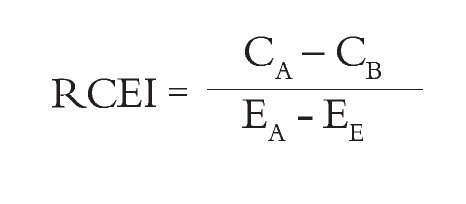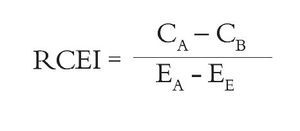¿INTRODUCCIÓN
La neutropenia es la complicación hematológica más grave de los pacientes con cáncer durante el tratamiento con quimioterapia mieloablativa.1,2 Esta complicación puede llevar a diferentes consecuencias, como el retraso en la continuación del tratamiento antineoplásico o el desarrollo de una infección sistémica.3 Se conoce que entre menor número de neutrófilos y mayor duración de la neutropenia existe mayor riesgo de infección.4 Los pacientes con cáncer, en la mayoría de los episodios de infección asociada a neutropenia, presentan fiebre como única manifestación, ya que la disminución de los neutrófilos reduce los signos y síntomas de los procesos infecciosos; a esta condición se le ha denominado neutropenia febril (NF).5
Los episodios de NF se consideran como una urgencia médica, ya que pueden llevar a infecciones graves y hasta la muerte. De ahí que la terapia inicial desde hace más de dos décadas consiste en la hospitalización de los pacientes y la administración de antibióticos de amplio espectro.6,7 Sin embargo, es conveniente mencionar que esta conducta tiene implicaciones económicas, por ejemplo, se ha estimado que anualmente sólo en Estados Unidos se hospitalizan 60,000 pacientes por NF y por infecciones relacionadas con la neutropenia.8 Ante esta situación, y a fin de ofrecer la mejor alternativa para los pacientes de manera que mejoren su calidad de vida, desde hace varios años se han implementado estrategias para disminuir la frecuencia de hospitalización. La demostración de la existencia de subgrupos de pacientes con NF que pueden evolucionar satisfactoriamente con tratamiento ambulatorio,9,10 ha ocasionado que en la actualidad algunas guías terapéuticas consideren la necesidad de identificar, en el momento de la primera evaluación durante los episodios de NF, a los pacientes de bajo riesgo de infección bacteriana grave, con objeto de brindarles tratamiento ambulatorio.11 Si bien esta forma de tratamiento puede disminuir los costos, se ha reportado que solamente se le puede brindar a una proporción muy limitada de pacientes, puesto que el desconocimiento de sus ventajas farmacoeconómicas hacen que el producto sea percibido como de mayor costo, considerando sólo el corto plazo y sin tomar en cuenta el impacto en mejoría de la calidad de vida del paciente y los ahorros considerables que se derivan de una profilaxis eficaz de la NF.12-14
En diversos ensayos clínicos y metaanálisis, se ha puesto en evidencia que el uso de factores estimulantes de colonias de granulocitos (FEC-G) como tratamiento profiláctico después del uso de quimioterapia, puede disminuir la frecuencia de NF, de infecciones relacionadas a neutropenia y de muerte, en más del 40%,15 por lo que las guías de las sociedades americanas y europeas de oncología recomiendan su utilización, principalmente cuando el riesgo de neutropenia es mayor a 20%, situación que ocurre con algunos tipos de quimioterapia con características mieloablativas y en situaciones particulares, como estadios avanzados de cáncer o en casos de NF recurrente.16,17
Kuderer y cols.18 pusieron de manifiesto que de los FEC, el Filgrastim, el Lenograstim, y de manera más reciente el Pegfilgrastim (compuesto de vida media prolongada, ya que es pegilado) son los que han demostrado efectividad para disminuir los episodios de NF. Debido a las diferencias en cuanto a su dosificación como tratamiento profiláctico entre Filgrastim (seis dosis, una cada 24 horas) y Pegfilgrastim (una sola dosis durante todo el ciclo), Eldar-Lissai A y cols.19 en 2008 publicaron un estudio económico donde evaluaron los costos directos e indirectos para determinar cuál de las dos sería la alternativa más costo-efectiva. De acuerdo a su análisis, los autores observaron que Pegfilgrastim parece ser la opción más costo-efectiva, ya que el costo calculado promedio por episodio de tratamiento con Filgrastim fue de 2,195 comparado contra 1,128 dólares americanos con Pegfilgrastim. Mientras que los días ajustados por calidad de vida (QALDs) fueron de 12,698 vs. 12,967, respectivamente. Son pocos los estudios farmacoeconómicos en nuestro país, de ahí que, en general, es muy limitada la información que disponemos sobre los costos de la atención. Por lo anterior, decidimos llevar a cabo un estudio económico para determinar los costos, en nuestro medio, del uso de los FEC para prevenir los episodios de neutropenia febril en pacientes con cáncer que requiere del uso de quimioterapia mieloablativa.
¿MATERIAL Y MÉTODOS
Se realizó una evaluación económica completa desde la perspectiva del pagador, mediante un análisis de costoefectividad (ACE) del efecto de tres posibles escenarios en el manejo profiláctico de la NF secundaria a una quimioterapia mieloablativa. Se desarrolló una cohorte hipotética de pacientes adultos de 18 a 65 años con cualquier tipo de cáncer que haya recibido este tipo de quimioterapia mieloablativa. El tiempo de evaluación fue durante el primer ciclo de quimioterapia (1 mes). Los escenarios que se consideraron fueron: 1) no dar factor estimulante de colonias de granulocitos (sin FEC-G) después del término del ciclo de quimioterapia mieloablativa, 2) administrar seis dosis de Filgrastim (300 mcg, por día, vía subcutánea) y 3) aplicar una dosis única de Pegfilgrastim (6 mg, vía subcutánea, dosis única).
¿ANÁLISIS DE DECISIÓN
Efectividad
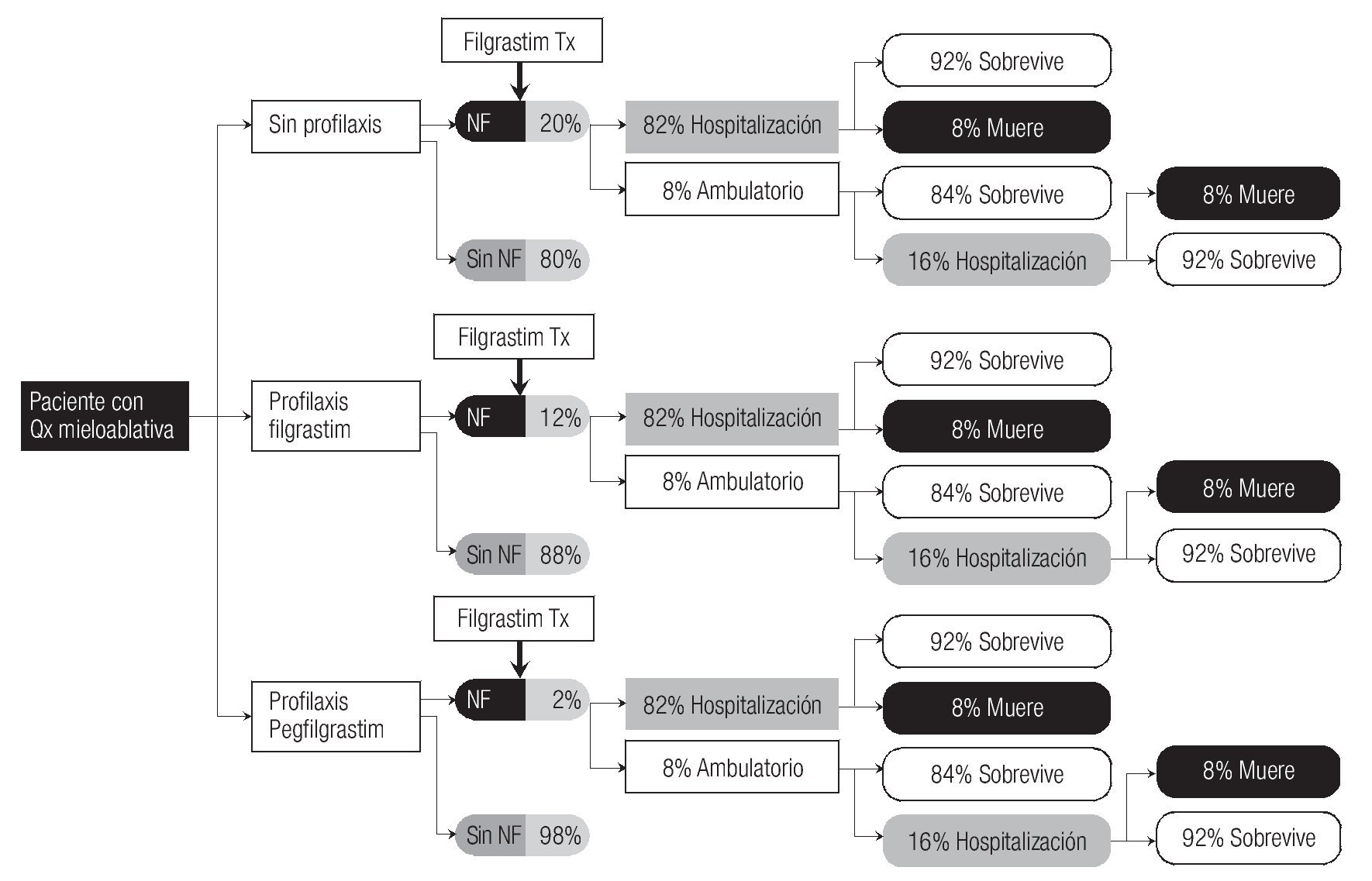
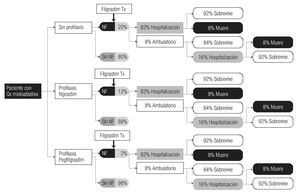
Los desenlaces evaluados fueron: proporción de episodios de NF, infecciones relacionadas y muerte presentados al administrar de forma profiláctica Filgrastim (300 mcg, 6 dosis), Pegfilgrastim (6 mg, dosis única), o bien, no dar FEC-G. Los tres escenarios se esquematizan en el árbol de decisiones que se presenta en la Figura 1. La probabilidad de estos desenlaces se determinó de acuerdo con lo reportado en estudios donde han evaluado el pronóstico de los pacientes con cáncer, durante los episodios de NF.20-24 Las estimaciones se efectuaron tomando en cuenta el punto de corte del 20% (probabilidad de presentar neutropenia) que consideran las guías clínicas para determinar los candidatos para recibir profilaxis, después del uso de quimioterapia.25
Figura 1. Escenarios de tratamiento profiláctico con factor estimulante de colonias de granulocitos en pacientes con cáncer tratados con quimioterapia (Qx) mieloablativa.
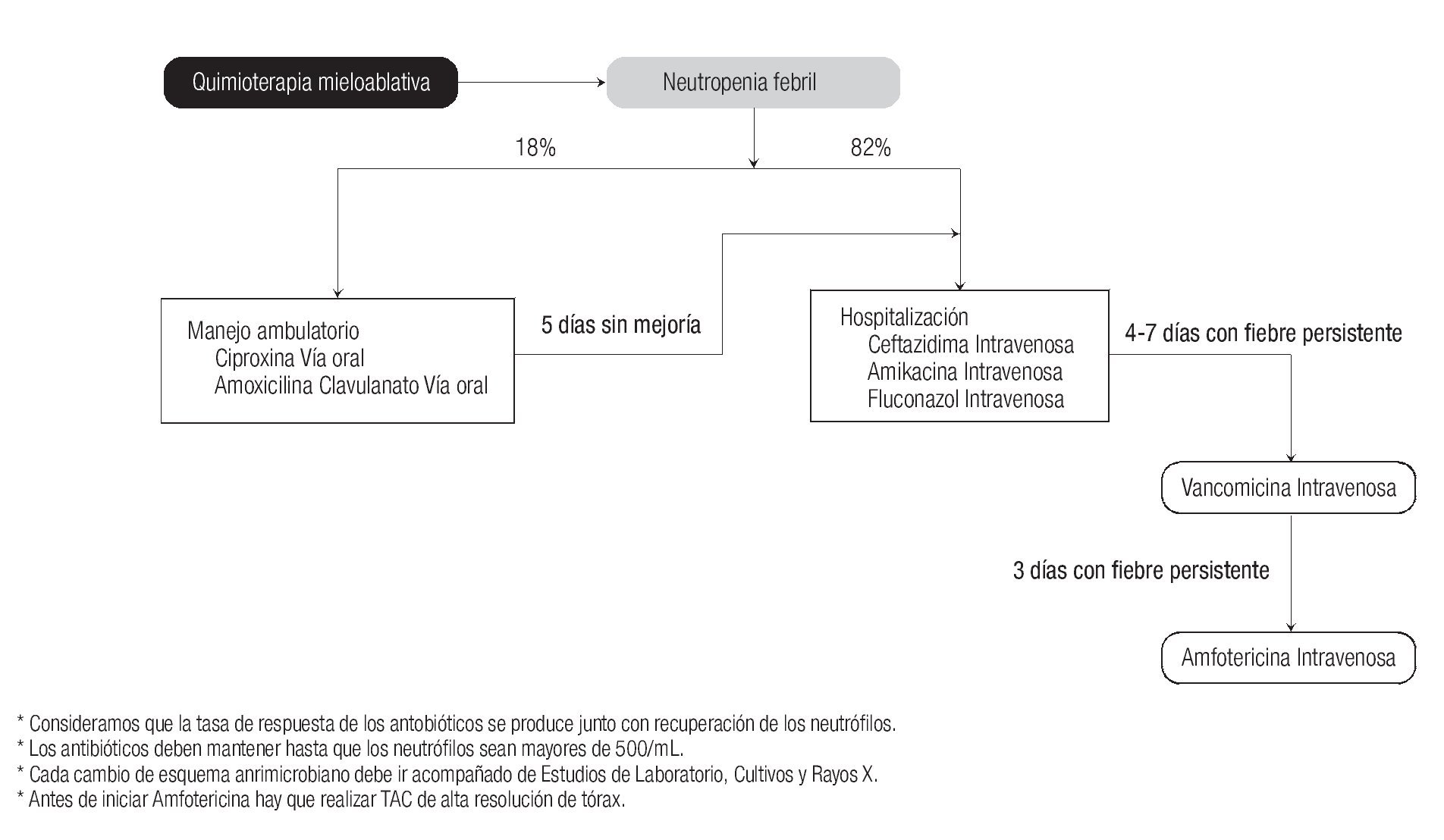
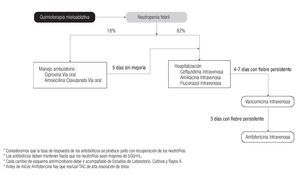
En la Figura 2 se describe el algoritmo de decisiones del tratamiento antimicrobiano que se empleó para el cálculo de los costos, tanto para el caso de pacientes clasificados de bajo riesgo (tratamiento ambulatorio) como los casos graves, donde el tratamiento se aplica a pacientes hospitalizados. Conviene señalar que como parte del tratamiento de la NF, en todos los escenarios se incluyó el uso de Filgrastim.
Figura 2. Descripción del tratamiento antimicrobiano considerado para calcular los costos del manejo de la neutropenia febril, tanto ambulatorio como hospitalario.
Costos
La principal variable de desenlace para estimar el beneficio de cualquiera de las tres intervenciones fue el costo total directo de cada una. Para estimar los costos en nuestro medio se llevó a cabo una entrevista estructurada a siete médicos oncólogos con más de siete años de experiencia. Durante la entrevista se les solicitó que calcularan los insumos que pensaban se utilizaban durante los episodios de NF. De esta forma, se preguntó sobre el número de consultas por paciente, así como el tiempo de estancia hospitalaria, los medicamentos y el número de exámenes de laboratorio y radiológicos que se aplican. La información solicitada fue tanto de los pacientes que tienen buena evolución, como de los pacientes que evolucionan hacia la gravedad (principalmente por infección) que requieren el uso de unidades de terapia intensiva, y que eventualmente fallecen. Una vez obtenida esta información por cada médico, se utilizaron las medianas de los insumos utilizados, para tener una base de cálculo para obtener los costos.
El modelo que se utilizó para la evaluación económica fue desde la perspectiva del pagador. En el modelo se consideran sólo los costos directos analizados en los siguientes rubros: costo de medicamentos, consultas, estudios clínicos, hospitalización y procedimientos/ equipo. Para disponer de una fuente confiable, se consideraron los precios reportados para estos rubros en la atención médica otorgada en el Instituto Mexicano del Seguro Social,26 en función de que anualmente se actualiza la información y por ser una de las instituciones que atiende el mayor número de pacientes oncológicos en el país.
Análisis estadístico
Se calcularon los costos promedio para cada una de las alternativas, a partir de una cohorte hipotética de 100 episodios de tratamiento, para todos los desenlaces considerados, posteriormente, se compararon entre cada una de las tres alternativas: no uso de FEC-G vs. Pegfilgrastim vs. Filgrastim, tanto para el costo en pacientes sin neutropenia como de pacientes con neutropenia y sobrevivientes.
Se calculó la razón costo-efectividad incremental (RCEI), con base en la diferencia en costos y en efectividades, con la fórmula:
¿RESULTADOS
Se describe la información más general que se utilizó para construir, tanto el árbol de decisiones como para estimar los costos, la cual se obtuvo de la revisión de la literatura y de la opinión de los expertos, respectivamente. Mientras que, como se muestra en la Figura 1, para cada una de las tres alternativas de tratamiento se incluyen los posibles escenarios, en función de la probabilidad o no de desarrollar NF. Sin profilaxis, la frecuencia estimada de NF fue del 20%; con la administración de Filgrastim la incidencia de NF se disminuye a 12%, pero con Pegfilgrastim es sólo del 2%. A partir de la aparición de NF, se consideraron dos opciones terapéuticas: tratamiento antimicrobiano ambulatorio o tratamiento hospitalario. Como también puede observarse en la Figura 1, la probabilidad de complicación y de resolución del episodio de NF es estable con cada una de las opciones.
Se presentan los costos directos calculados en pesos mexicanos ajustados a marzo del 2008, de cada uno de los posibles insumos que podrían utilizarse durante cada una de las fases del tratamiento de la NF. Cada uno de los insumos incluidos en el análisis se obtuvo de la entrevista con los expertos. Cabe señalar que con respecto al rubro de transfusiones, el costo se refiere al material necesario para realizarla, no al costo del tejido.
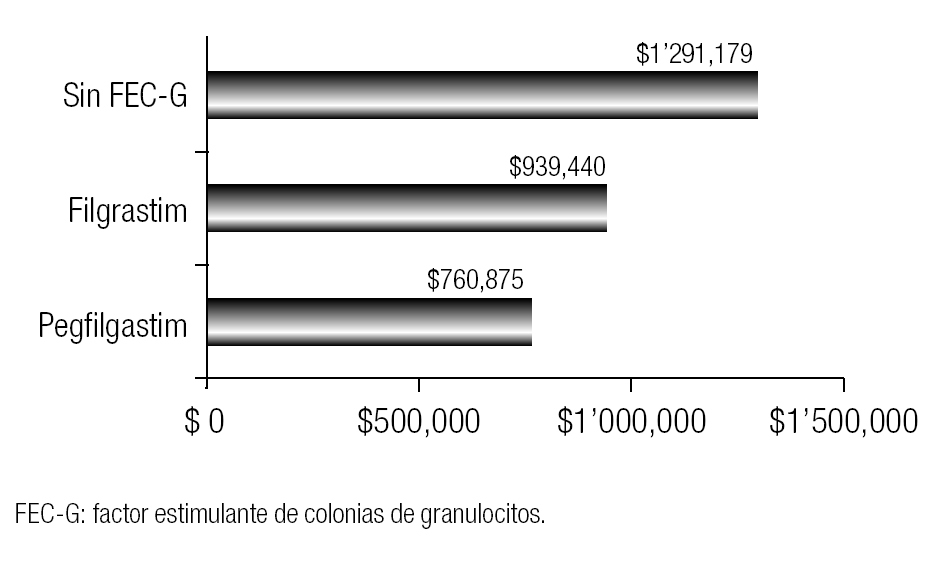
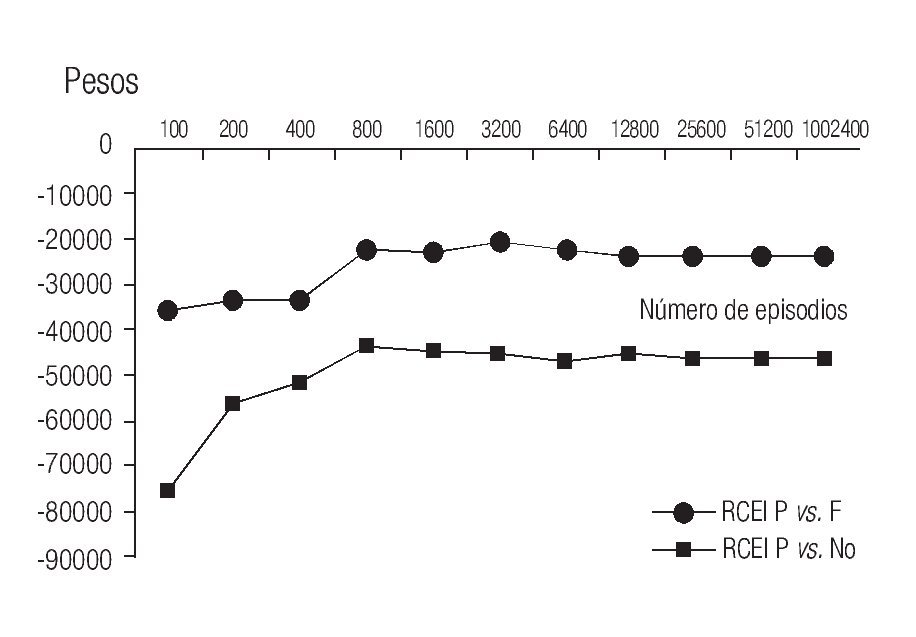
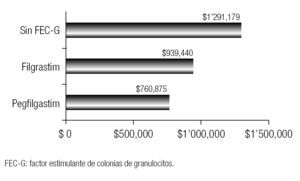
Al analizar la efectividad global de las alternativas estudiadas, y de acuerdo con la bibliografía disponible, se determinó que Pegfilgrastim es la mejor opción en función del menor número de eventos de NF (2%) que pueden presentarse en comparación con no brindar tratamiento profiláctico (20%) o con Filgrastim (8%). Además de ser la mejor opción para disminuir la NF, también lo fue para evitar muertes durante estos episodios. De acuerdo con la probabilidad de muerte de los episodios de NF, solamente se esperaría 0.2% con Pegfilgrastim en comparación con 0.8% de Filgrastim o de 1.5% sin tratamiento profiláctico. Esta información puede visualizarse mejor con tasas de mortalidad; la cual para Pegfilgrastim es de 1.4 por mil episodios de NF, 8.3 para Filgrastim y 13.6 sin el uso de FEC-G. En la Figura 3 se muestran los costos relacionados con cada una de las alternativas, teniendo como escenario a 100 pacientes después de haber recibido quimioterapia mieloablativa, se observó que los costos mayores fueron cuando no se brindó terapia profiláctica, seguido de Filgrastim y Pegfilgrastim debido a la proporción de pacientes que desarrollan NF, se infectan, se complican y mueren. El costo en pesos mexicanos (con base en precios del sector salud) de la falta de tratamiento profiláctico es de $1'291,179, comparado con $939,440 de Filgrastim y con $760,875 de Pegfilgrastim.
Figura 3. Costos de la profiliaxis y del manejo de la neutropenia febril en 100 episodios de quimioterapia mieloablativa de acuerdo al uso de dos diferentes FEC-G o sin el uso de profilaxis. Cada alternativa tuvo un número similar de pacientes (33% con cada una).
El análisis costo-efectividad utilizado como medida de efectividad tanto el número de pacientes libres de NF como los pacientes supervivientes, se demuestra que Pegfilgrastim es una terapia dominante en comparación con Filgrastim y con el no uso de FEC-G.
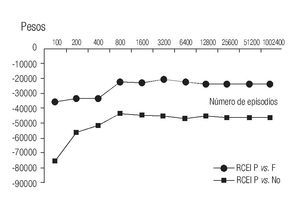
Figura 4. Comparación del ahorro con el uso de Pegfilgrastim (P) con Filgrastim (F), de acuerdo con el número de episodios de quimioterapia mieloablativa.
Por último, también se observó que en nuestro medio al incrementar el número de tratamientos, siempre existe una ventaja en los costos para Pegfilgrastim comparado contra Filgrastim y contra no administrar el tratamiento profiláctico (Figura 4).
¿DISCUSIÓN
Por su frecuencia, la neutropenia es la complicación hematológica más importante durante los tratamientos de quimioterapia mieloablativa para los pacientes con cáncer. Tanto por la posibilidad de no completar los tratamientos tal como se planean en el momento del diagnóstico de la enfermedad, como por las consecuencias de la misma neutropenia, siendo los procesos infecciosos, la más grave.
En la actualidad se han establecido ciertos parámetros o guías que pueden ayudar a los clínicos a predecir si la neutropenia será muy grave y prolongada, a fin de determinar la necesidad o no del uso de factores estimulantes de colonias (FEC). Las guías actuales, basadas en ensayos clínicos controlados y metaanálisis recomiendan el uso de FEC cuando la probabilidad de que ocurra neutropenia severa es mayor al 20%, o bien, cuando las características de los pacientes hacen suponer que presentarán NF, como en caso de los pacientes mayores de 65 años. Sin embargo, estas guías no orientan hacia cuál FEC disponible podría ser el que brinde las mejores ventajas. En particular, con la disponibilidad en los últimos años de FEC pegilados y que han mostrado su eficacia como tratamiento profiláctico para disminuir los eventos de neutropenia, se tiene una opción más, pero con la que los pacientes pueden ser beneficiados por su efecto a largo plazo y con menor número de aplicaciones que otros FEC, como el Filgrastim.
En este estudio, pudimos corroborar lo que diversas investigaciones han demostrado:27 que el Pegfilgrastim es la opción más costo-efectiva para disminuir la frecuencia de NF. Los estudios económicos en nuestro país son escasos, por lo que el presente análisis permite conocer con costos actuales (de acuerdo a los precios del sector público) y con la orientación de los médicos especialistas, el panorama de lo que podría ocurrir al utilizar en forma amplia los FEC disponibles. Nuestros resultados apoyan que el uso, tanto de Filgrastim como Pegfilgrastim son mejores alternativas para la salud del paciente, que no brindar tratamiento profiláctico, tanto para los pacientes al disminuir el número de eventos de NF y el riesgo de hospitalizaciones, complicaciones y muerte, como para los sistemas de salud, ya que con ambas alternativas se disminuyen los costos de la atención de los pacientes, hasta en aproximadamente 35%.
Si bien, los resultados muestran las ventajas del tratamiento profiláctico, este estudio tiene limitaciones. La más importante es que lo que se plantea son escenarios hipotéticos, más que información obtenida directamente de la atención de los pacientes, pero para la construcción de los diferentes escenarios y los posibles insumos se consultaron expertos de nuestro país, por lo que consideramos que es una buena aproximación a lo que sucede en la vida real. Es conveniente, en el futuro, tener datos más precisos para la estimación de los costos reales. Otra limitación es que se estimaron los costos desde la perspectiva del pagador de servicios, por lo que no sabemos lo que significa para los pacientes desde el punto de vista de los gastos que tienen durante los episodios de NF. Es de esperarse un ahorro, al no tener que desplazarse para la atención cuando ocurren, sin embargo, también son necesarios otros estudios para determinar su verdadera magnitud, así como posible impacto en días perdidos por incapacidad.
Por otro lado, conviene mencionar que aun cuando este estudio establece las ventajas del tratamiento profiláctico para disminuir los eventos de NF, ésta no es la única variable que debería medirse. El hecho de disminuir la frecuencia de eventos de neutropenia, también coadyuvaría para brindar la terapia antineoplásica de la forma que se planea en un principio.
En conclusión, podemos afirmar que el uso de los FEC-G en forma profiláctica disminuyen los costos de atención de los pacientes con cáncer que reciben quimioterapia mieloablativa en nuestro país, y que el uso de Pegfilgrastim es una alternativa dominante sobre Filgrastim.