La resistencia de Helicobacter pylori a los antibióticos es un problema creciente en nuestro medio y es necesario mejorar las tasas de erradicación. La cuádruple terapia con bismuto se ha considerado el tratamiento de primera o segunda línea en el nuevo consenso. Este estudio evalúa el uso de Pylera® en un escenario clínico real.
Pacientes y métodosSe llevó a cabo un estudio descriptivo transversal, entre marzo y septiembre de 2016, para evaluar los porcentajes de erradicación de Helicobacter pylori en pacientes tratados con Pylera®. Los pacientes (naïve o con fallo a terapias previas) fueron tratados durante 10 días. La erradicación fue confirmada usando un test del aliento con urea al menos 30 días después de la finalización del tratamiento. Además se recogieron datos demográficos, clínico-analíticos y relacionados con el tratamiento.
ResultadosFueron incluidos 185 pacientes (51,6±16,19 años); el 63,8% fueron mujeres y el 9,2% tenían historia familiar de cáncer gástrico. La indicación más frecuente fue la dispepsia (55,1%). El 57,8% recibieron Pylera® como primera línea de tratamiento. El 95,7% asociaron omeprazol. Se detectó una tasa de erradicación en primera línea de tratamiento del 78,15% por intención de tratar (86,6% por protocolo). No hubo diferencias estadísticamente significativas entre pacientes naïve y los tratados previamente. Nueve pacientes abandonaron el tratamiento (4,9%), 7 debido a efectos secundarios leves y 2 por toma incorrecta.
ConclusionesPylera® tiene unas aceptables tasas de erradicación como primera y segunda línea de tratamiento y muestra un adecuado perfil de seguridad.
The resistance of Helicobacter pylori to antibiotics is a growing problem in Spain and eradication rates must be improved. The new Spanish consensus considers quadruple therapy with bismuth as first- or second-line therapy. This study evaluated the use of Pylera® in real-life clinical practice.
Patients and methodsA cross-sectional descriptive study was conducted to evaluate the eradication rate of Helicobacter pylori in patients treated with Pylera® between March and September 2016. Patients (naïve or with previous treatment failure) were treated for 10 days. Eradication was confirmed using a breath test with urea 30 days or more after treatment. In addition, demographic, clinical-analytical and treatment-related data were collected.
ResultsA total of 185 patients were included (51.6±16.19 years); 63.8% were women and 9.2% had a family history of gastric cancer. The most frequent indication was dyspepsia (55.1%). Approximately 57.8% received Pylera® as first-line therapy, while 95.7% received Pylera® in combination with omeprazole. A first-line eradication rate of 78.15% was observed in the intention-to-treat population (86.6% per protocol). There were no statistically significant differences between naïve patients and those previously treated. Nine patients abandoned the treatment (4.9%), 7 due to mild side effects and 2 due to incorrect dosing.
ConclusionsPylera® has acceptable eradication rates in first- and second-line therapy and shows a suitable safety profile.
La infección por Helicobacter pylori es una de las infecciones bacterianas más comunes a nivel mundial y afecta al 50% de la población española. Es bien conocido que esta infección se asocia a gastritis crónica, úlcera y cáncer gástrico1. En los consensos españoles previos2–4 se estableció como aceptable un porcentaje de al menos el 80% de erradicación para los diferentes regímenes antibióticos. Sin embargo, ese porcentaje se ha incrementado al 90% en el último consenso español1. Además, la triple terapia se eliminó como primera línea de tratamiento ya que, debido a las resistencias crecientes, ofrecía resultados muy poco eficaces, de en torno al 70%, de acuerdo con publicaciones previas5,6.
La cuádruple terapia con bismuto se ha postulado como una alternativa terapéutica inicial, una vez que su eficacia sea confirmada en nuestro medio1. Existe evidencia de que la resistencia de Helicobacter pylori a las sales de bismuto no ha sido descrita, y muy raramente aquella a las tetraciclinas7. Además, recientemente se ha comercializado una nueva formulación galénica de la cuádruple terapia con bismuto (Pylera®), que consiste en 3 antibióticos dentro de la misma cápsula: 140mg de subcitrato de bismuto, 125mg de hidrocloruro de tetraciclina y 125mg de metronidazol8. Esta fórmula permite una mayor comodidad para los pacientes, lo que, a priori, podría mejorar la adherencia al tratamiento. Un ensayo europeo multicéntrico muestra una eficacia de erradicación del 90% con esta formulación9 y Delchier et al., en 2014, reportaron tasas de erradicación del 93,2 al 93,8% por intención de tratar (IT), en pacientes con fracaso previo al tratamiento10.
El presente estudio tiene como objetivo proporcionar una imagen real del tratamiento con la cuádruple terapia con bismuto, con la nueva formulación (Pylera®), que se utiliza como tratamiento de primera y segunda línea en nuestro país. Todavía existen pocos trabajos publicados hasta la fecha sobre el uso de este medicamento en la práctica clínica real en España.
El objetivo principal fue evaluar la tasa de erradicación en nuestro medio, en una población heterogénea tratada con Pylera®. Además, se analizaron las características de los pacientes con infección por Helicobacter pylori tratados con este fármaco en nuestro país y se trató de detectar el porcentaje de intolerancia al fármaco, así como las variables predictivas de respuesta al tratamiento.
Pacientes y métodosSelección de pacientes y diseño del estudioSe llevó a cabo un estudio descriptivo, transversal, entre marzo y septiembre de 2016, para evaluar la tasa de erradicación de Helicobacter pylori en la práctica clínica real, en el Servicio de Gastroenterología del Hospital Rey Juan Carlos de Madrid, un hospital terciario de España.
Los criterios de inclusión fueron: 1) pacientes adultos (edad≥18 años); 2) que fueron diagnosticados de infección por Helicobacter pylori; 3) que no habían recibido tratamiento previamente o que tuvieron un fracaso previo al tratamiento, y 4) que fueron tratados con Pylera®.
La detección de la infección por Helicobacter pylori se realizó mediante el test del aliento con urea (que precisa la siguiente preparación: sin tratamiento con antibióticos durante al menos el mes previo, sin tratamiento con inhibidores de la bomba de protones (IBP) durante las 2 semanas previas y sin fumar ni lavarse los dientes en la mañana de la prueba) o mediante análisis histológico de las biopsias de mucosa gástrica. La resistencia a los antibióticos no se estudió mediante cultivo de las muestras. A todos los pacientes con resultado positivo se les administró Pylera® en forma de 3 cápsulas cada 6h durante un total de 10 días. Se asoció a dicho tratamiento un IBP, como se prescribe en la ficha técnica de Pylera®. La erradicación se midió al menos 30 días después del final del tratamiento realizando un test del aliento con urea.
Análisis estadísticoPara cada paciente incluido en el estudio se obtuvo la siguiente información: datos demográficos (edad –estratificada en menores y mayores de 65 años, sexo-masculino o femenino y antecedentes familiares de cáncer gástrico –sí o no), variables clínicas y analíticas (método de detección de Helicobacter pylori –gastroscopia con biopsias o test del aliento con urea, hallazgos endoscópicos, presencia de úlcera péptica –sí o no, presencia de metaplasia en las muestras de anatomía patológica –sí o no, anemia por deficiencia de hierro –sí o no, trombocitopenia –sí o no, deficiencia de vitamina B12 –sí o no) y variables relacionadas con el tratamiento erradicador (línea de tratamiento, duración del tratamiento, frecuencia de las tomas, tipo de IBP asociado y dosis utilizada, uso de probióticos asociados al tratamiento y tasas de erradicación). Además, para los pacientes que tomaron Pylera® en segunda y tercera línea se revisaron los tratamientos erradicadores tomados previamente.
Las variables cuantitativas se expresaron con medidas de tendencia central y dispersión (media, desviación estándar e intervalos) y las variables cualitativas, utilizando frecuencias y porcentajes. La comparación entre las variables cualitativas se realizó mediante la prueba estadística de Chi-cuadrado (o test no paramétrico de Fisher).
Además, la estimación del riesgo se realizó mediante la determinación de la odds ratio y el intervalo de confianza, en el análisis univariante. Finalmente, se realizó un análisis multivariante para determinar qué variables se asociaron con una mayor tasa de erradicación de Helicobacter pylori, utilizando regresión logística. Todos los análisis se realizaron con el paquete estadístico SPSS 21.0.
Aspectos éticosEl estudio se realizó de acuerdo con los principios de la Declaración de Helsinki y la Conferencia Internacional de Armonización sobre directrices de buena práctica clínica. Además, el estudio fue aprobado por el Comité de Ética de nuestra institución, antes de que comenzara la investigación.
ResultadosSe incluyeron un total de 185 pacientes, con una edad media de 51,6 años (DE 16,19), predominantemente mujeres (n=118, 63,8%). El 9,2% (n=17) de los pacientes tenían antecedentes familiares de cáncer gástrico. Las características de nuestra muestra se exponen en la tabla 1. La indicación más frecuente fue la sintomatología dispéptica (55,1%). El diagnóstico de infección por Helicobacter pylori se realizó por gastroscopia con biopsias en la mayoría de los casos (n=129, 69,7%), pero también con el test del aliento con urea (n=50, 30,3%) y, en algunos casos, con ambos métodos (n=5, 2,7%). Los hallazgos más frecuentes en el estudio endoscópico fueron gastritis antral (37,98%), gastritis corporoantral (18,60%) y gastritis atrófica crónica (17,05%). Dieciséis pacientes tuvieron metaplasia intestinal (12.4%) y en un paciente se detectó cáncer gástrico (0,7%). En cuanto a las complicaciones de la infección por Helicobacter pylori, 3 pacientes tuvieron trombocitopenia (1,6%), 11 tuvieron deficiencia de vitamina B12 (5,9%), en 16 se detectó anemia ferropénica (8,6%) y 6 pacientes presentaron úlcera gástrica (el 4,7% de los que se sometieron a un estudio endoscópico).
Características generales de la muestra
| N | 185 |
| Sexo h/m, n (%) | 67 (36,2)/118 (63,8) |
| Edad (años), media±DE | 51,61±16,193 |
| Rango de edad (años), n (%) | |
| Jóvenes: 16-24 | 13 (7) |
| Adultos: 25-59 | 104 (56,2) |
| Adultos mayores: 60-75 | 55 (29,7) |
| Ancianos: >75 | 13 (7) |
| Antecedentes familiares cáncer gástrico, n (%) | |
| No | 75 (40,5) |
| Sí | 17 (9,2) |
| No registrado | 93 (50,3) |
| Indicaciones de estudio de Helicobacter pylori, n (%) | |
| Dispepsia | 102 (55,1) |
| Úlcera | 3 (1,6) |
| Metaplasia | 28 (15,1) |
| Antecedentes familiares cáncer Gástrico | 6 (3,2) |
| Gastropatía | 25 (13,5) |
| Otros | 21 (11,4) |
| Método diagnóstico para Helicobacter pylori, n (%) | |
| Test and Threat | 56 (30,3) |
| Gastroscopia (biopsias o test de la ureasa) | 124 (67,03) |
| Ambos | 5 (2,7) |
| Total | 185 (100) |
| Hallazgos gastroscopia, n (%) | |
| Gastritis antral | 49 (37,98) |
| Gastritis corporoantral | 27 (18,60) |
| Gastritis crónica atrófica | 22 (17,05) |
| Esofagitis | 11 (8,53) |
| Normal | 6 (4,65) |
| Úlcera | 5 (3,88) |
| Duodenitis | 4 (3,10) |
| Pólipos gástricos | 2 (1,55) |
| Esófago de Barrett | 2 (1,55) |
| Cáncer gástrico | 1 (0,78) |
| Total | 129 (100) |
| Complicaciones asociadas a Helicobacter pylori | |
| Anemia ferropénica | 16 (8,6) |
| Déficit vitamina B12 | 11 (5,9) |
| Trombocitopenia | 3 (1,6) |
| Úlcera péptica | 6 (4,7) |
| Metaplasia intestinal | 16 (12,4) |
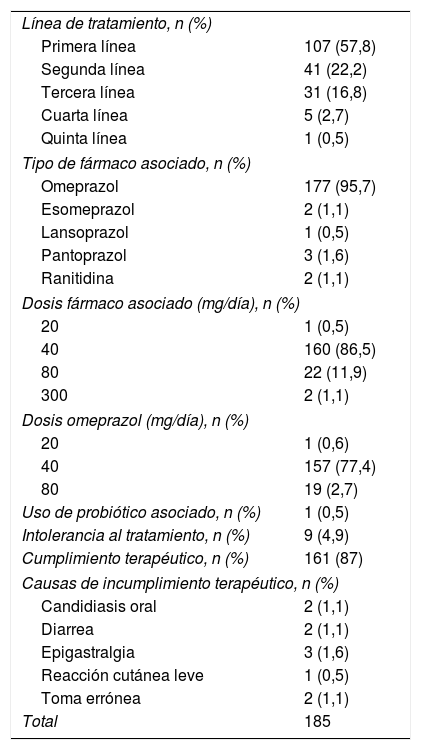
Los datos sobre las características del tratamiento se muestran en la tabla 2. Todos los pacientes tomaron Pylera®, con una frecuencia de 3 cápsulas cada 6h durante 10 días. En la mayoría de los casos se usó como primera línea de tratamiento (57,8%). El IBP que con mayor frecuencia se asoció al tratamiento fue omeprazol (n=177, 95,7%), a una dosis de 20mg cada 12h (86,5%). Se investigó el uso de probióticos asociados, pero solo un paciente tomó dicho tratamiento. Por esta razón, no es posible determinar su influencia en las tasas de erradicación. Nueve pacientes no completaron el tratamiento (4,9%), 7 de ellos por efectos secundarios y 2 por un tratamiento incorrecto. Estos efectos secundarios fueron leves en los 7 pacientes descritos (candidiasis oral en 2 pacientes, diarrea en otros 2, dolor de estómago en otros 2 y reacción cutánea leve en uno), mientras que ningún paciente tuvo efectos secundarios graves.
Características generales del tratamiento
| Línea de tratamiento, n (%) | |
| Primera línea | 107 (57,8) |
| Segunda línea | 41 (22,2) |
| Tercera línea | 31 (16,8) |
| Cuarta línea | 5 (2,7) |
| Quinta línea | 1 (0,5) |
| Tipo de fármaco asociado, n (%) | |
| Omeprazol | 177 (95,7) |
| Esomeprazol | 2 (1,1) |
| Lansoprazol | 1 (0,5) |
| Pantoprazol | 3 (1,6) |
| Ranitidina | 2 (1,1) |
| Dosis fármaco asociado (mg/día), n (%) | |
| 20 | 1 (0,5) |
| 40 | 160 (86,5) |
| 80 | 22 (11,9) |
| 300 | 2 (1,1) |
| Dosis omeprazol (mg/día), n (%) | |
| 20 | 1 (0,6) |
| 40 | 157 (77,4) |
| 80 | 19 (2,7) |
| Uso de probiótico asociado, n (%) | 1 (0,5) |
| Intolerancia al tratamiento, n (%) | 9 (4,9) |
| Cumplimiento terapéutico, n (%) | 161 (87) |
| Causas de incumplimiento terapéutico, n (%) | |
| Candidiasis oral | 2 (1,1) |
| Diarrea | 2 (1,1) |
| Epigastralgia | 3 (1,6) |
| Reacción cutánea leve | 1 (0,5) |
| Toma errónea | 2 (1,1) |
| Total | 185 |
Además, se revisaron los tratamientos que habían tomado previamente los pacientes que habían recibido Pylera® en segunda y tercera línea.
Entre los pacientes que tomaron la cuádruple terapia con bismuto como segunda línea (n=41), se encontraron 30 que tomaron previamente omeprazol-claritromicina-amoxicilina durante 10 días, uno que tomó omeprazol-claritromicina-amoxicilina durante 7 días, otro que tomó omeprazol-claritromicina-amoxicilina durante 14 días, otro que tomó omeprazol-claritromicina-metronidazol durante 10 días, otro que tomó omeprazol-levofloxacino-amoxicilina durante 10 días y 5 pacientes que tomaron omeprazol-claritromicina-amoxicilina-metronidazol durante 14 días.
Entre los pacientes que tomaron la cuádruple terapia con bismuto como tercera línea (n=31), se determinaron los siguientes tratamientos de primera línea: 26 pacientes que tomaron omeprazol-claritromicina-amoxicilina durante 10 días, uno que tomó pantoprazol-claritromicina-metronidazol durante 10 días, otro que tomó esomeprazol-amoxicilina-claritromicina-bismuto durante 14 días y 2 con tratamiento desconocido en primera línea. Se determinaron también los siguientes tratamientos de segunda línea: 18 pacientes tomaron omeprazol-levofloxacino-amoxicilina durante 10 días, 3 tomaron esomeprazol-levofloxacino-amoxicilina durante 10 días, uno tomó omeprazol-claritromicina-amoxicilina durante 10 días, 3 tomaron esomeprazol-levofloxacino-amoxicilina-bismuto durante 14 días, uno tomó omeprazol-claritromicina-levofloxacino durante 10 días, otro tomó pantoprazol-levofloxacino-metronidazol durante 10 días y 3 pacientes con tratamiento desconocido en segunda línea.
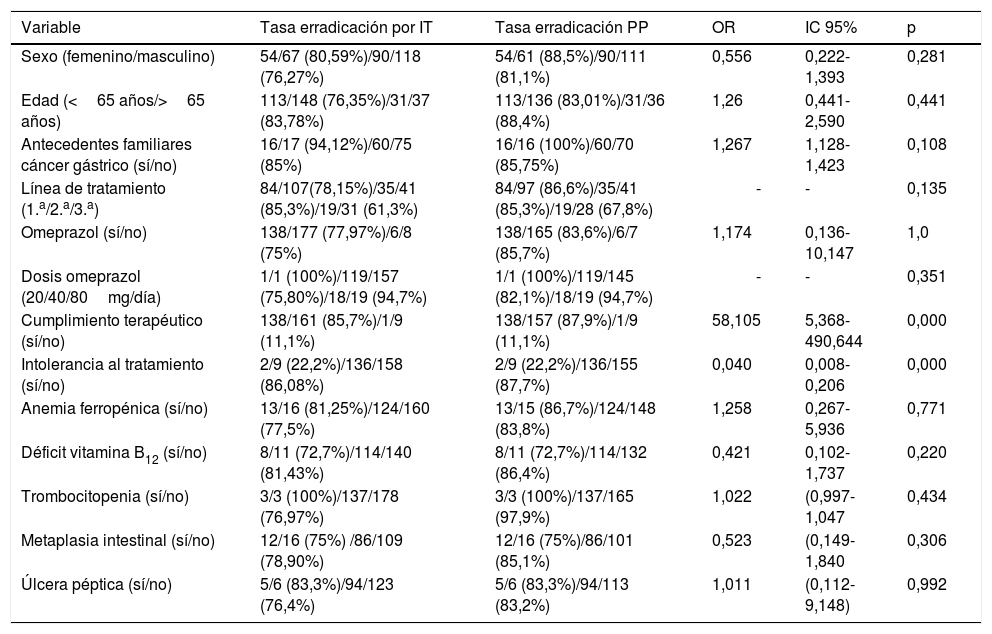
En el análisis univariante (tabla 3) se detectó un mayor porcentaje de erradicación en hombres (n=54/67, 80,6% por IT/n=54/61, 88,5% por protocolo [PP]), en pacientes mayores de 65 años (n=31/37, 83,8% por IT/n=31/36, 88,4% PP) y en aquellos con antecedentes de cáncer gástrico (n=16/17, 83,78% por IT/n=16/16, 100% PP), aunque ninguna de estas variables mostró significación estadística. Se detectó un mayor porcentaje de erradicación en el tratamiento de segunda línea (n=35/41, 85,3% por IT y PP) versus primera línea (n=84/107, 78,15% por IT y n=84/97, 86,6% PP) o tercera línea (n=19/31, 61,3% por IT y n=19/28, 67,9% PP), pero no se alcanzó significación estadística (p=0,135). Dado que la mayoría de los pacientes se sometieron a tratamiento con omeprazol, no se pudo realizar un estudio comparativo adecuado entre diferentes PPI. Sin embargo, la tasa de respuesta al tratamiento se comparó con las diferentes dosis de omeprazol utilizadas, que no mostraron diferencias estadísticamente significativas (p=0,351), aunque se objetivó una tendencia a mayores tasas de erradicación con mayor inhibición ácida: con 20mg cada 12h (75,8% de éxito con IT/82,1% PP) y con 40mg cada 12h (94,7% de éxito por IT y PP). Se obtuvo significación estadística en la tasa de erradicación en pacientes con un adecuado cumplimiento terapéutico (85,7% por IT y 87,9% PP; p=0,000) y en aquellos sin intolerancia al tratamiento (86,8% por IT y 87,7% PP, p=0,000).
Análisis univariante
| Variable | Tasa erradicación por IT | Tasa erradicación PP | OR | IC 95% | p | |
|---|---|---|---|---|---|---|
| Sexo (femenino/masculino) | 54/67 (80,59%)/90/118 (76,27%) | 54/61 (88,5%)/90/111 (81,1%) | 0,556 | 0,222-1,393 | 0,281 | |
| Edad (<65 años/>65 años) | 113/148 (76,35%)/31/37 (83,78%) | 113/136 (83,01%)/31/36 (88,4%) | 1,26 | 0,441-2,590 | 0,441 | |
| Antecedentes familiares cáncer gástrico (sí/no) | 16/17 (94,12%)/60/75 (85%) | 16/16 (100%)/60/70 (85,75%) | 1,267 | 1,128-1,423 | 0,108 | |
| Línea de tratamiento (1.a/2.a/3.a) | 84/107(78,15%)/35/41 (85,3%)/19/31 (61,3%) | 84/97 (86,6%)/35/41 (85,3%)/19/28 (67,8%) | - | - | 0,135 | |
| Omeprazol (sí/no) | 138/177 (77,97%)/6/8 (75%) | 138/165 (83,6%)/6/7 (85,7%) | 1,174 | 0,136-10,147 | 1,0 | |
| Dosis omeprazol (20/40/80mg/día) | 1/1 (100%)/119/157 (75,80%)/18/19 (94,7%) | 1/1 (100%)/119/145 (82,1%)/18/19 (94,7%) | - | - | 0,351 | |
| Cumplimiento terapéutico (sí/no) | 138/161 (85,7%)/1/9 (11,1%) | 138/157 (87,9%)/1/9 (11,1%) | 58,105 | 5,368-490,644 | 0,000 | |
| Intolerancia al tratamiento (sí/no) | 2/9 (22,2%)/136/158 (86,08%) | 2/9 (22,2%)/136/155 (87,7%) | 0,040 | 0,008-0,206 | 0,000 | |
| Anemia ferropénica (sí/no) | 13/16 (81,25%)/124/160 (77,5%) | 13/15 (86,7%)/124/148 (83,8%) | 1,258 | 0,267-5,936 | 0,771 | |
| Déficit vitamina B12 (sí/no) | 8/11 (72,7%)/114/140 (81,43%) | 8/11 (72,7%)/114/132 (86,4%) | 0,421 | 0,102-1,737 | 0,220 | |
| Trombocitopenia (sí/no) | 3/3 (100%)/137/178 (76,97%) | 3/3 (100%)/137/165 (97,9%) | 1,022 | (0,997-1,047 | 0,434 | |
| Metaplasia intestinal (sí/no) | 12/16 (75%) /86/109 (78,90%) | 12/16 (75%)/86/101 (85,1%) | 0,523 | (0,149-1,840 | 0,306 | |
| Úlcera péptica (sí/no) | 5/6 (83,3%)/94/123 (76,4%) | 5/6 (83,3%)/94/113 (83,2%) | 1,011 | (0,112-9,148) | 0,992 | |
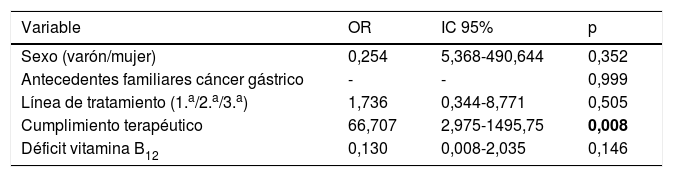
En el análisis multivariante (tabla 4) se obtuvo significación estadística en la tasa de erradicación para los pacientes que completaron el tratamiento (OR 66,7; IC 95% 2,98-1.495,75; p=0,008).
Análisis multivariante
| Variable | OR | IC 95% | p |
|---|---|---|---|
| Sexo (varón/mujer) | 0,254 | 5,368-490,644 | 0,352 |
| Antecedentes familiares cáncer gástrico | - | - | 0,999 |
| Línea de tratamiento (1.a/2.a/3.a) | 1,736 | 0,344-8,771 | 0,505 |
| Cumplimiento terapéutico | 66,707 | 2,975-1495,75 | 0,008 |
| Déficit vitamina B12 | 0,130 | 0,008-2,035 | 0,146 |
Los datos del último consenso español para el tratamiento de la infección por Helicobacter pylori estiman una prevalencia de hasta el 50% en todo el mundo1, considerándose un problema de salud en crecimiento. Además, las terapias de erradicación utilizadas anteriormente ofrecían tasas de erradicación subóptimas, en gran parte debido al aumento de la resistencia a los antibióticos utilizados en los tratamientos previos, como la claritromicina, que en nuestro país alcanzó el 14% en 200910 y el 18% en 20135, y en el centro-oeste y sur de Europa llegó a más de un 20%11.
En el último año, en España, se modificó el algoritmo terapéutico mediante la creación de un nuevo consenso1, basado en la evidencia disponible hasta la fecha. Este nuevo algoritmo introdujo la terapia cuádruple con bismuto como un tratamiento que debe tenerse en cuenta desde el momento del diagnóstico de la infección por Helicobacter pylori. Pylera® se incluyó en dicho algoritmo terapéutico como terapia de segunda línea en pacientes que no son alérgicos a la penicilina, y puede considerarse como la primera línea una vez que se confirme su eficacia en nuestro entorno.
Este tratamiento, en una sola formulación galénica (Pylera®), se ha comercializado recientemente en nuestro país. Este es un aspecto positivo que predispone a una mayor comodidad para los pacientes y, posiblemente, a una mejora en el cumplimiento terapéutico. En términos de eficacia, se demostró hasta un 90% de éxito en la erradicación en un ensayo clínico europeo multicéntrico en 20119 y en un estudio multicéntrico en 201410. Además, se han publicado datos recientes de práctica clínica en Italia, una muestra de 131 pacientes, con una eficacia global del 94,7% por IT12. Todos estos datos lo convierten en una alternativa terapéutica muy atractiva.
Nuestros resultados muestran que el tratamiento con Pylera®, 3 comprimidos cada 6h durante 10 días, como primera línea, logró una tasa de erradicación menor que las descritas en los estudios mencionados previamente (un 78,15% por IT y un 86,6% PP). Anteriormente, se llevaron a cabo 3 metaanálisis con tasas de erradicación similares, con la terapia cuádruple con bismuto (81, 78 y 77%), sin proporcionar ningún beneficio en comparación con la terapia triple. Aunque debe tenerse en cuenta que se trataba de tratamientos de 7 días de duración y no utilizaban la formulación galénica única, por lo que no se pueden considerar totalmente comparables con nuestro estudio13–15. Sin embargo, un ensayo clínico europeo de fase iii multicéntrico demostró una eficacia del 93% PP con el uso de Pylera®9, y un estudio multicéntrico estadounidense, una eficacia del 88% por IT16. La razón por la cual existe esta diferencia significativa con nuestro estudio podría explicarse por las altas tasas de resistencia al metronidazol, ya que los datos publicados en 2013 se refieren a una resistencia promedio a este antibiótico del 41% en nuestro país5. Sin embargo, no realizamos cultivos para la detección de resistencias a antibióticos en nuestro estudio.
En definitiva, en nuestra muestra, los pacientes naïve tratados con Pylera® obtuvieron una tasa de erradicación óptima de hasta un 86,6% PP (78% por IT), lo que podría respaldar el uso de dicho tratamiento en primera línea. En los pacientes previamente tratados que recibieron Pylera® como segunda línea, también se logró una eficacia aceptable del 85,3% por IT y PP. De esta forma, el uso de Pylera® podría tenerse en cuenta tanto en primera como en segunda línea de tratamiento, con porcentajes aceptables de eficacia del fármaco. En cuanto al uso en tercera línea, se obtuvieron tasas de erradicación mucho menores (61,3% por IT y 67,9% PP), lo que limitaría más su uso en esta línea de tratamiento.
Los datos del registro europeo del manejo de Helicobacter pylori, publicados como abstract en la reunión anual de la Asociación Española de Gastroenterología en 201817–19, mostraron resultados algo mayores en cuanto a la eficacia del tratamiento con Pylera®, fundamentalmente en primera y tercera línea. En primera línea se reportó una eficacia del 92% por IT (n=738 pacientes) y del 95% PP (n=706 pacientes)17. En segunda línea se reportó una eficacia más cercana a la de nuestro estudio, de un 76% por IT (n=169 pacientes) y de un 91% PP18. Y finalmente, en tercera línea se reportó una eficacia del 81% por IT (n=110 pacientes) y del 82% PP19. Además, con datos de este mismo registro se publicó otro abstract20 con 1.258 pacientes tratados con Pylera® donde los datos analizados mostraron: en primera línea, una eficacia del 92% por IT (n=666) y del 95% PP (n=633); en segunda línea, una eficacia del 89% por IT (n=273) y del 92% PP (n=260), y en tercera línea, una eficacia del 82% por IT (n=151) y del 85% PP (n=142). Posiblemente en este estudio los datos de eficacia mayores pueden explicarse por un tamaño muestral muy superior al de nuestro estudio y porque se trata de un registro europeo, donde se incluyen poblaciones diferentes a la española, con distintos perfiles de resistencias a antibióticos.
En estudios de eficacia previos con Pylera®9 y en su ficha técnica8, el tratamiento con omeprazol a dosis estándar se asocia cada 12h. Sin embargo, en los resultados preliminares recientes publicados como resúmenes en la reunión anual de la Asociación Española de Gastroenterología en 201721,22, el tratamiento asociado con esomeprazol a dosis doble cada 12h muestra unas tasas más altas de erradicación, hasta un 91,4% PP en la primera línea y un 85,9% en la tercera línea de tratamiento. En nuestro estudio, la mayoría de los pacientes fueron tratados con omeprazol, siendo anecdótico el uso de otros IBP. Sin embargo, encontramos que dosis de 20mg de omeprazol cada 12h obtuvieron una eficacia del 75,8% por IT y del 82,1% PP, y dosis de 40mg cada 12h mejoraron la tasa de erradicación al 94,7% por IT y PP en nuestro análisis. Aunque estas diferencias no fueron estadísticamente significativas, parece razonable pensar que con una mayor inhibición ácida, la eficacia del tratamiento tiende a mejorar.
El perfil de seguridad de Pylera® parece aceptable. En nuestra muestra, solo se registraron efectos secundarios menores en 7 pacientes (3,8%) y ningún efecto secundario grave. Teniendo en cuenta otras series, como la publicada recientemente en Italia12 con el 26,7%, así como el ensayo europeo multicéntrico que se refiere al 47% de los efectos secundarios menores, es posible que nuestra muestra presentara un sesgo significativo en la detección de efectos secundarios, posiblemente porque se consideran de poca relevancia y no se reflejan adecuadamente en la historia clínica de los gastroenterólogos, ya que solo se registraron aquellos que no completaron el tratamiento.
En nuestra serie, el cumplimiento terapéutico se logró en el 87% de los pacientes, y fue el único factor que tuvo un efecto estadísticamente significativo en la mejora de las tasas de erradicación. Nuestros resultados mostraron bajos porcentajes de efectos secundarios asociados con altas tasas de cumplimiento terapéutico. Finalmente, no se encontró una correlación significativa entre ninguna otra variable y las tasas de erradicación, lo que permite considerar el tratamiento con Pylera® para un amplio espectro de pacientes.
Las principales limitaciones de este estudio están relacionadas con el tamaño de la muestra, que puede haber limitado las conclusiones alcanzadas en el estudio. Sin embargo, presentamos el primer estudio de práctica clínica real en España, que permite una evaluación inicial del tratamiento con Pylera® en nuestro medio.
En conclusión, se puede considerar que el tratamiento con Pylera® presenta tasas de erradicación aceptables para primera y segunda línea en España. Además, estas tasas de erradicación pueden mejorarse si se asocian dosis más altas de omeprazol que las establecidas en la ficha técnica del medicamento. Este tratamiento presenta un perfil de seguridad adecuado y un alto porcentaje de cumplimiento terapéutico. Todo esto permite considerarlo para la infección por Helicobacter pylori en un amplio espectro de pacientes. Sin embargo, se necesitan más estudios clínicos con mayores tamaños muestrales que permitan confirmar estos resultados.
AutoríaLa Dra. Sandra Agudo-Fernández diseñó el proyecto, participó en la recogida de datos, en el análisis de los resultados y en la interpretación de los mismos, y escribió el presente documento.
La Dra. Ana González Blanco participó en la recogida de datos, en el análisis de los resultados y realizó la revisión crítica del presente estudio.
Conflicto de interesesLas autoras del presente estudio declaran que no tienen ningún conflicto de intereses y que la presente investigación no ha recibido becas específicas provenientes de agencias del sector público, sector comercial o sin ánimo de lucro.