La sonda XL de FibroScan® se diseñó para medir la rigidez hepática por elastografía de transición en pacientes obesos, pero se ha estudiado insuficientemente en pacientes no obesos. El objetivo de este trabajo fue comparar las sondas M y XL de FibroScan® en una serie de pacientes consecutivos con enfermedad hepática crónica, obesos y no obesos. Se realizó un estudio de elastografía con las sondas M y XL a 254 pacientes. Los resultados obtenidos con ambas sondas se compararon en la serie completa y en pacientes obesos (n=82) y no obesos (n=167) por separado. La fiabilidad del estudio se basó en los criterios de Castéra et al. La proporción de estudios fiables fue significativamente mayor con la sonda XL (83% versus 73%; p=0,001). Esta significación se mantuvo en el grupo de obesos (82% versus 55%; p<0,001), pero no en los no obesos (84% versus 83%). Existía una correlación significativa entre los valores de rigidez (R=0,897; p<0,001) y concordancia en la estimación de fibrosis (alfa de Cronbach=0,932) obtenidos con ambas sondas. Los valores de rigidez hepática obtenidos con la sonda XL fueron menores que los obtenidos con la sonda M en la serie global (9,5±9,1kPa versus 11,3±12,6kPa; p<0,001) y en los grupos de pacientes obesos y no obesos. En conclusión, la elastografía de transición con la sonda XL obtiene una mayor proporción de exámenes fiables en pacientes obesos, pero no en pacientes no obesos. La sonda XL obtiene valores de rigidez hepática inferiores a los de la sonda M.
The FibroScan® XL probe has been specifically designed for obese patients to measure liver stiffness by transient elastography, but it has not been well tested in non-obese patients. The aim of this study was to compare the M and XL FibroScan® probes in a series of unselected obese (body mass index above 30kg/m2) and non-obese patients with chronic liver disease.
Two hundred and fifty-four patients underwent a transient elastography examination with both the M and XL probes. The results obtained with the two probes were compared in the whole series and in obese (n=82) and non-obese (n=167) patients separately. The reliability of the examinations was assessed using the criteria defined by Castéra et al.
The proportion of reliable exams was significantly higher when the XL probe was used (83% versus 73%; P=.001). This significance was maintained in the group of obese patients (82% versus 55%; P<.001), but not in the non-obese patients (84% versus 83%). Despite a high correlation between the stiffness values obtained with the two probes (R=.897; P<.001), and a high concordance in the estimation of fibrosis obtained with the two probes (Cronbach's alpha value: 0.932), the liver stiffness values obtained with the XL probe were significantly lower than those obtained with the M probe, both in the whole series (9.5±9.1kPa versus 11.3±12.6kPa; P<0.001) and in the obese and non-obese groups.
In conclusion, transient elastography with the XL probe allows a higher proportion of reliable examinations in obese patients but not in non-obese patients. Stiffness values were lower with the XL probe than with the M probe.
La elastografía de transición por medio de FibroScan® (Echosens, París, Francia) es un método de medición de la rigidez hepática, una estimación de fibrosis hepática en pacientes con enfermedades hepáticas crónicas, sobre todo en pacientes con hepatitisC1. En la mayoría de los pacientes con enfermedad hepática crónica, la medición obtenida de esta manera no invasiva es fiable. Sin embargo, la obesidad supone una de sus principales limitaciones, ya que se obtienen valores fiables en menos del 50% de los pacientes2. La sonda XL, que ha sido diseñada específicamente para pacientes obesos, aumenta la proporción de medidas fiables de FibroScan® en estos pacientes3. Esta nueva sonda contiene un transductor ultrasónico de menor frecuencia y mayor sensibilidad, una longitud focal más profunda, una mayor amplitud de vibración y una mayor profundidad de medida bajo la superficie cutánea. Hasta el momento, pocos estudios han evaluado la utilidad de la sonda XL en pacientes obesos y con sobrepeso, y solo uno ha estudiado su fiabilidad en un gran número de pacientes, incluyendo pacientes con peso normal4.
El objetivo de este estudio fue el de comparar las sondas M y XL de FibroScan® en una serie de pacientes con enfermedad hepática crónica consecutivos, no seleccionados, obesos y no obesos.
Pacientes y métodosEste estudio prospectivo fue aprobado por la Comisión de Ética en Investigación del centro. Los pacientes fueron reclutados en un único centro entre septiembre de 2010 y marzo de 2011. Los pacientes adultos a los que se realizó una elastografía de transición fueron incluidos en el estudio en caso de que dieran su consentimiento informado por escrito. La investigación cumple con la Declaración de Helsinki y con las leyes españolas que afectan a la investigación biomédica y a la protección de datos. El Comité de Ética de Investigación de la Universidad de Navarra aprobó el estudio antes de su inicio.
Datos clínicosLos siguientes datos se obtuvieron antes de realizar el estudio de elastografía: edad, sexo, peso, talla, índice de masa corporal, perímetro de cintura e indicación de la elastografía. También se recogieron los siguientes datos bioquímicos: pruebas hepáticas (aspartato aminotransferasa [AST], alanina aminotransferasa [ALT], fosfatasa alcalina, gamma-glutamil transpeptidasa [GGT], bilirrubina), recuento de plaquetas y glucosa en ayunas. Se registró si los pacientes tenían antecedentes de hipertensión arterial, diabetes y dislipidemia.
Medida de la rigidez hepáticaTres operadores experimentados realizaron todos los estudios de elastografía, de acuerdo con las indicaciones del fabricante. Los 3 habían realizado al menos 250estudios previamente. Con el paciente en decúbito supino y el brazo derecho en abducción máxima, se realizó un estudio ecográfico para identificar una región del hígado con un mínimo de 6cm de espesor, libre de vasos de gran calibre. En este punto se midió la distancia entre la piel y la cápsula hepática (piel-cápsula) y se realizó el estudio de elastografía con ambas sondas, hasta obtener 10medidas válidas o hasta un máximo de 20disparos.
De acuerdo con Castéra et al.2, el estudio se consideró fallido si no se obtuvo ninguna medición válida en ninguno de los 20disparos, y se consideró fiable si: a)se obtuvieron 10mediciones válidas; b)la proporción de mediciones válidas fue al menos del 60%, y c)el rango intercuartílico (IQR [interquartile range], que refleja la variabilidad de las mediciones) fue menor del 30% del valor de la mediana de rigidez hepática obtenido (LSM [liver stiffness measurement]) (IQR/LSM<0,3).
Si el estudio se consideró válido, se admitió que existía fibrosis hepática significativa (mayor de F1) y cirrosis si la mediana de rigidez medida era mayor de 7 y 12kPa, respectivamente, de acuerdo con los resultados del metaanálisis de Tsochatzis et al.5. Se estudió el grado de concordancia del resultado obtenido con ambas sondas.
Comparación entre sondas M y XLSe compararon las proporciones de exploraciones fiables obtenidas con cada sonda y las causas de no fiabilidad del estudio. Este análisis se realizó en la serie completa, y después de forma independiente en el grupo de pacientes obesos y no obesos (definiendo obesidad como un índice de masa corporal mayor de 30kg/m2). Se compararon las proporciones de medidas válidas obtenidas con cada sonda. Cuando las exploraciones fueron fiables con ambas sondas, se compararon las medianas de los valores de rigidez hepática obtenidos con ellas.
Se realizó biopsia hepática percutánea con una diferencia de tiempo entre ambas pruebas menor de 3meses a 57pacientes. Las indicaciones de la biopsia fueron: hepatitisC (12pacientes), hepatitisC en pacientes trasplantados (8pacientes), cirrosis etílica (11pacientes), esteatosis/esteatohepatitis no alcohólica (6pacientes), esteatosis en pacientes trasplantados (8pacientes), hepatitisB (6pacientes), hepatitis autoinmune (4pacientes) y otras indicaciones (6pacientes). En las biopsias, la fibrosis se categorizó de acuerdo con la clasificación de Knodell6, que cataloga la fibrosis en 4estadios (0, 1, 3 y 4). Se consideró fibrosis no significativa a los estadios 0 y 1, fibrosis significativa sin cirrosis al estadio 3 y cirrosis al estadio 4. En estos pacientes se estudiaron la sensibilidad y la especificidad de la elastografía realizada con cada una de ambas sondas para detectar fibrosis significativa y cirrosis.
Análisis estadísticoLos estudios estadísticos se realizaron con el programa SPSS 15.0.1 para Windows. Las variables continuas se expresan como media±desviación estándar. Las comparaciones entre ambos grupos se realizaron por medio de la t de Student para datos pareados o el test de Wilcoxon (variables continuas) y el test de χ2 o el test exacto de Fisher (variables categóricas). Las correlaciones se obtuvieron por medio del coeficiente de correlación de Pearson. Se consideró estadísticamente significativa una p<0,05. La consistencia interna de los resultados obtenidos con cada sonda se expresó como el valor alfa de Cronbach, coeficiente de estabilidad test-retest y consistencia interna mediante el test de las 2 mitades. Se obtuvieron las áreas bajo la curva ROC (receiver operating characteristic) para valorar la fiabilidad diagnóstica de la elastografía con cada una de las sondas en el diagnóstico de fibrosis significativa o cirrosis.
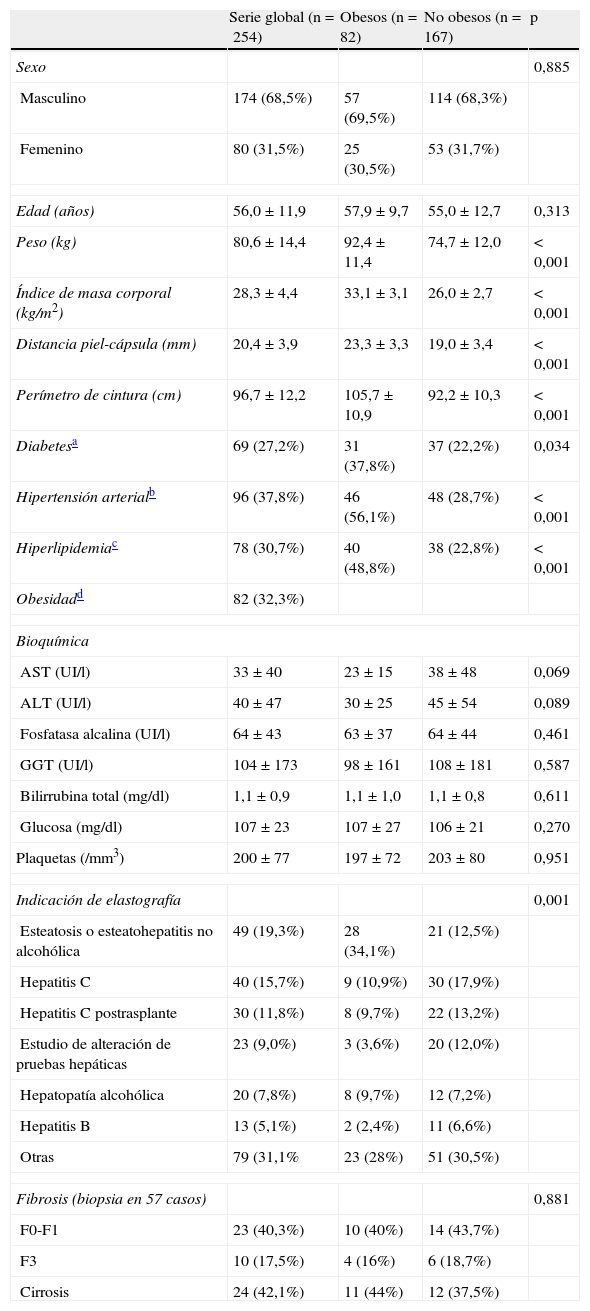
ResultadosResultados en la serie globalSe incluyeron en el estudio 254pacientes. El 68% de ellos eran varones y el 32% eran obesos. Las características generales de los pacientes se muestran en la tabla 1. Existía una correlación significativa entre: perímetro de cintura e índice de masa corporal (R=0,780; p< 0,001); perímetro de cintura y distancia piel-cápsula (R=0,571; p<0,001), e índice de masa corporal y distancia piel-cápsula (R=0,654; p<0,001).
Características generales de los pacientes
| Serie global (n=254) | Obesos (n=82) | No obesos (n=167) | p | |
| Sexo | 0,885 | |||
| Masculino | 174 (68,5%) | 57 (69,5%) | 114 (68,3%) | |
| Femenino | 80 (31,5%) | 25 (30,5%) | 53 (31,7%) | |
| Edad (años) | 56,0 ± 11,9 | 57,9 ± 9,7 | 55,0 ± 12,7 | 0,313 |
| Peso (kg) | 80,6 ± 14,4 | 92,4 ± 11,4 | 74,7 ± 12,0 | < 0,001 |
| Índice de masa corporal (kg/m2) | 28,3 ± 4,4 | 33,1 ± 3,1 | 26,0 ± 2,7 | < 0,001 |
| Distancia piel-cápsula (mm) | 20,4 ± 3,9 | 23,3 ± 3,3 | 19,0 ± 3,4 | < 0,001 |
| Perímetro de cintura (cm) | 96,7 ± 12,2 | 105,7 ± 10,9 | 92,2 ± 10,3 | < 0,001 |
| Diabetesa | 69 (27,2%) | 31 (37,8%) | 37 (22,2%) | 0,034 |
| Hipertensión arterialb | 96 (37,8%) | 46 (56,1%) | 48 (28,7%) | < 0,001 |
| Hiperlipidemiac | 78 (30,7%) | 40 (48,8%) | 38 (22,8%) | < 0,001 |
| Obesidadd | 82 (32,3%) | |||
| Bioquímica | ||||
| AST (UI/l) | 33 ± 40 | 23 ± 15 | 38 ± 48 | 0,069 |
| ALT (UI/l) | 40 ± 47 | 30 ± 25 | 45 ± 54 | 0,089 |
| Fosfatasa alcalina (UI/l) | 64 ± 43 | 63 ± 37 | 64 ± 44 | 0,461 |
| GGT (UI/l) | 104 ± 173 | 98 ± 161 | 108 ± 181 | 0,587 |
| Bilirrubina total (mg/dl) | 1,1 ± 0,9 | 1,1 ± 1,0 | 1,1 ± 0,8 | 0,611 |
| Glucosa (mg/dl) | 107 ± 23 | 107 ± 27 | 106 ± 21 | 0,270 |
| Plaquetas (/mm3) | 200 ± 77 | 197 ± 72 | 203 ± 80 | 0,951 |
| Indicación de elastografía | 0,001 | |||
| Esteatosis o esteatohepatitis no alcohólica | 49 (19,3%) | 28 (34,1%) | 21 (12,5%) | |
| Hepatitis C | 40 (15,7%) | 9 (10,9%) | 30 (17,9%) | |
| Hepatitis C postrasplante | 30 (11,8%) | 8 (9,7%) | 22 (13,2%) | |
| Estudio de alteración de pruebas hepáticas | 23 (9,0%) | 3 (3,6%) | 20 (12,0%) | |
| Hepatopatía alcohólica | 20 (7,8%) | 8 (9,7%) | 12 (7,2%) | |
| Hepatitis B | 13 (5,1%) | 2 (2,4%) | 11 (6,6%) | |
| Otras | 79 (31,1% | 23 (28%) | 51 (30,5%) | |
| Fibrosis (biopsia en 57 casos) | 0,881 | |||
| F0-F1 | 23 (40,3%) | 10 (40%) | 14 (43,7%) | |
| F3 | 10 (17,5%) | 4 (16%) | 6 (18,7%) | |
| Cirrosis | 24 (42,1%) | 11 (44%) | 12 (37,5%) | |
ALT: alanina aminotransferasa; AST: aspartato aminotransferasa; GGT: gamma-glutamil transpeptidasa.
De acuerdo con los criterios mencionados previamente, la proporción de pacientes sin fibrosis significativa, con fibrosis significativa pero sin cirrosis, y con cirrosis, fue del 52, del 23 y del 25%, respectivamente, cuando se usó la sonda M, y del 61, del 19 y del 20%, respectivamente, cuando se usó la sonda XL.
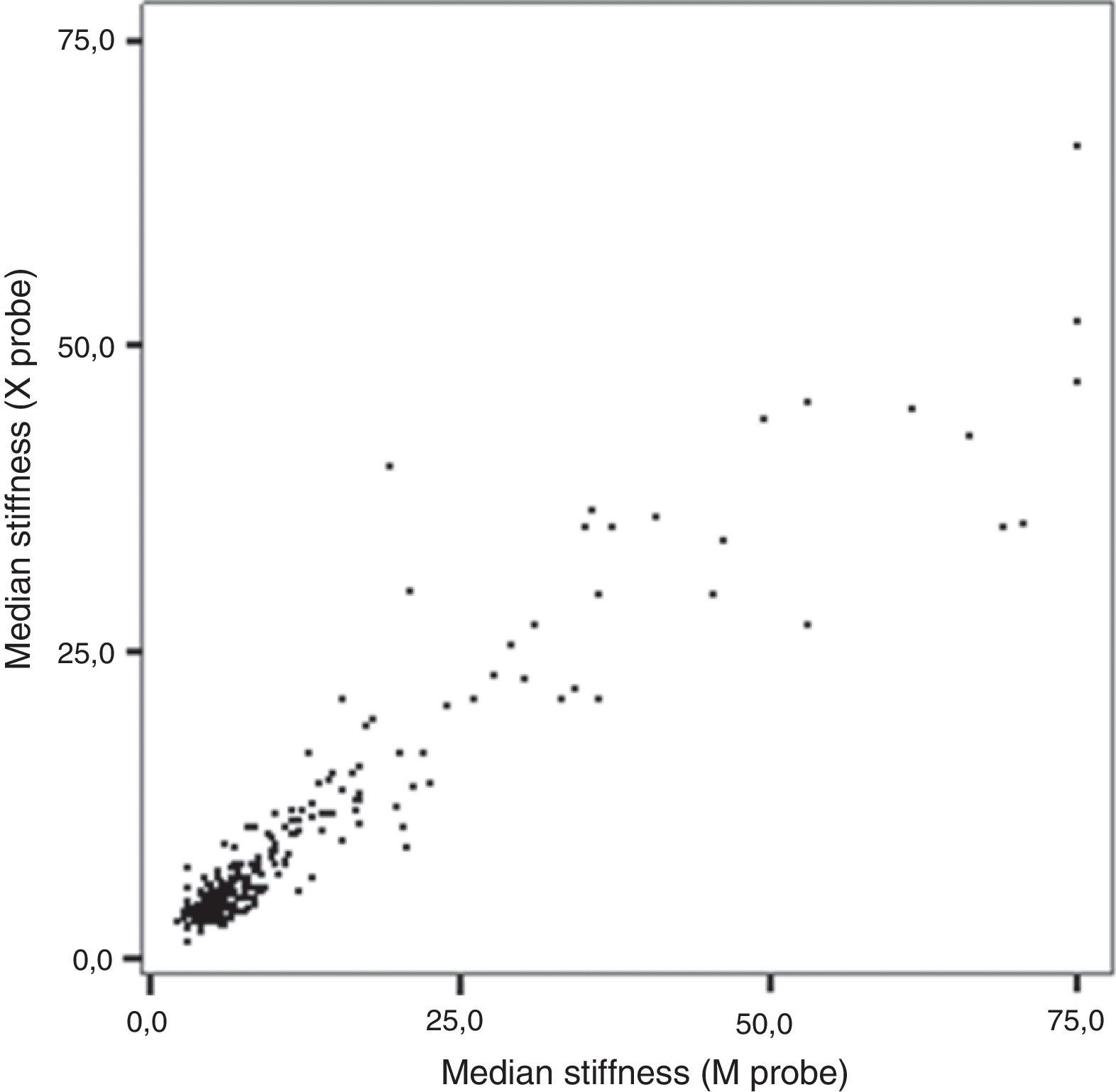
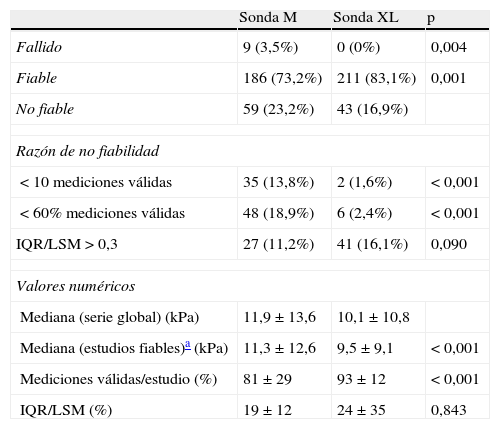
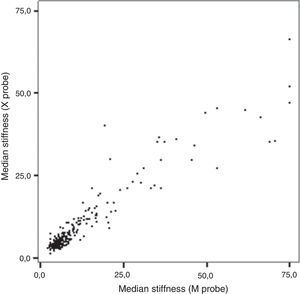
Los resultados de la comparación de ambas sondas se muestran en la tabla 2. La proporción de estudios fiables fue significativamente mayor con la sonda XL, principalmente porque la proporción de estudios con menos de un 60% de mediciones válidas fue menor. Entre los estudios fiables, la correlación entre los valores de rigidez medidos con cada una de las sondas fue significativa (R=0,897; p<0,001) (fig. 1). El grado de concordancia para las mediciones realizadas con cada una de las sondas fue del 88% para la presencia/ausencia de fibrosis y del 94% para la presencia/ausencia de cirrosis). El valor alfa de Cronbach fue de 0,932, el coeficiente de estabilidad test-retest fue de 0,876 y la consistencia interna en el test de las 2 mitades fue de 0,932. Sin embargo, la mediana de rigidez medida con la sonda XL fue significativamente inferior que la medida con la sonda M.
Comparación de los resultados obtenidos con las sondas M y XL de elastografía en los 254 pacientes estudiados
| Sonda M | Sonda XL | p | |
| Fallido | 9 (3,5%) | 0 (0%) | 0,004 |
| Fiable | 186 (73,2%) | 211 (83,1%) | 0,001 |
| No fiable | 59 (23,2%) | 43 (16,9%) | |
| Razón de no fiabilidad | |||
| < 10 mediciones válidas | 35 (13,8%) | 2 (1,6%) | < 0,001 |
| < 60% mediciones válidas | 48 (18,9%) | 6 (2,4%) | < 0,001 |
| IQR/LSM > 0,3 | 27 (11,2%) | 41 (16,1%) | 0,090 |
| Valores numéricos | |||
| Mediana (serie global) (kPa) | 11,9 ± 13,6 | 10,1 ± 10,8 | |
| Mediana (estudios fiables)a (kPa) | 11,3 ± 12,6 | 9,5 ± 9,1 | < 0,001 |
| Mediciones válidas/estudio (%) | 81 ± 29 | 93 ± 12 | < 0,001 |
| IQR/LSM (%) | 19 ± 12 | 24 ± 35 | 0,843 |
IQR: interquartile range (rango intercuartílico); LSM: liver stiffness median (mediana de rigidez hepática).
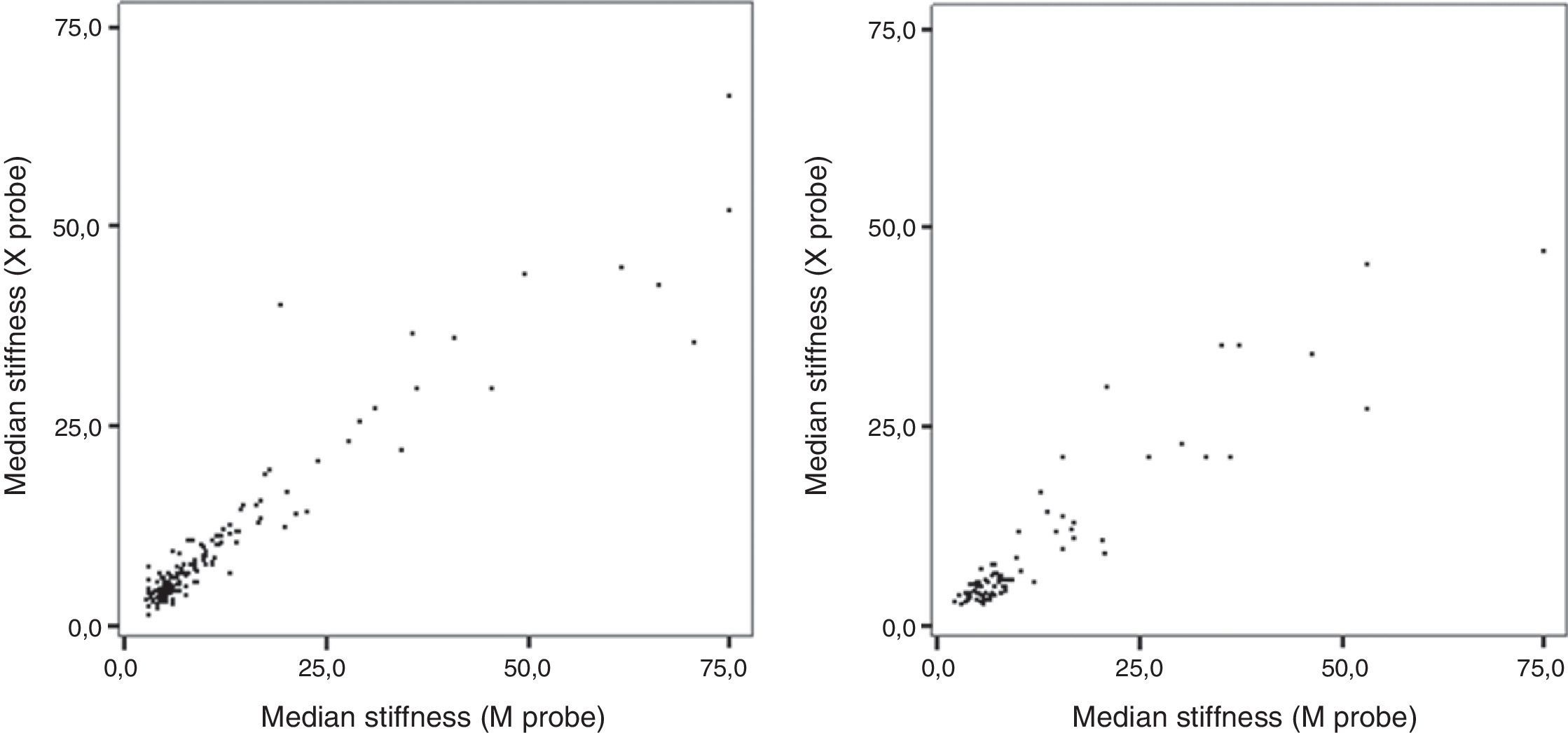
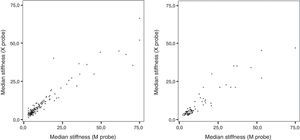
La comparación entre ambas sondas en pacientes no obesos se muestra en la tabla 3. La proporción de estudios fiables fue similar con ambas sondas. La concordancia entre las mediciones realizadas con ambas sondas fue del 91,8% para la presencia/ausencia de fibrosis significativa y del 96,7% para la presencia/ausencia de cirrosis. El valor alfa de Cronbach fue de 0,949, el coeficiente de estabilidad test-retest fue de 0,720 y la consistencia interna en el test de las 2 mitades fue de 0,949. La mediana de rigidez medida con la sonda XL fue significativamente inferior que la medida con la sonda M. La correlación entre los valores obtenidos con ambas sondas en pacientes no obesos se muestra en la figura 2a.
Comparación de los resultados obtenidos con las sondas M y XL de elastografía
| Sonda M | Sonda XL | p | |
| Pacientes no obesos (n=167) | |||
| Fallido | 4 (2,4%) | 0 (0%) | 0,123 |
| Fiable | 138 (82,6%) | 141 (84,4%) | 1,000 |
| No fiable | 25 (14,9%) | 26 (15,6%) | |
| Razón de no fiabilidad | |||
| < 10 mediciones válidas | 10 (6,0%) | 2 (1,2%) | 0,035 |
| < 60% mediciones válidas | 17 (10,2%) | 3 (1,8%) | 0,002 |
| IQR/LSM > 0,3 | 14 (8,6%) | 24 (14,4%) | 0,120 |
| Valores numéricos | |||
| Mediana (serie global) (kPa) | 11,2 ± 13,2 | 9,6 ± 10,0 | |
| Mediana (estudios fiables)a (kPa) | 10,6 ± 11,1 | 9,1 ± 8,4 | < 0,001 |
| Mediciones válidas/estudio (%) | 88 ± 22 | 95 ± 11 | < 0,001 |
| IQR/LSM (%) | 19 ± 12 | 22 ± 15 | 0,697 |
| Pacientes obesos (n = 82) | |||
| Fallido | 4 (4,8%) | 0 (0%) | 0,120 |
| Fiable | 45 (54,9%) | 67 (81,7%) | < 0,001 |
| No fiable | 33 (40,2%) | 15 (18,3%) | |
| Razón de no fiabilidad | |||
| < 10 mediciones válidas | 23 (28,0%) | 2 (2,4%) | < 0,001 |
| < 60% mediciones válidas | 29 (35,4%) | 3 (3,6%) | < 0,001 |
| IQR/LSM > 0,3 | 12 (16,0%) | 15 (18,3%) | 0,674 |
| Valores numéricos | |||
| Mediana (serie global) (kPa) | 12,5 | 13,4 | |
| Mediana (estudios fiables)b (kPa) | 12,2 ± 13,4 | 9,8 ± 10,6 | < 0,001 |
| Mediciones válidas/estudio (%) | 66 ± 33 | 91 ± 15 | < 0,001 |
| IQR/LSM (%) | 19 ± 11 | 28 ± 58 | 0,840 |
IQR: interquartile range (rango intercuartílico); LSM: liver stiffness median (mediana de rigidez hepática).
De acuerdo con los criterios mencionados previamente, la proporción de pacientes sin fibrosis significativa, fibrosis sin cirrosis y cirrosis fue del 54, del 22 y del 23%, respectivamente, cuando se usó la sonda M, y del 62, del 19 y del 19%, respectivamente, cuando se usó la sonda XL.
La comparación entre ambas sondas en pacientes obesos se muestra en la tabla 3. La proporción de estudios fiables fue significativamente mayor con la sonda XL que con la sonda M, debido a una menor proporción de estudios con menos del 60% de mediciones válidas. De la misma forma, la proporción de medidas válidas en cada estudio fue significativamente mayor con la sonda XL. La rigidez fue significativamente menor con la sonda XL que con la sonda M. La concordancia entre las mediciones realizadas con ambas sondas fue menor en obesos que en no obesos (76,9% para la presencia/ausencia de fibrosis significativa y 89,7% para la presencia/ausencia de cirrosis). El valor alfa de Cronbach fue de 0,888, el coeficiente de estabilidad test-retest fue de 0,801 y la consistencia interna en el test de las 2 mitades fue de 0,889. La correlación entre los valores obtenidos con ambas sondas en pacientes no obesos se muestra en la figura 2b.
De acuerdo con los criterios mencionados previamente, la proporción de pacientes sin fibrosis significativa, fibrosis sin cirrosis y cirrosis fue del 47, del 22 y del 31%, respectivamente, cuando se usó la sonda M, y del 63, del 18 y del 19%, respectivamente, cuando se usó la sonda XL.
Comparación entre los resultados de elastografía y anatomía patológicaSe dispuso de biopsia hepática de 57pacientes. De acuerdo con el índice de Knodell, 23pacientes (40,3%) no tenían fibrosis o tenían fibrosis mínima (F0 o F1) y 34pacientes (59,7%) tenían fibrosis significativa (mayor de F1). Veinticuatro pacientes (42,1%) tenían cirrosis. La elastografía realizada con ambas sondas tuvo una sensibilidad del 100% para el diagnóstico de fibrosis significativa, con una especificidad del 58,8% (con la sonda M) y del 68,4% (con la sonda XL). La sensibilidad para el diagnóstico de cirrosis estuvo en torno al 90%, con una especificidad del 71-72%. Los resultados se resumen en la tabla 4. El área bajo la curva ROC para el diagnóstico de fibrosis significativa fue de 0,936 con la sonda M y de 0,958 con la sonda XL, con unos puntos de corte óptimos de 9,4 y 7,9kPa, respectivamente. El área bajo la curva ROC para el diagnóstico de cirrosis fue de 0,934 con la sonda M y de 0,903 con la sonda XL, con unos puntos de corte óptimos de 13,0 y 13,5kPa, respectivamente.
Sensibilidad y especificidad de las sondas M y XL para la detección de fibrosis significativa o cirrosis en 57 pacientes con biopsia hepáticaa
| Sonda M | Sonda XL | |
| Serie global (n=57) | ||
| Fibrosis significativa | ||
| Sensibilidad | 100% | 100% |
| Especificidad | 58,8% | 68,4% |
| Cirrosis | ||
| Sensibilidad | 92,8% | 88,9% |
| Especificidad | 72,0% | 71,4% |
| No obesos (n=32) | ||
| Fibrosis significativa | ||
| Sensibilidad | 100% | 93,3% |
| Especificidad | 77,8% | 54,5% |
| Cirrosis | ||
| Sensibilidad | 88,9% | 88,9% |
| Especificidad | 73,7% | 70,6% |
| Obesos (n = 25) | ||
| Fibrosis significativa | ||
| Sensibilidad | 100% | 100% |
| Especificidad | 75% | 85,7% |
| Cirrosis | ||
| Sensibilidad | 100% | 95,7% |
| Especificidad | 57,1% | 70% |
De Tsochatzis et al.5.
Una de las situaciones en la que FibroScan® tiene más limitaciones en la medida de la rigidez hepática es en los pacientes obesos2. La nueva sonda XL ofrece un beneficio en estos pacientes. En nuestra serie, el número de estudios fiables aumenta del 55% al 82% en pacientes obesos, de acuerdo con los resultados encontrados por otros autores3,7,8. En este estudio también se ha evaluado la posibilidad de utilizar la sonda XL tanto para pacientes obesos como para no obesos. El uso de la sonda XL en pacientes no obesos no supuso ningún beneficio. La proporción de mediciones válidas en pacientes obesos fue mayor con la sonda XL (lo que reduce de forma no significativa la proporción de estudios no fiables por bajo porcentaje de mediciones válidas), pero produjo un aumento no significativo de estudios no fiables por un elevado cociente IQR/LSM.
Otro asunto de importancia es la posibilidad de comparar los resultados obtenidos con ambas sondas. Hemos encontrado que los valores de rigidez hepática obtenidos con la sonda XL son significativamente menores que con la sonda M. Estos resultados coinciden con los hallazgos de otros autores8. Por ello, los puntos de corte para el diagnóstico de fibrosis significativa o cirrosis deberían ser distintos cuando el estudio se hace con la sonda XL que cuando se hace con la sonda M. No obstante, la concordancia en el diagnóstico de fibrosis significativa o cirrosis con ambas sondas estuvo en torno al 90%, de forma similar a lo encontrado en otra serie4.
Por último, los resultados de este estudio muestran una alta sensibilidad de los resultados de la elastografía de transición. Con los puntos de corte seleccionados, la sensibilidad para detectar fibrosis significativa o cirrosis estuvo en el 90-100%, aunque la especificidad fue del 60-70%. Esto refuerza el concepto de que la elastografía es un excelente método para demostrar la presencia de fibrosis avanzada o cirrosis, pero su baja especificidad no permite que esta prueba sustituya a la biopsia hepática. En nuestro estudio, los puntos óptimos para la predicción de fibrosis significativa (mayor de F1) fueron algo mayores que los que se habían escogido a priori, en base al trabajo de Tsochatzis et al.5. Además, el punto de corte óptimo para la predicción de fibrosis significativa fue mayor con la sonda M que con la sonda XL. Estos hallazgos y la definición de los puntos de corte óptimos para cada sonda deberán ser confirmados en estudios prospectivos con mayor número de pacientes.
En conclusión, la elastografía de transición con la sonda FibroScan® XL permite la medición de la rigidez hepática en una mayor proporción de pacientes obesos, pero no en pacientes no obesos. Los valores de rigidez hepática obtenidos con la sonda XL son menores que con la sonda M. Sería necesario hacer nuevos estudios prospectivos que definan los puntos de corte óptimos cuando se usa la sonda XL.
FinanciaciónEl Centro de Investigación Biomédica en Red de Enfermedades Hepáticas y Digestivas (CIBERehd) está financiado por el Instituto de Salud CarlosIII.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.