Las fístulas aorto-entéricas (FAE) representan una entidad infrecuente como etiología de sangrado digestivo, asociándose a una elevada mortalidad si existe demora en su diagnóstico y por tanto en su tratamiento1–5. Dichas fístulas surgen de una comunicación directa entre la aorta y el tracto gastrointestinal, bien de forma primaria en pacientes con aneurismas ateroscleróticos de aorta abdominal o de forma secundaria en pacientes con prótesis de aorta abdominal insertadas previamente1.
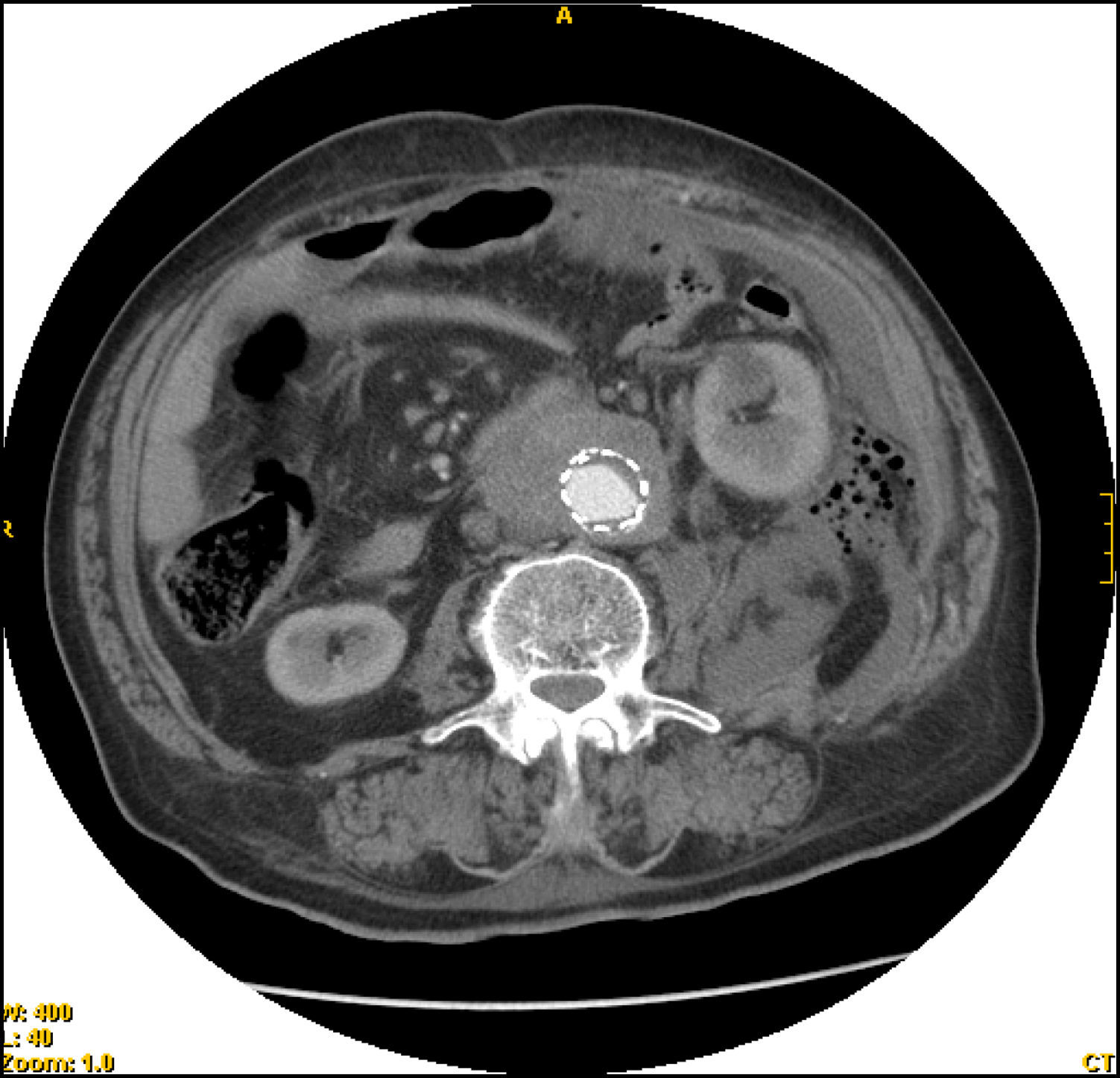
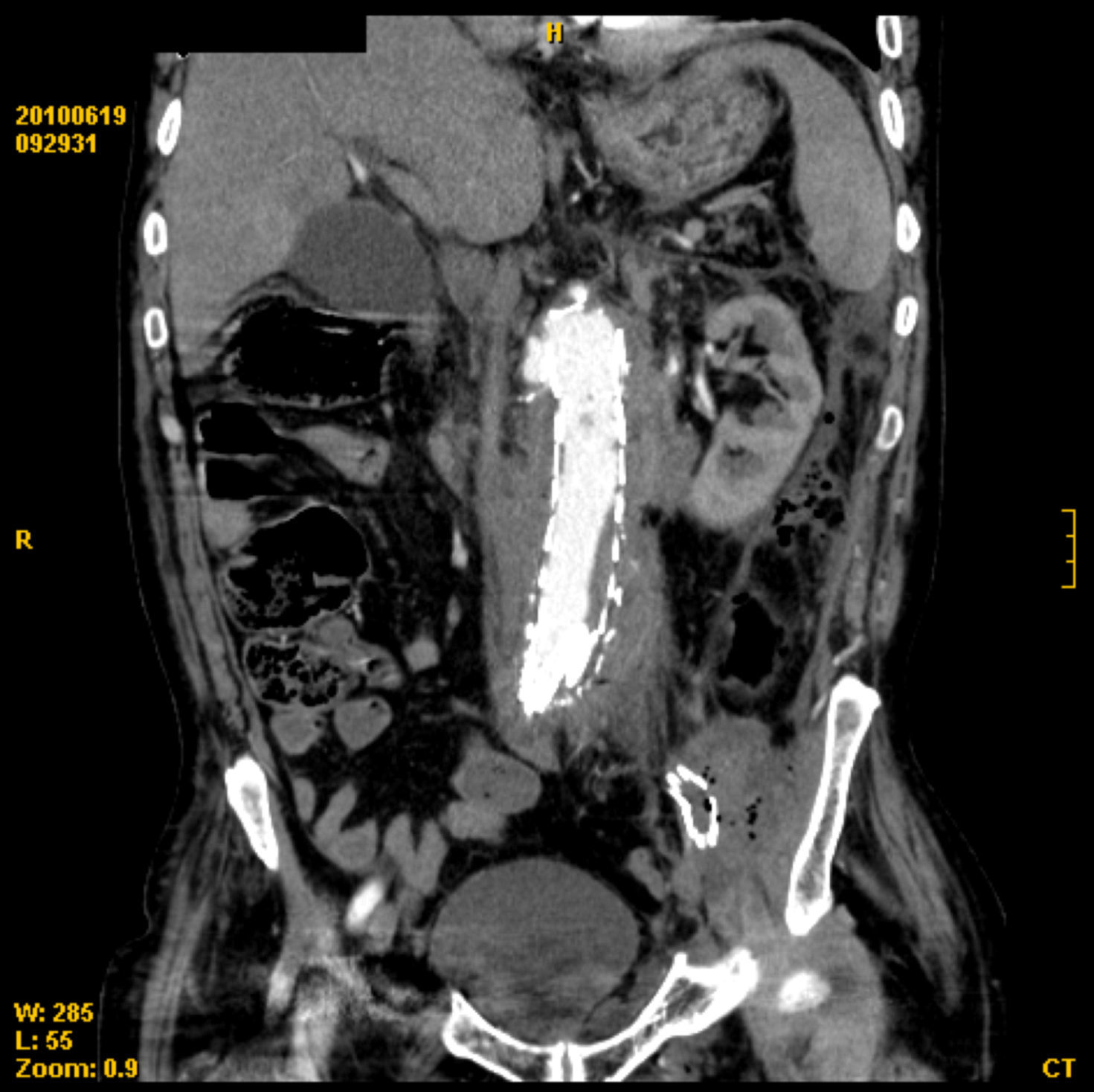
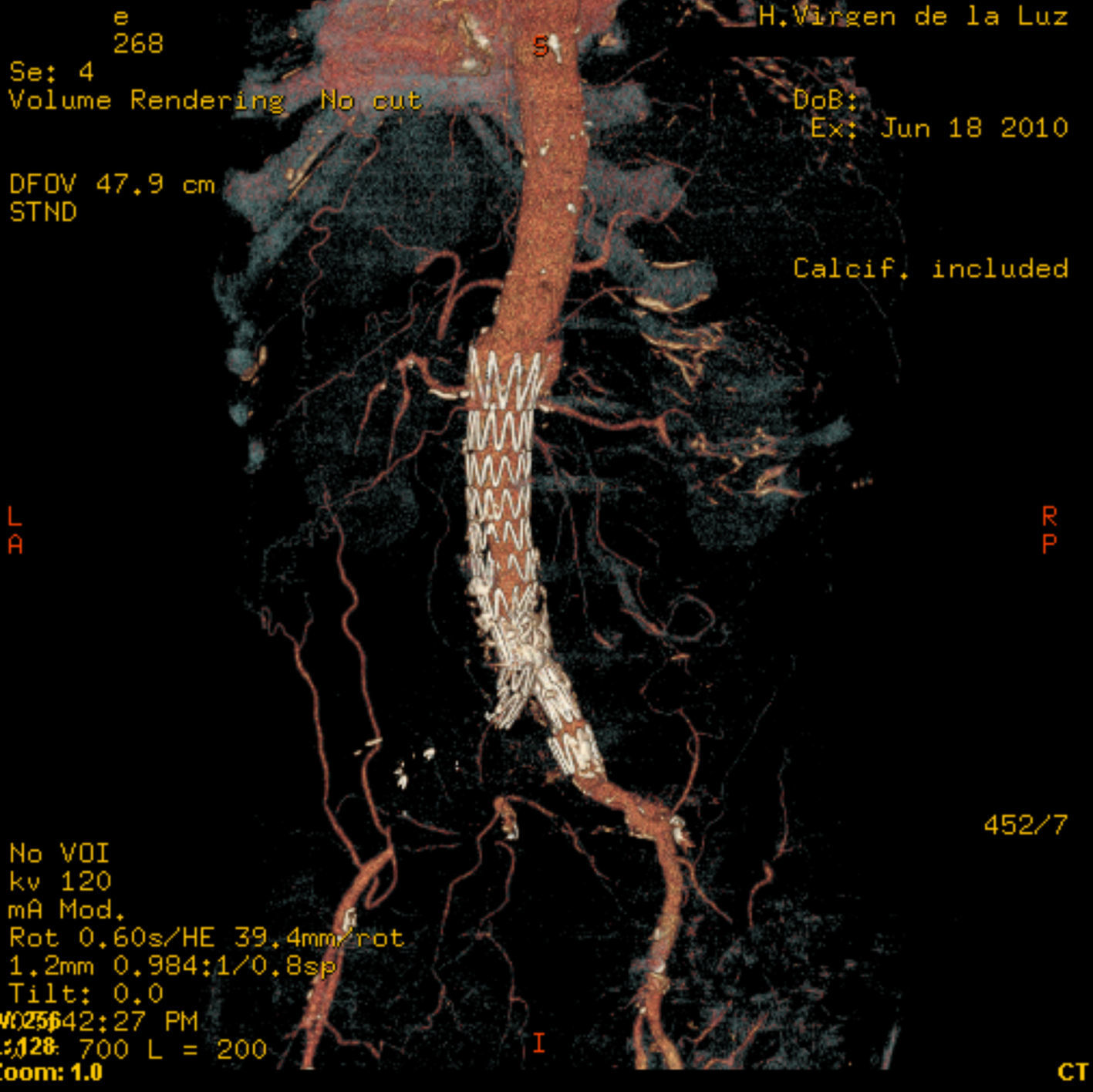
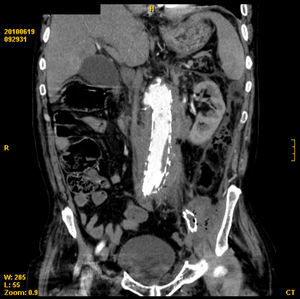
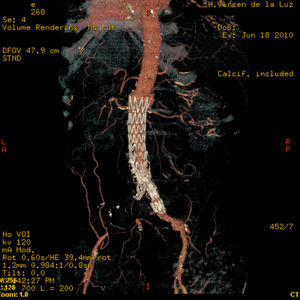
Presentamos el caso de un varón de 80 años que acudió a urgencias tras presentar un episodio de hematemesis. El paciente tenía antecedentes de perforación gástrica hace 28 años y fallo renal agudo en 2004 que requirió hemodiálisis. En ese momento fue diagnosticado de aneurisma inflamatorio de la aorta infrarrenal con afectación de ambas ilíacas comunes, afectación de ambos uréteres y vena cava inferior. Dicho aneurisma fue intervenido implantándose una endoprótesis aórtica-ilíaca. En la exploración física presentaba un abdomen ligeramente doloroso a la palpación en flanco izquierdo y ausencia de pulsos femoral y pedio izquierdos, evidenciando frialdad en miembro inferior izquierdo distal así como dolor a la movilización activa y pasiva de dicho miembro. En el tacto rectal no se observaron melenas. Analíticamente destacaban: anemia normocítica (Hb 8,3g/dl, Hto 25,3%), trombocitosis (552 mill/mmc), actividad de protrombina 56%, FNG 822mg/dl, CK 219 U/l y PCR 422,1mg/l. Se realizó gastroscopia urgente a su llegada a urgencias, observándose una hernia de hiato axial no complicada, estómago con cirugía gástrica previa Billroth II sin presencia de restos hemáticos, con muñón gástrico y ambas asas sin alteraciones. Durante las primeras 48h el paciente permaneció hemodinámicamente estable y con dolor persistente a nivel de fosa ilíaca izquierda. Ante la sospecha de HDA por fístula aorto-entérica se inició tratamiento antibiótico con imipenem y vancominina solicitando interconsulta al servicio de cirugía vascular. Se realizó angio-TAC aorto-ilíaca donde se observó un manguito de densidad de partes blandas rodeando la prótesis con presencia de una colección de gran tamaño con gas en el espacio pararrenal posterior izquierdo que se prolongaba caudalmente hasta la ingle desplazando centralmente al riñón izquierdo (fig. 1). El gas presente en la misma sería secundario a abscesificación o a la existencia de una fistulización con un asa intestinal (fig. 2). Se observó importante engrosamiento de la pared aórtica con presencia de burbujas aéreas en su interior, asociando infiltración de la grasa adyacente y adenopatías, todo ello compatible con aortitis. Tras la inyección de contraste se observaron algunas áreas hiperdensas por fuera del injerto, la mayor del lado derecho por encima de la arteria renal adyacente al extremo superior de la endoprótesis, en probable relación con fuga del contraste (endoleaks tipo I). Existían otras zonas de extravasación en la zona dependiente de la arteria mesentérica inferior (fuga tipo II) y en la zona anterior a la altura de la bifurcación aórtica (fig. 3). Juicio radiológico: hematoma retroperitoneal izquierdo secundario a rotura de aneurisma-stent aórtico. Con tales hallazgos se consideró no procedente la reparación quirúrgica intravascular dada la extravasación proximal de contraste a nivel suprarrenal ya que habría que excluir ambas arterias renales y probablemente la arteria mesentérica del torrente sanguíneo. Tras la desestimación del tratamiento quirúrgico se continuó tratamiento con imipenem y vancomicina a pesar de lo cual desarrolló un cuadro de infección de vías respiratorias altas, con empeoramiento progresivo del estado general, disnea manifiesta y vómitos biliosos falleciendo finalmente a los 4 días del ingreso.
Las FAE primarias se presentan con una baja frecuencia (0,04-0,07%). Fueron descritas por primera vez en 1982 por Cooper, publicando Salmon el primer caso clínico en 18436,7. La mayoría de ellas se originan de aneurismas de aorta abdominal (AAA) que erosionan el tracto gastrointestinal por inflamación o infección (80%). La segunda causa más frecuente de fístulas primarias es la aterosclerosis aórtica (75%), siendo más infrecuentes por traumatismo o infección (25%). Las metástasis, radiación, cáncer de páncreas, úlceras duodenales, colelitiasis, diverticulitis, apendicitis y necrosis quística son causas muy infrecuentes de FAE primaria1.
Las FAE secundarias por reconstrucción aorto-ilíaca son más frecuentes que las primarias, representando el 0,36-2%2,3. El intervalo medio de desarrollo de las mismas oscila entre 8 meses y 15 años tras la inserción de la prótesis8. La localización más frecuente es la tercera o cuarta porción duodenal debido a su proximidad a la aorta infrarrenal, seguida de la afectación de yeyuno e íleon. Esta localización distal explicaría por qué no se evidenció causa de sangrado en la gastroscopia realizada al ingreso. No obstante, la alteración anatómica de nuestro paciente tras la cirugía gástrica con anastomosis tipo Billroth II podría modificar dicha localización. A pesar de la distancia existente entre la aorta y el recto se han descrito casos de FAE rectales, aunque con mayor frecuencia suele tratarse de fístulas primarias2.
En más del 80% de los pacientes, como en nuestro caso, la manifestación clínica más frecuente para las FAE secundarias es el sangrado digestivo conocido como «hemorragia centinela» que en la mayoría de los casos obliga al paciente a acudir al hospital. La hemorragia se presenta en forma de hematemesis y/o hematoquecia y puede seguirse de un sangrado digestivo masivo2. Puede presentarse también en forma de sangrado intermitente debido a la existencia de un coágulo que ocluye temporalmente la fístula. Se han descrito otras manifestaciones clínicas como dolor abdominal, masa abdominal pulsátil, dolor en espalda, fiebre, sepsis3 e incluso se han publicado casos de obstrucción de intestino delgado9.
Se ha propuesto la infección protésica como un factor de riesgo predisponerte para la formación de las FAE secundarias, siendo el intervalo de tiempo entre la cirugía y la formación de las mismas menor en los casos en que hay infección2. En nuestro paciente se describía la formación de un hematoma retroperitoneal izquierdo infectado, así como un engrosamiento de la pared aórtica con burbujas aéreas en su pared, compatible con aortitis. Tales hallazgos pudieron precipitar el desarrollo de la fístula, en este caso, en un período de 6 años las la inserción protésica.
La mayoría de los autores sugieren la realización de una TAC abdominal con contraste intravenoso como la prueba diagnóstica inicial, teniendo dicha prueba mayor rentabilidad diagnóstica en los casos como el que nos ocupa en los que existe infección asociada periaórtica, estimándose para ellos una sensibilidad>90% y una especificidad del 100%2,4,5. No obstante, también se sugiere la endoscopia como prueba inicial para excluir otras causas de sangrado digestivo como pueden ser las úlceras. En el paciente que presentamos, la gastroscopia no evidenció datos de sangrado digestivo a ese nivel. Dada la localización de las fístulas aortoentéricas, para localizar la misma hubiese sido de utilidad una exploración con enteroscopio de pulsión o de doble balón que mostrase en duodeno distal, yeyuno o íleon, la presencia de una prótesis, una erosión o úlcera con coágulo adherido o una masa pulsátil de origen extrínseco. No obstante, al ser realizado el diagnóstico mediante angio-TAC y dada la evolución desfavorable del paciente, esta prueba carecía de utilidad en nuestro caso.
Ante la alta sospecha de FAE tras una «hemorragia centinela» o los hallazgos del angio-TAC o de la endoscopia se recomienda la reparación quirúrgica, ya que la mortalidad para estos pacientes está próxima al 100%10,11.
El tratamiento quirúrgico para las FAE secundarias infectadas se basa en la antibioticoterapia intravenosa y la intervención quirúrgica urgente. El procedimiento consiste en retirar la prótesis infectada y realizar un bypass extraanatómico, no estando la realización de este bypass exenta de complicaciones, alcanzando una mortalidad del 36 al 48%. Otra opción terapéutica es el recambio in situ de la prótesis infectada2,10,11. Recientemente se ha propuesto la cirugía intravascular como tratamiento en pacientes con comorbilidades o como tratamiento puente en pacientes inestables hemodinámicamente, aunque la principal limitación para este nuevo tratamiento es la imposibilidad de retirar la prótesis infectada y desbridar el tejido infectado, siendo en estos casos necesario la instauración de un tratamiento antibiótico prolongado en el tiempo2,10,12.
Por lo tanto, ante todo sangrado digestivo en pacientes portadores de prótesis vasculares resulta imprescindible incluir las fístulas aorto-entéricas dentro del diagnóstico diferencial.