Sr. Director: La risperidona es un nuevo fármaco antipsicótico introdu cido en la práctica clínica desde hace 10 años, con una eficacia superior a los neurolépticos convencionales y con mayor perfil de seguridad. Aunque la hepatotoxicidad está referida en la información del producto1 , hasta la fecha sólo se han publicado 7 casos2-8 , ninguno de los cuales evolucionó a una hepatitis autoinmune. Presentamos un caso en el que la risperidona provocó una hepatitis colestásica inicial, con posterior desarrollo de hepatitis autoinmune que se hizo patente clínica, analítica e histológicamente 7 meses más tarde, y que requirió tratamiento inmunodepresor permanente. Mujer de 36 años de edad con antecedente de traumatismo craneoencefálico con secuelas neurológicas graves y alteración del comportamiento, por lo que seguía tratamiento con carbamazepina y fluoxetina desde hacía 5 años. No presentaba historia de etilismo, consumo de drogas ni productos de herbolario, y tampoco antecedentes de enfermedad hepática. En los controles periódicos efectuados por neurología había presentado pruebas de función hepática normales. Diez días antes de su ingreso inició tratamiento con risperidona a dosis de 0,5 mg/día. En abril de 2002 fue hospitalizada por un cuadro de ictericia cutaneomucosa, coluria y acolia de una semana de evolución. En la analítica realizada al ingresar (tabla I) destacaban: bilirrubina total (BT) de 15 mg/dl, aspartatoaminotransferasa sérica (AST) de 736 U/l, alaninaminotransferasa sérica (ALT) de 818 U/l, fosfatasa alcalina (ALP) de 627 U/l, gammaglutamiltransferasa (GGT) de 517 U/l y tiempo de protrombina del 63%, siendo el cociente ALT/AST menor de 2. Los marcadores serológicos de la hepatitis A, B y C, citomegalovirus, herpes simple y virus de Epstein-Barr resultaron negativos. Los anticuerpos antinucleares (ANA) fueron positivos a 1/320; el resto de autoanticuerpos no organoespecíficos fueron negativos. La ecografía abdominal y la tomografía axial computarizada fueron normales. Con la sospecha clínica de hepatitis colestásica por mecanismo tóxico, se suspendió el tratamiento con carbamazepina, fluoxetina y risperidona, y a las 2 semanas del ingreso se realizó una biopsia hepática (fig. 1), cuyos hallazgos histológicos eran indicativos de un cuadro de hepatitis aguda con colestasis, compatible con una etiológia tóxica. Durante la tercera semana se produjo un incremento progresivo de las cifras de transaminasas y bilirrubina (tabla I), que alcanzaron los siguientes valores: AST, 1.723 U/l; ALT, 1.185 U/l, y BT, 29 mg/dl, con cociente ALT/AST mayor de 5, datos característicos de lesión hepatocelular. Dada la desfavorable evolución clínica y analítica a pesar de la retirada de fármacos, así como la positividad de los ANA, se inició tratamiento con prednisona a dosis de 1 mg/kg/día. Se objetivó entonces una rápida y acusada mejoría, y se dio el alta hospitalaria a la paciente a las 5 semanas del ingreso. En el control ambulatorio efectuado 3 meses después (julio de 2002), los ANA eran positivos a 1/320, las transaminasas se habían normalizado y la BT era de 1,4 mg/dl (tabla I).
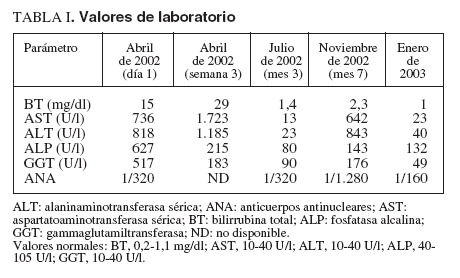
TABLA I . Valores de laboratorio
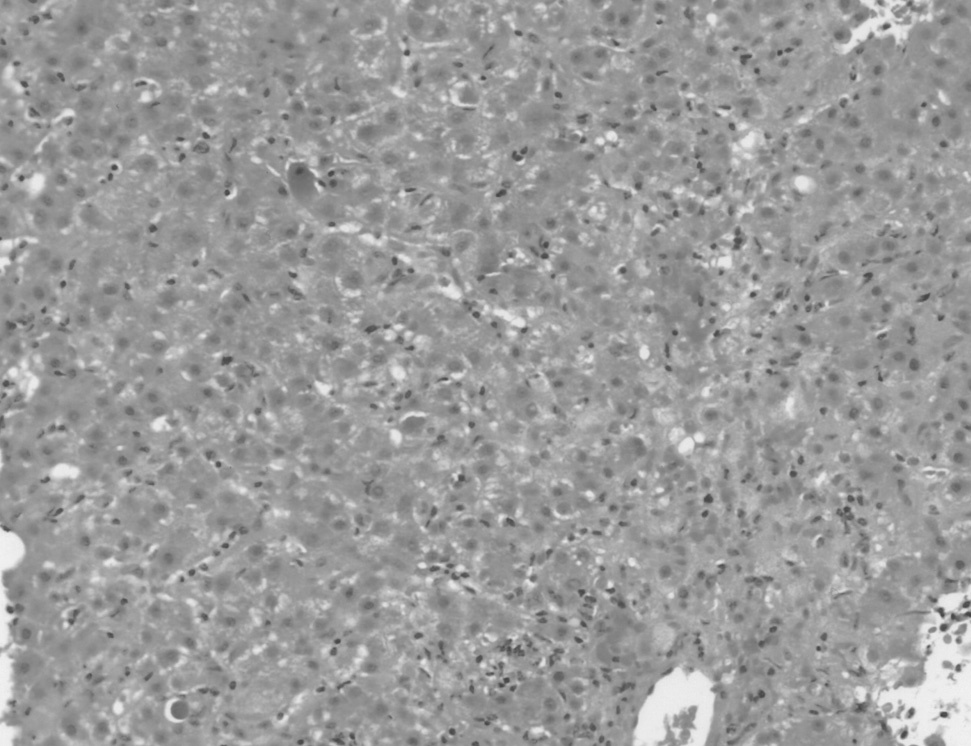
Fig. 1. Marcado componente inflamatorio en la zona centrolobulillar y en los espacios porta, constituido por linfocitos y, en menor número, por eosinófilos, con presencia de abundantes cuerpos acidófilos y coles tasis intrahepatocítica (hematoxilina-eosina, ×200).
En noviembre de 2002, a las 4 semanas de la retirada del tratamiento esteroideo, comenzó con un cuadro de astenia, anorexia e ictericia. En la analítica (tabla I) destacaba aumento de transaminasas y, en menor grado de BT, ALP y GGT, junto con elevación de los ANA a 1/1.280 e hipergammaglobulinemia policlonal; los restantes autoanticuerpos eran negativos. La biopsia mostró cambios característicos de hepatitis autoinmune. Se instauró tratamiento con 30 mg de prednisona y 50 mg de azatioprina, con el que se obtuvo de nuevo una rápida mejoría clínica y analítica. En enero de 2003 la paciente estaba asintomática, los ANA eran positivos a 1/160, la concentración de gammaglobulinas se había normalizado y la bioquímica hepática era normal (tabla I). Desde entonces se mantiene en remisión con tratamiento de mantenimiento con 50 mg/día de azatioprina. La risperidona es un nuevo agente antipsicótico con menos efectos adversos que las fenotiacinas. Las referencias a su potencial hepatotoxicidad son muy escasas2-8 y no hemos encontrado en la bibliografía consultada ningún caso similar al que se describe en el presente trabajo. Según la escala del Council for International Organizations of Medical Sciences (CIOMS)9 , y aplicando los criterios de enfermedades hepáticas inducidas por fármacos10 , la relación causal entre la lesión hepática inicial de tipo colestásico y el tratamiento con risperidona se califica como probable, tanto por la existencia de una relación cronológica compatible entre la administración del fármaco y las alteraciones en la bioquímica hepática como por la ausencia de otras causas potenciales de enfermedad hepática, siendo además la biopsia hepática indicativa de hepatitis colestásica tóxica. Inicialmente, los valores de ANA elevados se consideraron un epifenómeno, tanto por los hallazgos histológicos como por la negatividad de los anticuerpos antimúsculo liso y normalidad de las concentraciones de inmunoglobulinas. La implicación de la carbamazepina y fluoxetina parece improbable ya que, si bien pueden ser causa de hepatotoxicidad, suponían la base del tratamiento de la paciente desde hacía varios años, durante los cuales no se había apreciado alteración de las pruebas hepáticas; no obstante, podrían haber potenciado la hepatotoxicidad de la risperidona11 al ser inhibidores del citocromo P450. El mecanismo por el cual un fármaco puede inducir una hepatopatía autoinmune es variable12 . El fármaco puede actuar como hapteno, de tal forma que la unión de éste o de su metabolito, normalmente no inmunógeno, al hepatocito produciría un complejo antigénico previamente inexistente que estimularía el sistema inmunitario. Otro mecanismo podría ser a través del daño inicial del hepatocito por acción directa tóxica del fármaco, con la consiguiente liberación de constituyentes celulares inmunógenos, lo cual desencadenaría una reacción autoinmunitaria contra hepatocitos normales en un individuo genéticamente predispuesto. En esta situación, la supresión del fármaco no necesariamente frenaría la acción lesiva sobre el hígado, dado que el mecanismo inmunitario podría continuar dirigiéndose contra proteínas celulares previamente normales. Otra posibilidad es que el fármaco o su metabolito presenten una reacción cruzada con un epítopo de la superficie del hepatocito normal, que desencadenaría una reacción inmunológica sobre un hepatocito «espectador inocente».
En nuestra paciente, la risperidona o su metabolito indujo una hepatitis colestásica inicial con ANA positivos, que no disminuyeron a pesar de la retirada del fármaco, y más tarde se desarrolló una hepatitis autoinmune. Dicho diagnóstico está apoyado por los hallazgos histológicos, los ANA positivos a títulos elevados, la gammapatía policlonal, la exclusión de otras causas de hepatopatía junto a una mala evolución clínica hasta la instauración del tratamiento esteroideo y la recidiva a las pocas semanas de suprimir el tratamiento de mantenimiento. No conocemos la descripción de un caso similar en la bibliografía atribuible a la risperidona. A pesar de su excepcional frecuencia, y dada la amplia difusión de los nuevos agentes antipsicóticos, resulta imprescindible tener en cuenta los posibles efectos secundarios hepáticos, realizar monitorización periódica de los parámetros de la función hepática y, en caso de alteración de éstos, retirar la medicación y valorar los marcadores de autoinmunidad.