Este artículo señala las recomendaciones claves para una adecuada prescripción de antiinflamatorios no esteroideos a pacientes que presentan indicación de tratamiento con esta medicación, en base a la evidencia científica actual y teniendo en consideración aspectos de seguridad gastrointestinal y cardiovascular. Las recomendaciones se han consensuado por expertos designados por 3 sociedades científicas (Sociedad Española de Reumatología, Asociación Española de Gastroenterología y Sociedad Española de Cardiología), siguiendo una metodología Delphi a 2 rondas. Las áreas que se han tenido en cuenta engloban: eficacia, riesgo cardiovascular, riesgo gastrointestinal, riesgo hepático, riesgo renal, enfermedad inflamatoria intestinal, anemia, dolor postoperatorio y estrategias de prevención. Se propone un algoritmo de manejo de pacientes que recoge los aspectos fundamentales de las recomendaciones.
This article outlines key recommendations for the appropriate prescription of non steroidal anti-inflammatory drugs to patients with different musculoskeletal problems. These recommendations are based on current scientific evidence, and takes into consideration gastrointestinal and cardiovascular safety issues. The recommendations have been agreed on by experts from three scientific societies (Spanish Society of Rheumatology [SER], Spanish Association of Gastroenterology [AEG] and Spanish Society of Cardiology [SEC]), following a two-round Delphi methodology. Areas that have been taken into account encompass: efficiency, cardiovascular risk, gastrointestinal risk, liver risk, renal risk, inflammatory bowel disease, anemia, post-operative pain, and prevention strategies. We propose a patient management algorithm that summarizes the main aspects of the recommendations
Los antiinflamatorios no esteroideos (AINE) son fármacos con una estructura química heterogénea que comparten actividad antipirética, antiinflamatoria y analgésica a través de su capacidad para inhibir las enzimas ciclooxigenasa (COX), que intervienen en la síntesis de prostaglandinas, tromboxanos y leucotrienos. Son la piedra angular en el tratamiento del dolor y la inflamación en los pacientes con enfermedades musculoesqueléticas.
Las prostaglandinas se producen a partir de una ruta oxidativa del ácido araquidónico y las enzimas COX. Existen 3 formas de COX (COX-1, COX-2 y COX-3), siendo más relevantes las 2 primeras. La COX-3 es una isoforma de la COX-1, que solo difiere en la estructura de un aminoácido, y su función, aunque se cree que es antipirética, continúa siendo incierta. De una forma simple, se puede decir que la COX-1 actúa en el inicio de la agregación plaquetaria y a nivel de los mecanismos de defensa de la mucosa gastrointestinal (GI), mientras que la COX-2 parece estar involucrada en la mediación del dolor, la fiebre y la inflamación. La inhibición de las enzimas COX lleva aparejados los efectos beneficiosos y los no deseados en los principales órganos y sistemas donde la actividad COX juega un papel clave.
La introducción de fármacos inhibidores selectivos de la COX-2 indujo altas expectativas al presentar una eficacia igual a la de los AINE no selectivos pero con un perfil de toxicidad GI más seguro. Con posterioridad, la observación de un aumento en la frecuencia de enfermedades cardiovasculares (CV) enfrió estas expectativas pero abrió un camino muy importante para entender no solo los efectos beneficiosos, sino también todos los efectos adversos asociados al uso de los AINE. En octubre de 2006 el Comité de Medicamentos de Uso Humano de la EMEA emitió un informe1 respecto a la existencia de nuevos datos sobre los riesgos CV de tipo aterotrombótico de los AINE tradicionales. Así, hoy se considera que todos los AINE, en mayor o menor grado, se asocian a incremento de riesgo GI y CV. El aumento de riesgo CV por el uso de inhibidores selectivos de la COX-2 se explicó por un desequilibrio entre la inhibición de tromboxano y prostaciclina, pero dado que el aumento del riesgo CV se da también con los AINE no selectivos clásicos, el mecanismo se vislumbra más complejo. Además, tanto los AINE tradicionales como los inhibidores de la COX-2 se asocian a un aumento en la presión arterial y edema/s, en diversos grados.
En el año 2003, la Asociación Española de Gastroenterología (AEG) y la Sociedad Española de Reumatología (SER) colaboraron en la redacción de la «Estrategia clínica para la prevención de los efectos adversos sobre el tracto digestivo de los antiinflamatorios no esteroideos»2,3, y posteriormente, en el año 2009, se publicó un documento consenso de la SER y el Colegio Mexicano de Reumatología para el «Uso apropiado de los antiinflamatorios no esteroideos en reumatología»4. La actual revisión es fruto de la colaboración de la AEG, la SER y la Sociedad Española de Cardiología (SEC). Esta revisión tiene por objeto impulsar un uso racional de los AINE en función de nuevos estudios publicados en los últimos años y ayudar a una toma de decisiones óptima en el uso habitual de estos fármacos.
Definiciones operativas del documentoEl término AINE en estas recomendaciones hace referencia en conjunto a los AINE tradicionales, a los inhibidores selectivos de la COX-2 (COXIB) y al ácido acetilsalicílico (AAS) a dosis antiinflamatorias. Si alguna afirmación se refiere solo a AINE tradicionales, a COXIB o al AAS, se especificará así en la recomendación correspondiente. No se incluyen dentro de los AINE otros analgésicos, como el clonixinato de lisina o el metamizol.
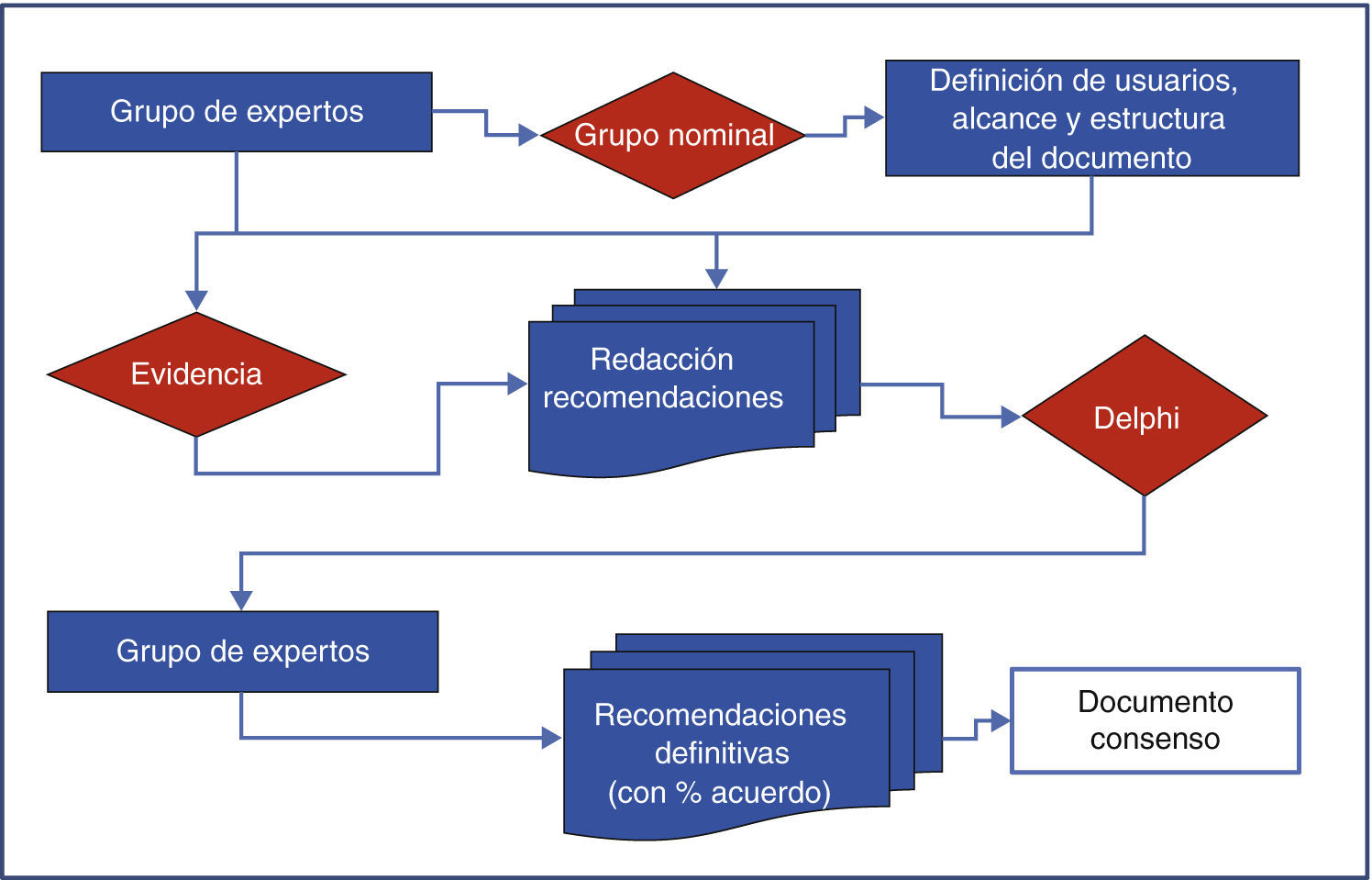
MetodologíaLa elaboración del consenso se ha realizado mediante grupo nominal y técnica Delphi según se muestra en la figura 1.
Grupo nominalNueve panelistas (3 reumatólogos, 3 gastroenterólogos y 3 cardiólogos) procedentes de las respectivas sociedades científicas (SER, AEG y SEC) y designados por las juntas de las mismas en base a su experiencia y/o publicaciones sobre esta temática en revistas incluidas en Medline, formaron el grupo nominal. Este grupo fue coordinado por un metodólogo de la Unidad de Investigación de la SER que estableció el alcance, los usuarios y los apartados del consenso, así como las definiciones a utilizar en el documento.
Para la realización del grupo se proporcionó a los panelistas los documentos previos sobre el tema, y se pidió a cada uno que, sin interacción entre ellos, elaborara su propuesta personal siguiendo un esquema proporcionado por la metodóloga de la Unidad de Investigación de la SER, que elaboró posteriormente un documento conjunto que incluía todas las propuestas. El día 15 de junio de 2012 se realizó la reunión presencial donde se revisaron los antecedentes del problema y los aspectos metodológicos relevantes del consenso. A continuación se trabajó sobre el documento conjunto y se fueron testando cada uno de los aspectos a consensuar (usuario, alcance y temas a incluir). Cada experto participante tuvo la oportunidad de votar la pertinencia o no de la inclusión de cada una de las recomendaciones propuestas, argumentando ordenadamente las razones para ello. Así, se reordenaron sucesivamente las opciones, la estructura final del documento y los responsables de los apartados del mismo. Finalmente se decidió que el consenso se dirigiría a médicos de atención primaria, reumatólogos, cardiólogos y gastroenterólogos (usuarios), y que se centraría en aspectos de eficacia, seguridad CV y seguridad renal (alcance). Los apartados y responsables quedaron distribuidos según se muestra en la tabla 1.
Apartados del consenso y responsables del mismo
| Apartado | Responsable/s |
| Introducción | Angel Lanas Arbeloa, Pere Benito Ruiz |
| Metodología | Milena Gobbo Montoya |
| Eficacia | |
| Indicaciones | Pere Benito Ruiz |
| Tiempos | Francisco García Llorente |
| Calidad de vida | Blanca Hernández Cruz |
| Apartado Riesgo cardiovascular | |
| Estratificación de riesgo cardiovascular | José Ramón González-Juanatey |
| Complicaciones cardiovasculares asociadas al uso de AINE | Joaquín Alonso Martín |
| Uso de anticoagulantes | Gonzalo Barón Esquivas |
| Uso antiagregantes | Gonzalo Barón Esquivas |
| Apartado Riesgo gastrointestinal | |
| Estratificación de riesgo digestivo | Ángeles Pérez Aisa |
| Complicaciones gastrointestinales asociadas al uso de AINE | Ángeles Pérez Aisa |
| Estrategias de prevención | Xavier Calvet Calvo |
| Riesgo hepático | Xavier Calvet Calvo |
| Dispepsia | Xavier Calvet Calvo |
| Enfermedad inflamatoria intestinal | Ángel Lanas Arbeloa |
| Apartado Riesgo renal | |
| Estratificación de riesgo renal | Blanca Hernández Cruz, Francisco García Llorente |
| Complicaciones renales asociadas al uso de AINE | Blanca Hernández Cruz, Francisco García Llorente |
| Otros aspectos relevantes | |
| Anemia | José Ramón González-Juanatey, Angel Lanas Arbeloa |
| Postoperatorio | Gonzalo Barón Esquivas, Pere Benito Ruiz |
Las recomendaciones fueron redactadas por los expertos, bien de forma individual o en grupos de trabajo. Se estableció un criterio común para su elaboración, de modo que cada responsable debía incluir un enunciado breve y sintético de la recomendación, seguido de un desarrollo argumentativo de la misma, apoyando la recomendación con la mejor evidencia disponible en base a las búsquedas bibliográficas realizadas al efecto por cada panelista. El nivel de evidencia y la fuerza de la recomendación se establecieron de acuerdo a la escala SIGN5.
Encuesta DelphiPara establecer el grado de consenso se realizó una encuesta Delphi a 2 rondas. Las recomendaciones enviadas por los panelistas se reformularon en forma de ítems a responder mediante una escala Likert que midiera el grado de acuerdo con el enunciado, graduándolo de 1 (completamente en desacuerdo) a 5 (completamente de acuerdo). Los cuestionarios fueron remitidos en formato electrónico vía mail a los panelistas, que los respondieron sin que existiera interacción entre ellos.
La primera ronda fue enviada el 28 de enero de 2013 (66 ítems agrupados en 17 apartados). En la primera ronda, los panelistas pudieron añadir nuevas aseveraciones, comentarios, citas o argumentos respecto a cada ítem cuando, desde su punto de vista, se tratara de aspectos relevantes que deberían figurar en el documento de consenso.
Se consideró que existía acuerdo con el ítem cuando la puntuación media era igual o superior a 4, y desacuerdo cuando la puntuación era inferior o igual a 2. En ambos casos (acuerdo y desacuerdo) existe consenso. En el resto de las posibilidades se consideró que el ítem era conflictivo y que no se podía afirmar que existiera un consenso al respecto. En base a los comentarios de los panelistas se modificó la redacción de algunos ítems, se desglosaron otros y se añadió una lista de posibles nuevas recomendaciones a incluir en el cuestionario de la segunda ronda.
La segunda ronda se envió el 11 de febrero de 2013 (73 ítems agrupados en 17 apartados). El análisis de la segunda ronda se realizó siguiendo la misma metodología y los mismos criterios que se utilizaron en la primera (acuerdo, desacuerdo e ítems conflictivos). Se consideró que existía consenso cuando más del 75% de los panelistas estaban de acuerdo con la aseveración (puntuación de acuerdo ≥4). El resto de los casos (ítems conflictivos) se han considerado recomendaciones sin consenso, y no se incluyen en este documento.
RecomendacionesEficaciaIndicacionesLas indicaciones aprobadas en ficha técnica para los AINE son variadas respecto del tipo de dolor y van desde el dolor de origen musculoesquelético o neurológico hasta la dismenorrea. Esto hace que la población diana a la que se puede prescribir estos fármacos sea amplia y muy heterogénea. La respuesta a los AINE varía de unos individuos a otros, lo que hace que la indicación y la evaluación de la respuesta a estos medicamentos deban individualizarse4.
No se puede recomendar ningún AINE sobre otro en función de su respuesta clínica. Diversas publicaciones muestran suficiente evidencia para aseverar que su eficacia es similar6,7.
Tiempo de usoPara el control del dolor, los AINE comparten indicación con otro tipo de intervenciones farmacológicas y no farmacológicas. Los AINE deben utilizarse durante el mínimo tiempo y a la mínima dosis posible, adecuando su utilización a las diferentes indicaciones aprobadas. Esta recomendación es recogida por las agencias reguladoras1,8, en base a datos que señalan la dosis-dependencia de los efectos adversos y a que el riesgo se mantiene en el tiempo. Por todo ello, y dada la posibilidad de efectos adversos, se recomienda su uso cuando las alternativas no son posibles, tanto por intolerancia como por ineficacia9-11.
En artrosis, el tratamiento continuado con AINE es más eficaz en el control de los síntomas que el uso a demanda. Pese a ello, este último se recomienda con frecuencia debido a los posibles efectos secundarios indeseables, tal y como se recoge en un estudio a 22 semanas para el prevención de los brotes de la artrosis de rodilla y cadera12. En otro estudio prospectivo multicéntrico y aleatorizado de 24 semanas en pacientes con artrosis de cadera o rodilla, la frecuencia de efectos adversos fue parecida entre los que tomaban celecoxib de manera continua frente a los que lo tomaban de manera intermitente en función de los síntomas de los pacientes13. En la artritis psoriásica, debido a los riesgos CV e intestinales específicos de estos pacientes, se recomiendan los AINE a la menor dosis y durante el mínimo tiempo posible debido a su potencial toxicidad14.
En la espondilitis anquilosante los AINE se recomiendan como primera línea de tratamiento si los pacientes presentan dolor lumbar inflamatorio y rigidez, siendo de elección el tratamiento continuado si la enfermedad es sintomática, activa y persistente15-18. Los AINE mejoran la función y disminuyen la actividad de la enfermedad en la espondilitis anquilosante, mientras que los fármacos modificadores de enfermedad no tienen efecto sobre estos parámetros19. También se ha constatado una reducción del grado de progresión radiográfica en pacientes que toman AINE de forma continua asociados a fármacos anti-TNF20. Igualmente, el tratamiento continuado con celecoxib está relacionado con una menor progresión radiográfica, comparado con su uso a demanda21. El grupo alemán German Early Spondyloarthritis Inception Cohort señala que los pacientes con espondilitis anquilosante asociada a una alta tasa de toma de AINE durante más de 2años tienen un enlentecimiento de la neoformación ósea de la columna comparados con los que tienen una tasa baja. Este aparente efecto protector es exclusivo de aquellos pacientes con proteínaC reactiva alta en el tiempo y la presencia de sindesmofitos al inicio22. Los pacientes con reactantes de fase aguda elevados se benefician más del tratamiento continuo con AINE23-25.
Calidad de vidaLa eficacia de los AINE en la reducción del dolor y los síntomas asociados a la inflamación en pacientes con patología reumática aguda o crónica es incuestionable26,27. Estos beneficios producen mejoría significativa en el subdominio de función física y en la calidad de vida de los enfermos28-30. Esta mejoría ocurrió con mayor frecuencia en los enfermos con peor función física basal, menor número de comorbilidades y menor duración de los síntomas.
Las tasas de retención (días de tratamiento sin abandono del mismo) de los AINE, especialmente COXIB, siguen siendo elevadas, particularmente en enfermos crónicos y mayores de 65años. La duración media del tratamiento en enfermos reumáticos para celecoxib, rofecoxib, naproxeno e ibuprofeno fue de 15, 13, 10 y 10meses, respectivamente7. Las diferencias en seguridad, sobre todo GI, podrían tener implicaciones relevantes en la calidad de vida de los pacientes31,32.
Riesgo cardiovascularEstratificación de riesgo vascularDado el riesgo CV asociado al tratamiento con AINE, se considera importante evaluar este parámetro a la hora de la prescripción y de la elección del tratamiento apropiado. La tercera Task Force conjunta de Prevención Cardiovascular en la Práctica Clínica recomendó el modelo Systematic Coronary Risk Evaluation (SCORE) para la estimación del riesgo CV en Europa33, que está basado en estudios de población europea. Dada la variabilidad geográfica del riesgo CV en Europa, se han desarrollado 2 modelos SCORE, para países de alto o bajo riesgo, situándose España en la zona de baja incidencia34,35.
El riesgo CV se estratifica en muy alto, alto, moderado o bajo riesgo CV36,37 (tabla 2). Esta nueva clasificación de los niveles de riesgo CV está relacionada de forma directa con la consecución de objetivos terapéuticos sobre los factores de riesgo CV clásicos cada vez más estrictos. Así, de forma específica se definen objetivos lipídicos de 70mg/dl en los niveles plasmáticos de colesterol-LDL para pacientes de muy alto riesgo CV, 100mg/dl para pacientes de alto riesgo CV y 115mg/dl en pacientes de riesgo CV moderado.
Evaluación del riesgo cardiovascular
| Muy alto |
| a) Enfermedad cardiovascular documentada mediante técnicas invasivas o no invasivas (angiografía coronaria, técnicas isotópicas, ecocardiografía de estrés y la evidencia de placas ateroscleróticas mediante ecografía carotídea), infarto de miocardio previo, síndrome coronario agudo previo, revascularización coronaria, otros procedimientos de revascularización arterial, accidente cerebrovascular y enfermedad arterial periférica |
| b) Diabetes mellitus tipo 2 o diabetes mellitus tipo 1 asociada a daño en órganos diana (como microalbuminuria: 30-300mg/24h) |
| c) Enfermedad renal crónica moderada-grave (filtrado glomerular estimado <60ml/min/1,73 m2) |
| d) SCORE ≥10%. |
| Alto |
| a) Algún factor de riesgo individual marcadamente elevado, hipercolesterolemia familiar o hipertensión arterial grave |
| b) SCORE ≥5% y <10% |
| Moderado |
| SCORE de ≥1 y <5% |
| Bajo |
| SCORE <1% y ausencia de otros factores de riesgo |
En el año 2010 se publicó el primer consenso «EULAR Standing Committee for International Clinical Studies Including Therapeutics» para el manejo del riesgo CV en pacientes con artritis reumatoide y otras poliartritis inflamatorias (espondiloartropatías). Estas enfermedades, en especial la artritis reumatoide, se han relacionado de forma directa con un aumento del riesgo CV y de la mortalidad CV a largo plazo. En este consenso se recomienda evaluar el riesgo CV a través de la tabla SCORE modificada (fig. 2), y propone un decálogo de recomendaciones en base a la evidencia científica38. En los aspectos generales de la estimación y manejo del riesgo CV, estas recomendaciones podrían hacerse también extensivas a los pacientes con artrosis.
Complicaciones cardiovasculares asociadas al uso de antiinflamatorios no esteroideosFrente a la ausencia de tratamiento, la administración de AINE aumenta el riesgo de desarrollar SCA u otros episodios CV de carácter aterotrombótico. Los ensayos clínicos que determinaron la asociación entre AINE y episodios CV no fueron diseñados específicamente para este objetivo39,40. Los estudios de tipo observacional y metaanálisis de ensayos clínicos y observacionales señalan que todos los AINE aumentan el riesgo CV aunque en grado variable y, en general, bajo. La revisión efectuada recientemente por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) y por el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos (EMA)41 han concluido que las evidencias recientes confirman las conclusiones previas publicadas en 2006, que indicaban un incremento de riesgo CV de tipo aterotrombótico para AINE, aunque el balance riesgo/beneficio continúa siendo positivo.
El incremento de riesgo CV varía mucho dependiendo del tipo de AINE utilizado.
NE: 1++; GR: A; GA: 100%
El naproxeno es uno de los AINE más seguros en cuanto a riesgo CV.
NE: 1++; GR: A; GA: 100%
Rofecoxib, diclofenaco, indometacina, etoricoxib y etodolaco son los AINE con más riesgo CV.
NE: 1+; GR B; GA: 100%
Diversos metaanálisis han señalado en mayor o menor medida que todos los AINE estudiados incrementan el riesgo CV, si bien la magnitud en términos absolutos es limitada42,43. Un metaanálisis de estudios observacionales publicado por McGettigan y Henry44 con poblaciones de bajo y alto riesgo CV estudió los AINE más utilizados actualmente (naproxeno, ibuprofeno, celecoxib, diclofenaco, indometacina, piroxicam, meloxicam, etodolaco, etoricoxib y valdecoxib). Las conclusiones globales de la revisión sugerían que el naproxeno y bajas dosis de ibuprofeno son los que se asocian a menores incrementos del riesgo CV. El diclofenaco elevó de manera clara el riesgo CV. Los datos para el etoricoxib son escasos, pero en las comparaciones con naproxeno e ibuprofeno presentó más riesgo CV. La indometacina también se asoció a incremento notable del riesgo CV. En el estudio MEDAL, etoricoxib presentó un riesgo CV igual a diclofenaco45.
El metaanálisis más reciente y extenso de ensayos clínicos con datos individuales de pacientes señala que COXIB y AINE presentan incremento del riesgo CV frente a placebo, no existiendo diferencias significativas entre ellos de manera global. De entre los AINE no selectivos, el de mayor riesgo CV fue el diclofenaco, que presentó un riesgo similar al de los COXIB. Naproxeno por su parte, a dosis de 500mg/12h, no se asoció a incremento del riesgo CV, a diferencia de ibuprofeno y diclofenaco, los únicos AINE no selectivos más estudiados46. También existe una clara asociación entre el riesgo de desarrollar insuficiencia cardiaca y la administración de este tipo de fármacos46, además de la bien conocida relación de la toma de AINE y el desarrollo de episodios o reagudizaciones de insuficiencia cardiaca.
Los pacientes con cardiopatía isquémica tienen más riesgo de episodios CV cuando se les administran AINE. Un estudio español47 de casos y controles, que incluyó 6.000 participantes, concluyó que el uso de AINE se asocia con un incremento global del riesgo coronario del 16% (OR: 1,16; IC95%: 0,95-1,42). La utilización de dosis altas lo aumentaba en un 64% (OR: 1,64; IC95%: 1,06-2,53) frente a los que tomaban dosis bajas. En los pacientes con cardiopatía isquémica previa, el incremento del riesgo fue del 84% (OR: 1,84; IC95%: 1,13-3,00). El metaanálisis de McGettigan y Henry44 también avala que las dosis altas se asocian a mayor riesgo.
Uso de anticoagulantesLa evidencia a través de estudios observacionales que demuestran un incremento del riesgo de hemorragia digestiva alta en pacientes que usan AINE y anticoagulantes es extensa. En general, los AINE se deben evitar en los pacientes que usan estos fármacos48–51. La seguridad de los nuevos anticoagulantes como dabigatrán, rivaroxabán o apixabán asociada a AINE no parece ser diferente a la de los anticoagulantes clásicos52.
Las interacciones con los anticoagulantes son diferentes para los distintos AINE. El AAS, la fenilbutazona o el ácido mefenámico potencian de forma muy significativa el efecto anticoagulante de la warfarina, desplazándola de la albúmina y disminuyendo su metabolismo en el hígado53. Tenoxicam, meloxicam, lornoxicam, nimesulida, etodolaco, nabumetona y celecoxib no incrementan significativamente el international normalized ratio (INR) en individuos anticoagulados. Por el contrario, diclofenaco, ibuprofeno y naproxeno incrementan el tiempo de hemorragia54–56.
Un estudio que evaluó 98.821 pacientes de edad avanzada en tratamiento continuo con warfarina señaló que el riesgo de hemorragia digestiva alta asociada a AINE o COXIB fue similar57. Sin embargo, estudios más recientes han señalado que warfarina combinada con celecoxib se asoció a menor riesgo de ingresos por sangrado GI que la asociación de warfarina con ibuprofeno, indometacina, etodolaco, nabumetona y naproxeno58,59. Todo ello hace que, aún con reservas, los COXIB se consideren de elección en situaciones donde se requiera el uso de AINE y no se pueda manejar el problema utilizando otras terapias.
Uso de antiagregantesSe debe evitar la utilización de AINE, incluso a corto plazo, en pacientes con infarto agudo de miocardio previo que toman AAS, ya que se asocia a incremento del riesgo CV.
NE: 2+; GR: B; GA: 78%
En pacientes que toman AAS a dosis bajas, la asociación con ibuprofeno y naproxeno interfiere con el efecto antiagregante del AAS, por lo que se debe evitar usarlos conjuntamente.
NE: 1+; GR: C; GA: 100%
Ibuprofeno, naproxeno e indometacina, pero no paracetamol, diclofenaco o COXIB, interfieren con el AAS en su capacidad de acetilar irreversiblemente la enzima COX-1 plaquetaria; por ello es probable que estos fármacos reduzcan el efecto protector del AAS sobre el riesgo de episodios arterioscleróticos60–62.
La evidencia existente no es suficiente todavía para hacer recomendaciones firmes63. No obstante, el ibuprofeno no debería tomarse al menos hasta 1h tras la ingesta del AAS. En el caso de pacientes que tomen AAS con recubierta entérica (la mayoría en España) el problema es mayor, pues el pico de liberación máxima es tardío (más allá de las 4h), lo cual hace que la interacción con el ibuprofeno sea muy probable. Así, un estudio demostró que el efecto antiplaquetario del AAS a dosis bajas con cubierta entérica se atenúa cuando el ibuprofeno se administra 2, 7 y 12h después del AAS64,65. En el caso del naproxeno la interacción fue menor al administrarlo al menos 2h después del AAS66. Existe controversia sobre en qué medida esta interacción puede tener impacto clínico en términos de mortalidad CV en pacientes que toman por ejemplo ibuprofeno y AAS, ya que los 2 estudios disponibles son contradictorios entre sí67,68.
Celecoxib, rofecoxib y lumiracoxib no interfieren con el AAS en su capacidad de acetilar irreversiblemente la enzima COX-1 plaquetaria60,69. De ellos, solo celecoxib está disponible en el mercado, lo cual reduce las opciones a esta combinación, ya que no hay datos para etoricoxib. Los problemas para utilizar COXIB junto con AAS vienen determinados por el riesgo CV asociado a los mismos y al hecho de que la EMA, pero no la FDA, ha señalado contraindicación para el uso de COXIB en pacientes con historia previa de episodios CV. Todo ello limita de forma considerable las opciones terapéuticas en esta población, habida cuenta además que naproxeno, aunque neutro desde el punto de vista CV a dosis de 500mg/12h, se asocia a mayor riesgo GI y puede interferir con el efecto del AAS. Así las cosas, en pacientes en tratamiento con AAS que no hayan presentado un episodio CV, celecoxib a dosis bajas y durante el menor tiempo posible es una opción terapéutica razonable basados en estudios epidemiológicos que señalan que este fármaco no presenta mayor riesgo que otros AINE clásicos44. Las recomendaciones de prescripción según el riesgo CV y GI se encuentran desarrolladas en el algoritmo adjunto descrito como figura 3.
Algoritmo de recomendaciones para el uso de AINE según el riesgo cardiovascular y gastrointestinal (tracto digestivo alto y bajo).
*En caso necesario naproxeno + IBP o celecoxib a dosis bajas (200mg/24h) ± IBP el menor tiempo posible en ambos casos.
**Datos más robustos para celecoxib que para etoricoxib
#Naproxeno debe tomarse 2h antes del AAS. Si se toma AAS con cubierta entérica las posibilidades de interacción son mayores.
##Si existe episodio cardiovascular previo la EMA y la AEM contraindican esta opción por el momento
Se asume que los pacientes con riesgo cardiovascular muy alto deben estar en tratamiento con AAS. Por ello, en el grupo de bajo riesgo gastrointestinal no se contempla muy alto riesgo cardiovascular, pues al estar con AAS, su riesgo gastrointestinal es ya intermedio como mínimo.
Las claves para realizar esta evaluación personalizada son las que se exponen en esta sección. El perfil de riesgo se establecerá para cada paciente según la tabla 3, y este perfil será el que guíe la estrategia de prevención.
Evaluación del riesgo gastrointestinal
| Alto |
| Antecedente de úlcera péptica complicada |
| Empleo de anticoagulantes, o |
| Combinación de >2 factores de riesgo restantes |
| Medio |
| Pacientes no anticoagulados ni con antecedentes de úlcera complicada pero que presentan algún factor de riesgo aislado |
| Bajo |
| Pacientes sin factores de riesgo. No toma: ácido acetilsalicílico |
Factores de riesgo aceptados: edad >60años, historia de úlcera péptica complicada y no complicada. Uso concomitante de AINE o COXIB con ácido acetilsalicílico, clopidogrel, anticoagulantes, corticoides o inhibidores de la recaptación de serotonina, dosis altas de AINE o 2AINE, comorbilidad grave.
A medida que se incrementa la edad, el riesgo de desarrollar complicaciones GI en pacientes que toman AINE aumenta también de manera progresiva70,71. La edad superior a 60años es por sí sola un factor de riesgo para la aparición de complicaciones GI, y este riesgo aumenta en los pacientes que reciben AINE72,73. Se estima que se producen aproximadamente 6 complicaciones del tracto GI superior por cada 1.000personas/año en pacientes que toman AINE con una edad comprendida entre los 60 y los 69años. Esta estimación asciende a 16 por 1.000personas/año en los pacientes con edad comprendida entre 70 y 79años70.
La existencia de historia previa de úlcera péptica gástrica o duodenal no complicada o historia de complicación GI (hemorragia o perforación) son un factor de riesgo independiente para el desarrollo de complicaciones por úlcera gastroduodenal asociada a la toma de AINE. Este dato se ha confirmado en la mayoría de los estudios observacionales y ensayos clínicos51,71,74–79.
La combinación de 2 o más AINE potencia el riesgo de hemorragia por encima del riesgo que se encuentra para cada AINE de manera individual80. Igualmente, y posiblemente ligado a este mismo fenómeno, se ha señalado que el cambio de un AINE a otro durante un episodio aumenta también el riesgo de hemorragia GI alta81.
Este aumento del riesgo con la combinación de 2 AINE se observa también con la asociación de un AINE clásico o COXIB con AAS a dosis bajas en prevención CV, la combinación actualmente más utilizada. En el estudio CLASS82 los pacientes que recibieron un AINE clásico junto con dosis bajas de AAS presentaron una tasa anualizada de complicaciones del 2,1%, más elevada que la observada en pacientes que solo recibieron AINE (1,2%). Un buen número de estudios observacionales han señalado que la combinación de AINE o COXIB con AAS potencia el riesgo de hemorragia digestiva alta por encima de los riesgos estimados para cada uno de los fármacos de forma individual81,83,84. Análisis post-hoc con comparaciones no aleatorizadas y estudios observacionales han señalado que posiblemente el riesgo asociado a la combinación AINE tradicional+AAS sea mayor que el asociado a la de COXIB+AAS85,86.
Finalmente, el uso concomitante de esteroides se ha incluido en algunas revisiones previas entre los factores de riesgo de complicación GI. Sin embargo, la evidencia más actualizada demuestra que la incidencia de complicaciones es muy baja, por lo que no se puede establecer que esta asociación de fármacos constituya un factor de riesgo GI esencial87,88.
El riesgo de complicación GI alta en pacientes tratados con AINE depende de la dosis. Si bien se ha señalado que el riesgo de desarrollar complicaciones GI altas es mayor durante el primer mes de tratamiento y que luego se mantiene estable durante el resto del periodo del tratamiento, los ensayos clínicos de larga duración señalan que el riesgo de desarrollar complicaciones es estable en el tiempo89.
Un estudio en pacientes con infarto agudo de miocardio previo señaló que el tratamiento a corto plazo con la mayoría de los AINE se asocia con mayor riesgo CV. Diclofenaco se asoció con un riesgo CV incrementado desde el comienzo del tratamiento hasta el final del mismo. Ibuprofeno mostró también un mayor riesgo cuando se utiliza durante más de una semana. Celecoxib se asoció con mayor riesgo de muerte después de una duración de tratamiento de 14 a 30días. Naproxeno fue el único AINE evaluado que no se asoció con un incremento del riesgo de infarto o muerte90.
No existe evidencia consistente de que el uso de paracetamol se asocie a incremento del riesgo CV91.
Complicaciones gastrointestinales asociadas al uso de antiinflamatorios no esteroideosEl tratamiento con AINE se asocia a efectos adversos graves que afectan tanto al tramo digestivo alto como al tramo digestivo bajo. Se pueden presentar como úlceras sintomáticas no complicadas, o bien como hemorragia digestiva alta, hemorragia digestiva baja y perforación GI. Estos efectos secundarios ocurren en el 1 al 4% de los pacientes tratados de AINE82. El riesgo relativo para desarrollar una complicación GI alta grave en pacientes tratados con AINE se ha estimado entre 3 y 5 veces frente a los no tratados92.
La incidencia de complicaciones graves del tramo digestivo bajo no está bien definida, pero podría suponer el 20% del total de la morbilidad asociada a AINE93. Hay estudios que señalan que el 70% de los pacientes que toman AINE de forma crónica desarrollan lesiones del tramo GI inferior, si bien muchas de ellas tienen poca relevancia clínica. Entre las lesiones descritas se incluyen aumento de la permeabilidad intestinal, inflamación, erosiones, úlceras, estenosis, anemia, enteropatía pierde proteínas, diverticulitis, hemorragia y perforación. Existen datos recientes sobre la tasa de perforación del tramo GI alto y bajo en pacientes con artritis reumatoide, de los cuales el 83% se refieren al tramo bajo94. Adicionalmente, algunos pacientes con determinadas patologías reumáticas de base inflamatoria tienen también asociada patología inflamatoria intestinal, con frecuencia subclínica, que posiblemente, pero no solo, puede deberse al uso crónico de AINE.
Estrategias de prevenciónLos antagonistas-H2 se han mostrado inferiores a los inhibidores de la bomba de protones (IBP), tanto para la curación como para la prevención de las úlceras asociadas al uso de AINE o de AAS95–99.
Los IBP se han mostrado superiores los antagonistas H2 para la prevención de úlceras endoscópicas por AINE y similares a misoprostol, pero mejor tolerados100,101. Estudios observacionales y ensayos clínicos han señalado que los IBP reducen el riesgo de complicaciones GI en pacientes que toman AINE26,53,71,76.
Los COXIB se han mostrado superiores a la combinación de AINE más placebo y tan efectivos como el uso de un AINE no selectivo asociado a IBP para la prevención de las lesiones y complicaciones gastroduodenales69,82,102–105. Datos de estudios aleatorizados señalan que los COXIB se asocian a menor frecuencia de lesiones GI bajas producidas por la asociación de un AINE no selectivo más un IBP103,106,107.
Estos fármacos se desarrollaron con intención de disminuir la toxicidad GI asociada al uso de AINE. Metaanálisis diversos han señalado que el riesgo de complicaciones GI altas con COXIB fue un 50% menor al riesgo observado con AINE clásicos85,108.
Los estudios CONDOR y GI REASON, por su parte, han demostrado que celecoxib se asocia a una frecuencia menor y baja de episodios clínicamente significativos de todo el tracto GI cuando se compara a diclofenaco asociado a IBP (CONDOR) o a AINE clásicos asociados o no a IBP (GI REASON)107,109. Un estudio demostró una tasa menor (no significativa) de complicaciones con etoricoxib frente a diclofenaco110. El estudio MEDAL señala por su parte que etoricoxib ni fue superior a diclofenaco en la incidencia de complicaciones GI altas y bajas110.
Las dosis antiagregantes de AAS duplican el riesgo de sangrado GI y hospitalización frente a las personas que no los utilizan92. Esto hace que en distintas situaciones clínicas de pacientes con patología CV y riesgo GI puedan plantearse dudas entre mantener el tratamiento con AAS o interrumpirlo. Dicha interrupción puede precipitar efectos CV graves, incluida la muerte111,112.
El tratamiento con AAS se asocia al desarrollo de úlcera péptica, incluida la esofágica, enfermedad de reflujo gastroesofágico (ERGE) o dispepsia, además de complicaciones GI altas. Por este motivo, los beneficios del tratamiento con IBP en pacientes que toman AAS se extienden también a un mejor control de los síntomas y lesiones asociadas a ERGE113.
Datos recientes señalan que el uso combinado de IBP, AAS a dosis bajas y clopidogrel en pacientes con riesgo CV se asocia a una baja frecuencia de hemorragias GI (1,8 casos por 100 pacientes-año). Sin embargo, se observa un desplazamiento de la localización de las mismas al tracto GI inferior, ya que, de todas las hemorragias, el 73% se localizaron en el delgado y en el colon (muchas de ellas como consecuencia de lesiones vasculares, posiblemente preexistentes). Estas hemorragias ocurrieron predominantemente de forma precoz durante el primer año de seguimiento114.
Riesgo hepáticoVarias revisiones sistemáticas que evalúan pacientes incluidos en ensayos clínicos muestran una incidencia muy baja de efectos graves hepáticos relacionados con el uso de AINE. Una revisión sistemática que incluye 132 estudios muestra que la necesidad de suspender el AINE por efectos adversos no fue significativamente superior a la del grupo placebo, excepto para diclofenaco115. Otro análisis que agrupa 41 estudios mostró una incidencia de efectos adversos hepáticos del 1,1% para celecoxib, del 4,2% para diclofenaco, del 1,5% para ibuprofeno y del 0,9% para placebo116; la tasa de efectos adversos hepáticos graves fue de 5/100.000 para celecoxib y de 21/100.000 para diclofenaco. La necesidad de hospitalización por toxicidad se ha estimado que oscila entre 3 y 23 por 100.000 pacientes117,118. Las elevaciones transitorias de las transaminasas son frecuentes, y en la mayoría de los casos no progresan115. Aunque se han descrito hepatitis tóxicas por AINE e incluso casos de hepatitis grave y muerte115,119–122, estos casos son excepcionales, y no existe un sistema de monitorización que permita determinar qué pacientes presentarán una reacción adversa hepática grave, por lo que no se recomiendan medidas de monitorización. El riesgo de toxicidad hepática es significativamente mayor con diclofenaco que con el resto de AINE115,116.
El uso de AINE en el paciente con cirrosis se ha relacionado con la aparición de hemorragia por varices123, y es bien conocida su capacidad para deteriorar la función renal en pacientes con cirrosis hepática, tanto compensada como descompensada124,125. Por dichos motivos se considera contraindicado el uso de AINE en pacientes con hepatopatía crónica y cirrosis.
Un estudio en 28 pacientes con cirrosis y ascitis evaluó durante 3días el efecto de celecoxib 200mg cada 12h, naproxeno 500mg cada 12h y placebo sobre la función renal y la agregación plaquetaria. Ni celecoxib ni placebo indujeron cambios en la función renal o plaquetaria. Por el contrario, naproxeno indujo una reducción marcada del filtrado glomerular, el flujo plasmático renal y la diuresis, junto con un significativo efecto antiagregante126. Por otro lado, Agrawal et al.127 observaron que etoricoxib fue bien tolerado por pacientes con insuficiencia hepática moderada o grave. Sin embargo, dada la limitada experiencia, se recomienda evitar también el uso de COXIB en los pacientes con hepatopatía, y especialmente en los que presenten cirrosis hepática descompensada.
DispepsiaSe estima que entre el 10 y el 30% de los pacientes que reciben un AINE presentan dispepsia, y que la dispepsia lleva a suspender el tratamiento en el 5 al 15% de pacientes128. La adición de un IBP frente a placebo se asoció a menor frecuencia de dispepsia en pacientes tratados con AINE101. Un metaanálisis publicado por Spiegel et al.129 evaluó 26 estudios comparando un COXIB vs. AINE tradicional o AINE tradicional más IBP vs. AINE solo. La comparación de COXIB vs AINE tradicional mostró una reducción relativa del riesgo de síntomas del 12% y una reducción absoluta del 3,7%. La comparación de AINE tradicional+IBP vs. AINE tradicional mostró una reducción del riesgo relativo del 66% y una reducción del riesgo absoluto del 9%. El número de pacientes a tratar para prevenir la dispepsia fue de 27 para los COXIB y de 11 para los AINE tradicionales más un IBP. Estos resultados deben evaluarse con cuidado, dado que no se ha realizado una comparación directa entre COXIB y AINE tradicionales+IBP. En una búsqueda sistemática realizada ad hoc se han detectado 6 estudios que comparan directamente un COXIB con AINE tradicional+IBP102,103,106,130–132. El metaanálisis de los 6 estudios en los que disponemos de datos sobre dispepsia sugiere, sin embargo, que este efecto es cierto. La incidencia de dispepsia fue del 11,8% (112/947) en los que recibieron un COXIB vs. 7,4% (72/977) en los tratados con un AINE tradicional o no selectivo+un IBP (OR: 2,2; IC95%: 1,3-3,6). Dada la alta eficacia de los IBP en el tratamiento de la dispepsia asociada a AINE, parece razonable recomendar también su utilización en el caso de los pacientes que presentan dispepsia asociada al uso de COXIB.
Enfermedad inflamatoria intestinalEn los pacientes que sufren enfermedad inflamatoria intestinal (EII) se debe evitar el uso de AINE.
NE: 1–; GR: B; GA: 89%
En los pacientes que sufren EII y en caso de que sea necesario utilizar AINE en fases quiescentes de la enfermedad, se recomienda el uso de COXIB a dosis bajas y durante un tiempo corto.
NE: 1–; GR: B; GA: 100%
Se estima que hasta un tercio de pacientes con EII desarrollan artritis que puede, o no, estar ligada patogénicamente con la misma133. Esto implica que muchos pacientes con algún tipo de EII precisen AINE en algún momento determinado de su evolución. Los estudios epidemiológicos existentes son en general de calidad baja y con resultados claramente contradictorios134–136. Por otra parte, no existen ensayos clínicos que demuestren que la toma de AINE produzca empeoramiento o recurrencia de la EII, si bien existen series de casos con números variables de pacientes que así lo sugieren134. En este sentido, un estudio relativamente reciente señaló que el 17-28% de pacientes en remisión con enfermedad de Crohn o colitis ulcerosa que recibieron AINE no selectivos como naproxeno, diclofenaco, nabumetona o indometacina durante 4 semanas, tuvieron recurrencia en los primeros 9días tras la toma del fármaco. Esto no se dio en los que tomaron nimesulida (inhibidor selectivo de la COX-2), AAS a dosis bajas o paracetamol137. Unos pocos ensayos clínicos han testado si el uso de inhibidores selectivos de la COX-2 se asocia a recurrencia de EII quiescente. En un ensayo aleatorizado doble ciego se comparó etoricoxib (60-120mg/día) frente a placebo durante un periodo de 3meses en pacientes con enfermedad de Crohn o colitis ulcerosa. La frecuencia de recurrencia fue del 10% en ambas situaciones138. En otro ensayo similar, pero con un periodo de observación corto de 14días, se compararon celecoxib 200mg/12h frente a placebo en pacientes con colitis ulcerosa, observando cifras de recurrencia iguales por debajo del 3%139.
Riesgo renalEstratificación de riesgo renalLos AINE interfieren con la homeostasis renal. Esto tiene repercusiones en la función renal, ya conocidas en los AINE clásicos, y que como resultado de las investigaciones más recientes con COXIB se han definido mejor. Las revisiones sistemáticas sobre el riesgo de desarrollar comorbilidad renal en enfermos reumáticos concluyen que es difícil establecer la magnitud del problema, debido a que los ensayos clínicos no miden los desenlaces renales de modo sistematizado ni como parte de los episodios primarios de interés140–142.
La Sociedad Española de Nefrología recomienda hacer una estimación anual de la función renal según el filtrado glomerular. De acuerdo con ello se categoriza la presencia de enfermedad renal crónica según la tabla 4143. Se considera riesgo moderado de desarrollar un episodio adverso renal si los enfermos cursan con enfermedad renal crónica estadio3 y/o depleción de volumen intravascular, hipertensión arterial o insuficiencia cardiaca congestiva y edema periférico.
Estimación del daño renal
| Estadio | FG (ml/min/1,73 m2) | Descripción |
| 1 | ≥ 90 | Daño renal con FG normal |
| 2 | 60-89 | Daño renal, ligero descenso del FGe |
| 3 | 30-59 | Descenso moderado del FGe |
| 4 | 15-29 | Descenso grave del FGe |
| 5 | < 15 o diálisis | Prediálisis/diálisis |
FG: filtrado glomerular; FGe: filtrado glomerular estimado.
Los estadios 4 y 5 se consideran riesgo elevado de desarrollar un episodio adverso renal.
Complicaciones renales asociadas al uso de antiinflamatorios no esteroideosEn pacientes con enfermedad renal crónica estadio3, o con comorbilidad renal y/o CV asociada, no se recomienda el empleo de AINE, salvo en situaciones especiales y con estricta vigilancia clínica.
NE: 2+; GR: C; GA: 100%
En pacientes con enfermedad renal crónica estadio3, o con comorbilidad renal y/o CV asociada, deberá evitarse el empleo de dosis de AINE mayores a las recomendadas, especialmente COXIB.
NE: 2+; GR: C; GA: 89%
En pacientes con enfermedad renal crónica estadio4 y 5 el empleo de AINE está contraindicado.
NE: 2+; GR: C; GA: 78%
Los AINE producen disminución de la función renal y retención de sodio y agua. Clínicamente puede manifestarse con elevación de las cifras de creatinina séricas, edema, hipertensión, desequilibrio de agua y electrólitos, fallo renal, necrosis papilar renal o síndrome nefrótico140. El riesgo relativo de presentar algún episodio adverso renal es diferente para cada tipo de AINE, y aparentemente no sigue ningún efecto de clase. Al igual que con otro tipo de toxicidad, estos efectos son dependientes de la dosis y acumulativos a través del tiempo de exposición. Además, en los enfermos reumáticos la comorbilidad renal y CV suele asociarse, lo que incrementa el riesgo140,141,144.
La disminución de la función renal (elevación de las cifras de creatinina sérica >1,3 veces el límite normal superior) ocurre con una frecuencia del 1%. Esta elevación se observa por igual en pacientes que reciben dosis terapéuticas de AINE, y es mayor con los AINE que con placebo.
Otro de los efectos secundarios clínicamente relevantes asociados a los AINE es el desarrollo de edemas periféricos, con un riesgo estimado del 3%. Este riesgo es aún mayor cuando se emplean COXIB frente a placebo (5-38%, más alta en los ensayos clínicos en los que el edema es una variable principal en la investigación). Sin embargo, celecoxib a dosis de 200mg/día no se asoció con incremento del riesgo de edema145. Esto hace pensar que la presencia de edema no sigue un efecto de clase específico para los COXIB. El desarrollo de insuficiencia cardiaca como consecuencia de la retención de sodio y agua en pacientes susceptibles es otro efecto secundario común a todos los AINE70.
Todos los AINE se asocian con incremento de la presión arterial en sujetos hipertensos, siendo este efecto escaso en individuos con presión arterial normal. De modo general, la frecuencia de hipertensión asociada a AINE es de ≈2%, y ocurre con mayor frecuencia en sujetos con comorbilidad renal y/o CV preexistente. El cambio medio mínimo en la presión arterial tras el inicio de AINE es una elevación de 5mmHg, siendo el significado clínico de este incremento incierto. El riesgo es mayor para los COXIB (rofecoxib>etoricoxib y menor para celecoxib). Es importante monitorizar la presión arterial tras el inicio de AINE sobre todo en ancianos, en sujetos con hipertensión arterial previa y en pacientes con enfermedad renal crónica. El empleo de AINE está contraindicado en pacientes con hipertensión arterial descontrolada146–148.
La presencia de daño renal grave asociado a AINE es un episodio raro, con datos escasos sobre su ocurrencia y factores de riesgo.
Otros aspectos relevantesAnemiaEl uso de AINE se asocia a hemorragia GI clínicamente evidente mediante hematemesis, melena o rectorragia, pero también a hemorragia GI oculta y anemia. El origen de estas pérdidas hemáticas ocultas se puede deber a lesiones mucosas que afectan a todo el tramo GI, desde el estómago al intestino delgado y el colon149. Diferentes estudios en voluntarios sanos han demostrado la aparición de petequias, sangre intraluminal y pérdidas de sustancia mucosa compatibles con erosiones y úlceras en intestino delgado. En estos estudios se ha objetivado que ibuprofeno o naproxeno junto a un IBP se asociaban a una mayor proporción de estas lesiones que celecoxib solo a dosis de 400mg/día o placebo106,107. En pacientes en tratamiento crónico con AINE o COXIB se ha objetivado también mediante cápsula endoscópica que el 40%150,151 de ellos presentaban lesiones en intestino delgado, si bien la frecuencia fue numéricamente inferior en los tratados con COXIB. El estudio CONDOR103 demostró que los pacientes con artrosis o artritis reumatoide en tratamiento con celecoxib 200mg/12h presentaban un riesgo 4 veces menor de desarrollar caídas de hematocrito o hemoglogina (>2g/dl) de origen GI o presumiblemente de intestino delgado, frente a diclofenaco 75mg/12h más omeprazol 20mg/día tras 6meses de tratamiento. Este estudio se ha visto confirmado en otro estudio aleatorizado y multicéntrico con diseño PROBE en el que se comparaba celecoxib frente a AINE tradicional asociado o no a IBP152. En el programa MEDAL, sin embargo, no se observaron diferencias significativas entre etoricoxib y diclofenaco en el número de complicaciones del tramo GI bajo110.
PostoperatorioSe recomienda el uso de la combinación paracetamol-AINE en el dolor postoperatorio a corto plazo, siempre y cuando no haya contraindicación para la administración de estos últimos.
NE: 1+; GR: A; GA: 78%
No puede priorizarse un AINE sobre otro en su uso postoperatorio.
NE: 2++; GR: B; GA: 89%
La combinación en cuanto a dosis y tipo de fármacos a usar en el postoperatorio debe ser balanceada de forma empírica.
NE: 3; GR: D; GA: 78%
Los analgésicos no opiáceos, paracetamol y AINE a menudo se administran junto con los opiáceos como parte de la analgesia multimodal después de la cirugía mayor. La elección del método de alivio del dolor postoperatorio debe ser bien balanceada, pudiendo combinarse distintos fármacos y diferentes vías de administración con el objetivo de emplear dosis más pequeñas y así minimizar los posibles efectos colaterales.
Una revisión sistemática reciente153 demostró una reducción estadísticamente significativa del consumo de morfina a las 24h tras la cirugía, al usar tratamiento combinado con paracetamol o AINE frente a placebo, existiendo además una diferencia clara entre paracetamol y AINE, a favor de estos últimos. También se demostró una diferencia estadísticamente significativa en el nivel de sedación y en la aparición de efectos adversos (náuseas y vómitos postoperatorios) con cualquiera de las combinaciones, sin que hubiera superioridad entre una u otra elección. En otra revisión154 se evaluó la función renal tras la administración de AINE para el control del dolor postoperatorio. En 1.459 pacientes de 23 estudios aleatorizados se determina el aclaramiento de la creatinina (48h), la creatinina sérica, el volumen de orina, Na/K urinario y la necesidad de diálisis. Los resultados demuestran una disminución del aclaramiento de la creatinina 16ml/min pero no hay diferencias en el resto de parámetros. Tampoco se observan diferencias entre los AINE estudiados ni casos de fallo renal que requirieran diálisis.
Una dosis única oral de celecoxib155 o de etoricoxib156 (120mg) es efectiva para el alivio del dolor postoperatorio, y los episodios adversos no difieren de los del placebo.
El dexketoprofeno administrado por vía parenteral tiene una eficacia analgésica en el postoperatorio similar a la de ketoprofeno y diclofenaco157,158. La dosis recomendada es de 50mg cada 8 o 12h limitada al período sintomático agudo (no más de 2días). La dosis total diaria debe limitarse a 50mg en los siguientes supuestos: a)en los ancianos que tengan disminución fisiológica leve de la función renal; b)en pacientes con insuficiencia hepática leve a moderada (puntuación Child-Pugh 5-9), que además deben ser cuidadosamente monitorizados, y c)en caso de insuficiencia renal leve (aclaramiento de creatinina 50-80ml/min).
Resumen y recomendaciones finalesUn resumen de las recomendaciones de este consenso, así como la expresión gráfica de los efectos secundarios de los AINE más utilizados, se encuentran detallados en las tablas 5 y 6. Finalmente, en la figura 3 se ha construido un algoritmo que trata de guiar hacia una correcta prescripción de AINE, basándose en la presencia de los diferentes niveles de riesgo GI y CV acorde a la evidencia disponible en 2013.
Resumen de los efectos de los diferentes AINE a dosis antiinflamatorias
| Tipo de AINE | Daño GI alto | Daño GI bajo | Necesidad de IBP para proteger el tracto GI alto | Interacción con AAS o ACO | Riesgo CV |
| Diclofenaco | ++ | ++ | ++ | + | +++ |
| Ibuprofeno | +++ | +++ | ++ | +++ | ++ |
| Naproxeno | ++++ | ++++ | +++ | +++ | – |
| Celecoxib | + | + | - | + | ++ |
| Etoricoxib | + | ++ | + | ¿? | +++ |
El número de cruces indica una evaluación semi-cuantitativa del nivel de riesgo frente a no uso. Los niveles de evidencia no son idénticos y en ocasiones limitados (ver recomendaciones más específicas).
AAS: ácido acetilsalicílico; ACO: anticoagulantes; CV: cardiovascular; GI: gastrointestinal; IBP: inhibidor de la bomba de protones.
Resumen de las recomendaciones del consenso
| Recomendaciones |
| Eficacia |
| 1. Indicaciones. La principal indicación para el empleo de los AINE es la disminución del dolor. Ningún AINE ha demostrado ser superior a otro, siendo la eficacia de los AINE tradicionales semejante a la de los COXIB |
| 2. Tiempos. Antes de usar AINE se deben valorar otras opciones terapéuticas, y se deben prescribir siempre a la dosis mínima eficaz y durante el mínimo tiempo posible. Solo en casos muy específicos, como la espondilitis anquilosante, puede estar justificado el uso continuado a largo plazo |
| 3. Calidad de vida. Los AINE producen una mejoría en la calidad de vida de los enfermos con patología reumática aguda o crónica |
| Riesgo cardiovascular |
| 1. Estratificación de riesgo cardiovascular. En todos los pacientes que tomen AINE de forma crónica debe realizarse una estimación del riesgo cardiovascular (CV) al menos una vez al año |
| 2. Complicaciones cardiovasculares asociadas al uso de AINE. La administración de AINE se asocia a un incremento de riesgo de desarrollar síndrome coronario agudo (SCA) u otros episodios cardiovasculares de carácter aterotrombótico (accidente cerebrovascular y problemas arteriales periféricos). El incremento de riesgo cardiovascular varía mucho dependiendo del tipo de AINE utilizado, siendo el naproxeno uno de los más seguros, mientras rofecoxib, diclofenaco, etodolaco e indometacina son los que se asocian a un mayor riesgo cardiovascular. Etoricoxib y diclofenaco tienen un perfil CV similar |
| 3. Uso de anticoagulantes. La combinación de anticoagulantes (warfarina, dicumarínicos, etc.) con AINE se debe evitar. En caso de ser absolutamente necesario, los COXIB parecen asociarse a menor riesgo de complicaciones hemorrágicas |
| 4. Uso de antiagregantes. Se debe evitar la utilización de AINE, incluso a corto plazo, en pacientes con infarto agudo de miocardio previo que toman AAS, ya que se asocia a incremento del riesgo cardiovascular. En pacientes que toman AAS a dosis bajas, la asociación con ibuprofeno y naproxeno interfiere con el efecto antiagregante del AAS, por lo que se debe evitar usarlos conjuntamente. En los pacientes que toman AAS para prevenir episodios cardiovasculares que requieran tratamiento crónico con AINE, los COXIB son una opción terapéutica a considerar |
| Riesgo gastrointestinal |
| 1. Estratificación de riesgo digestivo. Se debe realizar una evaluación personalizada del perfil de riesgo gastrointestinal basal de cada paciente y del AINE a utilizar. La edad superior a 60años es factor de riesgo por sí solo para la aparición de complicaciones gastrointestinales en pacientes que toman AINE, y este riesgo aumenta de forma progresiva con la edad. La presencia de antecedentes de úlcera péptica gastroduodenal, complicada o no complicada, es factor de riesgo para el desarrollo de complicaciones gastrointestinales en pacientes que toman AINE |
| 2. Complicaciones gastrointestinales asociadas al uso de AINE. No se recomienda usar 2 o más AINE de manera simultánea, ya que no se incrementa la eficacia y en cambio sí aumenta la toxicidad. El riesgo de complicaciones gastrointestinales aumenta si se usan dosis altas de AINE de forma mantenida. Este riesgo es constante, independientemente de la dosis, durante todo el tiempo que se mantiene el tratamiento. El uso de AINE se asocia a aumento del riesgo de lesiones y complicaciones del tracto gastrointestinal alto y bajo |
| 3. Estrategias de prevención. No se recomienda el uso de antagonistas-de los receptores H2 para la prevención de las complicaciones gastrointestinales de los AINE. El uso de inhibidores de la bomba de protones (IBP) asociado a un AINE no selectivo es una estrategia válida para la prevención de las complicaciones gastrointestinales de los AINE en pacientes de riesgo, siendo los COXIB (datos disponibles para celecoxib) superiores a la combinación de un AINE no selectivo con un IBP en la prevención de lesiones del tracto gastrointestinal bajo. El uso de un COXIB reduce las complicaciones en el tracto gastrointestinal alto y bajo. El uso de AAS a dosis bajas aumenta de 2 a 4 veces el riesgo de complicaciones, por lo que a los pacientes con factores de riesgo gastrointestinal se les debe prescribir gastroprotección |
| 4. Riesgo hepático. En pacientes tratados con AINE la toxicidad hepática grave es rara por lo que no se recomiendan medidas especiales de monitorización. En pacientes con cirrosis hepática se recomienda evitar el uso de AINE, y en el caso de que resulte totalmente indispensable, se recomienda el uso de un COXIB durante el menor periodo de tiempo posible |
| 5. Dispepsia. En los pacientes que presentan dispepsia asociada al tratamiento con AINE no selectivos o COXIB se recomienda tratamiento con un IBP como fármaco de primera elección |
| 6. Enfermedad inflamatoria intestinal. En los pacientes que sufren enfermedad inflamatoria intestinal se debe evitar el uso de AINE, y en caso de que sea necesario, utilizarlos en fases quiescentes de la enfermedad; se recomienda el uso de COXIB a dosis bajas y durante un tiempo corto |
| Riesgo renal |
| 1. Estratificación de riesgo renal. En los enfermos reumáticos crónicos que reciben AINE deberá evaluarse la función renal mediante estimación del filtrado glomerular, al menos una vez al año |
| 2. Complicaciones renales asociadas a uso de AINE. En pacientes con enfermedad renal crónica estadio 3, o con comorbilidad renal y/o cardiovascular asociada, no se recomienda el empleo de AINE, salvo en situaciones especiales y con estricta vigilancia clínica, y deberá evitarse el empleo de dosis de AINE mayores a las recomendadas. En pacientes con enfermedad renal crónica estadio 4 y 5 el empleo de AINE está contraindicado |
| Otros aspectos relevantes |
| 1. Anemia. El desarrollo de anemia o descensos de hemoglobina >2g/dl es frecuente en pacientes que toman AINE, aun asociado a IBP. El tratamiento con celecoxib se asocia a una menor probabilidad de desarrollar este efecto adverso |
| 2. Postoperatorio. Se recomienda el uso de la combinación paracetamol-AINE en el dolor postoperatorio a corto plazo, siempre y cuando no haya contraindicación para la administración de estos últimos. No puede priorizarse un AINE sobre otro en su uso postoperatorio. La combinación en cuanto a dosis y tipo de fármacos a usar en el postoperatorio debe ser balanceada de forma empírica |
Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesEl Dr. Lanas declara haber recibido en los dos últimos años ayudas a la investigación por parte de AstraZeneca, Pfizer y Bayer. Igualmente ha participado en Boards organizados por Pfizer y Bayer.
El Dr. Calvet declara haber participado en los dos últimos años en Boards organizados por Pfizer.
El Dr. P. Benito declara haber recibido en los dos últimos años ayudas a la investigación por parte de Pfizer, Abbott, Roche, UCB y Esteve.
El Dr. García Llorente manifiesta haber participado en los dos últimos años en reuniones científicas patrocinadas por Abbott, Pfeizer, UCB, Roche, BMS, así como en un advisory board de UCB.
La Dra. Blanca Hernández Cruz declara que en los últimos dos años ha recibido ayudas para la investigación, pago de honorarios por consultoría y pago de honorarios por ponencias con diversas empresas: Sociedad Española de Reumatología, Abbot, Roche, Pfizer, MSD y BMS.
El resto de los participantes declara no tener ningún conflicto de intereses.
Documento publicado simultáneamente en Reumatol Clin. 2014; 10: http://dx.doi.org/10.1016/j.gastrohep.2013.11.014