La infección por el virus SARS-CoV-2 ha producido una pandemia con graves consecuencias sobre nuestro sistema sanitario. Aunque el colectivo de pacientes trasplantados hepáticos representa solo una minoría de la población, los hepatólogos que seguimos a estos pacientes hemos intentado coordinar esfuerzos para protocolizar el manejo de la inmunosupresión durante la infección por SARS-CoV-2. Aunque no hay estudios sólidos que avalen recomendaciones generales, las experiencias con otras infecciones víricas (hepatitis C, citomegalovirus) sugieren que el manejo de la inmunosupresión sin micofenolato mofetilo ni inhibidores m-Tor (fármacos que además se asocian a leucopenia y linfopenia) puede resultar beneficiosa. Es importante además prestar atención a las posibles interacciones farmacológicas, especialmente en el caso de tacrolimus, con algunos de los tratamientos con efecto antiviral que se administran en el contexto de la covid-19 (lopinavir/ritonavir, azitromicina). Finalmente, deberá tenerse en cuenta el efecto inmunosupresor de fármacos inmunomoduladores (tocilizumab y similares) que se administran en pacientes con enfermedad pulmonar severa. En el artículo se revisan los mecanismos de actuación de los diferentes fármacos inmunosupresores, su potencial efecto sobre la infección por SARS-CoV-2 y se sugieren unas pautas en el manejo de la inmunosupresión.
SARS-CoV-2 infection has produced a pandemic with serious consequences for our health care system. Although liver transplant patients represent only a minority of the population, the hepatologists who follow these patients have tried to coordinate efforts to produce a protocol the management of immunosuppression during SARS-CoV-2 infection. Although there are no solid studies to support general recommendations, experiences with other viral infections (hepatitis C, cytomegalovirus) suggest that management of immunosuppression without mycophenolate mofetil or m-Tor inhibitors (drugs that are also associated with leukopenia and lymphopenia) may be beneficial. It is also important to pay attention to possible drug interactions, especially in the case of tacrolimus, with some of the treatments with antiviral effect given in the context of COVID 19 (lopinavir/ritonavir, azithromycin). Finally, the immunosuppressive effect of immunomodulating drugs (tocilizumab and similar) administered to patients with severe lung disease should be taken into account. The mechanisms of action of the different immunosuppressive drugs are reviewed in this article, as well as their potential effect on SARS-CoV-2 infection, and suggests guidelines for the management of immunosuppression.
La infección por el virus SARS-CoV-2 ha producido una pandemia con graves repercusiones sanitarias y económicas. En la lucha por la supervivencia de los pacientes, los médicos hemos probado con más o menos acierto múltiples fármacos dirigidos a combatir el virus o sus efectos en el organismo1–10. Los pacientes trasplantados hepáticos son una minoría de la población, pero su condición de inmunosuprimidos los hace en teoría más sensibles a la infección, por lo que los hepatólogos que nos dedicamos al trasplante hepático hemos estado muy pendientes de nuestros pacientes y hemos intentado ajustar la inmunosupresión tanto a la gravedad de la enfermedad como a los tratamientos que se han utilizado. En este artículo se detallan los mecanismos de actuación de cada inmunosupresor, se especifica el balance entre su efecto inmunosupresor y el antiviral en algunos casos, y finalmente se hace una propuesta de actuación en relación con el tratamiento inmunosupresor en pacientes con covid-19.
El virus SARS-CoV-2El virus SARS-CoV-2 es un virus que pertenece a la familia Coronaviridae, que incluye 4 géneros (alfa, beta, gamma y delta). Los coronavirus con capacidad de infectar a humanos pertenecen a los géneros alfa (HCoV-229E y HCoV-NL63) y beta (SARS-CoV, MERS-CoV, HCoV-OC43 y HCoV-HKU1)11,12. En este último género se incluyen los 3 agentes que hasta la fecha son conocidos por producir infecciones del tracto respiratorio inferior y que por tanto se pueden asociar a cuadros clínicos graves (SARS-CoV, MERS-CoV y SARS-CoV-2). Como otros agentes de su familia, SARS-CoV-2 es un virus RNA de cadena positiva, que codifica en diferentes marcos de lectura abierta u open reading frames proteínas estructurales (nucleocápside, membrana, envuelta y espiga o «S») y no estructurales (RNA polimerasa, proteasas)13–15. Muy recientemente se ha podido conocer que para su entrada en las células del organismo el virus utiliza los receptores ACE 2 y posiblemente otros receptores adicionales (como ocurre con muchos otros virus)16–19.
SARS-CoV-2 tiene como fuente primaria de contagio la transmisión entre personas a través de contacto estrecho o a partir de los fómites cuando un paciente tose. Tiene una elevada infectividad, principalmente durante las primeras fases, colonizando el organismo a través del tracto respiratorio y en especial infectando a las células epiteliales alveolares19,20. Su replicación es rápida y se generaliza la infección, que en la mayoría de los casos (80%) es asintomática o leve14. Se distinguen tres fases: una primera fase asintomática con una elevada carga viral; una segunda fase sintomática leve, con tos seca, odinofagia, anosmia, fiebre, cansancio y en ocasiones diarrea; y la tercera fase, que caracteriza a los casos graves, produce neumonía con insuficiencia respiratoria y disnea, puede conducir al síndrome de distrés respiratorio del adulto y finalmente a fallo multiorgánico y muerte14,18,20. En esta tercera fase la viremia puede ser baja y la afectación tanto pulmonar como endotelial, miocárdica, etc., se debe a la denominada tormenta citoquínica, que resultaría de la respuesta exagerada del sistema inmune a la infección por el SARS-CoV-221. La enfermedad clínica correspondiente a esta infección vírica es lo que conocemos como covid-19.
El sistema inmune en la respuesta ante el SARS-CoV-2Respuesta innataLa presencia de linfopenia con neutrofilia, niveles elevados de IL-6, incremento de la proteína C reactiva, así como el hallazgo de niveles elevados de citoquinas asociadas a la inmunidad innata como IP-10, MCP-1, MIP-1α y TNFα sugieren que esta juega un papel muy importante en la respuesta inflamatoria asociada a la infección (que también se observó con el SARS-CoV y MERS-CoV) y por tanto, que sea responsable de la evolución hacia la gravedad de covid-1921–25.
La respuesta efectora inmune innata contra los virus se basa mayoritariamente en el interferón (IFN-1)23. Para ello, las células de la respuesta inmune innata deben reconocer la invasión del virus a través de los patrones moleculares asociados a patógenos (PAMPs)23. Este reconocimiento conduce a la activación de IFN-1 y otras citoquinas proinflamatorias24,25. Sin embargo, tal y como ocurre con otras infecciones virales, SARS-CoV y MERS-CoV contienen algunas proteínas que antagonizan vías de señalización cruciales para la activación del interferón, como la asociada al reconocimiento de los PAMPs23. El bloqueo de las vías de interferón facilitaría la replicación del virus y la liberación de más citoquinas proinflamatorias que inducirían una respuesta excesiva. Una inhibición similar parece ocurrir durante la covid-1926.
Respuesta adaptativaEn general, la respuesta inmune tipo Th1 tiene un papel predominante en las infecciones virales22,25,27. Las citoquinas generadas por las células presentadoras de antígenos dirigen la respuesta de las células T: las células T reguladoras en general coordinan la respuesta adaptativa, mientras que las células T citotóxicas son esenciales para la eliminación del virus. La respuesta inmune humoral juega un papel en la limitación de la infección y la prevención de la reinfección por medio de la producción de anticuerpos neutralizantes27–33.
Inmunosupresión en el trasplante hepático y covid-19La inmunosupresión en el trasplante hepático, aunque utilice los mismos fármacos que los utilizados en otros trasplantes de órgano sólido, se caracteriza por ser de una menor intensidad34–37. Esta particularidad permite en determinados momentos retirar temporalmente alguno de los inmunosupresores que se estén utilizando, como es el caso de una infección grave, insuficiencia renal, alteraciones neurológicas, etc.34,35. Como hemos visto, la respuesta inmunitaria juega un papel muy importante en la enfermedad covid-19, y por tanto, los inmunosupresores habitualmente utilizados podrían ser determinantes tanto como favorecedores de la infección como atenuadores de la respuesta inflamatoria secundaria a la misma. Los pocos estudios publicados, algunos más que estudios son simples reportes de casos, no sugieren ni un aumento en la incidencia de casos en pacientes trasplantados, ni una mayor mortalidad que en la población general38,39. Resultados preliminares del estudio de la Sociedad Española de Trasplante Hepático (SETH) sugieren que la mortalidad se situaría alrededor del 15% de los pacientes infectados que se recogieron en las unidades de trasplante hepático en España40. Sin embargo, muchos de los resultados que se presentan en la bibliografía tienen el sesgo de no conocer la población real de infectados, por lo que las cifras que se proporcionan en relación con la incidencia de la infección, mortalidad, etc., deben contar con esta salvedad. Entre los argumentos que se exponen como razones para una menor incidencia de infectados en la población trasplantada se consideran: una mayor higiene personal y lavado de manos habitual, la utilización más habitual de medidas de protección y el ser mucho más conscientes de la utilidad del distanciamiento social.
En el trasplante hepático, como en el de otros órganos sólidos, el tratamiento inmunosupresor se basa en un inhibidor de la calcineurina, ciclosporina o tacrolimus, siendo este último el más utilizado, asociado o no a corticoides. Además, principalmente en casos con insuficiencia renal o con objeto de prevenirla, se utiliza micofenolato mofetilo (MMF) y menos frecuentemente un inhibidor de la m-Tor, como everolimus, para poder disminuir los niveles necesarios de anticalcineurínico.
En el contexto de una infección covid-19 en un paciente trasplantado hepático, es muy importante revisar la pauta inmunosupresora. Requieren una especial atención las potenciales interacciones de los inmunosupresores con fármacos antivirales o antibacterianos utilizados en las fases iniciales de la infección por SARS-CoV-2 (lopinavir/ritonavir, azitromicina). Así mismo, debe valorarse también la interacción con otros inmunomoduladores dirigidos directamente a la respuesta citoquínica (anti-IL6, anti-IL1), utilizados en el tratamiento de los pacientes graves covid-1926,41,42: inhibidores de la señal del receptor de interleucina 6 (tocilizumab, sarilumab), del receptor de la interleucina 1 (anakinra), o inhibidores selectivos de la Janus quinasa (JAK)42–44. Aunque el efecto que estos últimos pueden tener sobre el control del rechazo celular en pacientes trasplantados es poco conocido, sí existen datos que sugieren que pueden controlar el rechazo mediado por anticuerpos45. En cualquier caso, su administración deberá tenerse en cuenta a la hora de ajustar las dosis de corticoides y evitar así el riesgo de una excesiva inmunosupresión.
A continuación, se exponen los principales efectos inmunológicos de los inmunosupresores más habituales en el trasplante hepático.
GlucocorticoidesLos glucocorticoides (GC) inhiben diferentes aspectos de la inflamación al estimular o inhibir la transcripción de genes, y la expresión de mediadores, receptores, moléculas de adhesión y de citocinas. Es por ello que su efecto es múltiple y mientras que por un lado pueden favorecer la replicación viral, son potentes antiinflamatorios que pueden ayudar a contrarrestar la tormenta citoquínica de la enfermedad. Los GC pueden controlar la inflamación en el síndrome de distrés respiratorio del adulto (SDRA) y se utilizan en las formas primarias y secundarias de linfohistiocitosis hemofagocítica46–48. Sin embargo, resultados preliminares de la utilización de altas dosis de corticoides en SARS y covid-19 no han demostrado un efecto beneficioso sobre la lesión pulmonar49. No obstante, pautas cortas de dosis medias-bajas de GC se demostraron útiles en un estudio en enfermos críticos covid-19 en China47. Estos datos tan limitados en cuanto a eficacia y seguridad de los GC, la ausencia de estudios controlados y su asociación con otros tratamientos hacen prácticamente imposible extraer conclusiones fiables. La recomendación última es que los bolus de GC en altas dosis no deben usarse en el tratamiento de la covid-19.
Su utilización en el trasplante hepático es variable. Pueden usarse o no durante los 6 primeros meses en asociación con los otros inmunosupresores y se usan en bolus a altas dosis como tratamiento del rechazo celular grave. A partir de este período postrasplante (que puede oscilar entre 0 y 6 meses), los corticoides se retiran a excepción de los pacientes que hayan sido trasplantados por patología hepática de etiología autoinmune, en los que se suelen mantener dosis bajas de forma muy prolongada. Otro uso de los GC es complementar o substituir la inmunosupresión de base durante cortos períodos de tiempo, cuando se han producido complicaciones graves que obligan a la suspensión de la medicación inmunosupresora habitual, como por ejemplo en casos de sepsis grave e insuficiencia renal32. En función del tiempo transcurrido tras el trasplante se utilizan, por períodos de entre una y 2 semanas, corticoides a dosis variables que van en la mayoría de los casos de 20 a 60mg/día.
En caso de enfermedad grave covid-19, la substitución temporal de anticalcineurínicos y MMF por GC permite a estos pacientes evitar efectos indeseables secundarios a la interacción de dichos inmunosupresores con los múltiples medicamentos que reciben para el tratamiento de la infección por SARS-CoV-2. Además previene de los propios efectos secundarios de los inmunosupresores (insuficiencia renal, agravamiento de la linfopenia, etc.). Aunque se ha indicado que la retirada incontrolada de la inmunosupresión puede producir el rechazo del injerto50, lo cual es evidente, la peculiaridad del trasplante hepático permite la substitución temporal de anticalcineurínicos por GC con relativa seguridad51.
AnticalcineurínicosCiclosporina o tacrolimus son potentes inhibidores de la actividad fosfatasa de la calcineurina linfocitaria y se consideran los medicamentos base en la inmunosupresión en el trasplante hepático36. Actualmente se suelen utilizar conjuntamente con MMF o everolimus con objeto de mantener unos niveles plasmáticos más bajos y evitar sus efectos indeseables34,35. La ciclosporina A se une a ciclofilina (receptor intracelular) y forma un complejo activo que inhibe la actividad fosfatasa de la calcineurina. La calcineurina defosforila el componente citoplasmático del factor nuclear del linfocito T activado (NFATc), de forma que puede ir al núcleo y activar los genes involucrados en la síntesis de IL-2. IFN-γ, IL-4, TNF-β46. De esta forma, ciclosporina A, al inhibir la calcineurina, inhibe la proliferación de células T evitando la expansión clonal de las células T cooperadoras y citotóxicas52. Tacrolimus actúa de forma similar, pero se une a una inmunofilina específica (FKBP) para bloquear la actividad fosfatasa de la calcineurina e inhibir así la transcripción de los genes involucrados en la síntesis de IL-2. Su efecto neto sobre covid-19 y particularmente sobre el SARS-CoV-2 se desconoce. Sin embargo, existen datos que indicarían un efecto antiviral directo de los anticalcineurínicos. Hace ya algunos años se puso en evidencia que la sobreexpresión de proteínas no estructurales de CoV (Nsp1) y la infección con SARS-CoV vivo produjo un incremento muy significativo de la señal a través de la vía calcineurina/NFAT y un incremento de la IL-2, compatible con la inmunopatogénesis y disregulación tardía de las citoquinas observada en pacientes con SARS grave. Contrariamente, la inhibición de las ciclofilinas con ciclosporina A bloqueó la replicación de todos los géneros de coronavirus, incluyendo SARS-CoV, human CoV-229E, etc.52. Este efecto antiviral de los anticalcineurínicos, principalmente de la ciclosporina A, ya se había sugerido en el caso de otros virus como el virus de la hepatitis C (VHC)53. Sin embargo, el balance entre su efecto antiviral y su efecto inmunosupresor no permite, en la mayoría de los casos, observar un efecto neto antiviral. La información de la que se dispone en estos momentos no permite afirmar que los anticalcineurínicos tengan un efecto significativo (positivo o negativo) sobre covid-19.
Si efectuamos una división simple de los pacientes con covid-19, los podemos clasificar en dos: 1) leves, que incluiría aquellos asintomáticos o con síntomas como fiebre, tos seca, cansancio, etc., pero sin insuficiencia respiratoria; 2) pacientes con neumonía e insuficiencia respiratoria. Es evidente que se trata de una clasificación muy simple y que además no tiene en cuenta factores pronósticos como la linfopenia, LDH, etc.49, pero puede servir para una decisión inicial de tratamiento y de ajuste de los anticalcineurínicos. En los pacientes leves, la recomendación es no modificar los anticalcineurínicos, a no ser que se utilicen antivirales como ritonavir-lopinavir con una elevada interferencia, particularmente con tacrolimus54. En este caso, la dosificación de tacrolimus puede ser de 0,5mg cada 3-5días. Evidentemente ello requiere un control intensivo de los niveles. Deben valorarse igualmente las interacciones con otros tratamientos (azitromicina, hidroxicloroquina, etc.) que, aunque no obligan a una disminución inicial de las dosis, requieren un control de los niveles de los anticalcineurínicos. En el caso de los pacientes graves es mejor disminuir o retirar los anticalcineurínicos, pues evitaremos sus efectos indeseables, las interacciones con otros fármacos (en ocasiones múltiples) y los ascensos y descensos incontrolados de los niveles (muy difíciles de estabilizar en estas situaciones).
Micofenolato mofetiloEl MMF es un profármaco que se convierte en ácido micofenólico (MPA) en el organismo. El metabolismo del MPA implica principalmente la glucuronidación por la enzima uridina 5’-difosfato-glucuronosiltransferasa37. El MPA tiene recirculación entero-hepática, lo que alarga su vida media. MPA es un inhibidor reversible y no competitivo de la inosina-5’-monofostato deshidrogenasa (IMPDH). Inhibe la proliferación de los linfocitos T y B y la producción de inmunoglobulinas mediante la depleción del pool de guanosina y desoxiguanosina en los linfocitos37,54. Además de esta potente acción inmunosupresora, y por tanto facilitadora de infecciones, MPA tiene una amplia actividad in vitro y/o en modelos animales frente a diferentes virus, entre los que se incluyen virus del Nilo occidental55, de la encefalitis japonesa56, fiebre amarilla y dengue57, y Chikungunya58. MPA es también capaz de inhibir in vitro e in vivo la replicación del VHC mediante el incremento de la expresión génica del interferón y mediante la depleción de guanosina59. En relación con los coronavirus, MPA no fue efectivo contra el SARS-CoV en un modelo animal, pero sí contra MERS-CoV60.
A pesar de estos efectos antivirales in vitro y en modelos animales, la realidad en la práctica clínica del trasplante es muy diferente, en la que predomina claramente el efecto inmunosupresor tal y como se ha visto con el VHC y el citomegalovirus. Por tanto, en nuestra opinión, el MMF se debe retirar si un paciente trasplantado hepático presenta infección por SARS-CoV-2 en cualquier fase o gravedad de la enfermedad. Con independencia de su efecto inmunosupresor descrito, puede producir leucopenia, linfopenia, trombocitopenia y aplasia medular, complicaciones que pueden dificultar enormemente la resolución de la infección o poner en riesgo la vida del paciente.
Inhibidores de la m-Tor: sirolimus/everolimusSirolimus es un macrólido, proveniente del actinomiceto Streptomyces hygroscopicus descubierto en la Isla de Pascua (Rapa Nui) entre diciembre de 1964 y febrero de 1965 por la Canadian Medical Research Expedition61. Es metabolizado por el citocromo p450 3A4 requiriendo ajuste de niveles plasmáticos. El 90% de sus metabolitos se eliminan por las heces. Para actuar, los inhibidores de mTOR precisan formar un complejo con una inmunofilina. Al igual que tacrolimus, se unen a FKBP-12, pero a diferencia de este, no inhiben la calcineurina sino el mammalian target of rapamycin, provocando el bloqueo de la señal desde el receptor de IL-2 inhibiendo la proliferación de células T y B37. El everolimus es un derivado del sirolimus con una semivida de eliminación más corta y mayor biodisponibilidad oral.
Los inhibidores de mTOR presentan, además de su efecto inmunodepresor, antiproliferativo, etc., propiedades antivirales, bien demostradas en pacientes trasplantados en cuanto a la prevención y/o tratamiento de infecciones por citomegalovirus o virus BK62. Si bien se ha sugerido que a través de las vías asociadas a los complejos m-Tor 1 y 2 junto con la activación de la proteína quinasa (AMPK) podría tener un efecto antiviral frente a los coronavirus, no existe evidencia clínica. Solo un estudio en pacientes con neumonía e insuficiencia respiratoria por virus influenza halló una menor duración del cuadro y menos incidencia de fallo multiorgánico en los pacientes que recibieron rapamicina63. No se dispone de evidencia clínica para hacer recomendaciones sobre su utilización en la infección covid-19. Deben valorarse las interacciones farmacológicas con otros medicamentos y la posibilidad de leucopenia y linfopenia asociadas.
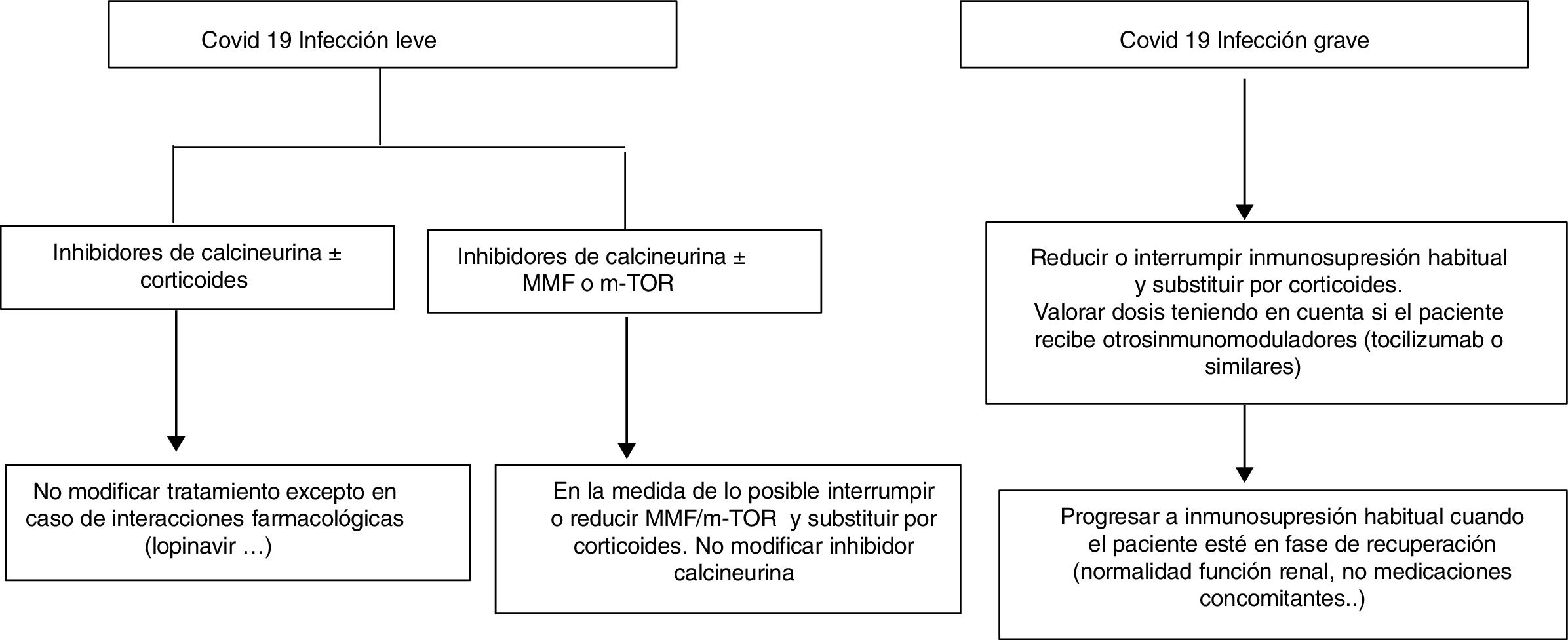
Propuesta de actuación en pacientes trasplantados hepáticos y covid-19Seguramente cada uno de los médicos que llevan pacientes trasplantados hepáticos podemos formular una propuesta. La siguiente propuesta solo pretende dar unas líneas generales de actuación que requerirán su adaptación a los pacientes. No es lo mismo un trasplantado hepático de hace un año que otro de hace 10, ni uno con muchas comorbilidades que otro sin, y así muchas situaciones que obligan a adaptar la inmunosupresión a las características de nuestros pacientes. Tal y como hemos mencionado, la propuesta parte de una clasificación muy sencilla pero que permite instaurar el cambio del tratamiento inmunosupresor antes de que se produzcan complicaciones asociadas al mismo (fig. 1).
- 1.
Trasplantados hepáticos con infección covid-19 asintomática o leve (tos seca, odinofagia, anosmia, fiebre, cansancio y en ocasiones diarrea):
- a)
Suspender/reducir MMF o everolimus si son parte del tratamiento siempre que sea posible, substituyéndolos por dosis bajas de prednisona.
- b)
Vigilar exhaustivamente las interacciones farmacológicas, sobre todo en aquellos pacientes con anticalcineurínicos que reciban antivirales https://www.hiv-druginteractions.org/checker
- 2.
Trasplantados hepáticos con infección grave (neumonía en cualquiera de sus fases):
- a)
Suspender MMF o everolimus.
- b)
Reducir o suspender anticalcineurínicos y sustituir por corticoides.
- c)
Tener en cuenta si el paciente ha recibido inmunomoduladores (tipo inhibidores receptor IL-6) al decidir la dosis de corticoides.
- d)
Vigilar exhaustivamente las interacciones farmacológicas, sobre todo en aquellos pacientes que reciban antivirales https://www.hiv-druginteractions.org/checker
La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
AutoríaTodos los autores han hecho contribuciones sustanciales en cada uno de los siguientes aspectos: (1) la concepción y el diseño de la revisión, o la adquisición de datos, o el análisis y la interpretación de los datos, (2) el borrador del artículo o la revisión crítica del contenido intelectual, (3) la aprobación definitiva de la versión que se presenta.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.