La hepatotoxicidad por antifúngicos es bien conocida1. La terbinafina es el único fármaco de la familia de las alilaminas usado en el tratamiento sistémico de la onicomicosis inducida por dermatofitos. Su potencial hepatotoxicidad ha sido descrita, pero anecdóticamente2, con una incidencia calculada de 0,5-3 casos/100.000 exposiciones.
Presentamos el caso de una mujer de 47 años, con el único antecedente de espondilitis anquilosante HLA B27+ diagnosticada 30 años antes, que fue tratada por una onicomicosis durante 28 días, con 250mg diarios de terbinafina. No existía historia previa de consumo de alcohol ni de productos de herboristería; su único tratamiento habitual adicional consistía en eterocoxib (90mg), usado desde años antes como analgésico puntual, a demanda, en una dosis diaria.
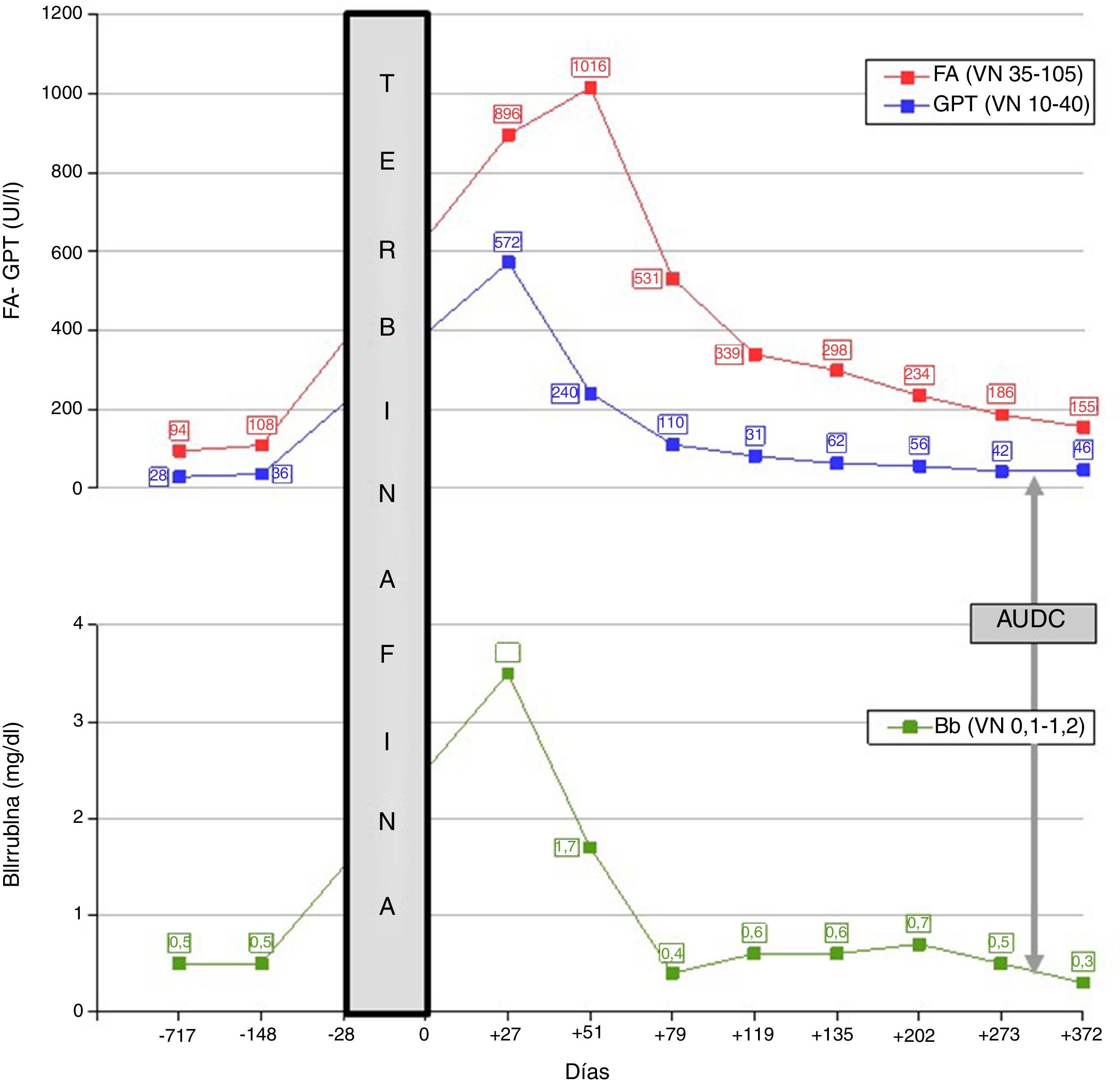
A las 3semanas de suspender el antifúngico comenzó con ictericia, prurito y astenia, sin rash ni adenomegalias. El índice de masa corporal era de 28kg/m2 y no cumplía datos de síndrome metabólico. Se disponía de análisis previos, de 2años y de 5meses antes, con bioquímica hepática normal. Las cifras máximas de bilirrubina (3,5mg/dl) y de transaminasas (GPT: 572 UI/l) se documentaron el día +27 tras la suspensión del fármaco; la cifra máxima de fosfatasa alcalina (1.016 UI/l) se alcanzó el día +51. La evolución cronológica de las alteraciones de la bioquímica hepática y su relación con el empleo y la retirada de la terbinafina se muestran en la figura 1, considerando el momento basal (día 0), el de la suspensión del antifúngico. El HBsAg y los anticuerpos IgG frente al VHC fueron sistemáticamente negativos. Se excluyeron igualmente otras causas de hepatopatía viral (IgM anti-VHA y anti-VHE negativas). La ceruloplasmina (44,5mg/dl), la α-1 antitripsina (185,5mg/dl), el índice de saturación de transferrina (29) y el hemograma fueron normales. Una ecografía descartó obstrucción biliar y trastornos vasculares hepáticos. Los anticuerpos antinucleares fueron positivos —a título 1/160, con patrón moteado citoplasmático— el día +51, negativizándose después (día +119); los anticuerpos antimitocondriales, anti-LKM y antimúsculo liso fueron repetidamente negativos. Las gammaglobulinas (1,3g/dl) y la IgG (1.373,8mg/dl) fueron normales.
Evolución cronológica de las alteraciones de la bioquímica hepática y su relación con el empleo y la retirada de la terbinafina; se consideró el momento basal (día 0), el de la suspensión del tratamiento antifúngico.
AUDC: ácido ursodesoxicólico; Bb: bilirrubina; FA: fosfatasa alcalina; VN: valores normales.
Se definió que existía daño hepático inducido por fármacos (drug-induced liver injury), atribuible a terbinafina, con patrón colestásico: (GPT/40)/(fosfatasa alcalina/105)=R 1,7, calculado al día+27. Se evaluó la causalidad mediante la escala CIOMS/RUCAM, considerándola probable (8 puntos): comienzo de los síntomas entre 5 y 90 días tras el inicio del tratamiento (+2); evolución analítica favorable, con descenso de la fosfatasa alcalina >50% en los 180 días posteriores a la retirada del fármaco (+2); exclusión completa de otras causas o toxinas (+2) y hepatotoxicidad previa conocida para la terbinafina, descrita en el etiquetado (+2). La tendencia a la desaparición de la colestasis hizo prescindible la biopsia hepática. Igualmente se obvió la reexposición, al considerarse desproporcionada.
Aunque la evolución fue favorable, no se llegó a la resolución completa, al menos hasta el noveno mes, por lo que se inició entonces tratamiento con ácido ursodesoxicólico: 300mg cada 12 h, con respuesta parcial (fig. 1).
Los mecanismos exactos por los que la terbinafina puede inducir daño hepático no han sido aún dilucidados. Recientemente se ha descrito la asociación entre el HLA-A*33:01 y la susceptibilidad para desarrollar hepatotoxicidad colestásica por terbinafina2. La terbinafina experimenta una compleja biotransformación hepática y alguno de los metabolitos resultantes presenta capacidad de unirse a proteínas hepatobiliares y de promover una reacción inmune3; en otras ocasiones, la toxicidad hepática es idiosincrásica. El patrón de toxicidad habitual es colestásico, típicamente prolongado (entre 2 y 12 meses), con capacidad, incluso, de progresar hacia la ductopenia4. El periodo de latencia (exposición-ictericia) oscila entre 2 y 6 semanas, mientras que el pico máximo de bilirrubina suele darse entre 3 y 5 semanas tras la suspensión del fármaco. La resolución tras la retirada suele ser la norma. No existe tratamiento específico, aunque se ha ensayado, con éxito, el ácido ursodesoxicólico5.
En nuestro caso quedó bien documentado que la colestasis fue imputable a la terbinafina, prescrita para su indicación habitual. Para que el diagnóstico de daño hepático inducido por fármacos sea precoz, es necesario un elevado nivel de sospecha clínica. La comunicación de casos como este pretende favorecer el conocimiento al respecto y promover el estado de alerta clínica, sobre la hepatotoxicidad farmacológica.