Las micropartículas (MP) son un grupo heterogéneo de vesículas derivadas de la membrana plasmática de diferentes tipos de células durante la apoptosis y la activación celular, que participan en la comunicación intercelular, hemostasia, angiogénesis, reactividad vascular e inflamación. En pacientes con lupus eritematoso sistémico (LES) se ha observado incremento en algunos tipos de MP circulantes. Recientemente se ha propuesto que estas estructuras pueden participar como fuente de autoantígenos en LES.
Microparticles (MPs) are a heterogeneous group of vesicles generated from the plasma membranes of different cell types during apoptosis and cell activation. They are involved in intercellular communication, haemostasis, angiogenesis, vascular reactivity and inflammation. An increase in some types of circulating MPs has been observed in patients with systemic lupus erythematosus (SLE). It has recently been proposed that these structures may act as a source of autoantigens in SLE.
La cromatina, sus componentes individuales (ADN de doble cadena e histonas) y diversos tipos de ARN son sustrato antigénico en LES, induciendo la producción de autoanticuerpos y complejos inmunes implicados en la patogenia de esta enfermedad1. El reconocimiento de micropartícula (MP) generadas durante la activación o muerte celular con capacidad de trasportar en su superficie ADN y en su interior ADN y ARN, sugiere que las MP pueden, por receptores tipo Toll en linfocitos B autorreactivos y células dendríticas plasmacitoides (CDp), comportarse como adyuvantes antigénicos y participar en la patogenia del lupus eritematoso sistémico (LES)2. Adicionalmente las partículas derivadas de membrana plasmática tienen propiedades protrombóticas y proinflamatorias3 que pudieran tener implicación en algunas de las complicaciones de esta enfermedad.
Definición, producción, composición y funcionesLas MP son pequeñas vesículas (0,1 a 1μm) intactas, liberadas de la membrana plasmática de diferentes tipos de células (plaquetas, monocitos, linfocitos, eritrocitos, neutrófilos y células endoteliales, principalmente) durante los procesos de activación celular o de apoptosis4–7. Fueron Identificadas por primera vez en 1967 como residuos celulares inertes («polvo de plaquetas») pero estudios y observaciones posteriores permitieron reconocerlas como estructuras subcelulares funcionalmente activas8. En el plasma de individuos sanos se encuentra una concentración basal de MP de 105 – 106 PMV/ml (vesículas derivadas de membrana plasmática por ml)9.
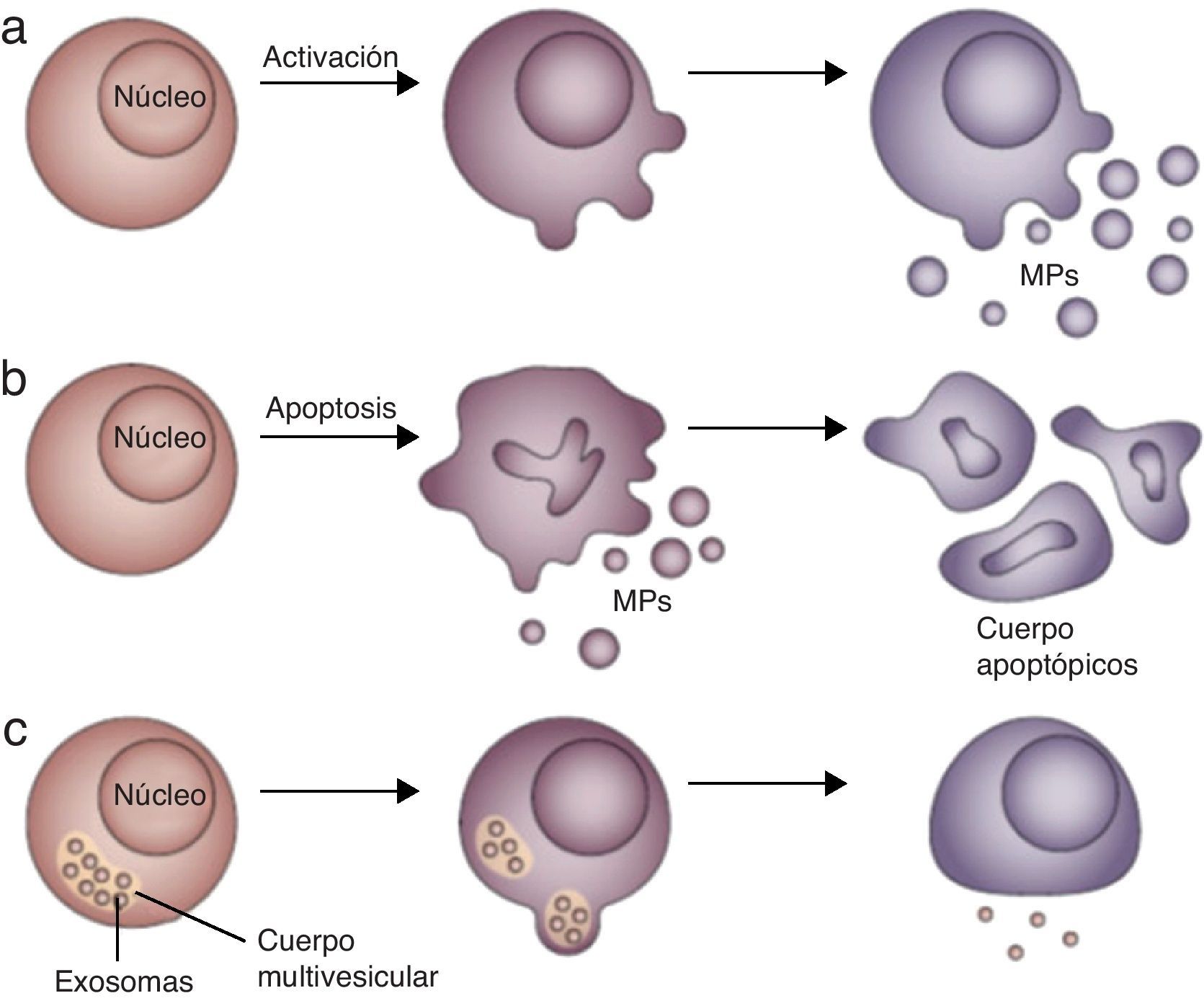
Las MP se diferencian estructural y funcionalmente de los cuerpos apoptóticos y de los exosomas (fig. 1). Los primeros, en contraste con las MP, se producen durante las fases tardías de la apoptosis, son de mayor tamaño (1-4μm) y generalmente son fagocitados sin generar inflamación; sin embargo, cuando se alteran los mecanismos de depuración pueden ser fuente de autoantígenos. Por su parte, el término exosoma se restringe para las vesículas más pequeñas que las MP (≤ 100nm) que son liberadas extracelularmente como consecuencia de fusión de cuerpos multivesiculares con la membrana plasmática.
Los cuerpos apoptóticos (b) a diferencia de las MP (a), se producen durante las fases tardías de la apoptosis, son de mayor tamaño (1-4μm) y generalmente son fagocitados sin generar inflamación; por su parte los exosomas (c) se forman intracelularmente por vesiculación interna de compartimientos endosómicos, se almacenan en cuerpos multivesiculares y se secretan por exocitosis. Modificada de: Beyer C, Pisetsky DS3.
Los exosomas son abundantes en líquidos corporales y al igual que las MP son secretados por muchos tipos de células10,11. Recientemente se ha demostrado que los exosomas provenientes de CDp contienen distintos tipos de microARN que pueden transferir a células blanco interfiriendo con su ARN mensajero11–14. También se ha descrito que los exosomas expresan moléculas del complejo mayor de histocompatibilidad clase i y ii y moléculas coestimuladoras5,10. Al igual que las MP, se ha propuesto que los exosomas tienen diferentes funciones fisiológicas que varían según la célula de origen: coagulación, regulación inmune, migración celular, diferenciación celular, entre otros y se han implicado en la patogénesis de diferentes enfermedades como tumores, enfermedad cardiovascular, enfermedades neurodegenerativas e infecciones virales, pero hasta el momento no se ha estudiado su participación en LES10–14.
Por su parte, las MP se generan durante la activación celular o la apoptosis temprana mediante la formación de protrusiones en la membrana celular que pueden desprenderse de la célula por escisión de su tallo de unión. Este proceso es debido a la reorganización del citoesqueleto. Durante la activación celular esta reorganización es secundaria a enzimas dependientes de calcio como calpaína que degrada proteínas estructurales del citoesqueleto. En la apoptosis se produce por activación de cinasas intracelulares (ROCK) que fosforilan las cadenas ligeras de miosina permitiendo el desarrollo de fuerzas de contracción y de deslizamiento12,15. En ambos procesos el incremento del calcio citosólico altera las enzimas que mantienen la asimetría de la bicapa lipídica (scramblasa, floppasa, flippasa) permitiendo la exteriorización de fosfolípidos aniónicos, principalmente fosfatidilserina8,16.
Las MP pueden contener en su superficie receptores de quimioquinas, moléculas de adhesión, marcadores como MHC clase ii y algunas moléculas coestimuladoras, factor tisular, diferentes tipos de ligandos, ADN, fosfolípidos (fosfatidilserina), entre otros; y en su interior, proteínas derivadas del citosol, el retículo endoplásmico y el núcleo, incluyendo las histonas, y ARN (ARN mensajero, microARN, ARN de cadena sencilla), de la célula origen11,17,18. Los marcadores de superficie que expresan permiten reconocer la célula de procedencia19–21.
Las MP participan en hemostasia, angiogénesis (induciendo la producción de factor de crecimiento de endotelio vascular), regulación del tono vascular (mediante liberación de prostaciclina, favoreciendo la inhibición o la producción de óxido nítrico y expresando tromboxano A2), comunicación intercelular (funcionando como vectores de información entre diferentes tipos de células) y en respuesta inflamatoria19,22,23. Como mediadores inflamatorios tienen la capacidad de aumentar la sensibilidad de las células a nuevos estímulos por medio de la transferencia intercelular de receptores de quimioquinas, inducir la expresión de moléculas de adhesión y la producción de IL6, IL1β y proteína quimiotáctica de monocitos 1 (MCP-1) en células endoteliales, favorecer el rodamiento de leucocitos y el contacto célula-célula, transferir ácido araquidónico a leucocitos y células endoteliales, y activar la vía clásica del complemento. También pueden participar trasportando Fas ligando hasta su receptor celular, adquiriendo una capacidad proapoptótica mayor que el Fas ligando soluble; y ser fuente de aminofosfolípidos que a su vez son sustrato de la fosfolipasa A2 soluble para la producción de ácido lisofosfatídico3,4,24–26.
Las MP tienen diferentes mecanismos para interactuar con otras células, transferir su contenido y ejercer las funciones descritas, como son: unión de las moléculas que contienen en la superficie con receptores de membrana de la célula blanco, fusión directa con la membrana plasmática o pueden ser endocitadas. Las MP endocitadas pueden fusionarse con la membrana del endosoma o sufrir transcistosis5,27.
Participación en patogeniaSe ha observado incremento en el número de MP en diferentes enfermedades; principalmente neoplasias, diabetes mellitus, enfermedad cardiovascular y enfermedades autoinmunes (artritis reumatoide, síndrome antifosfolípido, síndrome de Sjögren y LES)4,24,28,29. La participación de las MP en la patogenía de estas enfermedades se ha relacionado con su potencial proinflamatorio y protrombótico, este último dado por la expresión en su superficie de factor tisular, multímeros de von Willebrand y de aminofosfolípidos que ofrecen sitios de unión a los factores de la coagulación ixa, viii, va y iia, favoreciendo el ensamblaje del complejo protrombinasa19. Los mecanismos por los cuales las MP se incrementan y escapan a su regulación, perdiendo su papel fisiológico convirtiéndose en agentes de daño, pueden ser diferentes para cada enfermedad.
Sustrato antigénico en lupus eritematoso sistémicoEl LES se caracteriza por la producción de anticuerpos dirigidos contra autoantígenos nucleares y citoplasmáticos, principalmente: ADN de doble cadena, nucleosoma, histonas y ARN30–33. Las MP pueden contener estas moléculas, constituyendo una fuente de autoantígenos en este grupo de pacientes.
Algunos estudios han observado que la concentración y composición de las MP en pacientes con LES es diferente. Los trabajos iniciales reportaban incremento en el número de MP en pacientes con LES3,34–37, sin embargo, estudios más recientes han demostrado disminución en el recuento de MP derivadas de plaquetas y leucocitos en pacientes con LES, cuando hay concentraciones elevadas de IgG unida a MP, e incremento de las MP derivadas de células endoteliales38–40. Se ha encontrado aumento en la concentración de C1q, IgG e IgM unidas a MP, en pacientes con LES respecto a controles sanos39.
La presencia de IgG en la superficie de la MP, se ha asociado con aumento en antiADN, anticuerpos contra antígenos extractables del núcleo y anticuerpos antiC1q, así mismo con consumo del complemento39.
La alteración en la depuración y el aumento en la actividad celular y la apoptosis pueden ser los mecanismos responsables de los cambios en la concentración y composición de las MP en LES41–44.
Dado la posibilidad de contener autoantígenos en su interior o en la superficie, Pisetsky y Lipsky han propuesto a estas vesículas derivadas de membrana plasmática como probables mediadores de interacción entre ADN y ARN con componentes del sistema inmune, principalmente CDp y linfocitos B autorreactivos2. Las MP pudieran comportarse como adyuvantes potenciando la capacidad inmunogénica del ADN (inactivo en forma libre) y el ARN que contienen, al facilitar la interacción con receptores de linfocitos B (BCR) y con receptores de reconocimiento de patrones (PRR) ubicados intracelularmente2,45.
En el modelo planteado por Pisetsky y Lipsky, las MP participan como sustrato antigénico y adyuvantes tanto en activación celular como en tolerancia central. Respecto a la participación en tolerancia central se propone que en médula ósea el BCR de linfocitos B inmaduros reconoce moléculas de ADN localizadas en la superficie de las MP con mayor avidez, lo cual promueve la deleción o selección negativa de estos linfocitos2,46,47. En la periferia, el modelo postula que en pacientes con LES en quienes confluyen diferentes alteraciones en los puntos de control de la regulación de la tolerancia, favoreciendo la presencia de linfocitos autoreactivos41, estos pueden reconocer el ADN expresado en la superficie de las MP. El linfocito B que ha unido la MP por medio de su BCR la endocita y una vez en su interior el ADN y el ARN contenidos en la microvesícula interactúa con receptores endosomales tipo Toll 9 y 7 (TLR9 y TLR7)48–51, y con receptores de reconocimiento de patrones no Toll. La activación de los TLR genera las señales intracelulares necesarias para la activación y diferenciación de linfocitos B, constituyendo un mecanismo de producción de autoanticuerpos independiente de linfocitos T49,50,52.
Por otra parte, las CDp que expresan constitutivamente TLR 7 y 9, pueden reconocer MP a través de CD32 y endocitarlas, facilitando el contacto de su contenido con estos receptores53. La activación de TLR en estas CDp conduce a su maduración y a la producción de IL6, quimioquinas e interferon alfa (INF-α) que a su vez aumenta la expresión de TLR7 en CDp e induce su maduración convirtiéndolas en presentadoras de antígenos más eficientes debido al incremento en los niveles de moléculas coestimuladoras en su superficie y favoreciendo la producción de factores de supervivencia para linfocitos B54.
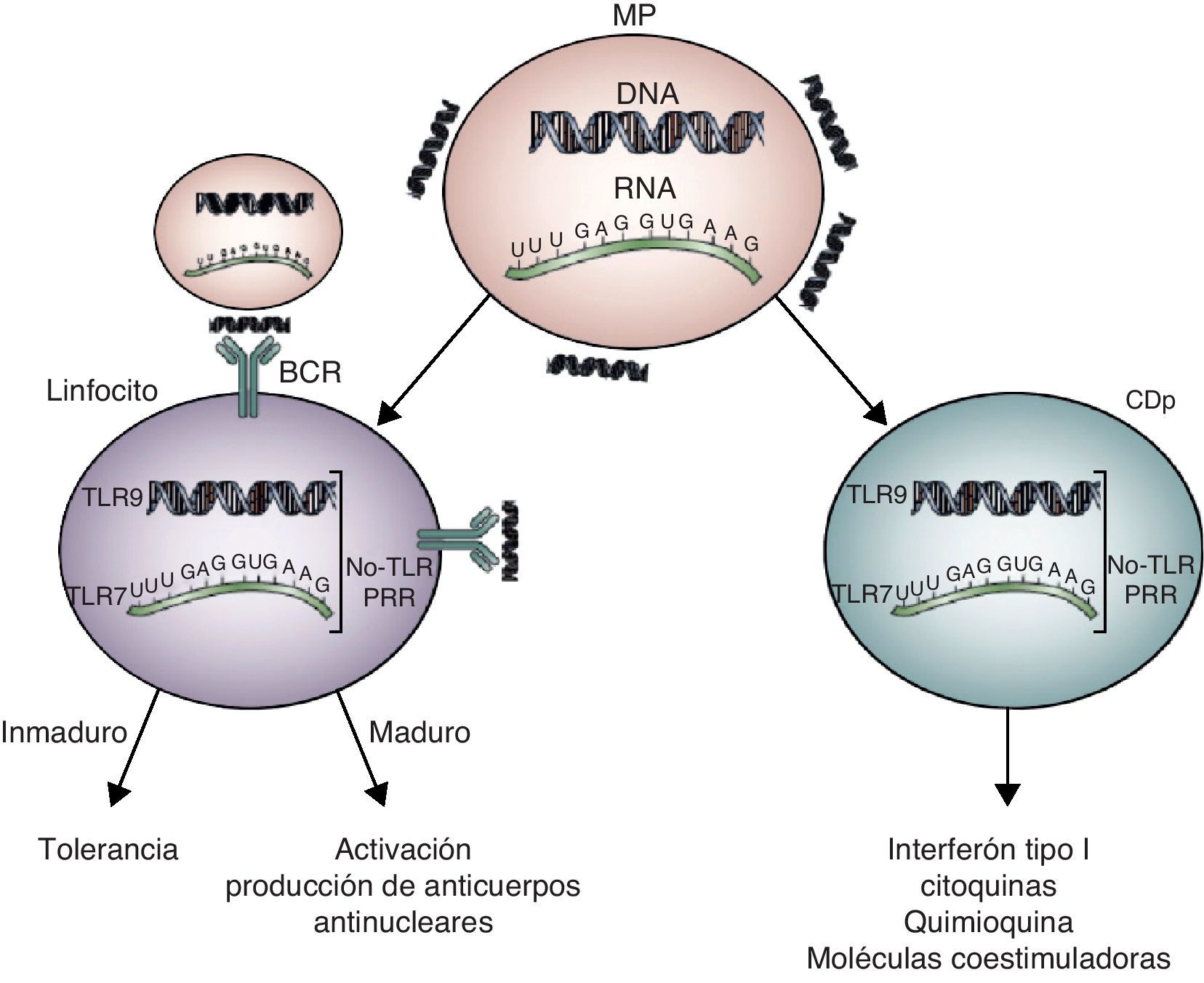
Este nuevo concepto, basado en el contenido de ácidos nucleicos en las MP, las presenta como una rica fuente de antoantígenos y mediadores de interacción con linfocitos B y con células dendríticas plasmacitoides, en pacientes con LES (fig. 2).
Probable interacción de MP con linfocito B y célula dendrítica plasmacitoide (CDp), en LES. Las MP pudieran comportarse como adyuvantes potenciando la capacidad inmunogénica del ADN y el ARN que contienen, al facilitar la interacción con receptores de linfocitos B (BCR) y con receptores de reconocimiento de patrones (PRR) ubicados intracelularmente. El BCR de linfocitos B inmaduros reconoce moléculas de ADN localizadas en la superficie de las MP con mayor avidez, lo cual promueve la deleción de estos linfocitos. Las CDp que expresan constitutivamente TLR 7 y 9 pueden reconocer MP a través de CD32 y endocitarlas, facilitando el contacto de su contenido con estos receptores. La activación de TLR en estas CDp conduce a su maduración y a la producción de IL6, quimioquinas e interferon alfa (INF-α) que a su vez aumenta la expresión de TLR7 en CDp. Modificado de Pisetsky DS, Lipsky PE2.
Las MP son estructuras pleiotrópicas que interactúan con diferentes tipos de células. Pueden participar en la patogenia de diversas enfermedades debido a sus propiedades proinflamatorias y protrombóticas.
Estudios recientes han encontrado diferencias en la composición y concentración de MP en pacientes con LES, resaltando el aumento en la concentración de IgG en la superficie de las MP, y su correlación con antiADN y otros autoanticuerpos importantes en la patógenesis del lupus y sus manifestaciones clínicas.
La presencia de ácidos nucleicos en la superficie y el interior de las MP las convierte en una rica fuente de autoantígenos; en el contexto del LES, el cual se caracteriza por la formación de autoanticuerpos dirigidos contra estos antígenos, las MP desempeñarían un papel fundamental como sustrato antigénico.
La propuesta de que las MP facilitan la interacción con receptores tipo Toll en linfocitos B tanto a nivel central como periférico, y en células dendríticas plasmacitoides, introduce a las MP en un escenario nuevo, adicional al conocido de proinflamación y protrombosis.
Es necesario realizar más estudios que respalden el papel de las MP en la patogénesis del LES, y ayuden a establecer su utilidad como biomarcadores.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.