La ecografía abdominal continúa siendo la primera exploración a realizar en los pacientes con sospecha de enfermedad pancreática. Pese a los recientes avances tecnológicos en las pruebas de imagen, la ecografía no ha sido desplazada como primer escalón diagnóstico debido a su inocuidad, accesibilidad y bajo coste.
Se trata de una técnica fundamental en el estudio de los procesos inflamatorios, ya que no solo valora las alteraciones del parénquima pancreático, sino que orienta la etiología (biliar o alcohólica), es fundamental en la detección y el seguimiento de las posibles complicaciones y sirve como guía en las punciones tanto diagnósticas como terapéuticas.
Es también la primera técnica a utilizar en el estudio de los tumores pancreáticos, con una sensibilidad en la detección de los mismos en torno al 70%, y una especificidad del 90%.
Despite the recent technological advances in imaging, abdominal ultrasonography continues to be the first diagnostic test indicated in patients with a suspicion of pancreatic disease, due to its safety, accessibility and low cost.
It is an essential technique in the study of inflammatory processes, since it not only assesses changes in pancreatic parenchyma, but also gives an indication of the origin (bile or alcoholic). It is also essential in the detection and tracing of possible complications as well as being used as a guide in diagnostic and therapeutic punctures.
It is also the first technique used in the study of pancreatic tumors, detecting them with a sensitivity of around 70% and a specificity of 90%.
Antes de los años 70, los estudios por imagen del páncreas se limitaban a mostrar las estructuras adyacentes o su vascularización mediante las angiografías. La llegada de la ecografía convirtió la visualización del páncreas en una realidad.
Hoy en día la ecografía abdominal es la primera exploración que debemos realizar en los pacientes con sospecha de enfermedad pancreática.
Los principales objetivos del ecografista son distinguir un páncreas normal de otro anormal y diferenciar las pancreatitis de las neoplasias malignas1.
AnatomíaEl páncreas es una estructura retroperitoneal no encapsulada que se localiza en el espacio pararrenal anterior entre el marco duodenal y el hilio esplénico, a la altura de la primera y la segunda vértebras lumbares. Tiene forma de coma, con un diámetro longitudinal que oscila entre 12,5 y 20cm, y se divide en cabeza, proceso uncinado, cuello o istmo, cuerpo y cola. Los diámetros anteroposteriores presentan gran disparidad entre los distintos valores publicados, variando entre 2,5 y 4cm, por lo que su medición es de escasa utilidad en la práctica clínica. El proceso uncinado es una extensión medial de la cabeza, localizada posterior a los vasos mesentéricos superiores2.
Los vasos mesentéricos superiores discurren por detrás del cuello pancreático, separando la cabeza del cuerpo. No hay un límite anatómico entre el cuerpo y la cola.
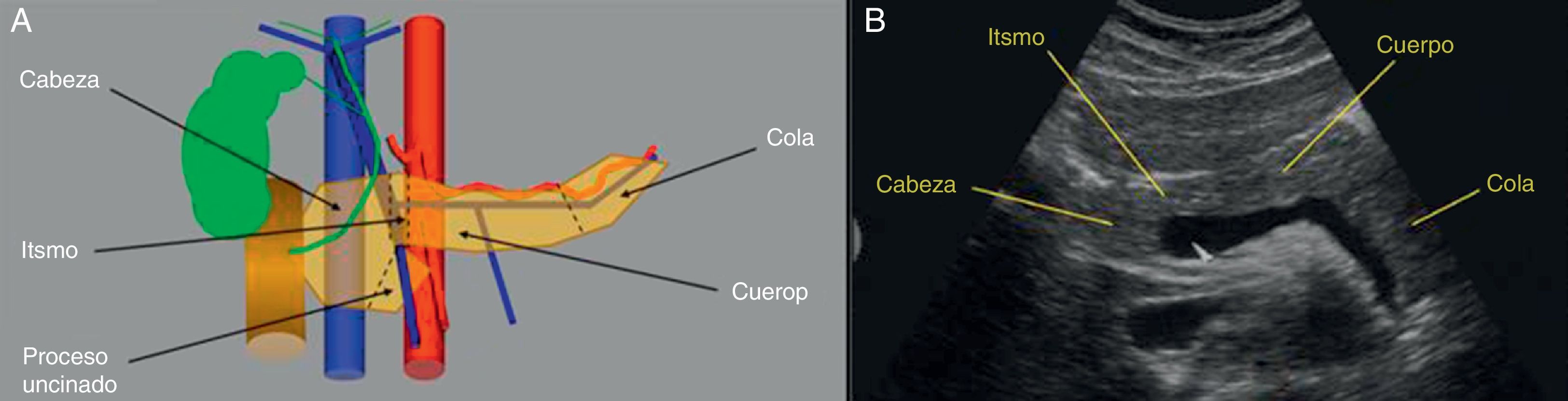
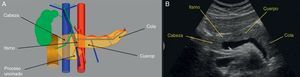
Relaciones: en su cara anterior, con la cavidad posterior de los epiplones, la cara posterior del estómago, la cara inferior del lóbulo hepático izquierdo y el colon transverso. Por su cara superior discurren las arterias hepática y esplénica. Sus relaciones posteriores son con la vena esplénica en sentido transversal, y con la cava, aorta, y vena y arteria mesentéricas en sentido longitudinal. Lateralmente la cabeza se encuentra en relación con el duodeno, el colédoco, la vesícula, el lóbulo caudado y el hilio hepático. La cola se relaciona con el riñón izquierdo, el bazo y el colon descendente3 (fig. 1).
A. Anatomía pancreática. Relaciones anatómicas. Cabeza, proceso uncinado, cuello o istmo, cuerpo y cola pancreáticos. En rojo, la arteria aorta y la arteria esplénica. En azul, la vena cava y la vena esplénica, así como las venas mesentéricas inferior (posterior al cuerpo pancreático) y superior (posterior al istmo). En marrón, el duodeno. En verde, la vesícula y la vía biliar. B. Imagen ecográfica de un corte transversal a nivel de epigastrio, mostrando la típica imagen ecográfica del páncreas con en su eje longitudinal.
La ecoestructura es homogénea o discretamente heterogénea. La ecogenicidad es igual o ligeramente mayor que la hepática, siendo frecuente encontrar páncreas hiperecogénicos en pacientes obesos, diabéticos y en ancianos, en relación con infiltración grasa4–6.
Aspectos técnicosHay 2 factores fundamentales que impiden una buena visualización del páncreas: la grasa y la interposición de gas gastrointestinal. La visualización completa del páncreas se consigue aproximadamente en un 75% de las ecografías.
El conducto pancreático principal se visualiza aproximadamente en la mitad de los casos como una delgada línea sonolucente, de unos 2mm, paralela al eje mayor de la glándula, limitada por 2 líneas hiperecogénicas que corresponden a sus paredes.
No es estrictamente necesario el ayuno para la correcta visualización del páncreas, si bien este puede ayudar a disminuir la distensión aérea del tracto gastrointestinal, y se recomienda.
La mayor información de la víscera se obtiene mediante cortes ecográficos transversales a nivel subxifoideo7,8.
Procesos inflamatoriosPancreatitis agudaEnfermedad frecuente con etiología múltiple, si bien en el 60-85% de los casos se debe a litiasis biliar o a alcoholismo crónico.
La ecografía abdominal constituye la primera técnica de imagen en la evaluación inicial de una pancreatitis aguda, debiendo realizarse en las primeras 24h. Tiene importancia en el diagnóstico de la pancreatitis aguda, pero sobre todo adquiere relevancia en el establecimiento de su etiología, siendo más sensible que la tomografía axial computarizada o la resonancia magnética en el diagnóstico de litiasis biliar9,10. Además, puede detectar signos que evidencien la etiología alcohólica, como son la infiltración grasa hepática o las calcificaciones pancreáticas, muy indicativas de pancreatitis crónica alcohólica subyacente11–13.
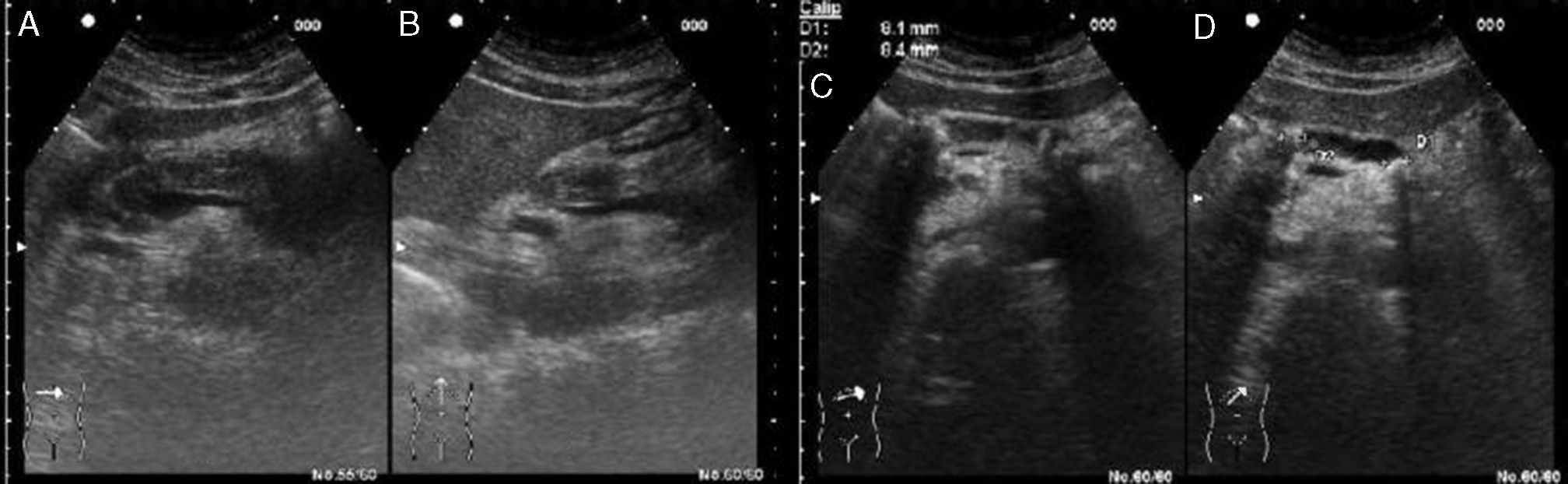
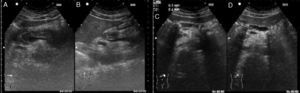
La pancreatitis aguda se presenta, la mayoría de las veces, como un aumento difuso y generalizado del tamaño del páncreas, junto con límites y contornos más imprecisos y disminución de la ecogenicidad del órgano (fig. 2A).
A y B. Pancreatitis aguda: corte transversal (A) y corte longitudinal a nivel de epigastrio, detectándose un páncreas hipoecogénico, aumentado de tamaño (B). C y D. Pancreatitis crónica: corte transversal (C) y corte longitudinal a nivel de epigastrio, donde se detecta un páncreas de ecogenicidad heterogénea, bordes mal definidos e irregulares, y múltiples calcificaciones intraductales en un conducto de Wirsung dilatado (D).
En la forma edematosa el parénquima es uniforme y homogéneo, aunque hipoecogénico con respecto al parénquima normal. En las formas más graves se pueden observar áreas intraparenquimatosas de carácter quístico, indicativas de la existencia de necrosis o hemorragia14.
Los resultados técnicos de la exploración mejoran 48h después del episodio agudo, al resolverse el íleo paralítico.
La exploración ecográfica seriada desempeña un papel importante para monitorizar la evolución: resolución, formación de seudoquistes o pancreatitis crónica.
Los hallazgos ecográficos en la pancreatitis aguda pueden clasificarse por su distribución (focal o difusa) y por la severidad (leve, moderada y grave).
La pancreatitis focal, que consiste en un aumento de tamaño focal del páncreas, constituye un problema para el ecografista. Se localiza generalmente en la cabeza, y es más frecuente en pacientes alcohólicos y con historia previa de pancreatitis o dolor, lo que demuestra que las pancreatitis focales tienden a ocurrir en el contexto de una pancreatitis crónica.
En una pancreatitis difusa el páncreas es hipoecogénico respecto al hígado normal y está aumentado de tamaño. A medida que la inflamación es más severa son más evidentes la disminución de la ecogenicidad y el aumento de tamaño debidos al mayor contenido líquido en el intersticio.
La ecografía no permite distinguir, como lo hace la tomografía axial computarizada, entre pancreatitis necróticas y no necróticas15,16.
Las manifestaciones extrapancreáticas en los pacientes con pancreatitis aguda son importantes y hay que buscarlas, dado que las alteraciones intrapancreáticas tienden a ser subjetivas. Consisten en colecciones líquidas y edema a lo largo de los diferentes planos de partes blandas, y, en general, se ven en los casos severos. Los cambios en las partes blandas peripancreáticas se ven como bandas hipoecogénicas adyacentes al páncreas o rodeando el sistema venoso portal.
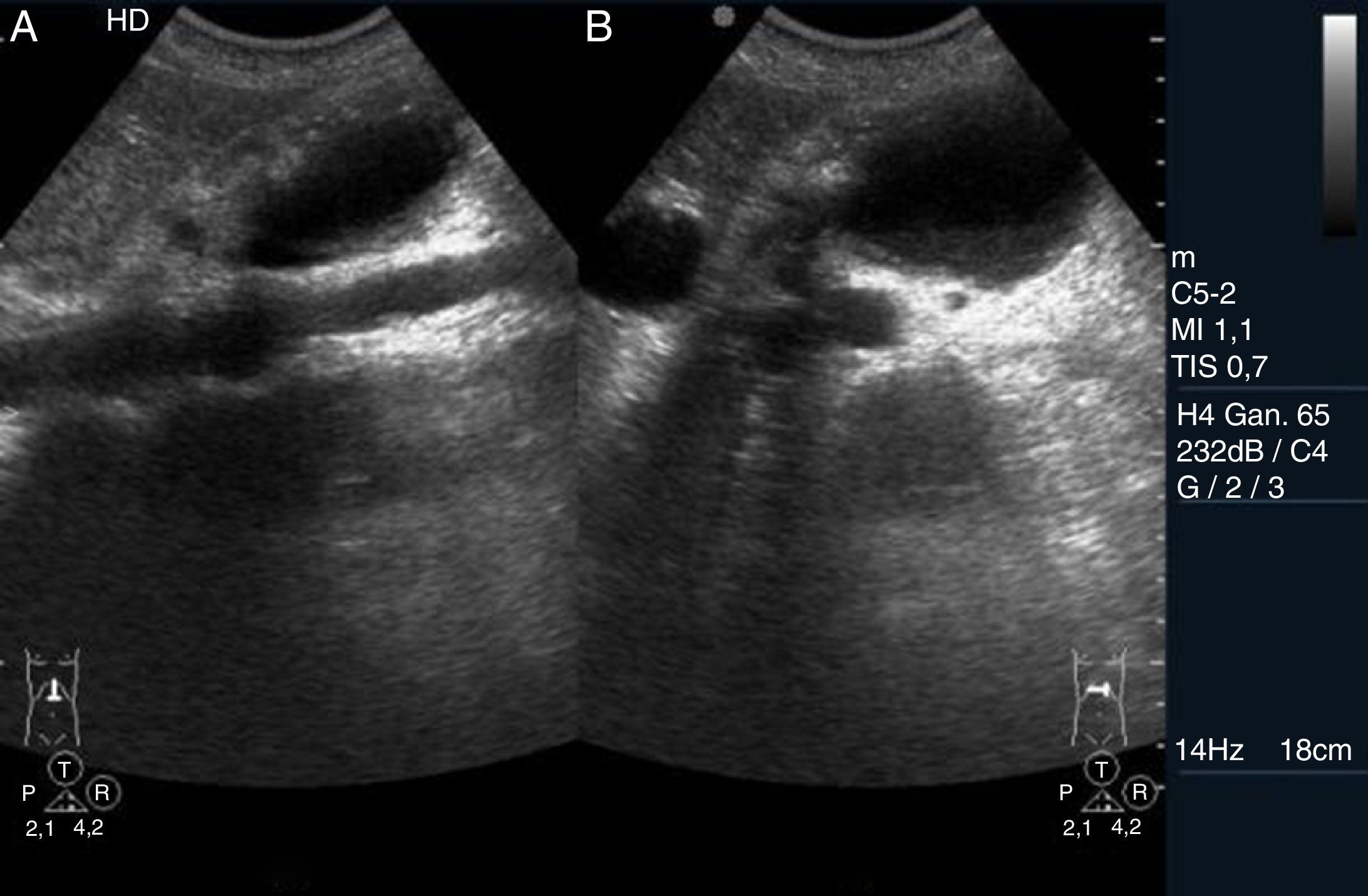
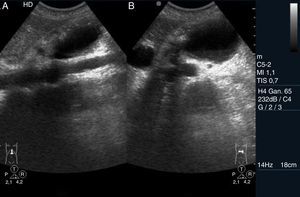
Las colecciones líquidas extrapancreáticas ocurren dentro de las 4 semanas desde el inicio de la inflamación aguda. Se emplea el término «seudoquiste» cuando se desarrolla una colección líquida con la pared bien definida, que permanece en exploraciones seriadas durante un intervalo de al menos 4 semanas desde el inicio de la infamación aguda. Se necesitan aproximadamente de 4 a 6 semanas para que una colección líquida se circunscriba con una pared de colágeno y tejido de granulación vascular. Los seudoquistes ocurren en un 10-20% de los pacientes con pancreatitis aguda y en un 25-40% de los pacientes con pancreatitis crónica, y es la lesión quística más frecuente del páncreas. En la fase inicial pueden existir ecos internos y contornos peor definidos, al no estar aún organizado el quiste. Posteriormente la forma es más o menos ovoidea, con contenido anecogénico y con una pared mejor definida17,18 (fig. 3).
Los seudoquistes que se forman durante una pancreatitis necrosante aguda tienen una alta tendencia a la resolución espontánea, mientras que los resultantes de una pancreatitis crónica no suelen resolverse por sí mismos, sobre todo cuando hay calcificaciones en su pared. En general, los seudoquistes que persisten más de 6 semanas requieren descompresión, y el riesgo de complicaciones aumenta significativamente.
Los abscesos pancreáticos se desarrollan por licuefacción y sobreinfección de la necrosis pancreática, o bien como consecuencia de la infección de un seudoquiste. Son difíciles de diferenciar de un seudoquiste, siendo necesaria la punción para el diagnóstico.
Otros hallazgos extrapancreáticos incluyen: ascitis, engrosamiento del tracto gastrointestinal adyacente (estómago, duodeno y colon) y engrosamiento de la pared de la vesícula, con o sin líquido perivesicular.
En cuanto a las complicaciones vasculares, la más frecuente es la trombosis de las venas peripancreáticas como resultado de la compresión y el estasis sanguíneo. La vena esplénica se afecta con mayor frecuencia, pero también pueden afectarse las venas mesentérica superior y porta. También pueden formarse seudoaneurismas como resultado de la erosión de arterias adyacentes por las enzimas pancreáticas proteolíticas. La arteria esplénica se afecta con mayor frecuencia, pero cualquier rama del tronco celiaco puede ser afectada.
Pancreatitis crónicaLa pancreatitis crónica es una destrucción progresiva e irreversible del páncreas por episodios repetidos de pancreatitis leve o subclínica. La causa principal es el alcoholismo crónico, que constituye un 70-90% de todas las pancreatitis crónicas.
La ecografía abdominal tiene un papel relevante en el diagnóstico, siendo su sensibilidad de entre el 60 y el 70%, y su especificidad, de un 80-90%.
Los contornos del páncreas suelen ser irregulares, la ecogenicidad suele estar aumentada, y la ecoestructura es heterogénea. Los hallazgos más específicos y de elevado valor diagnóstico son las calcificaciones intrapancreáticas y la dilatación del conducto de Wirsung, con un diámetro mayor de 2-3mm y una morfología frecuentemente tortuosa. La presencia de calcificaciones es patognomónica de pancreatitis crónica y pueden ser parenquimatosas o localizarse dentro del conducto de Wirsung (intraductales), siendo estas últimas las más frecuentes. Se detectan en el 57% de las pancreatitis crónicas19 (fig. 2B).
Una masa o aumento de tamaño focal se encuentra en aproximadamente un 40% de los pacientes. La presencia de calcificaciones ayuda a distinguir estos aumentos de tamaño focales de neoplasias20.
NeoplasiasCarcinoma pancreáticoEl carcinoma pancreático es un adenocarcinoma originado en el epitelio ductal, y constituye más del 90% de todos los tumores pancreáticos. Mucho más infrecuentes son los carcinomas acinares, los tumores neuroendocrinos y los cistoadenocarcinomas, que constituyen entre el 2 y el 5%.
La localización más frecuente del adenocarcinoma es la cabeza, donde asientan aproximadamente un 70%; el 15-20% lo hacen en el cuerpo, y un 5-10% en la cola. En un 20% el tumor está distribuido de forma difusa por la glándula.
Es más probable que los adenocarcinomas del cuerpo y de la cola se presenten con metástasis, posiblemente como resultado de su diagnóstico más tardío. Son características las grandes metástasis hepáticas. Las metástasis ocurren con más frecuencia en los ganglios regionales, el hígado, los pulmones, el peritoneo y las suprarrenales.
El hallazgo ecográfico más frecuente es una masa hipoecogénica, homogénea o heterogénea, mal definida. En el momento del diagnóstico ecográfico los carcinomas pancreáticos suelen medir más de 2cm21,22.
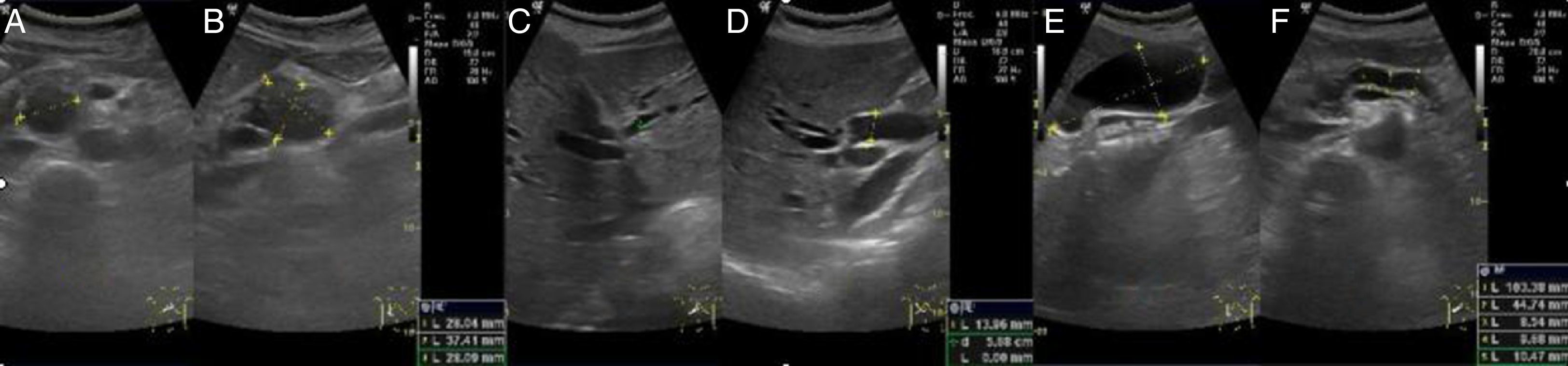
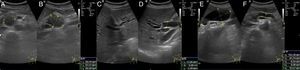
Son signos indirectos la dilatación del conducto pancreático proximal a la masa y la dilatación de la vía biliar, si bien esta última es frecuente solo en los tumores de la cabeza pancreática (fig. 4).
Adenocarcinoma en la cabeza pancreática con distensión de la vesícula biliar y dilatación de la vía biliar intrahepática y extrahepática, así como del conducto de Wirsung. A. Corte transversal. B. Corte longitudinal a nivel de epigastrio, donde se detecta una lesión sólida, bien delimitada, hipoecogénica, de unos 3cm de diámetro máximo, localizada en la cabeza pancreática. C. Corte oblicuo a nivel de hipocondrio derecho, donde se detectan en la unión de los lóbulos hepáticos izquierdo y derecho imágenes tubulares anecogénicas en «brazos de pulpo», indicativas de dilatación de la vía biliar intrahepática. D. Corte oblicuo a nivel de hipocondrio derecho donde se detecta la típica imagen en «cañón de escopeta» a nivel del hilio hepático, con un colédoco aumentado de calibre midiendo unos 14mm. E. Corte longitudinal en hipocondrio derecho en la línea medioclavicular, donde se detecta una vesícula biliar distendida con unos diámetros de 103×45mm en los ejes longitudinal y anteroposterior. F. Corte transversal a nivel de epigastrio, que muestra un conducto de Wirsung dilatado, con un calibre de entre 8 y 10mm.
El principal diagnóstico diferencial del carcinoma pancreático es con la pancreatitis focal o con una masa focal asociada a la pancreatitis crónica23.
Los adenocarcinomas ampulares deben diferenciarse de los adenocarcinomas pancreáticos porque los primeros tienen un mejor pronóstico. La mayoría de los pacientes se presentan con dilatación tanto del colédoco como del conducto pancreático24.
Neoplasias quísticasRepresentan el 10-15% de todos los quistes pancreáticos y un 1% de los carcinomas de páncreas. Hay 2 categorías principales de neoplasias quísticas: el tipo microquístico o seroso y el macroquístico o mucinoso.
El cistoadenoma microquístico o seroso es una neoplasia siempre benigna y no requiere cirugía. Suele ocurrir en pacientes de edad avanzada. Ecográficamente son tumores relativamente bien definidos, con lobulaciones externas. Dependiendo del tamaño de los quistes individuales, el aspecto ecográfico varía desde una masa sólida bien definida y ligeramente ecogénica, pasando por una masa de aspecto parcialmente sólido con áreas quísticas, más frecuente periféricamente, hasta una masa multiquística. Los quistes individuales tienen un tamaño que varía de 1 a 20mm. En un 20% de los casos hay una cicatriz definida con la ecografía como una zona central estrellada ecogénica.
El cistoadenoma y cistoadenocarcinoma macroquístico son masas quísticas malignas o potencialmente malignas, si bien tienen un pronóstico mejor que los adenocarcinomas. Suelen manifestarse ecográficamente como lesiones quísticas uniloculares o multiloculares bien circunscritas, de superficie lisa y tamaño variable, normalmente mayores de 2cm e inferiores a 6 en número. La presencia de un componente sólido en una masa predominantemente quística es diagnóstica de esta entidad. Los quistes con múltiples tabiques gruesos, así como las masas multiquísticas con quistes dominantes mayores de 2cm también son muy indicativos de tumor macroquístico25–27.
Tumores de células de los islotesLos tumores de células B (insulinomas) son los tumores de células de los islotes más frecuentes. Se localizan con más asiduidad en el cuerpo y la cola del páncreas. Suelen estar bien encapsulados. El 90% son menores de 2cm de diámetro en el momento del diagnóstico.
Los tumores de células G (gastrinomas) son los segundos tumores de células de los islotes más frecuentes, tras el insulinoma. La mayoría se localizan en el páncreas, y un 10-15% en el duodeno. De los que se localizan en el páncreas, solo un 25% son únicos.
La exploración ecográfica para detectar tumores de los islotes suele ser difícil y su identificación varía de un 25 a un 60%. Los tumores pequeños suelen ser hipoecogénicos y bien definidos, sin calcificaciones ni necrosis. Los tumores más grandes pueden ser ecogénicos e irregulares, y pueden tener calcificaciones o zonas de necrosis. Su diferenciación del adenocarcinoma con ecografía convencional es prácticamente imposible28–30.
Desde el Grupo de Trabajo de Ecografía de SEMERGEN continuamos impulsando la introducción de la ecografía en Atención Primaria dada la inocuidad, accesibilidad y bajo coste31, y creemos que la utilización de la misma permitirá, desde la propia consulta de Atención Primaria, el diagnóstico y el seguimiento de la enfermedad pancreática, así como su derivación orientada si fuera preciso.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.