El objetivo es evaluar los resultados del protocolo en 3 dispositivos móviles de cuidados críticos y urgencias rurales, así como los retrasos y estrategias de reperfusión empleadas en el síndrome coronario agudo con elevación del segmento ST.
Material y métodosEstudio de cohortes retrospectivo (n=52) con control histórico (n=20) de los síndromes coronarios agudos con elevación del segmento ST atendidos. Se revisaron los informes de los dispositivos móviles de cuidados críticos y urgencias y de alta hospitalaria, la historia informatizada y el registro ARIAM, recogiendo características epidemiológicas y clínicas, datos de la asistencia, reperfusión, intervalos temporales y mortalidad.
ResultadosLas características de ambos grupos no difieren significativamente. Aumentó la concordancia diagnóstica de los dispositivos móviles de cuidados críticos y urgencias-hospital (85,3 versus 76,9%), sin significación estadística. Hubo un uso similar de nitroglicerina, mórficos y AAS; aumento significativo (p<0,0001) de clopidogrel/prasugrel (55 versus 90,4%) y enoxaparina/fondaparinux (35 versus 76,9%), así como de fibrinólisis prehospitalaria (5 versus 30,8%, p<0,03), que se aplica en<2h al 71,4%, con un tiempo puerta-aguja de 40min, mientras la fibrinólisis hospitalaria y la angioplastia primaria se realizan a partir de la tercera hora (p<0,01). Los retrasos se asocian a la demora del paciente (p<0,02). Aumenta más la estrategia farmacoinvasiva (62,5 versus 84,6%) que la angioplastia primaria (15 versus 17,3%), disminuyendo la fibrinólisis hospitalaria (35 versus 19,2%), todas ellas sin significación estadística. Las complicaciones son similares, disminuyendo la mortalidad al año (p<0,67).
ConclusionesEl protocolo es efectivo, seguro, fiable, reduce las demoras y mejora la atención prehospitalaria. La estrategia farmacoinvasiva es una opción válida.
The aim is to evaluate the outcomes obtained from the implementation of a pre-hospital thrombolysis protocol in 3 rural emergency care teams, as well as delays and strategies of reperfusion applied in the treatment of the ST-segment elevation myocardial infarction.
Material and methodsRetrospective cohort study (n=52) with historical control (n=20) of the patients assisted for ST-segment elevation myocardial infarction. Medical emergency care teams, hospital, computerized medical history and ARIAM register reports were revised, obtaining epidemiological and clinical features, off-hospital management, reperfusion, time intervals and mortality.
ResultsThe baseline features in both groups were not significantly different. There was a non-significant improvement of emergency care teams-hospital diagnostic concordance (85.3 versus 76.9%). We found a similar use of nitroglycerin, morphine and aspirin; significant increase (P<0.0001) of clopidogrel/prasugrel (55 versus 90.4%) and enoxaparin/fondaparinux (35 versus 76.9%), as well as pre-hospital thrombolysis (5 versus 30,8%, P<0.03), that was applied within the first 2h to 71.4%, with a median door-needle of 40min, whereas in-hospital thrombolysis and primary angioplasty were performed after 3h from the symptoms onset (P<0.01). Delays are associated with the patient's own lateness (P<0.02). Pharmaco-invasive strategy increases (62.5 versus 84.6%) more than primary angioplasty (15 versus 17.3%), reducing in-hospital thrombolysis (35 versus 19.2%), all of them non-significant. Complications are similar and one-year mortality is reduced (P<0.67).
ConclusionsThe protocol is effective, safe, and reliable. It reduces delays and improves pre-hospital attention. The pharmaco-invasive strategy is a valid option.
La enfermedad coronaria es la causa individual más frecuente de muerte en el mundo. Diversos estudios señalan un descenso en la mortalidad, en paralelo con el aumento de las terapias de reperfusión, la intervención coronaria percutánea primaria (ICPp), el tratamiento antitrombótico moderno y la prevención secundaria1.
La reperfusión precoz es la clave en el manejo del síndrome coronario agudo con elevación del segmento ST (SCACEST). Desde el inicio de los síntomas, las demoras hasta la reperfusión dependen tanto del propio paciente como del sistema sanitario, siendo considerablemente mayores en zonas rurales2.
El Plan integral de atención a las cardiopatías de Andalucía 2005-20093 establece la reperfusión precoz entre sus líneas de acción, recomendando la fibrinólisis prehospitalaria (FxPH) en<30min desde el inicio de la asistencia, sobre todo en zonas alejadas del hospital, o bien ICPp cuando esté disponible y pueda realizarse en 90-120min.
La ICPp es el tratamiento de elección2,4–9. Sin embargo, existen problemas de logística que la hacen difícil de aplicar4, como la falta de centros con capacidad permanente para realizarla, por lo que sus resultados en los ensayos clínicos podrían no ser extrapolables al mundo real2. De hecho, las guías se basan en estudios que la comparan con la fibrinólisis sola10, y la mayoría con fibrinólisis hospitalaria (FxH) (salvo el ensayo CAPTIM)11, sobre la que la FxPH ha demostrado una reducción de mortalidad1,9.
La FxPH es una técnica de sumo interés y eficiencia12 que reduce más la mortalidad en las primeras 2h de evolución1, incluso comparada con la ICPp2,13. Además, es una técnica segura14.
La necesidad de una red con buen funcionamiento para la ICPp limita su aplicación a una minoría de pacientes5,15, por lo que se han investigado alternativas como la ICP facilitada, que se descartó ante la ausencia de beneficio clínico2,4–6,10,16,17. La ICP de rescate (ICPr) tras una fibrinólisis fallida obtiene mejores resultados que repetir la fibrinólisis o un tratamiento conservador1,18. La ICP diferida (ICPd), en SCACEST>12h de evolución, podría beneficiar en la mortalidad a largo plazo, aunque aún no hay suficiente nivel de evidencia4.
Numerosos estudios han abordado la «estrategia farmacoinvasiva», que consiste en la realización sistemática de una coronariografía tras la fibrinólisis seguida de ICP si es preciso (ICPsis), además de una ICPr cuando la fibrinólisis falla1. Esta estrategia puede reducir la diferencia de supervivencia entre la fibrinólisis y la ICPp15,19–21, por lo que constituye una estrategia de reperfusión razonable y válida5,22, ya que podría tener beneficios similares o superiores2,10,11,15,20,22.
Andalucía cuenta con 2 recursos extrahospitalarios para la atención al SCACEST3. El primero son los equipos móviles (EM) y helicópteros de la empresa pública de emergencias sanitarias (061), con una amplia experiencia en FxPH, que cubren el 57% de la población de la provincia de Córdoba. El segundo lo forman los EM de cuidados críticos y urgencias (DCCU), en los que el desarrollo de la FxPH es más heterogéneo. Varios estudios se ocupan de la FxPH realizada por el 06114,23–25, y de la atención en hospitales andaluces26, pero no existen publicaciones referentes a los DCCU.
Se elaboró un protocolo entre el Servicio de Urgencias del Hospital Universitario Reina Sofía, la Unidad de Cuidados Intensivos (UCI) y los EM DCCU del Distrito Sanitario Guadalquivir, que incluye un periodo de formación, rotación por la UCI e implantación del protocolo de FxPH, iniciado en diciembre de 2011. Transcurridos 2 años, nos planteamos evaluar los resultados obtenidos en los pacientes atendidos por SCACEST, así como describir los retrasos y las estrategias de reperfusión empleadas en aquellos que residen en zonas alejadas de su hospital de referencia, en el que el laboratorio de hemodinámica está disponible de 8:00 a 15:00h.
Material y métodosEl Distrito Sanitario Guadalquivir (Córdoba) tiene 3 EM DCCU, formados por médico/a, enfermero/a y técnico, responsables de la asistencia urgente de 8:00 a 20:00h. Las activaciones de los EM procedentes de los usuarios o de médicos de familia que atienden puntos de atención continuada se realizan a través del Centro Coordinador de Urgencias y Emergencias. El hospital de referencia es el Hospital Universitario Reina Sofía.
El EM de Montoro da cobertura a una población de 46.633 habitantes de la Zona Básica de Salud de Montoro (37-55km hasta el hospital) y la de Bujalance (29-68km); el EM de La Carlota, a 44.181 habitantes de la Zona Básica de Salud de La Carlota (21-35km), Fuente Palmera (53-68km) y parte de Posadas (17-32km), y el EM de Palma del Río, a 29.795 habitantes de la Zona Básica de Salud de Palma del Río y parte de Posadas (50-58km).
Se diseñó un estudio de cohortes retrospectivo con control histórico. La cohorte analizada la forman los SCACEST atendidos por los DCCU desde el 20 de diciembre de 2011 hasta el 31 de diciembre de 2013. El grupo de controles históricos lo constituyen los SCACEST atendidos entre junio de 2009 y junio de 2010.
La información se obtuvo de la revisión de las historias clínicas del DCCU, las historias informatizadas de DCCU y el Servicio de Urgencias, informes de Cardiología y UCI, así como los tiempos registrados en el programa ARIAM.
Se incluyeron los pacientes con diagnóstico de: SCACEST, infarto agudo de miocardio con elevación del segmento ST (IAMCEST), infarto agudo de miocardio (IAM), síndrome coronario agudo (SCA), o sospecha de ellos, en los que figurase en la descripción del electrocardiograma (ECG) «elevación del segmento ST», aunque no cumpliera los criterios de otros estudios14. Se evaluó la concordancia con el diagnóstico hospitalario, excluyendo del análisis final los errores diagnósticos.
El protocolo de FxPH establecía la indicación ante: cuadro clínico compatible con SCA>30min de evolución, ECG con ascenso persistente del segmento ST y clasificación ARIAM I (dolor típico que no cede con nitroglicerina [NTG], ST elevado≥2mm en 2 o más derivaciones contiguas,<75 años y<6h de evolución, sin contraindicaciones para fibrinólisis, tensión arterial sistólica >100mmHg o diastólica<100mmHg, frecuencia cardíaca>50lpm, sin bloqueo auriculoventricular ni taqui o bradiarritmias).
El médico responsable contacta telefónicamente con el intensivista de guardia, eligiendo conjuntamente la estrategia de reperfusión más adecuada. La ICPp está indicada si: horario de 8 a 15h, evolución>3h, tiempo puerta-balón<90min, Killip≥3, SCACEST dudoso, fibrinólisis contraindicada.
Premedicación: NTG/mórficos+AAS+clopidogrel/prasugrel. ECG seriados. Administración de fondaparinux 2,5mg iv (enoxaparina si no disponible)+tenecteplasa según peso. Fondaparinux 2,5mg sc (enoxaparina si contraindicado o no disponible).
Las variables incluidas en el estudio fueron:
- -
Número de la seguridad social, edad y sexo. Fecha de asistencia.
- -
Factores de riesgo cardiovascular: cardiopatía isquémica (cualquier forma de la misma), dislipidemia, hipertensión arterial, diabetes y tabaquismo (consumo actual y exfumador hace menos de un año). Número de factores de riesgo cardiovascular.
- -
Error diagnóstico: dicotómica.
- -
Dolor típico: dicotómica. Tensión arterial sistólica. Frecuencia cardíaca.
- -
Localización del IAM: a) anterior; b) inferoposterior.
- -
Clasificación Killip: I) no insuficiencia cardíaca; II) insuficiencia cardíaca; III) edema agudo de pulmón; IV) shock cardiogénico.
- -
Criterios ECG: a) elevaciones del segmento ST, medidas desde el punto J, en 2 o más derivaciones contiguas≥0,2mV en las derivaciones V1-V3 y≥0,1mV en el resto de derivaciones; b) no cumple criterios.
- -
Prioridad ARIAM (revisada por UCI): 1, 2 o 3.
- -
Traslado: a) DCCU; b) helicóptero 061.
- -
Tratamiento: NTG, mórficos, AAS, clopidogrel, prasugrel, fondaparinux, enoxaparina.
- -
Reperfusión: a) no; b) FxPH; c) FxH; d) ICPp; e) ICPd.
- -
Reperfusión adicional: a) ICPr; b) ICPsis.
- -
Tiempos: hora de inicio de los síntomas, contacto con el sistema sanitario, asistencia DCCU, llegada al hospital, administración fibrinolítico y realización ICPp.
- -
Ingreso: a) observación Urgencias; b) Cardiología; c) UCI.
- -
Complicaciones DCCU y planta. Mortalidad al año: dicotómica.
Los análisis estadísticos se realizaron con el programa informático SPSS® 17.0. Se han usado frecuencias absolutas y porcentajes para las variables cualitativas y medidas de centralización y dispersión para las cuantitativas. Se ha analizado la normalidad de la distribución mediante test gráficos y la prueba de Kolmogorov-Smirnov. Las variables cuantitativas de distribución normal se expresan en media±desviación estándar, mientras las de distribución no normal lo hacen como mediana y rango (mínimo y máximo). Se utilizó la prueba χ2 y el test de Fisher para comparar variables categóricas, y la prueba de Levene para la igualdad de varianzas, así como la prueba T para la igualdad de medias en caso de variables cuantitativas continuas de distribución normal y pruebas no paramétricas para las de distribución no normal.
ResultadosDesde la implantación del protocolo se han atendido 61 pacientes con diagnóstico o sospecha de SCACEST. Se encontraron 9 casos con error diagnóstico, de los que 7 fueron también de etiología cardíaca: 2 ángor inestable, una miocardiopatía hipertrófica, 2 pericarditis agudas, una taquiarritmia y una disfunción de marcapasos. Los otros 2 fueron de etiología no cardíaca. La concordancia diagnóstica DCCU-hospital es del 85,3%, pero alcanza el 95,8% si incluimos solo los casos que cumplen los criterios ECG. En los pacientes a los que se realizó FxPH la concordancia es del 100%.
Se incluyen 52 pacientes del periodo 2012-2013 con diagnóstico confirmado. Los controles históricos de 2009-2010 fueron 26 casos, con 6 errores diagnósticos (23,07%), por lo que se incluyeron 20 de ellos.
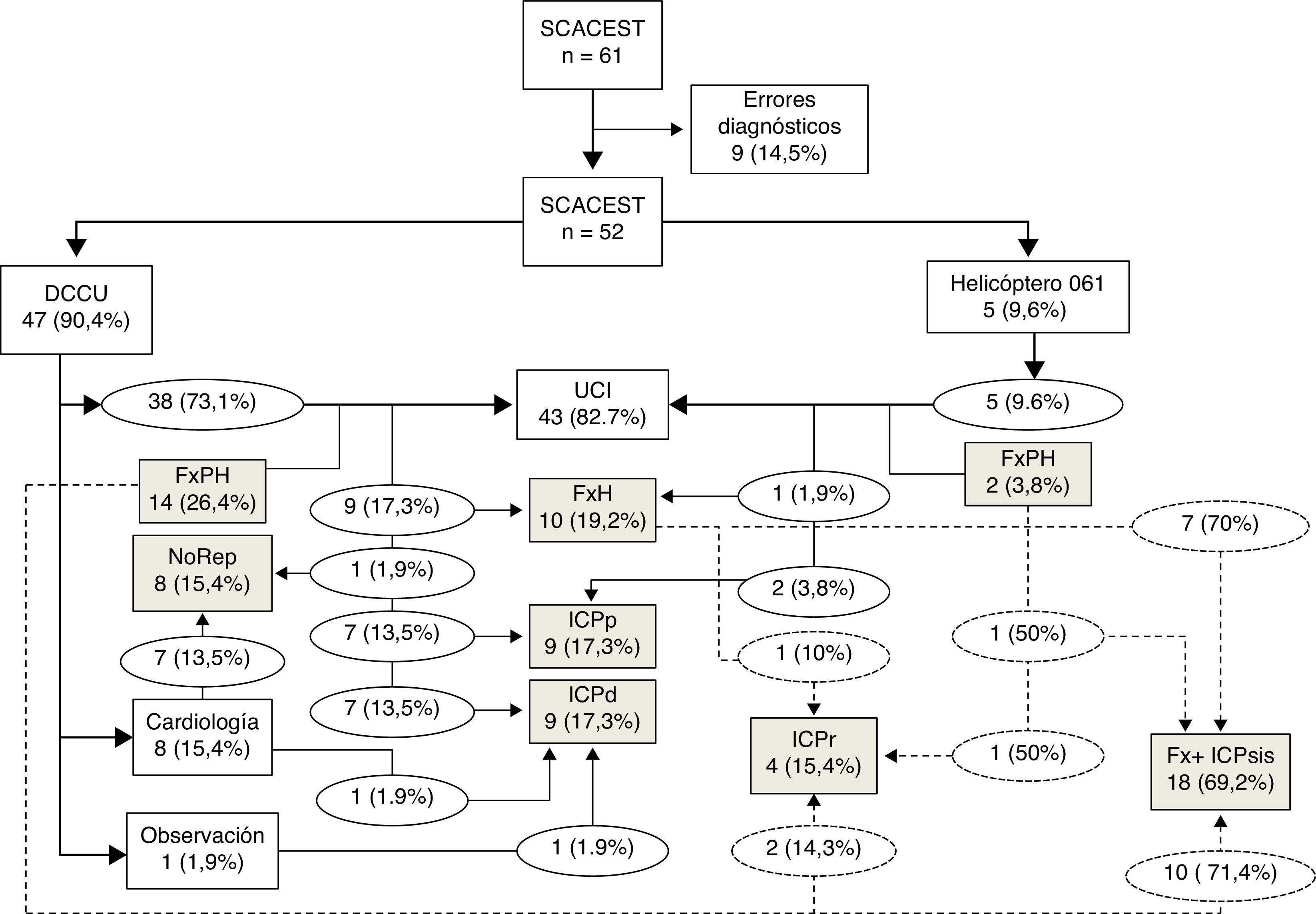
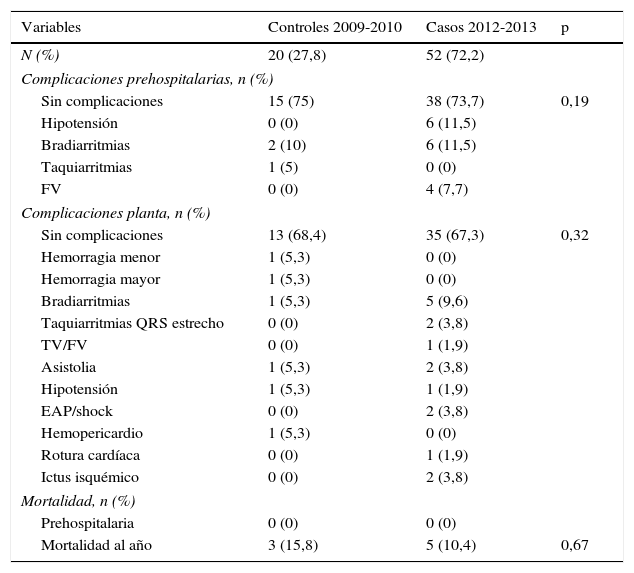
En la figura 1 se recoge el diagrama de flujo de los pacientes atendidos tras la implantación del protocolo.
Diagrama de flujo de los pacientes atendidos. DCCU: dispositivo de cuidados críticos y urgencias; Fx; fibrinólisis; FxH: fibrinólisis hospitalaria; FxPH: fibrinólisis prehospitalaria; ICPd: intervención coronaria percutánea diferida; ICPp: intervención coronaria percutánea primaria; ICPr: intervención coronaria percutánea de rescate; ICPsis: coronariografía sistemática tras fibrinólisis±intervención coronaria percutánea; NoRep: no reperfusión; SCACEST: síndrome coronario agudo con elevación del segmento ST; UCI: unidad de cuidados intensivos.
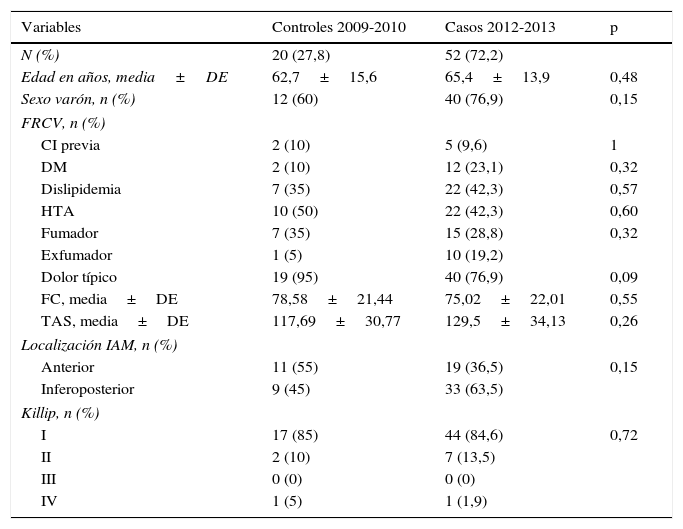
Las características generales y clínicas de los 2 grupos se muestran en la tabla 1. No se encuentran diferencias significativas entre ambos, si bien los casos actuales presentan más edad, menos mujeres, mayor porcentaje de diabetes mellitus, dislipidemia y exfumadores, menor número de factores de riesgo cardiovascular, mayor frecuencia de dolor atípico y localización inferoposterior del IAM, así como menos casos con Killip I que los controles históricos. Se observa una mejoría en la concordancia diagnóstica de los casos de 2012-2013 (85,3 versus 76,9%), aunque sin significación estadística.
Características generales y clínicas de los casos y controles históricos
| Variables | Controles 2009-2010 | Casos 2012-2013 | p |
|---|---|---|---|
| N (%) | 20 (27,8) | 52 (72,2) | |
| Edad en años, media±DE | 62,7±15,6 | 65,4±13,9 | 0,48 |
| Sexo varón, n (%) | 12 (60) | 40 (76,9) | 0,15 |
| FRCV, n (%) | |||
| CI previa | 2 (10) | 5 (9,6) | 1 |
| DM | 2 (10) | 12 (23,1) | 0,32 |
| Dislipidemia | 7 (35) | 22 (42,3) | 0,57 |
| HTA | 10 (50) | 22 (42,3) | 0,60 |
| Fumador | 7 (35) | 15 (28,8) | 0,32 |
| Exfumador | 1 (5) | 10 (19,2) | |
| Dolor típico | 19 (95) | 40 (76,9) | 0,09 |
| FC, media±DE | 78,58±21,44 | 75,02±22,01 | 0,55 |
| TAS, media±DE | 117,69±30,77 | 129,5±34,13 | 0,26 |
| Localización IAM, n (%) | |||
| Anterior | 11 (55) | 19 (36,5) | 0,15 |
| Inferoposterior | 9 (45) | 33 (63,5) | |
| Killip, n (%) | |||
| I | 17 (85) | 44 (84,6) | 0,72 |
| II | 2 (10) | 7 (13,5) | |
| III | 0 (0) | 0 (0) | |
| IV | 1 (5) | 1 (1,9) | |
CI: cardiopatía isquémica; DE: desviación estándar; DM: diabetes mellitus; FC: frecuencia cardíaca; FRCV: factores de riesgo cardiovascular; HTA: hipertensión arterial; IAM: infarto agudo de miocardio; TAS: tensión arterial sistólica.
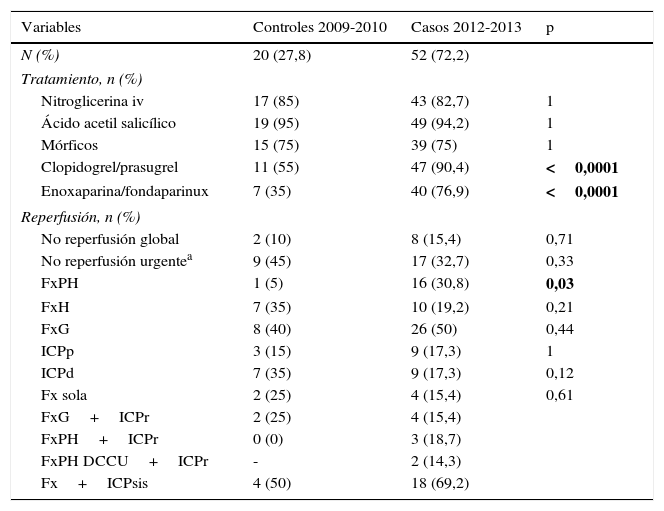
En la tabla 2 encontramos el tratamiento recibido en los 2 grupos y las terapias de reperfusión empleadas. Como se observa, las cifras de administración de NTG, AAS y mórficos son muy similares, obteniendo diferencias significativas con p<0,0001 en la utilización de clopidogrel/prasugrel (antes del protocolo solo se disponía de clopidogrel), y fondaparinux/enoxaparina (antes, solo enoxaparina).
Análisis del tratamiento recibido y las terapias de reperfusión empleadas
| Variables | Controles 2009-2010 | Casos 2012-2013 | p |
|---|---|---|---|
| N (%) | 20 (27,8) | 52 (72,2) | |
| Tratamiento, n (%) | |||
| Nitroglicerina iv | 17 (85) | 43 (82,7) | 1 |
| Ácido acetil salicílico | 19 (95) | 49 (94,2) | 1 |
| Mórficos | 15 (75) | 39 (75) | 1 |
| Clopidogrel/prasugrel | 11 (55) | 47 (90,4) | <0,0001 |
| Enoxaparina/fondaparinux | 7 (35) | 40 (76,9) | <0,0001 |
| Reperfusión, n (%) | |||
| No reperfusión global | 2 (10) | 8 (15,4) | 0,71 |
| No reperfusión urgentea | 9 (45) | 17 (32,7) | 0,33 |
| FxPH | 1 (5) | 16 (30,8) | 0,03 |
| FxH | 7 (35) | 10 (19,2) | 0,21 |
| FxG | 8 (40) | 26 (50) | 0,44 |
| ICPp | 3 (15) | 9 (17,3) | 1 |
| ICPd | 7 (35) | 9 (17,3) | 0,12 |
| Fx sola | 2 (25) | 4 (15,4) | 0,61 |
| FxG+ICPr | 2 (25) | 4 (15,4) | |
| FxPH+ICPr | 0 (0) | 3 (18,7) | |
| FxPH DCCU+ICPr | - | 2 (14,3) | |
| Fx+ICPsis | 4 (50) | 18 (69,2) | |
DCCU: dispositivo de cuidados críticos y urgencias; Fx: fibrinólisis; FxG: fibrinólisis global; FxH: fibrinólisis hospitalaria; FxPH: fibrinólisis prehospitalaria; ICPd: intervención coronaria percutánea diferida; ICPp: intervención coronaria percutánea primaria; ICPr: intervención coronaria percutánea de rescate; ICPsis: coronariografía sistemática tras fibrinólisis+intervención coronaria percutánea.
En Negrita: valores de “p” estadísticamente significativos (p<0,05).
Centrándonos en las estrategias de reperfusión, la realización de FxPH aumenta significativamente tras la implantación del protocolo. De los SCACEST clasificados como ARIAM 1 en este periodo: el 68,2% recibieron FxPH, el 13,6% FxH y el 18,2% fueron derivados para ICPp.
Existe un ligero aumento de pacientes sin reperfusión, pero se incrementan los casos con reperfusión urgente. Se observa una menor utilización de ICPd y FxH, así como un ligero aumento de ICPp. Encontramos, del mismo modo, un incremento de la estrategia farmacoinvasiva debido a la disminución de la cifra de pacientes que reciben solo fibrinólisis y el incremento de ICPsis. La mitad de los pacientes recibió como tratamiento la fibrinólisis intravenosa, complementada con ICPr o ICPsis en el 84,6% de los casos.
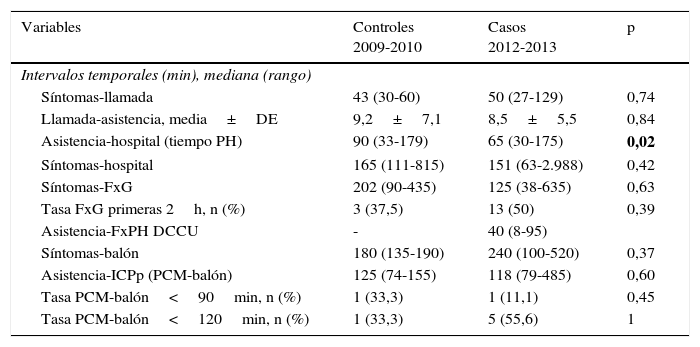
Las tablas 3 y 4 recogen el análisis de los intervalos temporales y los retrasos en la reperfusión. Se observa una reducción estadísticamente significativa del tiempo prehospitalario en los casos actuales, a pesar de la demora que puede suponer la realización de FxPH. El tiempo de administración del fibrinolítico desde el inicio de los síntomas se reduce en 77min, lo que permite aplicar esta terapia en<2h a la mitad de los pacientes, si bien no alcanza significación estadística.
Análisis de los intervalos temporales en los casos y controles históricos
| Variables | Controles 2009-2010 | Casos 2012-2013 | p |
|---|---|---|---|
| Intervalos temporales (min), mediana (rango) | |||
| Síntomas-llamada | 43 (30-60) | 50 (27-129) | 0,74 |
| Llamada-asistencia, media±DE | 9,2±7,1 | 8,5±5,5 | 0,84 |
| Asistencia-hospital (tiempo PH) | 90 (33-179) | 65 (30-175) | 0,02 |
| Síntomas-hospital | 165 (111-815) | 151 (63-2.988) | 0,42 |
| Síntomas-FxG | 202 (90-435) | 125 (38-635) | 0,63 |
| Tasa FxG primeras 2h, n (%) | 3 (37,5) | 13 (50) | 0,39 |
| Asistencia-FxPH DCCU | - | 40 (8-95) | |
| Síntomas-balón | 180 (135-190) | 240 (100-520) | 0,37 |
| Asistencia-ICPp (PCM-balón) | 125 (74-155) | 118 (79-485) | 0,60 |
| Tasa PCM-balón<90min, n (%) | 1 (33,3) | 1 (11,1) | 0,45 |
| Tasa PCM-balón<120min, n (%) | 1 (33,3) | 5 (55,6) | 1 |
DCCU: dispositivo de cuidados críticos y urgencias; DE: desviación estándar; FxG: fibrinólisis global (prehospitalaria+hospitalaria); FxPH: fibrinólisis prehospitalaria; ICPd: intervención coronaria percutánea diferida; ICPp: intervención coronaria percutánea primaria; PCM: primer contacto médico; PH: prehospitalario.
En Negrita: valores de “p” estadísticamente significativos (p<0,05).
Retrasos en la reperfusión de los casos de 2012-2013
| Estrategia reperfusión | Primera hora | Segunda hora | Tercera hora | >Tercera hora | p |
|---|---|---|---|---|---|
| Retrasos según la estrategia empleada (h), n (%) | |||||
| FxPH | 1 (6,3) | 11 (68,8) | 3 (18,8) | 1 (6,3) | <0,01 |
| FxH | 0 (0) | 1 (10) | 5 (50) | 5 (50) | |
| ICPp | 0 (0) | 0 (0) | 3 (33,3) | 6 (66,7) | |
| Mediana/media en minutos | Primera hora | Segunda hora | Tercera hora | >Tercera hora | p |
|---|---|---|---|---|---|
| Retrasos en la fibrinólisis prehospitalaria (h) | |||||
| Mediana síntomas-llamada | 30 | 30 | 45 | 133 | <0,02 |
| Media llamada-asistencia | 1 | 9 | 11 | 8 | 0,75 |
| Mediana asistencia-FxPH | 8 | 40 | 37 | 50 | 0,41 |
| Mediana asistencia-hospital | 33 | 80 | 75 | 76 | 0,24 |
FxH: fibrinólisis hospitalaria; FxPH: fibrinólisis prehospitalaria; ICPp: intervención coronaria percutánea primaria.
En Negrita: valores de “p” estadísticamente significativos (p<0,05).
Los retrasos en la reperfusión presentan diferencias significativas según la estrategia elegida (p<0,01). Pese a que el tiempo puerta-aguja extrahospitalario se sitúa por encima del objetivo de 30min, los retrasos se deben fundamentalmente a la demora del paciente en solicitar asistencia, encontrando diferencias estadísticamente significativas con p<0,02.
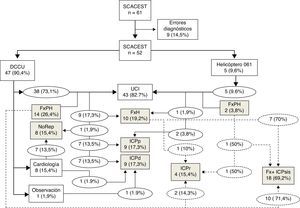
En la tabla 5 se analizan las complicaciones durante la atención prehospitalaria y el ingreso en planta, así como la mortalidad. No hubo diferencias significativas en la ausencia de complicaciones tras la implantación del protocolo, obteniendo cifras muy similares. Todos los casos de fibrilación ventricular durante la fase prehospitalaria fueron desfibrilados con éxito. No se observó ninguna complicación hemorrágica secundaria a la fibrinólisis, mientras que hubo 2 casos en los controles históricos. La mortalidad prehospitalaria fue nula, y se observó una mejoría de la mortalidad al año, aunque sin diferencias estadísticamente significativas.
Complicaciones durante la asistencia prehospitalaria y el ingreso. Mortalidad
| Variables | Controles 2009-2010 | Casos 2012-2013 | p |
|---|---|---|---|
| N (%) | 20 (27,8) | 52 (72,2) | |
| Complicaciones prehospitalarias, n (%) | |||
| Sin complicaciones | 15 (75) | 38 (73,7) | 0,19 |
| Hipotensión | 0 (0) | 6 (11,5) | |
| Bradiarritmias | 2 (10) | 6 (11,5) | |
| Taquiarritmias | 1 (5) | 0 (0) | |
| FV | 0 (0) | 4 (7,7) | |
| Complicaciones planta, n (%) | |||
| Sin complicaciones | 13 (68,4) | 35 (67,3) | 0,32 |
| Hemorragia menor | 1 (5,3) | 0 (0) | |
| Hemorragia mayor | 1 (5,3) | 0 (0) | |
| Bradiarritmias | 1 (5,3) | 5 (9,6) | |
| Taquiarritmias QRS estrecho | 0 (0) | 2 (3,8) | |
| TV/FV | 0 (0) | 1 (1,9) | |
| Asistolia | 1 (5,3) | 2 (3,8) | |
| Hipotensión | 1 (5,3) | 1 (1,9) | |
| EAP/shock | 0 (0) | 2 (3,8) | |
| Hemopericardio | 1 (5,3) | 0 (0) | |
| Rotura cardíaca | 0 (0) | 1 (1,9) | |
| Ictus isquémico | 0 (0) | 2 (3,8) | |
| Mortalidad, n (%) | |||
| Prehospitalaria | 0 (0) | 0 (0) | |
| Mortalidad al año | 3 (15,8) | 5 (10,4) | 0,67 |
EAP: edema agudo de pulmón; FV: fibrilación ventricular; TV: taquicardia ventricular.
Las características epidemiológicas de los pacientes de nuestro estudio son similares a las de otras publicaciones en cuanto a edad, sexo, diabetes mellitus, hipertensión arterial y tabaquismo14,23,25–29. Presentan más prevalencia de dislipidemia14,23,25,26 y menos de cardiopatía isquémica14,23,26.
El porcentaje de Killip I también es similar14,23,26. Sin embargo, en otros28,30 existe una proporción mayor de pacientes con Killip>I, lo que puede suponer un mayor perfil de riesgo. Las características clínicas muestran una atipicidad del dolor torácico, frecuencia cardíaca y tensión arterial similar14, con mayor frecuencia de localización posteroinferior.
La concordancia diagnóstica mejora con respecto a los controles. Si la comparamos con el registro PEFEX14 (92,2% de concordancia global y 98,5% en los que recibieron FxPH), equiparando previamente sus criterios de inclusión, las cifras son ligeramente superiores en nuestro trabajo. El 100% de concordancia en los casos con FxPH es muestra de la fiabilidad, ya que no se aplicó esta terapia a ningún paciente en que no estuviera indicada25.
La administración de NTG, mórficos y AAS es superior a la del registro PEFEX14 (80,1, 74,7 y 89,2%, respectivamente), mejorando asimismo la cifra de AAS del estudio MASCARA28 (90,4%). La mayor administración de antitrombóticos con respecto a los controles evidencia, junto con la mayor concordancia diagnóstica, que la implantación del protocolo ha supuesto una mejoría en la calidad de la atención del SCACEST más allá de la disponibilidad de una nueva estrategia de reperfusión.
Se obtuvieron diferencias significativas en la realización de FxPH respecto a los controles históricos, con un porcentaje mayor que en otros estudios14,22,29. Todos presentaban una prioridad ARIAM 1, salvo un paciente con 75 años que cumplía el resto de las condiciones. El 13,6% de ARIAM 1 recibió FxH, cifra que debemos disminuir, aunque un tercio de los casos se debió a la no disponibilidad de tenecteplasa. La tasa de ICPr tras FxPH fue menor que la de otros trabajos31, pero superior al 11,1% de PEFEX14. La tasa de ICPsis tras FxPH fue superior al 57,7% del SUMMA 11231. Se realizaron menos FxH que en el registro PEFEX14 (35,8%) y más que en otros estudios22,30. La tasa de ICPr tras FxH es similar a la de PEFEX14. En conclusión, se realizó fibrinólisis en porcentajes similares a estudios realizados en Andalucía14,26 y superior a otros22,25,28–30. Se empleó la estrategia farmacoinvasiva en el 84,6% de los fibrinolisados, con un incremento respecto a los controles (97% en el registro francés22, 9,3 y 32% en los hospitales andaluces sin/con sala de hemodinámica, respectivamente29).
La ICPp aumentó ligeramente. El porcentaje es similar al del resto de los hospitales andaluces con sala de hemodinámica (16,1%) y muy superior al de los que no disponen de ella (1,9%)26. Es inferior al estudio MASCARA28 (24,7%), al registro francés (39%)22 y a las comunidades donde se ha apostado por esta estrategia (76 y 56,9%)29,30.
La proporción de pacientes que no recibe ningún tipo de reperfusión es menor que en otros estudios22,26, pero superior a los controles, lo que podría ser debido a su menor edad. Sin embargo, aumentan los pacientes que reciben reperfusión urgente.
El intervalo síntomas-llamada es similar al del registro PEFEX14, e inferior a otros27,29,30. El tiempo medio llamada-asistencia es inferior al de otros trabajos14,31, lo que puede atribuirse a que hay pacientes que consultan en el mismo centro de salud donde se ubica el EM. El intervalo síntomas-hospital es superior al de PEFEX14 (128min) y MASCARA28 (96min), a pesar de que el tiempo prehospitalario disminuye respecto a los controles. Estos datos confirman las importantes demoras en nuestra zona, por lo que las estrategias de reperfusión hospitalarias difícilmente pueden cumplir los tiempos recomendados1,3. De hecho, solo un paciente recibe la FxH en<2h, y en casi la mitad de los pacientes se incumple el objetivo del intervalo puerta-balón, con una mediana superior a la de otros estudios27–30.
Es en este contexto donde adquiere sentido la realización de FxPH. De esta forma, se ha logrado reperfundir en<2h al 75% de los pacientes que reciben FxPH, ligeramente superior al registro PEFEX14 (68%) y SUMMA 11231 (65%), lo que es muestra de su efectividad, con una mediana síntomas-fibrinólisis inferior14,25,31. El intervalo puerta-aguja extrahospitalario ha sido superior al de otros trabajos14,31, cumpliendo el objetivo en el 41,7% de los casos. Probablemente la adquisición de experiencia repercutirá en un mayor número de FxPH28 y una menor demora.
Respecto a la asociación de los retrasos en la reperfusión con la demora del paciente en solicitar asistencia, el público debe saber cómo reconocer los síntomas comunes de un infarto agudo de miocardio y cómo llamar al servicio de emergencias, aunque la efectividad de las campañas públicas aún no se ha establecido claramente1.
Otro punto fundamental en la evaluación de los resultados es la seguridad25. Observamos cifras similares de complicaciones en DCCU y planta respecto a los controles. En un trabajo reciente26 este porcentaje es del 39,5%, superior al nuestro. No se observó ninguna complicación hemorrágica tras la FxPH25,31, mientras en otros estudios se sitúa alrededor del 4%14,23,28. La aparición de fibrilación ventricular durante la fase prehospitalaria es similar14,29. La mortalidad prehospitalaria fue nula (1,1% en PEFEX)14. La mortalidad al año mejora respecto a los controles, sin diferencias significativas, y es menor que en este estudio (22,4%)14.
Entre las limitaciones del estudio cabe destacar el reducido tamaño muestral, que intentaremos subsanar manteniendo el registro de manera continua, la imposibilidad de seguimiento al año de los pacientes no residentes en Andalucía y la ausencia del registro de tiempos en algunos casos.
ConclusionesEl protocolo de FxPH es efectivo, seguro y fiable. No solo disminuye las demoras en el tratamiento, sino que mejora la atención al paciente con SCACEST, con un aumento de la concordancia diagnóstica y del tratamiento antitrombótico. La apuesta realizada por la estrategia farmacoinvasiva, extendiendo la FxPH a los DCCU en una población que difícilmente puede recibir la ICPp en los tiempos adecuados, constituye una opción válida, segura y realista.
Las necesidades de mejora son: ampliar la cobertura DCCU y, por tanto, la disponibilidad de FxPH 24h, aumentar la tasa de SCACEST ARIAM 1 que reciben FxPH, el registro de tiempos en la historia clínica, y la disminución de los tiempos puerta-aguja extrahospitalario y PCM-balón.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónNo existe ninguna fuente de financiación.
Conflicto de interesesNo existe conflicto de intereses para ninguno de los autores.