Se trata de una mujer de 28 años que consulta por secreción lactosa por ambos pezones en los 15 días previos, sin ninguna otra sintomatología acompañante.
No refiere antecedentes personales ni familiares de interés: no tiene alergias, no se ha sometido a intervenciones quirúrgicas relevantes y no ha tenido ingresos hospitalarios previos. Acude anualmente a la consulta de Planificación Familiar para control anticonceptivo mensual intramuscular con una combinación de enantato de estradiol 10 mg y acetofénido de algestona 150 µg desde hace 2 años. No toma ningún otro fármaco.
La paciente tiene ciclos menstruales de 28-30 días de duración, regulares. No ha tenido gestaciones. Las revisiones ginecológicas han sido normales según la paciente.
En la exploración física se registra: un peso de 70 kg, una talla de 157 cm, tensión arterial de 115/75 mmHg y frecuencia cardiaca de 70 latidos/min. La cabeza y cuello son normales; no se aprecia hirsutismo; y no presenta focalidades neurológicas. La inspección y la palpación de ambas mamas es normal; no se observa salida de secreción tras la presión de los pezones, ni se aprecian masas ni adenopatías axilares o supraclaviculares. El resto de la exploración física por aparatos es anodina.
Se solicitó una bioquímica general, hemograma y hormonas tiroideas que fueron normales. Además, se solicitó un perfil hormonal que mostró hormona foliculoestimulante (FSH) y hormona luteinizante (LH) normales y prolactina (PRL) de 58 ng/ml.
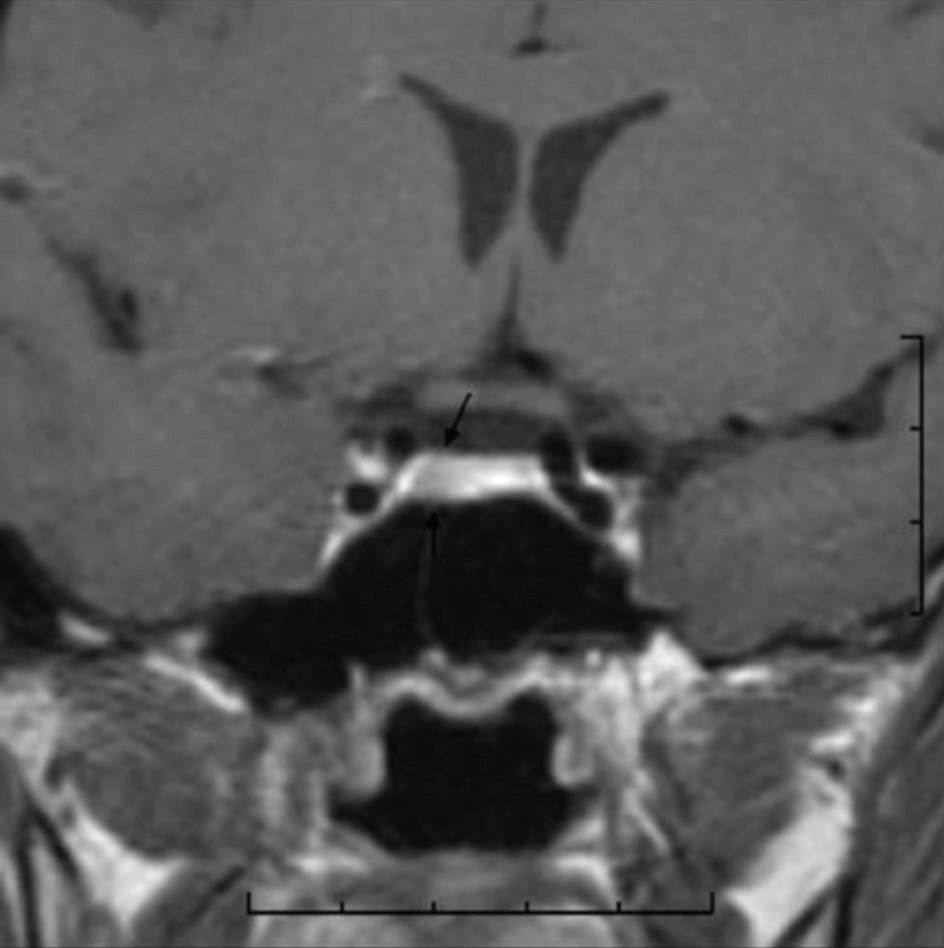
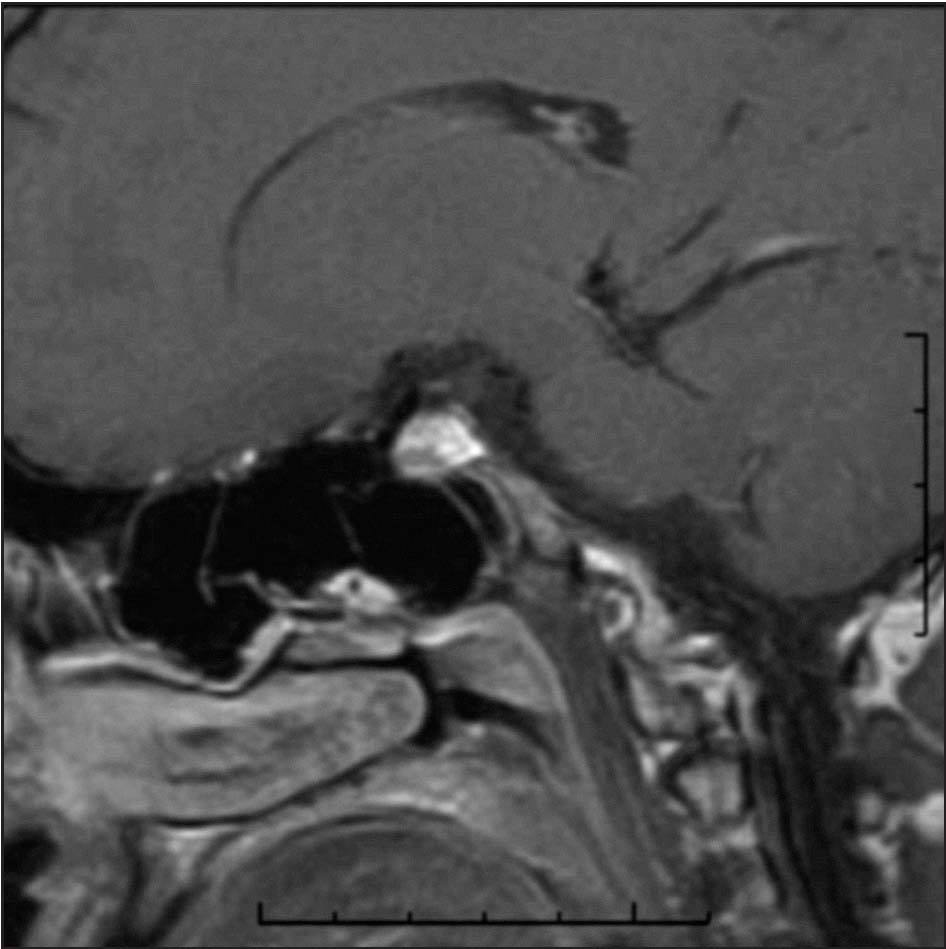
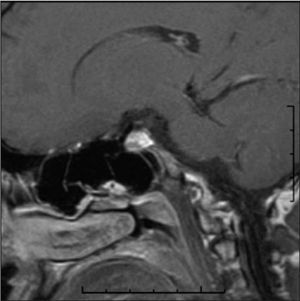
Ante los hallazgos descritos se remite a la consulta de Endocrinología para el estudio de galactorrea-hiperprolac-tinemia. Se solicita resonancia magnética (RM) craneal que muestra una imagen compatible con microadenoma hipofisario (figs. 1 y 2). El endocrinólogo adopta una actitud expectante: no se ha iniciado tratamiento farmacológico adicional y se ha retirado el tratamiento anticonceptivo previo –recomendándole el uso de métodos de barrera–. En la actualidad la galactorrea ha cedido.
Figura 1. Imagen de resonancia magnética de corte coronal que muestra una zona de menor captación en la vertiente derecha de la glándula (flecha).
Figura 2. Imagen de resonancia magnética en corte sagital que muestra la misma lesión hipocaptante en la zona inferior de la glándula.
DISCUSIÓNSe define galactorrea como la presencia de secreción líquida de contenido lechoso de la mama, que surge a través del pezón fuera de los periodos fisiológicos –embarazo, puerperio y post-aborto–. Supone el 1% de las consultas ginecológicas, pero se estima que el 20-25% de las mujeres tiene galactorrea en algún momento de su vida1. La secreción no lechosa –marrón-verdosa, sanguino-lenta– no se asocia a endocrinopatía, y deben buscarse otras causas (neoplasias de mama, mastitis, etc.). Se considera que en la mayoría de los casos de galactorrea hay un aumento de los niveles de PRL; sin embargo, hasta la mitad de las pacientes con galactorrea tiene concentraciones séricas de PRL normales2 o al menos con picos intermitentes. Estos casos se atribuyen a aumento de sensibilidad de la glándula mamaria a la PRL circulante o a alteraciones del ritmo circadiano de secreción de la PRL.
La PRL es una proteína (198 aminoácidos, 21.500 kDa) que se segrega en las células lactotropas de la hipófisis anterior. Su mecanismo de control central predominante es inhibitorio y es la dopamina segregada en el hipotálamo la encargada de suprimir su liberación3; cualquier causa que interfiera con la síntesis, el transporte a la glándula hipofisaria o la acción sobre los receptores de dopamina produce hiperprolactinemia4. Se considera que el límite superior de normalidad de concentración de PRL es 20 ng/ml en hombres y 25 ng/ml en mujeres.
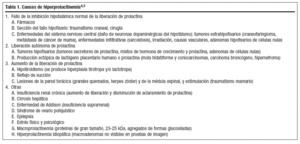
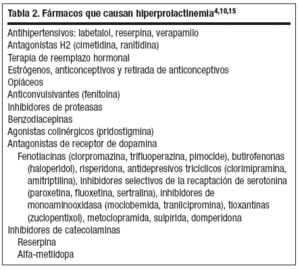
La hiperprolactinemia se puede producir, al margen de las causas fisiológicas (embarazo y lactancia), principalmente por tres mecanismos: fallo de la inhibición hipotalámica normal de la liberación de PRL, aumento en los factores liberadores de PRL o secreción autónoma de PRL por tumores, aunque también puede haber otras causas (tabla 1). La causa más importante de hiperprolactinemia es el adenoma hipofisario de células lactotropas secretor de PRL (prolactinoma); el 90% de los prolactinomas son microadenomas intraselares; en las mujeres más del 90% son microadenomas, sobre todo entre los 20 y los 40 años, mientras que en los varones el 60% de estos tumores son macroadenomas (se cree que esta discordancia se puede deber a escasa sintomatología, retraso en consultar por disfunción eréctil o por una mayor tasa de crecimiento)4. La causa más frecuente de hiperprolactinemia es la ingesta de fármacos4 (tabla 2); generalmente la concentración sérica de PRL se eleva a las pocas horas o días de la administración del fármaco y se normaliza 2-4 días tras suprimirlo. Teniendo en cuenta el nivel de PRL, si es superior a 100 ng/ml la causa más frecuente es un adenoma hipofisario secretor, mientras que si es menor el origen más frecuente es la toma de fármacos5.
Tabla 1. Causas de hiperprolactinemia4,5
Tabla 2. Fármacos que causan hiperprolactinemia4,10,15
Las manifestaciones clínicas de la hiperprolactinemia son habitualmente fáciles de reconocer. Los síntomas típicos son infertilidad, oligo-amenorrea y galactorrea. También puede aparecer aumento de peso e hirsutismo leve, sequedad vaginal, dispareunia y pérdida de libido. Las manifestaciones clínicas suelen guardar relación con el grado de elevación de PRL: elevaciones superiores a 100 ng/ml se asocian a hipogonadismo evidente y secreción infranormal de estradiol con amenorrea, osteoporosis, sofocos y sequedad vaginal, mientras que niveles menores, de 20-50 ng/ml, pueden causar insuficiente secreción de progesterona, con acortamiento de la fase lútea del ciclo menstrual, e infertilidad –que incluso se puede presentar sin anomalías del ciclo–. Pueden aparecer síntomas neurológicos en los macroadenomas4. Tras excluir el embarazo, la hiperprolactinemia supone el 10-20% de casos de amenorrea6. Otra causa de hiperprolactinemia leve e infertilidad es el síndrome de ovario poliquístico, en el que éstas se asocian a hirsutismo7.
En cuanto al diagnóstico de estas situaciones (tabla 3), se debe realizar una exploración física detallada haciendo hincapié en datos de afectación quiasmática (hemianopsia bitemporal), cefalea (afectación intracraneal), valorar la pared torácica (lesiones de herpes zóster) y buscar signos de hipogonadismo, hipotiroidismo e insuficiencia renal. Dentro de la batería de exploraciones complementarias a solicitar debemos determinar la concentración sérica de PRL, una bioquímica general, hormonas tiroideas, FSHLH y una prueba de embarazo4,8.
Tabla 3. Etapas diagnósticas de una hiperprolactinemia
La secreción de PRL es pulsátil, por lo que se deben realizar 2 o más determinaciones séricas de PRL4,9: en situación basal, en reposo, en ausencia de relaciones sexuales o situaciones de estrés físico-psíquico, y tras haber suprimido cualquier medicación que interfiera en su cuantificación. Los niveles de PRL sérica son sólo orientativos sobre la causa de hiperprolactinemia: cifras ligeramente elevadas (20-40 ng/ml) requieren confirmación antes de catalogar-las como hiperprolactinemia; valores de 20-200 ng/ml pueden aparecer en hiperprolactinemias iatrógenas o extrahipofisarias; concentraciones de 40-100 ng/ml sugieren hiperprolactinemia idiopática, tumores no productores de PRL o ingesta de fármacos, sin excluir la existencia de prolactinoma (un 10-20% de ellos presenta cifras inferiores a 100 ng/ml, raros por debajo de 75 ng/ml); entre 100 y 200 ng/ml, tras descartar el embarazo, son sugerentes de microprolactinoma (adenoma secretor de PRL de < 1 cm) o macroadenoma no productor de PRL; y por encima de 200 ng/ml hay que pensar en macroprolactinoma (adenoma secretor de PRL > 1 cm)4,5. La secreción de PRL por adenomas de células lactotrofas suele ser proporcional a su tamaño10. La determinación de PRL se ve dificultada por el “efecto gancho” (hook-effect)11,12: cuando existen concentraciones sumamente elevadas de PRL y se cuantifica por métodos modernos (inmunorradiométricos o quimioluminiscencia) se obtienen valores falsamente bajos al saturarse los anticuerpos usados en la determinación; el fenómeno se evita haciendo una dilución de las muestras, lo que tiene interés para evitar el falso diagnóstico de un macroprolactinoma no secretor. Las pruebas de estimulación y supresión (TRH, L-DOPA) ya no se utilizan por inespecíficas o inconsistentes13.
Cuando existe hiperprolactinemia el estudio se centra en buscar un tumor hipofisario, una vez se descartan causas farmacológicas e hipotiroidismo. Pueden existir concentraciones de PRL poco elevadas junto a tumores hipofisarios descubiertos casualmente (incidentalomas)14 que pueden dar falsos diagnósticos de microprolactinoma. También hay casos de hiperprolactinemia con valores mínimamente elevados y tumor hipofisario mayor de 1 cm: en estos casos debemos hacer el diagnóstico diferencial con otro tipo de tumores del área hipotálamo-hipofisaria y con macroadenomas no secretores que pueden producir valores de PRL elevados (habitualmente menores de 200 ng/ml) por compresión del tallo hipofisario (se denominan pseudoprolactinomas)15.
La RM es la técnica de imagen que se debe realizar ante cualquier grado de hiperprolactinemia no explicada, con el fin de descartar etiología en la zona hipotálamo-hipofi-saria6,16.
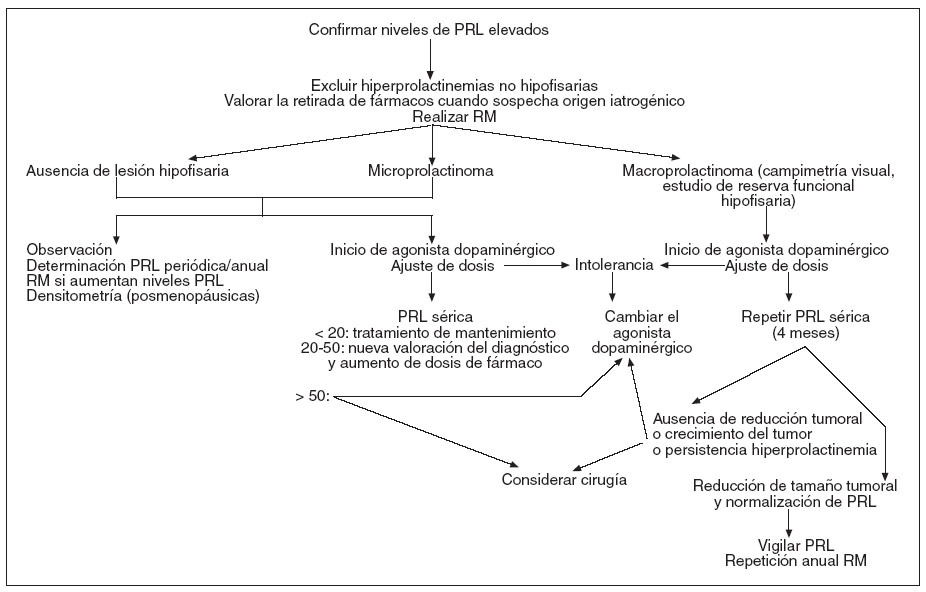
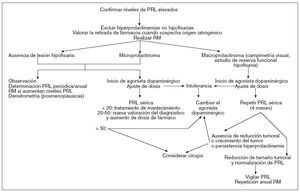
El tratamiento de las hiperprolactinemias es etiológico (fig. 3), por lo que hay que tener en cuenta los pros y los contras de la retirada de fármacos cuando su origen es iatrogénico.
Figura 3. Algoritmo de tratamiento de las hiperprolactinemias4,5. PRL: prolactina; RM: resonancia magnética.
Si no hay lesión hipofisaria, puede considerarse no tratar, realizando una determinación anual de PRL (con la práctica de una RM si los niveles aumentan) y una densitometría en situaciones de amenorrea posmenopáusica5.
Si hallamos un microprolactinoma podemos llevar a cabo observación con determinación periódica de la concentración de PRL (con RM si aumentan) y densitometría anual; hasta en un tercio de los microadenomas desaparecen los síntomas y se normaliza la PRL sérica de forma espontánea, y un 90% de los microprolactinomas no aumenta el tamaño en un periodo de seguimiento de 4-6 años4,15,17,18. Tanto si no hay lesión hipofisaria como si se trata de un microadenoma se iniciaría tratamiento médico con agonistas dopaminérgicos (bromocriptina, cabergolina) si hay síntomas (hipogonadismo, galactorrea, trastornos sexuales, deseo de embarazo y disminución de la densidad mineral ósea). Los fármacos agonistas dopaminérgicos deben administrarse a la mínima dosis eficaz. Si el tratamiento médico es eficaz y no existe evidencia de tumor en la RM puede interrumpirse el tratamiento médico al cabo de 2 años o tras la menopausia (entre el 20 y el 50% de casos el tratamiento puede ser suspendido sin recidiva de la hiperprolactinemia); debemos probar esta opción en pacientes asintomáticos con normoprolactinemia en tratamiento con bajas dosis de agonistas dopaminérgicos y sin evidencia de lesión morfológica en la RM15; se reanudará el tratamiento si en controles seriados aumentan los niveles de PRL4.
Los macroadenomas deben tratarse siempre, con tratamiento médico y/o quirúrgico. El tratamiento médico con agonistas dopaminérgicos es de elección en estos tumores. Estos fármacos logran un descenso de los niveles séricos de PRL en 2-3 semanas y una reducción del tamaño tumoral en 6 semanas. La cirugía se reserva para los casos en los que exista intolerancia o ausencia de efectividad de los agonistas dopaminérgicos, y en pacientes con pérdida visual persistente resistente al tratamiento farmacológico. A veces los tumores grandes con hiperprolactinemia leve son prolactinomas atípicos peor diferenciados, por lo que son menos sensibles a tratamiento con agonistas dopaminérgicos y más susceptibles al tratamiento quirúrgico4,13. La interrupción del tratamiento farmacológico en los macroadenomas es más controvertida; se puede considerar sólo en tumores de 1-1,5 cm con normoprolactinemia mantenida durante al menos 2 años y sin evidencia de tumor durante el tratamiento. En los restantes macroadenomas se debe mantener el tratamiento de forma permanente incluso tras la menopausia, ya que existe un alto riesgo de recurrencia de la hiperprolactinemia y de recrecimiento tumoral4.
Debemos hacer un diagnóstico diferencial entre tumores clínicamente no funcionales y grandes, que causan una modesta hiperprolactinemia (generalmente menor de 150 ng/ml) por compresión del tallo hipofisario y el macroprolactinoma (mayores de 250-300 ng/ml). Si nos encontramos valores en rango intermedio, debemos instaurar un tratamiento farmacológico de prueba e investigar la normalización de la concentración de PRL y la reducción del tamaño tumoral. Si no hay una clara reducción de ambas, ello va más a favor de la primera opción.
Con el uso cada vez más generalizado de la RM se detectan con relativa frecuencia imágenes hipointensas (adenomas pequeños no secretantes, quistes o infartos) que son indistinguibles de un microprolactinoma; si en esta situación existe una hiperprolactinemia leve, por ejemplo inducida por medicación, se corre el riesgo de interpretar la imagen como un microprolactinoma16. El diagnóstico diferencial es difícil y sólo el control evolutivo puede aclararlo.
El interés de nuestro caso radica en la dualidad de la causa subyacente de esta hiperprolactinemia. La paciente tomaba anticonceptivos y esto puede justificar el nivel de PRL en sangre y la galactorrea. Sin embargo, la presencia de un microadenoma hipofisario hizo recomendable la vigilancia posterior. Controles sucesivos de PRL sérica normales nos harían suponer que el hallazgo del microadenoma es casual (incidentaloma) y que el origen de la hiperprolactinemia es atribuible exclusivamente a los anticonceptivos. Niveles elevados mantenidos de PRL nos decantarían por el microadenoma como responsable del cuadro, pasando a valorar la utilidad de tratamiento médico inicialmente, y quirúrgico en función de la evolución de la enferma. Niveles mantenidos de PRL en rango medio-bajo con clínica de compresión del tallo hipofisario y hemianopsia bitemporal irían a favor de un adenoma no secretor de PRL. Sólo la evolución nos ayudará a realizar el diagnóstico.
El médico de Atención Primaria debe conocer la indicación de la solicitud de la determinación de PRL sérica, para una vez detectada, encauzar el diagnóstico2 y, si es necesario, derivar al endocrinólogo para el uso de técnicas no disponibles en el centro de salud y el inicio de su tratamiento.
AGRADECIMIENTOSLos autores desean expresar su agradecimiento a la Dra. Guillermina Montoliu Fornas, jefa de sección de Resonancia Magnética del Hospital Universitario La Fe (Valencia), por su ayuda en la elaboración de este trabajo.
Correspondencia: M.Á. Rosero Arenas. Avda. Dr. Peset Aleixandre, 81, puerta 21. 46007 Valencia. España. Correo electrónico: mangelesymangel@hotmail.com
Recibido el 12-07-2007; aceptado para su publicación el 23-04-2008.