La granulomatosis eosinofílica con poliangitis (GEPA) es una enfermedad sistémica poco frecuente, caracterizada por rinitis alérgica, asma y eosinofilia en sangre periférica. Su prevalencia en Europa es de 10,7-14 casos/millón de habitantes1.
Presentamos el caso de un paciente de 47 años con antecedentes de alergia a aspirina y sulfamidas, déficit psicomotor connatal leve, gastritis crónica y trastorno de ansiedad generalizada. Diagnosticado en octubre de 2019 de alergia a polen y epitelio de perro, rinosinusitis y poliposis nasosinusal. En diciembre de 2019 inicia asma bronquial. Recibe tratamiento con: ebastina 10mg/día, fluticasona 400mcg nasal/día, budesonida/formoterol (320/9)mcg/12h, lansoprazol 30mg/día, lorazepam 1mg/8h y fluoxetina 10mg/día.
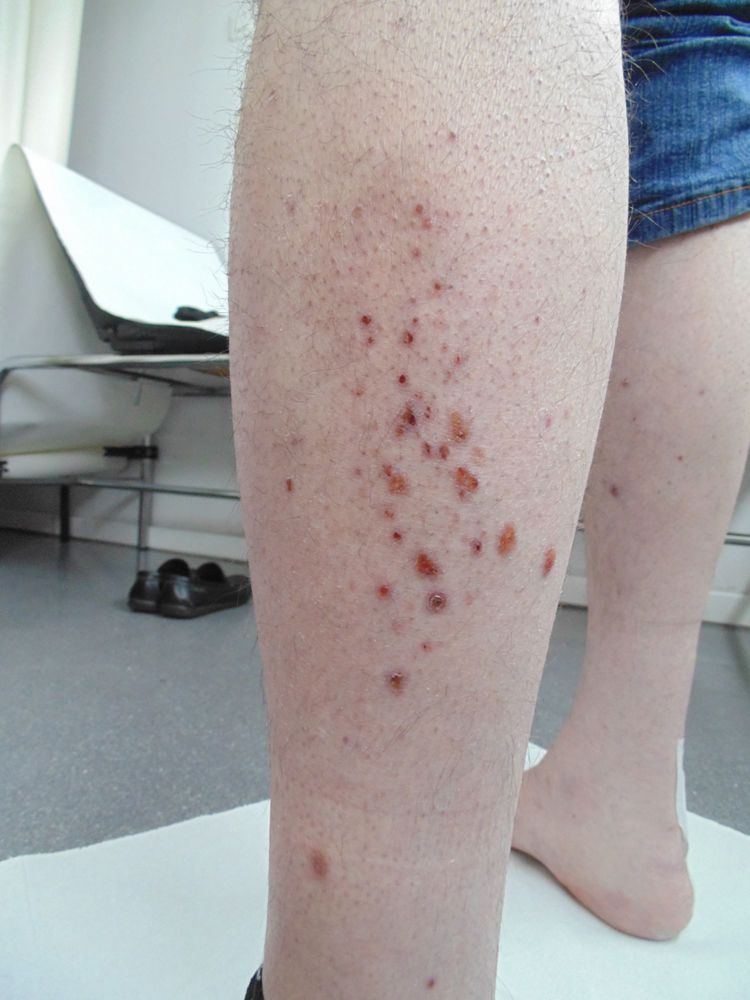
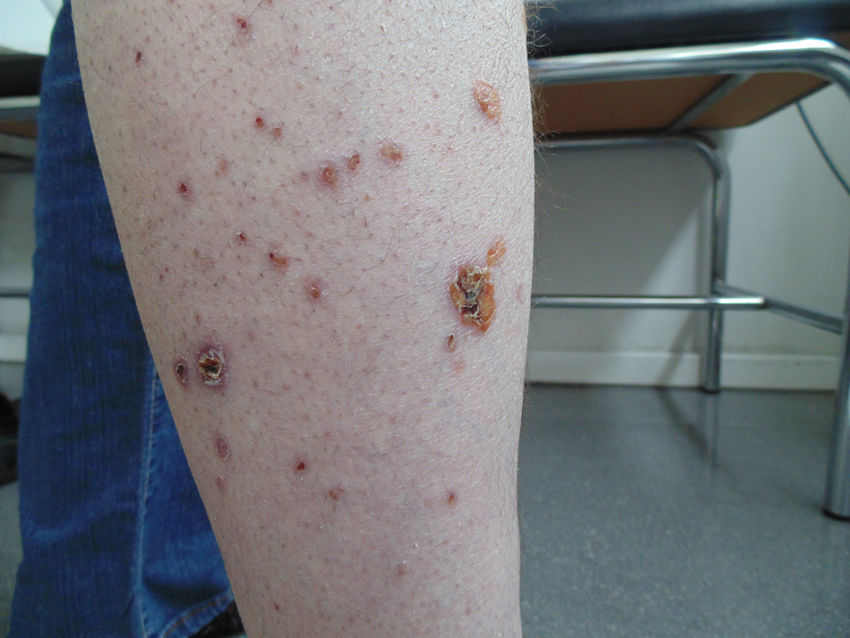
Consulta en febrero de 2021 por inicio de mialgias en extremidades superiores e inferiores, con exploración normal. Un mes después solicita visita domiciliaria por empeoramiento y aparición de lesiones papulosas purpúricas dispersas en tronco, extremidades y cuero cabelludo (figs. 1, 2). Refiere haberse realizado 2 analíticas recientes, la primera solicitada en control de Salud Mental y la segunda en Hematología, tras derivación desde Salud Mental por alteraciones analíticas. Se accede a la historia clínica hospitalaria. Se constata una eosinofilia (41,6% con 7,3×103 eosinófilos absolutos) que se confirma en el segundo análisis (42,3% y 8,5×103 eosinófilos). Otras alteraciones a destacar son: PCR 5,73mg/dL; GOT 86U/L; IgE 646,6KU/L y dímero D 2960ng/mL (que podría reflejar un estado de hipercoagulabilidad), con función renal, marcadores de daño cardiaco, ANA y resto de inmunglobulinas normales. Queda pendiente resultado de anticuerpos anticitoplasma de neutrófilos (ANCA). Ante estos hallazgos (eosinofilia), los antecedentes personales del paciente (asma, rinusinusitis crónica y poliposis nasal) y los nuevos síntomas por los que consulta (mialgias con GOT elevada como posible manifestación de miositis y lesiones en piel), se plantea el diagnóstico de una enfermedad multisistémica (posible GEPA) y se deriva a dermatología para filiar las lesiones. Se realiza biopsia, que muestra una zona de necrosis epidérmica, con un área de pústula constituida por linfocitos, polinucleares y restos necróticos. En dermis superior y media aparece un intenso infiltrado inflamatorio constituido por polinucleares, muy frecuentes eosinófilos, linfocitos y plasmocitos con afectación preferentemente perivascular. Los ANCA-MPO resultan positivos. Con impresión diagnóstica de GEPA, se remite al paciente a Medicina Interna para valoración del tratamiento y ampliación de estudios pertinentes. Se inicia tratamiento con glucocorticoides vía oral, con mejoría clínica y normalización de datos de actividad analítica.
La vasculitis granulomatosa con poliangitis (GEPA) forma parte del grupo de vasculitis de pequeño y mediano vaso, asociadas a ANCA. Se diferencian 3 formas clínicas: granulomatosis con poliangitis (previamente conocida como granulomatosis de Wegener), granulomatosis eosinofílica con poliangitis (previamente síndrome de Churg-Strauss) y poliangitis microscópica. GEPA es la menos frecuente. Es importante realizar un diagnóstico temprano para evitar daños orgánicos irreversibles2–4.
La edad media al diagnóstico de GEPA son 40 años. Es infrecuente en mayores de 65, niños y adolescentes. La patogenia es incierta. Se creen implicados alteraciones del sistema inmunitario, factores genéticos y algunos medicamentos1.
La enfermedad se desarrolla en 3 fases, aunque no siempre se distinguen claramente. La fase prodrómica se caracteriza por rinitis alérgica y asma. Puede preceder años a la fase vasculítica. En la fase eosinofílica aparece eosinofilia en sangre periférica e infiltración eosinofílica en múltiples órganos, sobre todo pulmón y tracto gastrointestinal. En la tercera fase o vasculítica, se desarrolla una vasculitis sistémica con afectación multiorgánica, que puede acompañarse de síntomas constitucionales inespecíficos (pérdida de peso, fiebre, astenia y malestar general). El asma está presente en más del 90% de casos. Otras manifestaciones pulmonares serían opacidades pulmonares con eosinofilia, derrame pleural y nódulos. La afectación otorrinolaringológica incluye poliposis nasal, rinitis alérgica, sinusitis crónica y otitis serosa media. La piel es el segundo órgano más afectado después del pulmón. Se presenta con nódulos subcutáneos, púrpura palpable de predominio en extremidades inferiores, a veces asociada a pequeñas ulceraciones. La implicación cardiaca es responsable de la mitad de las muertes debidas a GEPA. Pueden darse insuficiencia cardiaca, alteraciones del ritmo o pericarditis. Hay aumento del riesgo tromboembólico. La neuropatía periférica se presenta como mononeuropatía múltiple. Puede afectarse el sistema nervioso central. El compromiso renal se da en el 45% de casos en forma de hematuria, proteinuria y lesión renal. La gastritis eosinofílica se presenta con dolor abdominal, diarrea, sangrado y colitis. A nivel musculoesquelético encontramos mialgias y poliartralgias migratorias, miositis y artritis5.
Las exploraciones complementarias a solicitar según la sospecha diagnóstica y para valoración de afectación orgánica, serán hemograma completo, reactantes de fase aguda, ANCA, bioquímica con función renal, sistemático y sedimento de orina. Otras pruebas a considerar serían IgE, proteinograma, factor reumatoide, ANA, complemento sérico, troponina y péptido natriurético. Se pedirá radiografía de tórax, electrocardiograma y biopsia si es posible, seleccionando el lugar más accesible. Los principales hallazgos histológicos son infiltración eosinofílica, áreas extensas de necrosis, vasculitis eosinofílica de células gigantes, especialmente de pequeñas arterias y venas y granulomas intersticiales y perivasculares. En función de los resultados, se ampliarán estudios1,4,5.
El Colegio Americano de Reumatología estableció 6 criterios diagnósticos de GEPA. La presencia de 4 o más se considera diagnóstica (85% sensibilidad y 99,7% especificidad). Los criterios son la presencia de asma, eosinofilia en sangre periférica mayor a 10%, mononeuropatía o polineuropatía, infiltrados pulmonares transitorios, anomalías de senos paranasales y eosinofilia extravascular en la biopsia3,5. Una vez realizado el diagnóstico, se debe evaluar la posible afectación renal, cardiaca, gastrointestinal o del sistema nervioso, ya que se asociaría a peor pronóstico. El diagnóstico diferencial incluirá la enfermedad respiratoria exacerbada por aspirina, neumonía eosinofílica crónica, aspergilosis broncopulmonar alérgica, síndrome hipereosinofílico, otras vasculitis y otras enfermedades eosinofílicas5.
El primer paso en el manejo de GEPA es evaluar la actividad de la enfermedad con escalas como FFS (five-factors Score) y BVAS (escala de actividad de vasculitis de Birmingham)2,4,6. El tratamiento depende de la severidad de la enfermedad y del órgano afectado. Existen 2 fases de tratamiento. En la fase de inducción se utilizan glucocorticoides vía sistémica. La mayoría de los pacientes remiten solo con corticoides, pero si hay afectación severa, requerirán añadir ciclofosfamida, azatioprina o metotrexato. En la segunda fase o mantenimiento, se utilizarán glucocorticoides a bajas dosis junto a inmunosupresores como azatioprina. Otras alternativas serían metotrexato, leflunomida, anticuerpos monoclonales anti-interleuquina 5, micofenolato de mofetilo, inmunoglobulinas intravenosas, hidroxiurea, rituximab, interferón alfa, terapia anti-IgE o plasmaféresis6.
Para el enfoque diagnóstico de este caso ha sido fundamental la atención longitudinal propia de atención primaria y la colaboración de atención especializada.
Conflicto de interesesNinguno.
FinanciaciónNinguna.
Consideraciones éticasPara la publicación del caso se ha contado con el consentimiento firmado del paciente y se han seguido los protocolos del centro de trabajo para la publicación de datos del paciente y se ha respetado la privacidad.