Los linfomas primarios de las glándulas salivales son neoplasias muy poco frecuentes, comprometiendo principalmente la parótida1. Ante una hipertrofia parotídea debemos tener en cuenta esta enfermedad, ya que requiere un estudio histológico para su correcto diagnóstico.
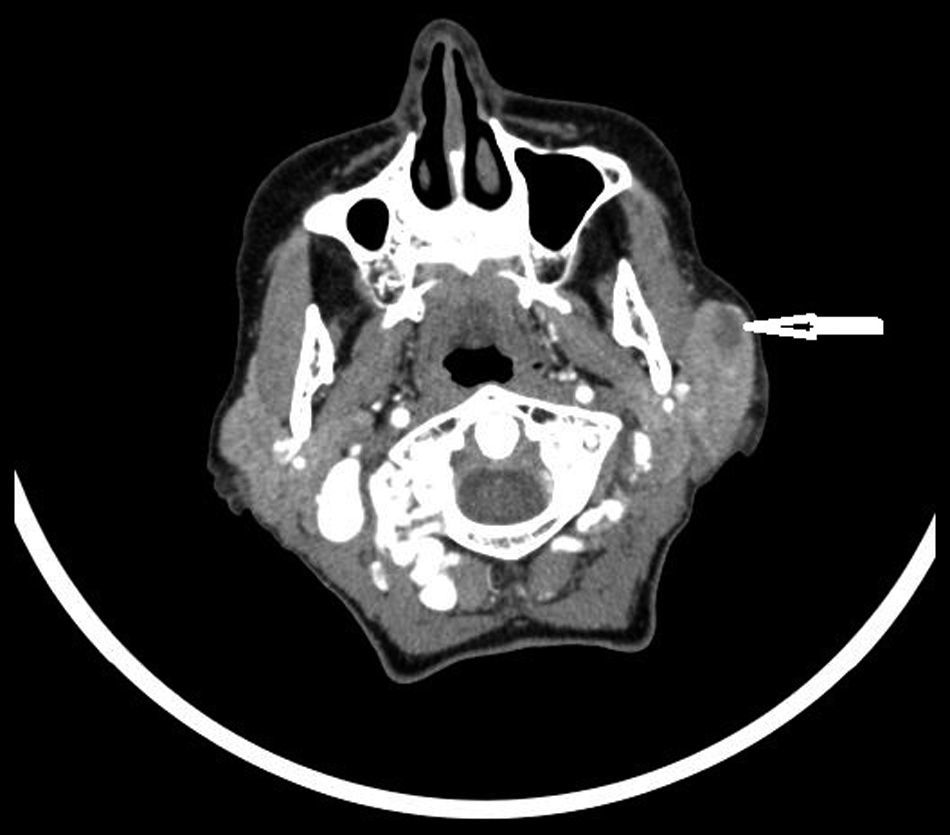
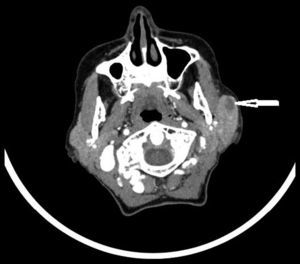
Presentamos el caso de una mujer de 68 años, exfumadora, intervenida de varices en miembros inferiores, sin otros antecedentes de interés. Consultó por tumefacción parotídea izquierda de 2 meses de evolución, no dolorosa, sin signos inflamatorios ni fiebre. Negaba historia de sequedad bucal, sudoración nocturna o pérdida de peso. Presentaba buen estado general y se palpaba una adenopatía supraclavicular izquierda con exploración de orofaringe y tiroides normal. No tenía adenopatías en otros territorios ni organomegalias. En una analítica inicial, hemograma con velocidad de sedimentación globular, proteína C reactiva y bioquímica completa eran normales, inmunoglobulina G de citomegalovirus, virus herpes simple, virus de Epstein-Barr (VEB), virus varicela zoster y virus de parotiditis positiva, con inmunoglobulina M negativa para todos ellos, y serología del virus de la inmunodeficiencia humana, virus de hepatitis B y C negativa. La radiografía de tórax era normal. Se realizó una tomografía axial computarizada (TAC) craneocervical que mostró una lesión en el lóbulo superficial de la parótida izquierda de 27×20mm (fig. 1) y una punción con aguja fina (PAAF) que aisló células con positividad para los marcadores CD15 y CD30. Con la sospecha de linfoma se solicitó una biopsia por escisión de la adenopatía, donde se visualizó una proliferación neoplásica compuesta por células de Reed-Sternberg con expresión de CD15, CD30, PAX-5 débil, así como negatividad para VEB-LMP1. Por lo tanto se diagnosticó de linfoma de Hodgkin clásico con patrón de celularidad mixta primario de la glándula parótida izquierda. El estudio de extensión mediante tomografía de emisión de positrones y TAC determinó estadio IIA, y recibió tratamiento con quimioterapia y radioterapia consiguiendo la remisión completa.
Los linfomas son procesos linfoproliferativos malignos que afectan a los ganglios linfáticos. Ocasionalmente se puede presentar como enfermedad extranodal, generalmente en el aparato gastrointestinal, sin embargo la afectación de la glándula parótida es muy poco frecuente2. La mayoría de estos linfomas son no Hodgkin, de los cuales el folicular y tipo MALT son los más frecuentes. La incidencia de linfoma de Hodgkin en la parótida es extremadamente rara, corresponde al 4% de los procesos linfoproliferativos que afectan a la glándula, y se piensa que el compromiso del parénquima es secundario a la afectación de los ganglios intraglandulares3.
Se considera primario cuando la masa tumoral es la primera manifestación, independientemente de que haya afectación ganglionar simultánea clínicamente oculta, como sucedió en este caso. La variante histológica que predomina en esta localización es la forma clásica tipo esclerosis nodular, siendo muy pocos los casos descritos de celularidad mixta4.
En cuanto a la etiopatogenia no está esclarecido ningún factor etiológico específico. La relación más importante es la descrita con enfermedades autoinmunes que afectan las glándulas salivales, principalmente el síndrome de Sjögren, que se asocia con linfoma no Hodgkin tipo MALT, aunque también hay algún caso relacionado con linfoma de Hodgkin5, y puede aumentar el riesgo de enfermedad hasta 40 veces. Otro factor etiológico puede ser el VEB, que ha sido identificado como inductor de linfoproliferación. El hecho de que la inmunoglobulina G del VEB sea positiva no evidencia relación causal, solo implica contacto pasado con el virus. Sí lo implicaría el hallazgo de proteínas del virus, latentes en la membrana de las células tumorales (VEB-LMP1), que resultó negativo en este caso.
En cuanto a los diagnósticos diferenciales6 debemos tener en cuenta otros tumores, procesos inflamatorios de tipo autoinmunitario o la sialoadenitis crónica esclerosante (tumor de Kuttner) cuyo aspecto histológico es muy parecido. Sin embargo es más importante el diagnóstico diferencial con procesos reactivos no neoplásicos, ya que son mucho más frecuentes, y el tratamiento difiere completamente. En principio sospecharemos de un linfoma cuando encontremos síntomas B, historia previa de linfoma, enfermedades autoinmunes, inmunosupresión o el hallazgo de adenopatías7. El diagnóstico se basa en la visualización de células de Reed-Sternberg. La PAAF muchas veces es inadecuada por su alta tasa de falsos negativos y se debe recurrir a la biopsia8. En este caso se realizó una PAAF de la glándula salival, y la biopsia se tomó de la adenopatía, que se considera el procedimiento más adecuado cuando hay afectación ganglionar9.
Los linfomas de Hodgkin de la glándula parótida tienen mejor pronóstico que los no Hodgkin y que los que afectan a otras localizaciones, con una supervivencia a los 5 años mayor del 90%. La edad y el estadio se consideran los mejores factores pronóstico, y parece que el tipo histológico no influye tanto10. El tratamiento se basa en protocolos de quimioterapia y radioterapia.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores expresan que no hay conflicto de intereses al redactar el manuscrito.