Los bifosfonatos, análogos estables de los pirofosfatos inorgánicos, han demostrado su eficacia para el tratamiento de las lesiones osteolíticas asociadas a metástasis óseas o al mieloma múltiple, la hipercalcemia maligna, la enfermedad de Paget y la osteoporosis. Numerosas publicaciones durante los últimos años consideran que la osteonecrosis de los maxilares está asociada al tratamiento con bifosfonatos. El manejo diagnóstico y terapéutico de los pacientes con osteonecrosis de los maxilares es de una enorme dificultad. Es importante que los pacientes sean informados del riesgo de presentar esta complicación para tener la oportunidad de recibir procedimientos dentales previos al inicio del tratamiento. Las medidas preventivas deben realizarse antes, durante y después del tratamiento con bifosfonatos. Ante una osteonecrosis de los maxilares establecida, la actitud debe ser conservadora: enjuagues con clorhexidina y antibióticos. El tratamiento quirúrgico debe reservarse para aquellos pacientes que presenten síntomas.
The bisphosphonates are stable inorganic pyrophosphate analogs that have demonstrated their efficacy in treatment of osteolytic lesions associated with bony metastases, and multiple myeloma, malignant hypercalcemia, Paget's disease, and osteoporosis. Several publications within the last few years have suggested that osteonecrosis of the jaw is associated with bisphosphonate therapy. The diagnosis and management strategies of the patients with bisphosphonate-related osteonecrosis of the jaw is very difficult. It is important for patients to be informed of the risk of this complication, so that they have the opportunity to assess the need for dental treatment before starting therapy. Preventive measures must be taken before, during, and after treatment with bisphosphonates. If osteonecrosis of the jaw is present, management should be conservative: oral chlorhexidine and antibiotics. Surgical treatment should be reserved for those patients who are symptomatic.
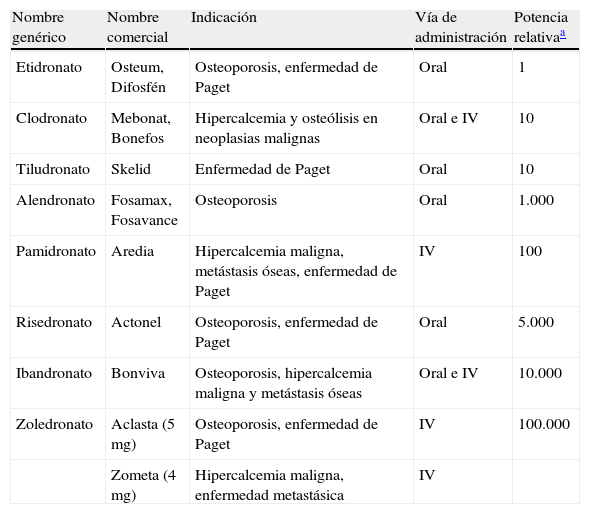
Los bifosfonatos (BF) son análogos del pirofosfato (P-O-P) que se caracterizan por la presencia de 2 átomos de fósforo unidos a un átomo de carbono (P-C-P), lo que les confiere una gran resistencia a la hidrólisis enzimática y les permite unirse fuertemente a la hidroxiapatita de la matriz mineralizada. Los BF se incorporan al hueso, donde permanecen largo tiempo: se calcula que la vida media del alendronato es de unos 10 años1. Los BF de uso clínico disponibles en nuestro país aparecen reflejados en la tabla 1. Su mecanismo de acción se basa en la inhibición de la reabsorción ósea mediante la inhibición de la actividad osteoclástica2–5. También tienen un efecto inhibidor de la proliferación celular tumoral y de la angiogénesis5–8. Se usan en la osteoporosis, la enfermedad de Paget, la osteogénesis imperfecta, las lesiones osteolíticas asociadas a metástasis óseas o al mieloma múltiple y en la hipercalcemia maligna2,5,8–11.
Bifosfonatos de uso clínico comercializados en España
| Nombre genérico | Nombre comercial | Indicación | Vía de administración | Potencia relativaa |
| Etidronato | Osteum, Difosfén | Osteoporosis, enfermedad de Paget | Oral | 1 |
| Clodronato | Mebonat, Bonefos | Hipercalcemia y osteólisis en neoplasias malignas | Oral e IV | 10 |
| Tiludronato | Skelid | Enfermedad de Paget | Oral | 10 |
| Alendronato | Fosamax, Fosavance | Osteoporosis | Oral | 1.000 |
| Pamidronato | Aredia | Hipercalcemia maligna, metástasis óseas, enfermedad de Paget | IV | 100 |
| Risedronato | Actonel | Osteoporosis, enfermedad de Paget | Oral | 5.000 |
| Ibandronato | Bonviva | Osteoporosis, hipercalcemia maligna y metástasis óseas | Oral e IV | 10.000 |
| Zoledronato | Aclasta (5mg) | Osteoporosis, enfermedad de Paget | IV | 100.000 |
| Zometa (4mg) | Hipercalcemia maligna, enfermedad metastásica | IV |
IV: intravenosa.
A partir del año 2003 se empiezan a publicar un número creciente de pacientes tratados con estos fármacos que presentan una «osteonecrosis de los maxilares», lo que se denomina osteonecrosis de los maxilares relacionada con los BF (OMRB)2,4,7,12–22. Este inusitado interés se debe a las enormes dificultades del manejo de esta entidad, por lo que se están publicando una gran cantidad de artículos que intentan establecer pautas o recomendaciones e incluso estrategias y protocolos para su diagnóstico, prevención y tratamiento1,3–6,8–11,14,21,23–26.
En la actualidad, al menos académicamente, se puede hablar de 2 entidades con diferentes grados de información científica: la OMRB en relación con la administración intravenosa (IV) de estos medicamentos para pacientes oncológicos (pamidronato y zoledronato) y la OMRB en relación con la administración oral de los mismos (aquí se incluyen también los BF IV con las indicaciones clásicas de los orales: osteoporosis, enfermedad de Paget, etc.). Para el primer grupo las estrategias de prevención y tratamiento empiezan a estar consolidadas, mientras que para el segundo se precisará de una mayor documentación científica para alcanzar este objetivo9.
DefiniciónCon objeto de diferenciar a la OMRB de otras enfermedades que cursan con exposiciones óseas y retrasos en la cicatrización de los procesos alveolares, los pacientes deben cumplir las 3 características siguientes10,11:
- 1.
Tratamiento actual o previo con BF.
- 2.
Hueso necrótico expuesto en la región maxilofacial que persiste más de 8 semanas.
- 3.
No antecedentes de radioterapia en la región maxilofacial.
Las entidades que deben considerarse dentro del diagnóstico diferencial son: osteítis alveolar, sinusitis, gingivitis y periodontitis, caries, enfermedad periapical y alteraciones de la articulación temporomandibular10,11.
EpidemiologíaLa incidencia de la OMRB en pacientes oncológicos que reciben BF IV oscila entre el 0,8 y el 12%10,11,25,27 y con los BF orales entre el 0,01 y el 0,04%9–11,27. Aunque se ha descrito en una gran variedad de tumores, el mieloma múltiple es el más frecuente, seguido del cáncer de mama9,21,28,29. La edad media es de 65,5 años, encontrándose el pico de edad entre la séptima y octava década. La relación hombre/mujer es 2:2,6 e incluso 2:38,21,29. La mandíbula es el hueso más afectado1,4,21,29.
Entre los factores de riesgo (tabla 2), los más importantes son los relacionados con el fármaco, los factores locales (exodoncias y prominencias óseas) y algunos factores demográficos y sistémicos como la edad avanzada, raza caucásica, diagnóstico de cáncer y osteoporosis11,24,28.
Factores de riesgo de la osteonecrosis de los maxilares relacionada con el tratamiento con bifosfonatos
| 1. Relacionados con el fármaco |
| Potencia del bifosfonato |
| Vía de administración |
| Dosis acumulada |
| Duración de la terapia |
| 2. Factores de riesgo locales |
| Cirugía dentoalveolar |
| Exodoncias |
| Colocación de implantes |
| Cirugía periapical |
| Cirugía periodontal que implique daño óseo |
| Anatomía local |
| Mandíbula |
| Torus lingual |
| Línea milohioidea |
| Maxilar |
| Torus palatino |
| Enfermedad oral concomitante |
| 3. Factores demográficos y sistémicos |
| Edad avanzada |
| Raza caucásica |
| Diagnóstico de cáncer |
| Diagnóstico concomitante de osteopenia/osteoporosis |
| Otros posibles factores |
| Corticoterapia |
| Diabetes |
| Tabaquismo |
| Alcoholismo |
| Quimioterapia |
| Higiene oral deficiente |
| Anemia y talasemia |
| Malnutrición |
| Dislipidemia |
| Obesidad |
| Enfermedades del tejido conjuntivo |
| Coagulopatías |
| Inmunodeficiencias |
| Hipotiroidismo |
| Enfermedad de Gaucher |
| Lupus eritematoso sistémico |
| Terapia con estrógenos |
| Artrosis |
| 4. Factores genéticos |
| Gen del citocromo P450-2C |
| 5. Factores preventivos |
| Intervenciones dentales preventivas |
| Modificación de dosis de bifosfonato intravenoso |
El mecanismo exacto que lleva a la aparición de la OMRB todavía se desconoce. Parece estar causada por una falta de aporte vascular, de remodelado y de regeneración ósea. El principal problema en la OMRB es la incapacidad de los osteoclastos para remover, reparar o contener áreas de hueso enfermo o que ha cumplido con su vida útil, por lo que la capacidad de adaptación funcional del tejido óseo está disminuida5.
Manifestaciones clínicasLa OMRB se manifiesta clínicamente como una exposición ósea (hueso de color blanco amarillento) en la cavidad oral. Al principio, es asintomática, pero se convierte en sintomática cuando se genera una infección secundaria o un traumatismo en el tejido blando adyacente y/u opuesto. Pueden producirse pérdidas de piezas dentarias, inflamación de tejidos blandos, fístulas, dolor, disestesias, abscesos dentales, etc.1,3,26. Los síntomas pueden aparecer espontáneamente en el hueso o, más frecuentemente, en el sitio de una extracción dental previa23.
Pruebas complementariasLa más utilizada es la ortopantomografía, que en estadios precoces no aporta información. Posteriormente se ven áreas radiolúcidas y radioopacas, relacionadas con secuestros óseos e incluso destrucción ósea (osteólisis)5,9.
La tomografía computarizada y la resonancia magnética permiten un diagnóstico precoz y establecen la verdadera extensión de la osteonecrosis (estadio clínico)8,9.
Se recomienda la realización de cultivos microbiológicos y antibiograma5,9.
La biopsia ósea solo se hará si se sospecha que la lesión guarda relación directa con la enfermedad (neoplasia) que motivó la utilización IV de los BF9.
La determinación sérica del telopéptido c-terminal del colágeno tipo I (CTX) no es predictiva del desarrollo de OMRB a nivel individual, pero puede identificar a aquellos pacientes que se encuentran en zona de riesgo8:
- -
Si CTX<100pg/ml=riesgo alto.
- -
Si CTX entre 100 y 150pg/ml=riesgo moderado.
- -
Si CTX>150pg/ml=riesgo bajo.
Se basa en el cumplimiento de los criterios de la American Association of Oral and Maxilofacial Surgeons (AAOMS) descritos en la definición10,11.
Tratamiento y prevenciónEn la actualidad, no se dispone de un tratamiento eficaz y definitivo de la OMRB3,26. El tratamiento de la OMRB establecida es difícil, requiere largo tiempo, es invasivo y de pronóstico incierto3,5. Por lo tanto, es muy importante encaminar todos los esfuerzos a mejorar la prevención, comenzando por la identificación de aquellos pacientes con mayor riesgo de desarrollarla3. Las medidas preventivas y terapéuticas se basan en series de casos de pacientes y en opiniones de expertos.
PrevenciónPacientes tratados con bifosfonatos intravenososDado que no se han publicado casos de OMRB por debajo de los 6 meses de administración del BF IV, hay autores9 que proponen que no se contraindiquen los procedimientos invasivos que puedan ser necesarios durante los 3 primeros meses de tratamiento.
Antes y durante los 3 primeros meses de la administración del tratamiento IV en pacientes asintomáticos.
El objetivo en este grupo de pacientes es minimizar el riesgo de desarrollar la OMRB. Se debe retrasar el inicio de la terapia con BF hasta que la salud dental sea óptima10,11.
Se debe informar al paciente de los riesgos relacionados con la cirugía dentoalveolar una vez que se ha instaurado el tratamiento y de la persistencia del riesgo un largo periodo de tiempo después del mismo9,24.
Se debe educar al paciente sobre la importancia del mantenimiento de la higiene bucal y acudir lo más pronto posible a su odontólogo ante cualquier síntoma5,9,19.
Se deben realizar todos los tratamientos odontológicos no invasivos apropiados para alcanzar un buen nivel de salud oral, los cuales pueden realizarse durante la administración del BF9–11,24.
Si el paciente presenta focos infecciosos, tanto dentoalveolares como periodontales, deben ser tratados de inmediato y deben ser extraídas todas las piezas dentales de pronóstico incierto10,11,24,25. Se recomienda esperar 14 a 21 días entre la exodoncia y el inicio del BF IV para que se cure la misma9–11.
La colocación de implantes intraóseos es un tema controvertido2,3,14,31,32. No se recomienda la colocación de implantes antes de la administración IV de BF si se espera que no haya finalizado el periodo de osteointegración en ese momento9.
Si el paciente precisa una cirugía dentoalveolar debe ser completada en este momento10,11,26.
Se debe evaluar y corregir la posible existencia de traumatismos protésicos9–11,24,25.
Durante la administración del tratamiento IV (después de los 3 primeros meses de tratamiento) en pacientes asintomáticosSe recomiendan revisiones odontológicas periódicas cada 3-4 meses según unos autores24,26 o cada 6 meses según otros9,25,26. Es de capital importancia mantener una buena higiene oral para prevenir una enfermedad dental que pueda requerir cirugía dentoalveolar10,11,26.
Debe evitarse la realización de cualquier tipo de cirugía oral que dañe el hueso9–11,24.
Ante la presencia de un foco infeccioso, el tratamiento de los conductos debe ser la primera indicación, procurando un mínimo traumatismo periapical y periodontal, con cobertura antibiótica9.
Si hay piezas dentales inviables, debe extraerse la corona y tratar con endodoncia las raíces10,11,25,26.
No deben realizarse implantes dentales en los pacientes oncológicos expuestos a los BF IV más potentes (zoledronato y pamidronato) o administrados con mucha frecuencia (4 a 12 veces al año)10,11.
Después del tratamiento intravenoso en pacientes asintomáticos9Deberá evitarse la realización de cualquier tipo de cirugía oral, al menos, durante un periodo no inferior a los 10 años de la última administración del BF. Aunque es cierto que se ha demostrado la presencia de zoledronato hasta 12 años después, no hay datos al respecto en la literatura médica, por lo que este punto permanece controvertido.
El odontólogo deberá motivar y mantener un riguroso control de la salud oral del paciente durante largo tiempo.
Pacientes tratados con bifosfonatos oralesAntes de la administración del bifosfonato oralSe debe informar y recomendar a los pacientes evaluar su salud oral y los especialistas en salud oral tienen 3 años para poder realizar el tratamiento que consideren necesario para alcanzar el óptimo estado de salud oral9–11.
Pacientes asintomáticos con menos de 3 años de tratamiento con bifosfonato oral y sin factores de riesgoSe puede realizar cualquier tipo de tratamiento quirúrgico y rehabilitador, pero se deberá obtener un consentimiento informado que incluya el riesgo de desarrollar OMRB y se deberá controlar periódicamente (al menos anualmente) el estado de salud oral9–11.
Pacientes asintomáticos con menos de 3 años de tratamiento con bifosfonato oral y con factores de riesgo (glucocorticoides y edad por encima de 70 años)Se recomienda la suspensión del BF oral durante, al menos, 3 meses antes de la cirugía oral y no se debe reiniciar hasta que haya concluido la cicatrización de la herida quirúrgica9–11, además del consentimiento informado y del control periódico, al menos anual, del estado de salud oral9.
La utilidad del CTX9–11 y las vacaciones terapéuticas del BF oral10,11 precisan de mayor evidencia científica para su recomendación.
Pacientes asintomáticos con más de 3 años de tratamiento con bifosfonato oral, con o sin factores de riesgo (gucocorticoides y edad por encima de 70 años)Las mismas recomendaciones que en el grupo precedente9–11.
Tratamiento de la osteonecrosis de los maxilares relacionada con los bifosfonatosLas pautas generales del tratamiento de la OMRB son: higiene oral y colutorios con clorhexidina al 0,12%, tratamiento antibiótico (tabla 3) de forma continua o intermitente y evitar cirugía o desbridamiento amplio en la medida de lo posible12,19.
Antibióticos utilizados en el tratamiento de la osteonecrosis de los maxilares relacionada con el tratamiento con bifosfonatos
| De primera elección |
| Amoxicilina 500mg/6h, oral |
| Penicilina V-K 500mg/6h, oral |
| Amoxicilina/ácido clavulánico 2.000/125mg/12h, oral |
| Alérgicos a la penicilina |
| Ciprofloxacino 500mg/12h, oral |
| Levofloxacino 500mg/24h, oral |
| Eritromicina 400mg/8h, oral |
| Azitromicina 250mg/24h, oral |
| Clindamicina 300mg/8h, oral |
| Doxiciclina 100mg/24h, oral |
| Si la infección es resistente o muy sintomática |
| Se añade al tratamiento previo Metronidazol 500mg/8h, oral |
| Si la infección es severa (celulitis): paciente ingresado |
| Amoxicilina-clavulánico 1.000/200mg cada 6h, IV |
| + |
| Metronidazol 500mg/8h, IV |
| En caso de alergia a penicilina |
| Ciprofloxacino 500mg/12h, IV |
| + |
| Metronidazol 500/8h, IV |
| Eritromicina 400/8h, IV |
| + |
| Metronidazol 500mg/8h, IV |
IV: intravenoso.
Se deben evitar los procedimientos quirúrgicos dentoalveolares electivos en los pacientes con OMRB establecida, porque el área quirúrgica puede llevar a una nueva área de hueso necrótico expuesto10,11.
Otras modalidades terapéuticas utilizadas en algunos casos son: el oxígeno hiperbárico10,11,20,31, plasma rico en plaquetas con factores de crecimiento5,11, proteína morfogenética ósea11, hormona paratiroidea5,11 y laserterapia de bajo nivel24.
Hasta el momento actual, no hay evidencias claras de que la suspensión del BF IV mejore la evolución del cuadro clínico de la OMRB19,24. La suspensión del tratamiento con los BF IV no ofrece beneficios a corto plazo10,11. Sin embargo, si las condiciones sistémicas lo permiten, la interrupción a largo plazo puede ser beneficiosa en la estabilización de los sitios de OMRB ya establecidos, en la reducción del riesgo de desarrollarla en nuevos sitios y en la reducción de los síntomas clínicos10,11,19,24. Los riesgos y beneficios de continuar con la terapia con BF deben ser consensuados entre el oncólogo, el cirujano oral y maxilofacial y el paciente10,11.
La AAOMS10,11 considera que la suspensión del BF oral en los pacientes con OMRB se asocia a una mejoría clínica gradual de la misma. Por lo tanto, si las condiciones sistémicas del paciente lo permiten, se debe consensuar la suspensión del BF oral con el médico prescriptor y con el paciente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.