Pocos hitos médicos, en particular en las enfermedades infecciosas, han tenido la transcendencia e impacto de la vacunación en cuestiones de longevidad, ahorro económico y calidad de vida. Desde que se aislase, en enero de 2020, el betacoronavirus que finalmente se denominó SARS-CoV-2, la vacuna frente a este nuevo virus y su expansión se ha convertido en una necesidad y prioridad mundial. Para observar un esfuerzo internacional similar, quizás, nos tenemos que remontar hasta el siglo XVIII, periodo de especial azote de la viruela. En este sentido, cabe mencionar la figura de Edward Jenner en la creación de la «vacuna». Pero no menos importante fue la figura de Xavier de Balmis, cirujano militar español, director de la Real Expedición Filantrópica de la Vacuna (REFV), 1803-1810, cuya meta era propagar la vacuna contra la viruela a los territorios hispanos de ultramar. Este hecho representa la primera campaña mundial de vacunación1.
Las diferentes vacunas frente a SARS-CoV-2 han demostrado, en numerosos estudios, ser seguras y eficaces. Los efectos adversos recogidos en los ensayos clínicos fueron de carácter leve. En estos estudios (vacuna ChAdOx1 nCoV-19 [AZD1222]) no se recoge la vasculitis leucocitoclástica cutánea (VLC) como efecto adverso de la vacuna2. En la literatura consultada (buscadores PubMed y Medline) hemos encontrado tan solo una referencias bibliográfica acerca de VLC inducida por vacuna frente a SARS-CoV-2 (palabras claves leukocytoclastic vasculitis, vaccine COVID-19)3.
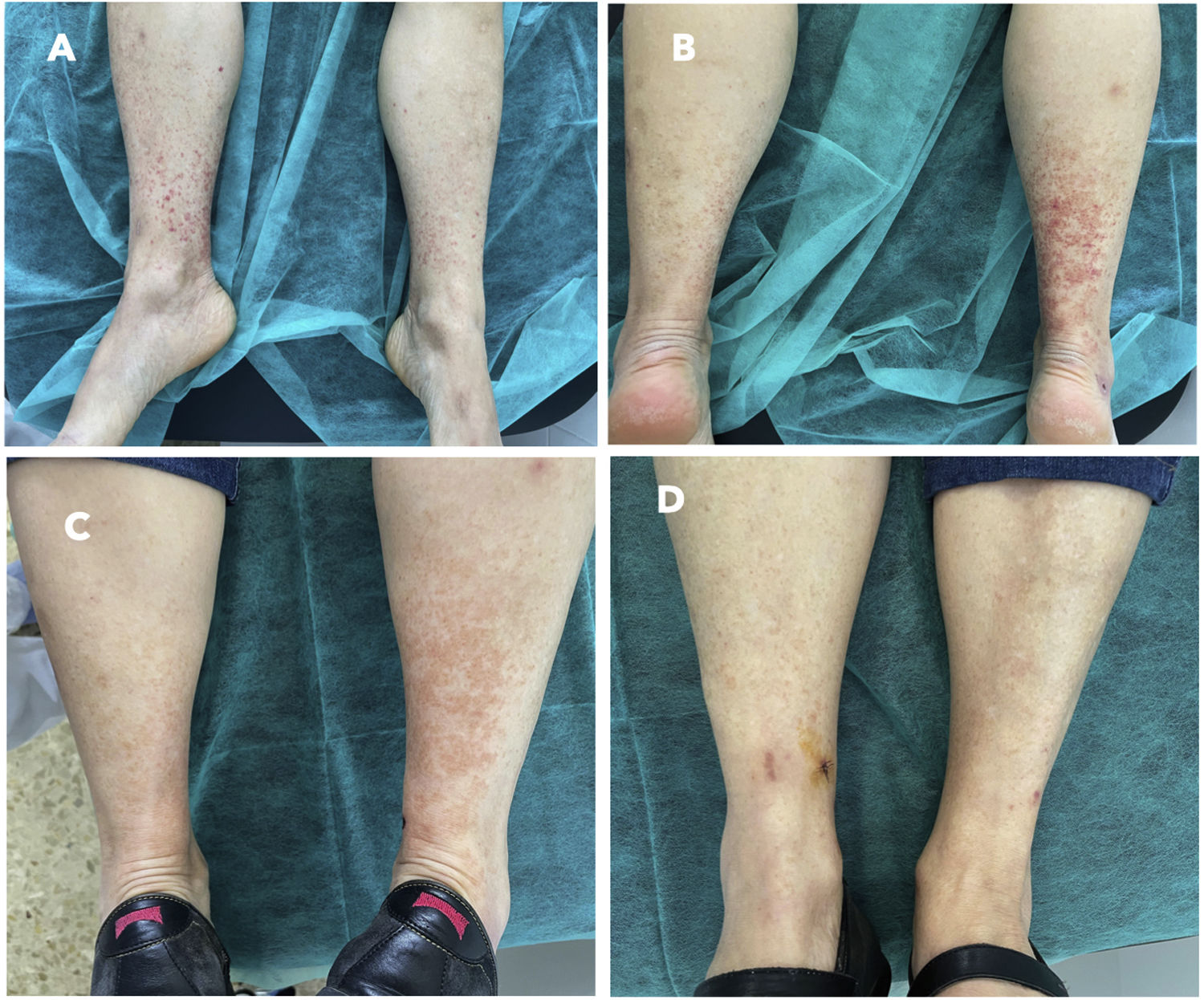
Mujer de 70 años con antecedentes de enfermedad de Parkinson en tratamiento con ropirinol, y levodopa/carbidopa. Presentaba una excelente situación basal, era independiente para las actividades básicas de la vida diaria (índice de Barthel: 100/100) y no tenía deterioro cognitivo (Mini Mental State Examination [MMSE] 30/30). Consultó por lesiones purpúricas en extremidades inferiores, cuatro días antes se había inoculado primera dosis de vacuna ChAdOx1 nCoV-19 (AZD1222). La exploración manifestó las lesiones purpúricas referidas (fig. 1a-b). Analíticamente destacaba una PCR de 35 mg/l (valor normal [vn] hasta 5 mg/l) y una VSG de 24 (vn hasta 20 mm). La orina de 24 horas no evidenció proteinuria. Los anticuerpos antinucleares (ANA), anticitoplasma de neutrófilos (ANCA), crioglobulinas y factor reumatoide (FR) fueron negativos. Las serologías frente a los virus A, B y C de la hepatitis, VIH, CMV, VEB, VHS I y II, Mycoplasma pneumoniae, Borrelia burgdorferi y Brucella fueron negativas. La biopsia cutánea confirmó la VLC. Se instauró tratamiento con antiinflamatorios no esteroideos (AINE) con desaparición de las lesiones (fig. 1 c-d). Tras este episodio, la paciente rehusó la administración de la segunda dosis y el efecto adverso fue comunicado al sistema de farmacovigilancia de medicamentos de uso humano.
La VLC es el tipo más común de vasculitis cutánea en el adulto, con una incidencia de 15 a 38 casos por 1.000.000 habitantes/año. En cuanto a la etiología, se han descrito causas farmacológicas, infecciosas, neoplásicas y autoinmunes. Aunque en un porcentaje de casos, que oscila del 3 al 72%, no se encuentra ninguna causa desencadenante4. La inmunización frente a distintos virus (virus influenza, VHB y virus del papiloma humano) ya se había postulado como causa desencadenante de VLC. La inmunización que acumula mayor número de casos de VLC tras su administración es la vacuna frente al virus de la influenza con 43 casos5.
En cuanto a la vacuna frente a SARS-CoV-2 se han descrito tan solo dos casos de vasculitis tras su administración, uno de ello resultó ser una VLC y el otro una vasculitis IgA. En el caso de la VLC, se trataba de una mujer con antecedente de artritis psoriásica y VLC, aunque no había presentado ningún brote en los dos años previos.
Se desconoce el mecanismo fisiopatológico, pero quizás se deba a una activación inmunológica anormal con antígenos de la vacuna que promueven el desarrollo de anticuerpos y la deposición de complejos inmunes. En el momento actual, no existen datos en los ensayos clínica ni estudios prospectivos sobre esta posible complicación y, mucho menos, sobre su pronóstico. La posibilidad de un nuevo rebrote tras la administración de una segunda o tercera dosis, sumado a la falta de experiencia acerca de una eventual evolución a afectación sistémica, debería hacernos balancear, con especial cuidado, el riesgo/beneficio de la administración de la segunda o tercera dosis3 o en todo caso, plantear un seguimiento a corto plazo para anticiparnos a eventuales complicaciones.
En conclusión, presentamos el primer caso de VLC secundaria a vacuna frente a SARS-CoV-2 en una paciente sin antecedentes de vasculitis, por lo que debería tenerse en cuenta como agente causal en el estudio etiológico de VLC en paciente con antecedentes vacunación reciente frente a SARS-CoV-2.
Para finalizar, nos parece relevante incidir en que la VLC secundaria a vacuna frente a SARS-CoV-2 puede sospecharse desde el primer contacto con el paciente por el antecedente de vacunación y un signo típico en la exploración física accesible a cualquier profesional.
Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes, y han solicitado los permisos correspondientes.
Conflicto de interesesLos autores declaran que no tienen ningún conflicto de intereses.