El sistema inmune del ser humano, así como el de todos los organismos animales, no es un conjunto de procesos estáticos, pues sufre cambios morfológicos y fisiológicos continuos a lo largo de la vida de la persona. Característicamente, se ha comprobado que las respuestas inmunes, tanto celulares como humorales, tienden a ser más efectivas en la pubertad y las etapas adultas iniciales, declinando de forma insidiosa con el envejecimiento, proceso que se ha dado en llamar «senescencia inmunológica» (inmunosenescencia) y que, sin lugar a duda, colabora en el aumento de la morbimortalidad en la tercera edad. El proceso de envejecimiento, según algunas investigaciones, acopla dos procesos separados pero convergentes en un momento determinado: los procesos considerados primarios, es decir, los inherentes a la especie y que tienen incluso lugar en individuos como parte del crecimiento, y los procesos secundarios, relacionados con la influir de agentes externos, tanto alimenticios como infecciosos o ambientales, estos últimos susceptibles de una teórica modificación y regulación. Otros investigadores han sugerido que la involución del timo en la etapa infantil y su continuación a lo largo de la vida ejerce un papel relevante en la regulación linfocitaria, y mediante algunas acciones específicas puede influir estados futuros de inmunosupresión o disregulación inmune en individuos susceptibles y predispuestos. Por otro lado, se ha descrito una tendencia a responder de manera insuficiente a los antígenos endógenos y por contrapartida, de forma exagerada o anómala a antígenos propios, lo que puede estar asociado al desarrollo de neoplasias y susceptibilidad a
infecciones oportunistas en las personas de edad avanzada.
A continuación, se exponen brevemente algunos de los mecanismos propuestos en la actualidad como relevantes en los procesos de envejecimiento o remodelado inmunológico y como resultado de la expresión clínica de las enfermedades en este grupo de edad. Las diversas alteraciones que a continuación se describen han sido extraídas de un número reducido de estudios, aunque en el futuro surgirán nuevos ensayos, que realicen una evaluación profunda de los procesos de envejecimiento y remodelado inmunológico.
Alteraciones del sistema inmune asociadas a la edad
Dos principales mecanismos han sido descritos como responsables del deterioro senil del sistema inmune: las alteraciones en la inmunidad celular y en la inmunidad humoral (tabla 1).
Inmunidad celular
Existen cada vez más evidencias obtenidas en modelos experimentales murinos de la presencia de un cierto grado de pérdida en la función de las células T, un incremento en la carga de células nulas (linfocitos no B-no T) y una probable disminución de las células existentes en fases G1 o fase S quedando limitadas para sus funciones inmunes.
A pesar de que no existen cambios importantes en el recuento total de leucocitos con la edad, se ha encontrado en algunos trabajos recientes que la expresión de estas células puede estar atenuada en la etapa senil. Por ejemplo, Potesio et al han documentado un considerable aumento de la expresión de la molécula relacionada con la apoptosis CD95+/CD28 y del número total de linfocitos CD16+ en el suero de 148 individuos
sanos con más de 85 años de edad, en comparación con las muestras obtenidas en individuos de diferentes edades.
Inmunidad humoral
Recientes estudios describen la producción alterada de ciertas citocinas como causa o factor modulador del proceso de inmunosenescencia. Estudios in vitro aplicados sobre cultivos celulares demuestran que la estimulación del crecimiento de tejidos expuestos a IL-5 de individuos voluntarios sanos es casi dos veces mayor a la observada en tejidos procedente de personas mayores. Por otro lado, es una constante en los trabajos publicados la evaluación en la función de los valores de inmunoglobulinas. Rink et al, en 1997, evaluaron los valores séricos de diferentes parámetros biológicos en población geriátrica, encontrando entre sus resultados un aumento importante en la producción de inmunoglobulinas como IgG, IgM e IgA, niveles de beta-2-microglobulina, concentraciones de cinc, número total de células NK, así como marcadores de linfocitos CD16, CD56, CD 57 y citocinas, como IL-1, IL-6, IL-8 y TNF-α. Por otro lado, estos autores observaron una relativa disminución en el número de linfocitos CD3, CD8, CD 45 RA, CD19, otras células T, IL-2 e interferón δ. Otras alteraciones descritas han sido los efectos sobre el sistema inmune de factores extrínsecos (dieta, fármacos, ejercicio), el aumento en la expresión de CD95 con la edad (Potensio, 1999), una disminución de las citocinas Th1/aumento de las citocinas Th2 (Lio, 1999; Rink, 1997), las alteraciones en la apoptosis de los polimorfonucleares (Falop, 1997), el aumento en los valores séricos de IgG, IgM e IgA (Rink, 1997) y la atrofia tímica progresiva (Rose, 1994). Sin embargo, las causas, y sobre todo las implicaciones prácticas de estos hallazgos, no han sido esclarecidas y no se tiene hasta el momento conocimiento acerca de su importancia como desencadenantes de enfermedades autoinmunes o neoplásicas en el paciente anciano. En resumen, entre las principales alteraciones de la inmunidad humoral debe descartarse la no alteración en el número total de linfocitos B, una mayor respuesta policlonal frente a diversos mitógenos, menos respuestas específicas del antígeno, un defecto intrínseco de la maduración de los linfocitos B y una mayor frecuencia de síntesis de anticuerpos.
Interpretación de las alteraciones inmunológicas en la edad geriátrica
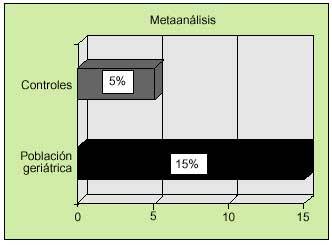
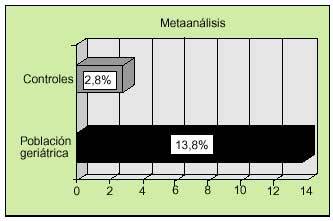
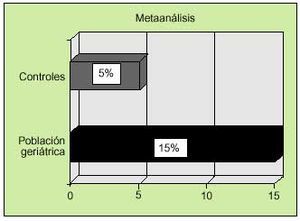
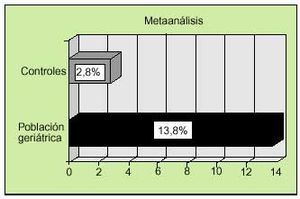
No existen estudios amplios dedicados a evaluar los títulos de autoanticuerpos y su significado clínico en la población geriátrica. Sin embargo, se han publicado trabajos aislados sobre algunos valores de anticuerpos en pacientes ancianos. El factor reumatoide (FR) fue el primer autoanticuerpo descrito con mayor frecuencia en la población geriátrica. Se han descrito porcentajes variables según las series, elevados en algunos casos (19-42%). El metaanálisis de los principales estudios realizados demuestra una mayor prevalencia en la población geriátrica (15%) frente a la población control (5%) (fig. 1). Por otra parte, los estudios realizados sobre la prevalencia de ANA positivos en población geriátrica respecto al grupo control demuestran una importante diferencia (13,8 frente a 2,8%, según un metaanálisis de los principales estudios) (fig. 2). La prevalencia de otros autoanticuerpos en edad geriátrica, como los antiADN, antimúsculo liso y anticélula parietal, es similar respecto a poblaciones más jóvenes. Otros autores, como Potocka, han encontrado aumentos en la expresión de algunos autoanticuerpos, como los anticuerpos antinucleares (ANA), antimúsculo liso (SMA), anticuerpos antimitocondriales (AMA), antitiroglobulina y anticélula parietal (PCA) con porcentajes de 42,1, 10,5, 5,3, 5,2 y 5,3 respectivamente; no obstante, estas cifras parecen no ser estadísticamente significativas. Existen otros trabajos, tanto clínicos como de laboratorio, donde se ha descrito una tendencia al aumento de autoanticuerpos en el suero de enfermos seniles; sin embargo, ninguno ha logrado encontrar cifras significativas, por lo que hasta el momento la hipótesis formulada por estos autores no ha sido confirmada. Uno de los estudios más representativo fue el realizado por Candore, en 1997, donde se encontró una prevalencia de antitiroglobulina, anti-PCA y ANA relativamente superior en individuos octogenarios que en individuos más jóvenes. Este estudio se llevó a cabo únicamente en 26, 54 y 56 pacientes de cada grupo (centenarios, octogenarios y jóvenes, respectivamente), por lo que no se puede otorgar una significación estadística a los resultados dado el número reducido de pacientes incluidos. Existe más controversia respecto a la prevalencia de los anticuerpos antitiroideos en población geriátrica, ya que existe el mismo número de estudios que demuestran una mayor prevalencia que los que indican una prevalencia similar en población adulta. Recientemente, Hak et al publica ron un interesante trabajo que valoraba las titulaciones de anticuerpos antitiroideos en pacientes con episodios cardiovasculares conocidos y su relación con el hipotiroidismo subclínico. En este trabajo se encontró una mayor prevalencia de hipotiroidismo subclínico en pacientes con antecedentes de cardiopatía isquémica y se postuló una relación directa entre ambos hechos. Con relación a los anticuerpos anticardiolipina, Juby, en 1995, encontró una prevalencia aumentada de dichos autoanticuerpos en pacientes de edad avanzada con antecedentes de ictus de alrededor del 18% cuando los comparó con un grupo control; no obstante, sus resultados tampoco fueron significativos desde el punto de vista estadístico. Finalmente, Maillefert et al analizaron la prevalencia de anticuerpos anticitoplasma del neutrófilo en una población de 137 pacientes con una media de edad de 82,2 ± 6,9 años y ausencia de enfermedades neoplásicas, inmunológicas o infecciosas que pudieran alterar los resultados, sin encontrar una diferencia significativa en cuanto a los porcentajes de resultados positivos respecto a una población control (2,2% en ambos grupos).
Fig. 1. Metaanálisis de los principales estudios realizados sobre la prevalencia de factor reumatoide positivo en población geriátrica frente de población control.
Fig. 2. Metaanálisis de los principales estudios que analizan la prevalencia de ANA en población geriátrica respecto a población control.
Tratamiento de las enfermedades autoinmunes sistémicas en geriatría
Las enfermedades autoinmunes son un grupo heterogéneo de procesos en cuya etiopatogenia parecen desempeñar un importante papel los factores genéticos. Por lo general, comparten ciertas características clínicas e inmunológicas; por ello, su diferenciación puede ser frecuentemente difícil. Una característica propia de las enfermedades autoinmunes es que cada una de ellas presenta una especial predilección por afectar a determinados grupos de edad.
Hasta el momento existen pocos estudios enfocados a caracterizar la presentación de estas enfermedades en la edad geriátrica. Aunque no existe aún consenso acerca de la existencia de un comportamiento típico de algunas entidades autoinmunes en edades geriátricas, se han establecido algunos patrones, tanto clínicos como de laboratorio, de aparición frecuente en estos grupos, coincidiendo casi todos con manifestaciones atípicas, de inicio insidioso y con una menor expresión en los parámetros de laboratorio. En la tabla 2 se resumen las principales características diferenciales en la presentación de las enfermedades autoinmunes sistémicas en la edad geriátrica.
Enfermedades autoinmunes de presentación típica en la edad geriátrica
Polimialgia reumática
Es la enfermedad autoinmune típica de la edad geriátrica, ya que se diagnostica frecuentemente en enfermos mayores de 60 años. La polimialgia reumática se diagnostica clínicamente y se caracteriza, sobre todo, por la presencia de rigidez de la cintura pélvica y escapular, fiebre y malestar general. La anemia y la VSG aumentada son datos de laboratorio constantes. Algunos casos pueden cursar con inflamación articular de rodillas, codos, muñecas y uniones esternoclaviculares. Los enfermos suelen tener, hasta en el 75% de los casos, entre 65 y 75 años de edad, y manifestar en la vida cotidiana dificultades para peinarse, alcanzar objetos elevados o levantarse de la silla. Las dosis de 10 a 20 mg de prednisona suelen ser eficaces para mejorar la enfermedad espectacularmente, que podrán ir reduciéndose hasta que los datos clínicos y analíticos desaparezcan. La supresión de los corticoides de manera rápida y brusca suele asociarse a recidiva clínica. Por lo general, esta entidad suele estar infradiagnosticada, ya que en muchos casos lo insidioso de su comportamiento hace que los enfermos portadores de la misma realicen innumerables visitas médicas sin un diagnóstico certero; de ahí que su detección en el ámbito de la medicina general reviste una sustancial importancia.
Enfermedad de Horton
La arteritis de la temporal es otra de las enfermedades autoinmunes que afectan característicamente a la edad geriátrica. Es una vasculitis de los vasos medianos que afecta sobre todo a la arteria temporal, así como a otras ramas extracraneales de la carótida. La cefalea, el enrojecimiento y la tumefacción local, los síntomas visuales y el dolor mandibular son datos clínicos frecuentes, al igual que la ceguera secundaria a la arteritis oclusiva de la rama ciliar de la arteria oftálmica, cuyos cambios fundoscópicos pueden estar ausentes las primeras 48 h. Esta enfermedad representa del 15 al 20% de todos los casos de fiebre de origen desconocido en enfermos mayores de 65 años, después de descartar procesos infecciosos. El tratamiento con dosis altas de prednisona (1 mg/kg) y la biopsia de la arteria temporal (positiva en el 85% de los casos) deben ser utilizados de forma inmediata una vez que se sospeche el diagnóstico. Los hallazgos histológicos demuestran un infiltrado inflamatorio linfocítico e histiocitario con presencia de células gigantes. Ocho semanas de tratamiento suelen ser suficientes para lograr la remisión en la mayoría de los casos, obteniéndose la normalización de la VSG y del cuadro clínico. No obstante, las recidivas no son infrecuentes, por lo que debe mantenerse el tratamiento con corticoides durante varios meses, siendo preciso en algunos casos una dosis de mantenimiento.
Miopatías inflamatorias
Es un proceso patológico que combina la afección muscular (debilidad muscular proximal simétrica) y la afección cutánea característica (edema y pigmentación periorbitaria en heliotropo y parches cicatrizales de Gottron). Su aparición suele tener dos picos clásicos de incidencia, uno en la juventud y el otro entre los 40 y los 60 años. Afecta predominantemente a mujeres, en una relación con los varones de 2:1, y su patogenia hasta el momento no ha podido ser esclarecida, aunque se han implicado factores, intrínsecos (radiaciones ultravioleta o exposición a algunos virus, como el VIH) y extrínsecos como un cierto grado de predisposición genética relacionada con el HLA DQ, el DR3, el DR7 y el B8. La aparición de síntomas o signos sugestivos de miopatía inflamatoria en personas con edades superiores a 65 años obliga a estudiar exhaustivamente la presencia de neoplasias, dato que se encuentra presente en la historia de más del 30% de todos los enfermos diagnosticados en estas edades, ya sea como manifestación posterior o incluso, en un porcentaje nada despreciable, como dato inicial de la enfermedad, anticipándose a los hallazgos miopáticos en unos meses o incluso años. Se han publicado casos de enfermos que desarrollan la alteración muscular hasta 5 o 10 años después del diagnóstico de alguna neoplasia maligna, siendo considerado por algunos autores como un tipo de síndrome paraneoplásico. Los tumores malignos más relacionados con esta enfermedad autoinmune suelen encontrarse, según la mayoría de los estudios retrospectivos, predominantemente en la zona cervicouterina, pulmonar y gástrica, aunque se han reportado casos con aparición de neoplasias prácticamente en cualquier localización, lo que obliga al escrutinio en todos los pacientes con diagnóstico confirmado, realizado mediante biopsia muscular en el contexto de un enfermo con debilidad muscular proximal y dermatosis característica. El pronóstico en estos enfermos suele ser menos favorable dado este hallazgo y la mortalidad sumatoria de ambas enfermedades, autoinmune y neoplásica.
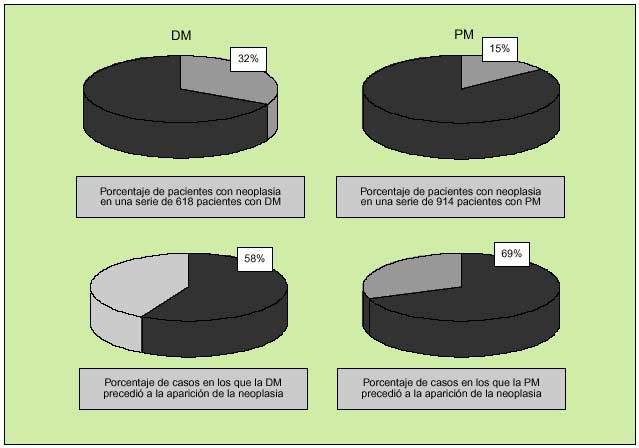
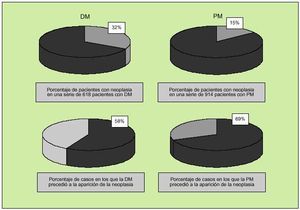
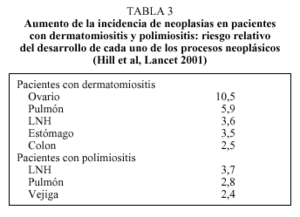
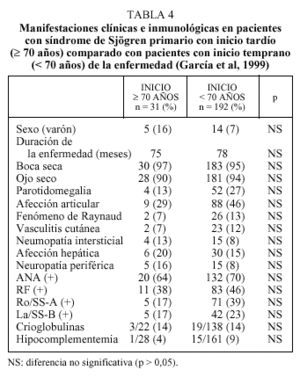
Recientemente, Marie et al han analizado las características clínicas y analíticas de la miopatía inflamatoria según la edad en el diagnóstico, describiendo en pacientes con más de 65 años de edad una mayor prevalencia de ciertas características clínicas (infecciones, neoplasias y mortalidad) y analíticas (anemia, elevación de reactantes de fase aguda). En otro reciente trabajo, Hill et al revisaron el Registro de Salud de los países nórdicos e identificaron 618 casos de dermatomiositis y 914 de polimiositis, detectando neoplasias en un 32 y un 15% de casos, respectivamente (fig. 3). Al analizar el riesgo relativo de desarrollo de neoplasia, se encontraron cifras distintas según se tratara de los pacientes con dermatomiositis o polimiositis (tabla 3).
Fig. 3. Porcentaje de pacientes con neoplasias y miopatía inflamatoria y porcentaje de casos en los que la miopatía precedió a la aparición de la neoplasia, según el estudio de Hill et al, al analizar 618 casos de dermatomiositis (DM) y 914 de polimiositis (PM).
Enfermedades autoinmunes de presentación atípica en la edad geriátrica
Síndrome de Sjögren
Es un trastorno autoinmune asociado a la disfunción crónica de las glándulas exocrinas en muchos territorios corporales. Se caracteriza por sequedad de boca, ojos y otras zonas cubiertas por membranas mucosas (exocrinopatía autoinmune). El síndrome de Sjögren primario (SSP) es más frecuente en mujeres (con una relación con los varones de 9:1) y una mayor incidencia entre los 40 y los 60 años de edad.
La queratoconjuntivitis sicca resulta de una inadecuada producción lagrimal por infiltración inflamatoria por células plasmáticas y linfocitos de las vías lagrimales. La sintomatología típica incluye irritación ocular y alteraciones visuales secundarias. En la mayoría de los casos existe una sequedad bucal (xerostomía) y un crecimiento parotídeo asociado con dificultad para la deglución de alimentos sólidos, caries frecuentes y falta de lubricación al hablar. La afección en otras localizaciones suele ocasionar sequedad en la nariz, la garganta, los bronquios, la piel y la vagina. Las manifestaciones sistémicas suelen incluir disfagia, afección articular, fenómeno de Raynaud, pancreatitis, pleuritis, tiroiditis, trastornos neuropsiquiátricos y vasculitis. La aparición de algunos procesos linfoproliferativos en enfermos con síndrome de Sjögren suele ser 50 veces mayor que en la población general.
En la población en edad geriátrica, la xerostomía es un síntoma frecuente, pero no debe considerarse simplemente como expresión del envejecimiento, ya que las causas también son múltiples. En un estudio de Screebny et al, en el que se analizaba la presencia de xerostomía en la población general, la prevalencia fue mayor en el grupo de más de 55 años de edad (40%). Sin embargo, el uso de fármacos xerogénicos es la causa más frecuente de xerostomía en la edad geriátrica, ya que más del 50% de los ancianos consume fármacos con acción xerogénica. En un estudio realizado en mujeres mayores de 65 años de una residencia de ancianos, se encontró que el 25% refería síntomas de xerostomía, pero el 60% de ellas seguía tratamientos con fármacos con capacidad xerogénica.
Durante el envejecimiento, se ha propuesto la disminución del estímulo de los receptores periféricos como uno de los mecanismos principales de la xerostomía. En este período de edad, la hiposecreción salival se produce a expensas de la secreción basal o de reposo en las glándulas submaxilares y, en cambio, existe una buena respuesta a la estimulación gracias a la capacidad de respuesta o «reserva salival» de las parótidas.
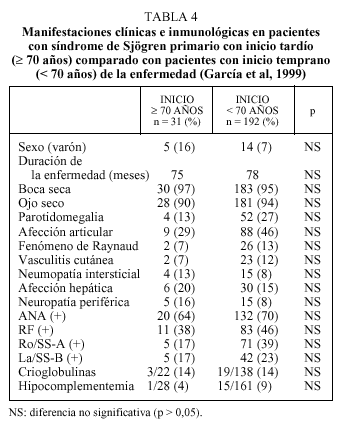
Existen pocos trabajos que hayan estudiado la expresión clínica e inmunológica del SSP en pacientes con inicio tardío de la enfermedad (después de los 65 años). En un trabajo reciente se han estudiado 223 pacientes con SSP, de los cuales el 14% presentó un inicio de la sintomatología después de los 70 años. La media de edad fue de 75 años y el tiempo promedio de la duración de la enfermedad fue de 25 meses, cursando el 97% de ellos con xerostomía y el 90% con xeroftalmía. Las manifestaciones extraglandulares fueron, en orden decreciente, articulares (29%), hepáticas (20%), neuropáticas (16%), pulmonares (13%), vasculíticas (7%) y un porcentaje similar para el fenómeno de Raynaud. Los ANA fueron positivos en el 42% de los casos, el FR en el 38%, los anti-Ro en el 17%, los anti-La en el 17%, las crioglobulinas en el 14% y los valores bajos de complemento en el 4%. En la tabla 4 se incluyen las diferencias entre el grupo geriátrico y el grupo control, no existiendo diferencias estadísticamente significativas entre ambos en lo concerniente al sexo, la duración, el cuadro clínico, las características inmunológicas y los hallazgos en la biopsia salival. De todas formas, parece existir una tendencia a una menor prevalencia de ciertas afecciones extraglandulares y una menor frecuencia de marcadores inmunológicos, aunque no existan diferencias en cuanto a la positividad de las principales pruebas diagnósticas.
Artritis reumatoide
Típicamente, la artritis reumatoide (AR) suele describirse como una enfermedad sistémica más que articular, por la alta prevalencia de alteraciones sistémicas (carditis, pleuritis, vasculitis, neumonitis, queratoconjuntivitis y algunas manifestaciones hematológicas e incluso neurológicas). Hasta el momento, se han asociado a su patogenia diversos factores, tanto genéticos como la expresión de antígenos HLA del tipo DR4 y DR1, inherentes al huésped, como la influencia hormonal, o bien ambientales, como la sospecha reciente de agentes infecciosos (p. ej., factores desencadenantes en individuos predispuestos), hecho que se demuestra por altas titulaciones de anticuerpos antivirus Epstein Barr o parvovirus B19 encontrados en pacientes con la enfermedad. El comportamiento clínico típico en un paciente promedio suele contar con la aparición de, por lo menos, 4 de los criterios requeridos para su diagnóstico (según el American College of Rheumatology), que incluyen rigidez articular matutina de más de 30 min de duración, presencia de artritis simétrica de predominio metacarpofalángico proximal (dolor, calor y eritema) en, por lo menos, 3 grupos articulares, así como existencia de cambios radiológicos (osteopenia yuxtaarticular en la radiografía de manos) y positividad serológica para anticuerpos IgM frente a IgG (factor reumatoide), la cual suele encontrarse en un 70% de los casos. Otros parámetros útiles son la presencia de otros reactantes de fase aguda, como la VSG y la PCR, en etapas de mayor actividad. Su comportamiento clásico suele ser insidioso y su tratamiento difícil, basado principalmente en el uso de antiinflamatorios no esteroides en fases iniciales, y en casos refractarios algunos agentes moduladores del curso de la enfermedad, como el metotrexato o los antipalúdicos.
Aunque la AR es típicamente una enfermedad de presentación entre los 40 y los 60 años de edad y con un claro predominio femenino, recientemente se han descrito casos en enfermos mayores de 65 años, en quienes la sintomatología no es de expresión típica y los marcadores inmunológicos para su detección no son de expresión clásica. Algunos individuos mayores de 65 años en quienes incluso puede existir evidencia previa han presentado rigidez matutina diferente de la experimentada con anterioridad, fiebre de origen no determinado, eritema y dolor en las articulaciones proximales con valores discretamente elevados de FR, lo cual hace difícil el diagnóstico superpuesto de
AR, inclusive con la aparición de osteopenia yuxtaarticular y quistes subcondrales en las articulaciones metacarpofalángicas e interfalángicas proximales, hallazgos que la mayoría de las veces son pasados por alto.
En 1993, Harley et al propusieron una clasificación para la AR de inicio tardío, donde estratifican en tres grupos las formas de presentación de esta entidad (tabla 5). Destacando la existencia de grupos de enfermos con manifestaciones clínicas características y factor reumatoide positivo (grupo I), las manifestaciones infrecuentes o insidiosas con factor reumatoide igualmente positivo (grupo II) y, por último, las formas clínicas atípicas con factor reumatoide ausente y sin evidencia radiológica (tipo III).
En dichos casos, la fuerte sospecha de AR del anciano suele justificar la necesidad de determinaciones seriadas de FR o bien iniciar un tratamiento de prueba con AINE o metotrexato para observar la respuesta al mismo, pues algunos otros datos, sobre todo de tipo extraarticular, suelen estar ausentes como formas auxiliares para el diagnóstico. Hasta ahora, el pronóstico en estos enfermos no ha podido ser esclarecido por tratarse de casos relativamente poco frecuentes.
A pesar de que el pico de incidencia de la AR es entre los 30 y los 50 años de edad, casi un 30% de los pacientes suele iniciar su sintomatología en edades cercanas a los 70 años, e incluso mayores, presentando cuadros clínicos variables y atípicos. El inicio, en estos casos, suele ser insidioso y tiene una prevalencia por sexos más equitativa. Suele afectar a las articulaciones proximales, semejando en ocasiones una polimialgia reumática. Cuenta con mayores manifestaciones sistémicas y un síndrome de desgaste superior al de la AR de las personas jóvenes, cursa con frecuencia con determinaciones negativas de FR, además de presentar un pronóstico más deletéreo según algunas investigaciones, probablemente debido a una mayor frecuencia de comorbilidad y otras enfermedades más graves.
Por otro lado, otros síndromes, como el de polimialgia reumática y la sinovitis remitente simétrica, han sido asociados como partes de un complejo único con un mismo fondo fisiopatológico en donde la AR del anciano también tendría un lugar. El tratamiento de la AR del anciano no presenta diferencias con respecto a la juvenil; sin embargo, algunas consideraciones deben tenerse en cuenta, como el uso de AINE a dosis elevadas que puedan favorecer la aparición de hemorragias digestivas, o bien de esteroides en pacientes con una enfermedad diabética de base que puedan ser susceptibles a presentar un descontrol glucémico.
Lupus eritematoso sistémico
El lupus eritematoso sistémico (LES) es una enfermedad autoinmune con afección multiorgánica y una gran heterogeneidad en las manifestaciones clínicas e inmunológicas. Aunque predominantemente afecta a mujeres jóvenes en la segunda o tercera década de la vida, hasta en el 20% de los casos el diagnóstico puede realizarse en la quinta década o incluso más tarde. Muchos investigadores han reportado que la edad de inicio tiene un efecto modificador de la evolución de la enfermedad, pues se ha observado que el inicio de ésta en pacientes mayores suele ser más insidioso y con manifestaciones clínicas atípicas, lo cual muchas veces ocasiona la realización de diagnósticos tardíos. Se ha observado en estos casos que afecciones orgánicas graves, como la nefritis o la afección del sistema nervioso central, suelen ser menos comunes conforme avanza la edad, coexistiendo, por otro lado, con anormalidades serológicas diversas y, por lo general, sutiles.
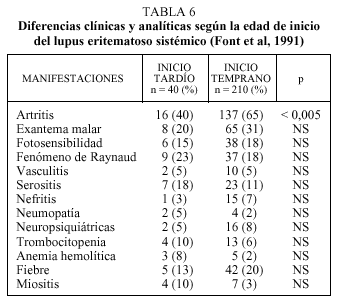
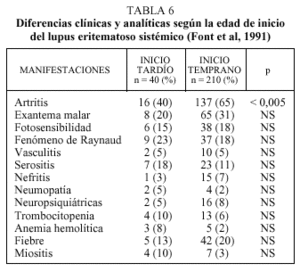
De todas formas, existen pocos estudios que hayan investigado las características del LES de inicio tardío en grandes series de pacientes. En una serie de enfermos lúpicos se encontró un inicio tardío de la enfermedad (después de los 50 años) en el 16% de los casos. La artritis como síntoma de aparición inicial fue menor en los enfermos mayores de 50 años, y se observó también una baja prevalencia de eritema malar, fotosensibilidad y nefropatía, encontrándose, por otro lado, una alta frecuencia de miositis. Títulos positivos de anticuerpos anti-ADN se observaron con menor frecuencia en los enfermos de mayor edad, cuando éstos se presentaban, por lo general, los valores eran menores que los observados en pacientes jóvenes, fenómeno que ocurrió de manera similar con los anticuerpos anti-Ro/SS-A. Los resultados de esta comparación se reflejan en la tabla 6.
No se pueden extraer grandes conclusiones debido al número limitado de trabajos; sin embargo, parece ser que, en general, las manifestaciones del LES en la población geriátrica, así como su evolución, suelen ser insidiosas y de comportamiento atípico, lo cual, como ya se ha comentado, en general retarda su diagnóstico y tratamiento. La causa de ello no es clara y se considera que pueden influir factores demográficos y diferencias genéticas.
Otras enfermedades autoinmunes sistémicas en edades avanzadas
Esclerodermia sistémica
La relativa rareza de esta enfermedad, junto a una considerable variabilidad en su expresión clínica, así como la falta de un marcador sensible para su diagnóstico certero, ha determinado que los estudios epidemiológicos efectuados sean escasos. Puede detectarse a cualquier edad, pero su máxima incidencia se sitúa entre los 30 y los 50 años, aunque se han descrito en enfermos con edades comprendidas entre 65 y 75 años. El patrón clásico de presentación suele iniciarse, en un 70% de los casos, con alteraciones estructurales de los vasos sanguíneos, los cuales presentan, asimismo, trastornos funcionales manifestados principalmente por el fenómeno de Raynaud, cuya presencia es casi constante y frecuentemente como única manifestación, incluso durante años. Para el diagnóstico, de acuerdo con la ACR, se necesita un criterio mayor y dos criterios menores, siendo los primeros la existencia de esclerodermia proximal y los segundos la presencia de esclerodactilia, cicatrices digitales puntiformes y fibrosis pulmonar bibasal. La presencia de anticuerpos anticentrómero ha podido ser detectada en el 30% de los
enfermos, que en su mayoría corresponde a la forma limitada de la enfermedad, a diferencia de los anticuerpos antitopoisomerasa I (anti-scl70) que predominan en las formas difusas. Los cambios cutáneos faciales, que en ocasiones se presentan en etapas avanzadas de la enfermedad, así como la esclerodactilia, revisten una dificultad de apreciación en los casos geriátricos, dadas las características propias del envejecimiento. Las formas limitadas de la enfermedad (afección cutánea aislada) tienden a ser más frecuentes en enfermos jóvenes, reportándose casos con afección predominantemente visceral en enfermos mayores de 50 años. No hay trabajos que hayan estudiado de forma específica el distinto comportamiento de la enfermedad en personas de edad avanzada.
Poliarteritis nudosa
La poliarteritis nudosa (PAN) es una enfermedad inflamatoria de las capas adventicias vasculares que principalmente afecta a las arterias de mediano calibre, ocasionando complicaciones graves según la localización. El riñón suele afectarse hasta en el 70% de los casos y representa un importante factor pronóstico, al ser responsable de hasta el 50% de las muertes, ya sea por glomerulonefritis necrosante o micropoliarteritis renal. La afección en el sistema nervioso central es la segunda causa de mortalidad. La afección cardíaca y digestiva sigue a las anteriores en orden de frecuencia y sus espectros clínicos de presentación suelen ser variados, dando origen a cardiopatía isquémica progresiva, arteritis hepática, hepatitis crónica activa, náuseas, vómitos, diarreas, dolor abdominal inespecífico, hemorragia digestiva, perforación y aneurismas mesentéricos.
Una vez confirmado el diagnóstico mediante biopsia cutánea, en los casos de poliarteritis aislada, o renal, según el caso pueden utilizarse corticoides a dosis elevadas, que han demostrado en algunos estudios un aumento de la supervivencia del 13 al 48%, incidiendo de forma relativamente importante en el curso de la enfermedad, la cual sin tratamiento suele dar índices de supervivencia del 25% a los 5 años. La ciclofosfamida ha sido utilizada recientemente en el tratamiento de la PAN, en forma aislada en enfermos con resistencia a los corticoides o bien aunada a ellos en casos graves y rápidamente progresivos.
A diferencia de otras enfermedades autoinmunes sistémicas, en el caso de la PAN la edad es un factor importante de mal pronóstico, pues se ha advertido un aumento de la mortalidad en enfermos de edades avanzadas, tanto en los grupos de enfermos tratados con corticoides como en los que reciben inmunosupresores. Se ha documentado que los índices de mortalidad aumentan del 50 al 75% a los 3 años en enfermos mayores de 60 años, porcentaje que aumenta exponencialmente después de la séptima década.
Crioglobulinemia
La alta prevalencia de infección por el virus de la hepatitis C en las personas mayores de 50 años hace que algunos tipos de vasculitis, que recientemente han sido asociados a este virus hepatotropo, puedan tener mayor prevalencia en la población geriátrica. Tal es el caso de la vasculitis secundaria a crioglobulinemia que, si bien es poco común, debe ser considerada cuando un paciente se presenta con lesiones purpúricas palpables en las extremidades inferiores, hematuria y proteinuria asociada a glomerulonefritis y/o neuropatía periférica, junto con una alteración del perfil hepático. La confirmación del diagnóstico se basa en las manifestaciones clínicas y en una determinación positiva de crioglobulinas. La edad avanzada de estos enfermos suele contraindicar el uso de interferón y ribavirina y puede obligar al tratamiento con prednisona a dosis elevadas y otros agentes inmunosupresores con el fin de evitar, sobre todo, las complicaciones viscerales, como la insuficiencia renal y la neuropatía. El pronóstico, por lo general, empeora conforme el momento del diagnóstico es más tardío.
Bibliografía general
Font J, Pallarés L, Cervera R, López-Soto A, Navarro M, Bosch X, et al. Systemic lupus erythematosous in the elderly: clinical and immunological characteristics. Ann Rheum Dis 1991;50:702-5.
García-Carrasco M, Cervera R, Rosas J, Ramos-Casals M, Morla RM, Siso A, et al. Primary Sjögren's syndrome in the elderly: clinical and immunological characteristics. Lupus 1999;8:20-3.
Hak EA, Pols HA, Visser TJ, Dexhage HA, Hofman A, Witteman JC. Subclinical hypothyroidism is an independent risk factor for atherosclerosis and myocardial infarction in elderly women: the Rotterdam Study. Ann Intern Med 2000;132:270-8.
Hill CL, Zhang Y, Sigurgeirsson B, Pukkala E, Mellenkjaer L, Airio A, et al. Frequency of specific cancer types in dermatomyositis and polymyositis. Lancet 2001;357:96-100.
Manoussakis MN, Tzioufes AG, Silis MP, Pange PJ, Goudevenos J, Moutsopoulos HM. High prevalence of anti-cardiolipin and other autoantibodies in a healthy elderly population. Clin Exp Inmunol 1987;69: 557-65.
Marie I, Hatron PY, Levesque H, Hachulla E, Hellot MF, Michon-Pasturel U, et al. Influence of age on characteristics of PM and DM in adults. Medicine (Baltimore) 1999;78:139-47.
Strickland RW, Tesar JT, Berne BH, Hobbs BR, Lewis DM, Welton RC. The Prevalence of Sjögren's syndrome and associated rheumatic diseases in an elderly population. Arthritis Rheum 1984;27: S25.
Van Schaardemburg D, Legaay AM, Breedveld FC, Hijmans W, Vanderbroucke JP. Rheumatoid artritis in a population of persons aged 85 years and over. Br J Rheumatol l993;32:104-9.