La supresión del gen del sustrato 2 del receptor de insulina (IRS-2) induce una alteración del eje hipotálamo-ovárico como consecuencia de la inducción de resistencia central a leptina. Las hembras IRS-2−/− se caracterizan por una anovulación persistente, acompañada de la ausencia del ciclo estral, que se traduce en una marcada reducción de la fertilidad (tasa embarazo: 9% IRS-2−/− frente 100% IRS-2wt). El tungstato sódico (Na2WO4) ha demostrado su capacidad para revertir estados de resistencia a la leptina mediante una inhibición de fosfatasas implicadas en la cascada de señalización de diversas citoquinas. El objetivo del presente trabajo es realizar una aproximación experimental para determinar el potencial interés del Na2WO4 en la capacidad reproductiva de ratones hembra anovuladoras IRS-2−/−.
Material y métodosSe administró Na2WO4 (2g/l en agua de bebida) a ratones hembra IRS-2−/−. Se estudió el ciclo estral mediante citologías vaginales y la tasa de embarazo tras el cruce de machos IRS-2wt.
ResultadosDurante la fase de pretratamiento se confirmó la ausencia de ciclo estral en los ratones IRS-2−/−. Tras 7 días de tratamiento todos los animales mostraban fases tardías del ciclo (estro y metaestro) en las citologías, indicando una recuperación del ciclo ovulatorio normal. Al final del estudio, tras realizar los cruces con machos IRS-2wt competentes, un 80% de las hembras tratadas con Na2WO4 habían quedado embarazadas. Estos resultados indican una recuperación de la fertilidad, en contraposición a la tasa de embarazo descrita para las hembras IRS-2−/− sin tratamiento (9%).
ConclusionesPor primera vez, se describe el efecto directo del Na2WO4 en la restauración de la función ovárica y de la fertilidad en ratones hembra IRS-2−/−.
Insulin receptor substrate-2 (IRS-2) gene suppression induces an alteration of hypothalamic-ovarian axis as a result of central leptin resistance induction. IRS-2−/−females mice are characterised by persistent anovulation, accompanied by the absence of the oestrous cycle, which results in a marked reduction in fertility (pregnancy rate: 9% IRS-2−/−vs. 100% IRS-2wt). Sodium tungstate (Na2WO4) has demonstrated its ability to reverse the leptin resistance state through an inhibition of phosphatases involved in the signalling pathway of several cytokines. The objective of this work is to present an experimental approach to determine a potential interest towards Na2WO4 in the reproductive ability of anovulatory IRS-2−/− female mice.
Material and methodsNa2WO4 was administered in drinking water (2g/L) to female mice. The oestrous cycle was assessed through vaginal smears, and pregnancy rates were measured after mating with IRS-2wt males.
ResultsLack of oestrous cycle was confirmed in the mice during the pre-treatment period. After 7 days of treatment all animals showed delayed cycle phases (oestrous and meta-oestrous) in vaginal smears, indicating a recovery of normal ovulatory cycle. At the end of the study, after mating with competent IRS-2wt male, 80% of females treated with Na2WO4 were pregnant. These results show a fertility recovery, as opposed to the pregnancy rate described in untreated IRS-2−/− (9%).
ConclusionsFor the first time, a description is presented of the direct effect of Na2WO4 in the restoration of ovarian function and fertility in IRS-2−/− female mice.
La leptina, hormona secretada por adipocitos, es una proteína clave en diversas funciones más allá de las descritas inicialmente como indicador de las reservas energéticas periféricas y controlador de la homeostasis energética (Friedman y Halaas, 1998). Se ha descrito el papel crucial de la leptina en procesos biológicos como la angiogénesis, la función inmune, la inflamación y la función reproductora (Brewer y Balen, 2010; Cervero et al., 2005; Pérez-Pérez et al., 2015).
La leptina juega un rol crítico en la función reproductora, es esencial en el inicio de la pubertad, en el dimorfismo sexual y en la regulación de la señalización neuronal para modular el eje hipotálamo-hipófiso-ovárico (HHO) (Moschos et al., 2002). La hormona se une a su receptor a nivel hipotalámico y activa una cascada de señalización bien establecida en la que participa el sistema janus kinase/signal transducer and activator of transcription (JAK/STAT) (Villanueva y Myers, 2008). Esta cascada de señalización está compartida por otras citoquinas, como interleucinas o el factor inhibidor de la leucemia. También se han descrito acciones directas de la leptina en otros tejidos relacionados con la función reproductora, estableciéndose acciones directas de la hormona en el ovario, el embrión y el endometrio, capaces de modular el desarrollo folicular, la calidad embrionaria, la tasa de implantación y la placentación (Brewer y Balen, 2010; Cervero et al., 2005; Elias y Purohit, 2013; Pérez-Pérez et al., 2015). Se ha descrito su actividad como un activador inicial de la cascada de señalización obligatoria en el proceso de implantación embrionaria (Ramos et al., 2005), en la que JAK/STAT son pasos críticos del proceso (Gonzalez et al., 2004; Salamonsen et al., 2010).También se ha establecido la implicación de la leptina en la prevención del aborto (Maheshwari et al., 2007). Por lo tanto, no parece sorprender que en enfermedades o alteraciones metabólicas dependientes de leptina, obesidad o síndrome del ovario poliquístico, entre otras, exista un alto riesgo de infertilidad debido a deficiencias en la ovulación y a la implantación embrionaria (Duggal et al., 2000). Así, la ausencia, el exceso y/o la resistencia a la leptina están claramente relacionadas con una baja eficiencia reproductiva o infertilidad (Elias y Purohit, 2013).
El tungstato sódico modula la señal de citoquinasEl tungstato sódico (Na2WO4) es una sal inorgánica de tungsteno con una actividad inhibidora de fosfatasas moderada, que ha evidenciado que ejerce un incremento de la actividad de leptina, entre otras citoquinas, modulando la señalización intracelular de estas hormonas señalizadoras, especialmente la cascada que involucra a JAK-2/STAT-3 (Amigó-Correig et al., 2011; Canals et al., 2009). La seguridad y la tolerabilidad de esta molécula tras su administración en humanos y animales son conocidas por los diversos estudios preclínicos y clínicos (estudios de fasei yii) realizados hasta la fecha (Hanzu et al., 2010).
Se ha demostrado que el Na2WO4 es capaz de disminuir la glucemia y mejorar la diabetes a través de una mejoría de la sensibilidad a la insulina, entre otros mecanismos (Claret et al., 2005). También se ha demostrado un claro efecto sobre el peso corporal, a través del control del gasto energético y la ingesta, a través de un mecanismo dependiente de leptina y mediante la modulación de JAK-2/STAT-3 (Amigó-Correig et al., 2011; Canals et al., 2009; Claret et al., 2005).
La evidencia disponible sugeriría que el Na2WO4 podría mejorar la eficiencia reproductiva a través de efectos sistémicos sobre el eje HHO y efectos directos en el endometrio, el ovocito y el embrión para alcanzar mayores tasas de implantación.
Ratón knock-out IRS-2: un modelo para el estudio de la infertilidad femeninaEn el modelo de ratón IRS-2−/−, desarrollado por Burks et al. (2000), se induce una deleción del gen insulin receptor substrate-2 (IRS-2), que se traduce en un claro dimorfismo sexual en relación con la fertilidad y al metabolismo de los hidratos de carbono.
Los machos de este modelo presentan resistencia a la insulina y una severa hiperglucemia iniciada desde edades tempranas. Por contra, en edades tempranas las hembras se mantienen relativamente euglucémicas y desarrollan una ligera resistencia a la insulina, que se mantiene hasta edades avanzadas (4-5meses). Las hembras IRS-2−/− en edades tempranas, alrededor de 10 semanas de edad, muestran un bajo desarrollo folicular y una anovulación persistente, acompañada de la ausencia del ciclo estral en la mayoría de los ratones. La tasa de embarazos de los ratones hembra IRS-2−/− es del 9%, frente a una tasa del 100% en ratones hembra IRSwt (IRS-2+/+ wild-type). Dado que en estas edades las hembras se mantienen euglucémicas y que únicamente desarrollan una ligera resistencia a la insulina, la profunda alteración en la fertilidad no es una consecuencia directa de las anomalías en el metabolismo de la glucosa. Las hembras de este modelo presentan alteraciones en los niveles circulantes de leptina desde edades tempranas. Así, ya en las 4 primeras semanas de edad los niveles circulantes de esta leptina son 2,5 veces superiores a los animales wild-type y a las 8 semanas son 5 veces superiores. Una evidente resistencia hipotalámica a la leptina se sugiere como el mecanismo más plausible responsable de la infertilidad en las hembras de este modelo animal.
Las características de este modelo animal le hacen útil para el estudio de la infertilidad relacionada con estados de resistencia a la leptina como la obesidad o el síndrome del ovario poliquístico, entre otros. Por lo tanto, este modelo animal abarca una serie de factores importantes relacionados con infertilidad, y como tal es un modelo adecuado para estudiar la eficacia del Na2WO4 en el tratamiento de la infertilidad.
El trabajo actual pretende hacer una primera aproximación experimental para determinar el efecto del Na2WO4 sobre la capacidad reproductiva de un modelo animal, ratones hembra IRS-2−/−, en los que se ha descrito una limitada capacidad reproductiva como consecuencia de una profunda anovulación. Los resultados de esta prueba de concepto permitirán determinar el interés del Na2WO4 en el tratamiento de la fertilidad, que deberá confirmarse con estudios controlados y bien diseñados para determinar su alcance.
Material y métodosAnimalesPara la realización de esta prueba de concepto se utilizaron ratones hembra IRS-2−/− mantenidos en una colonia con background genético mixto C57Bl/6 x 129Sv, generados como ha sido previamente descrito (Withers et al., 1998, 1999). Ratones hembra IRS-2−/− y ratones macho wild-type (IRS-2wt) de edades comprendidas entre 6 y 8 semanas se estabularon en ciclo luz/oscuridad de 12h y temperatura y humedad normales. Los animales tuvieron acceso ad libitum tanto al agua de bebida como al alimento (pienso estándar tipo A04 Panlab, Barcelona).
Todos los procedimientos realizados en este estudio fueron realizados de acuerdo a las guías de cuidado de animales de laboratorio (regulación local y europea) y aprobados por el comité de experimentación animal de la Universitat de Barcelona.
TratamientoLos ratones hembra IRS-2−/− se estabularon en grupos de 4-6 ratones/jaula. Tras un periodo de aclimatación, los animales se mantuvieron 2 semanas en fase de pretratamiento, durante las que se administraron comida y bebida en las condiciones previamente descritas. Tras este periodo se administró Na2WO4 (tungstato sódico dihidrato CAS-num 6132-04-3 Sigma-Aldrich) en el agua de bebida (2mg/ml en agua bidestilada) con acceso ad libitum. El tratamiento se inició inmediatamente después de la fase de pretratamiento (día 0 de tratamiento) y hasta 4 semanas antes del sacrificio de los animales. La dosis diaria de Na2WO4 ingerida por los ratones no fue controlada, pero se estima que fue aproximadamente de 180mg/kg de peso corporal, según ha sido descrito previamente en modelos animales y diseños experimentales similares (Canals et al., 2009; Claret et al., 2005). En un grupo de animales se monitorizó el peso corporal y la glucemia durante los primeros 12días de tratamiento. Tras 6h de ayuno se midieron los niveles de glucosa en sangre en los días 2, 5, 7, 9 y 12 de tratamiento, las medidas se realizaron con un sensor de glucosa Accutrend (Roche Diagnostics, Mannheim, Alemania). Este grupo de animales no se incluyó en la determinación del ciclo estral ni en el análisis posterior de la tasa de embarazo, con la intención de evitar interferencia que pudiesen ser causadas por el estrés generado por los repetidos periodos de ayuno.
Citologías vaginalesSe eligieron 6 ratones hembras IRS-2−/− al azar para la determinación del ciclo estral. Se les realizaron frotis vaginales en los días pretratamiento (−8, −5, −2 y −1) y en los días de tratamiento (7, 8, 14, 15 y 22). Para la realización de los frotis vaginales se introdujo en la vagina de los ratones entre 1 y 2ml de solución salina con una pipeta Pasteur. Con la misma pipeta se recogió el exudado vaginal y se extendió en un portaobjetos. Una vez secado al aire, se fijó y se tiñó con la técnica de Papanicolaou. Las preparaciones se analizaron por personal entrenado y a ciego simple para eliminar el sesgo del evaluador. Las muestras se clasificaron en las siguientes fases: diestro, proestro, estro, metaestro, anestro o no evaluable.
Tasa de fertilidadA partir la tercera semana de tratamiento, los ratones hembra IRS-2−/− se estabularon por parejas junto a un ratón macho IRS-2wt competentes durante 12semanas. Los ratones se observaron diariamente en busca de signos de embarazo o parto. El tratamiento con Na2WO4 se mantuvo durante las 8semanas de estabulación conjunta de machos y hembras, periodo tras el que se retiró el tratamiento. En el caso de embarazo las hembras fueron estabuladas individualmente hasta el parto, manteniendo el tratamiento según el diseño del estudio. Estas hembras no se reincorporaron al estudio Transcurridas las 12semanas, las hembras que permanecían en el estudio fueron sacrificadas y biopsiadas en busca de indicios de embarazo, para calcular la tasa de fertilidad.
ResultadosEl tungstato sódico restaura la ciclicidad del ciclo en ratones hembra IRS-2−/−En la evaluación de las citologías de ratones hembra IRS-2−/− se identificaron fases anestro/diestro, proestro, estro, metaestro. La presencia de las 4 fases del ciclo en periodos de 4 a 6días es indicativa de la ciclicidad estral y de un ciclo ovárico normal. Sin embargo, la persistencia en fases anestro/diestro o proestro son indicadores de la ausencia de ciclicidad. Teniendo en consideración este patrón, se pueden determinar patrones diferenciales en el ciclo estral entre las fases de pretratamiento y tratamiento (tabla 1). Así, se observa que en las fases de pretratamiento todos los animales estudiados permanecen en fases anestro/diestro o proestro, mientras que en la fase de tratamiento se observa que todos los animales alcanzan fases tardías del ciclo (estro y metaestro), indicando que han recuperado el ciclo estral. Estos cambios en el ciclo se observan ya desde la primera medida realizada durante el periodo de tratamiento (día7), indicando una rápida recuperación del ciclo estral con la administración de Na2WO4. Adicionalmente se puede observar una reducción de los ciclos en estro y metaestro en las citologías realizadas en el día22 de tratamiento. No obstante, el diseño del estudio no permite determinar si se trata de un efecto aleatorio en el que la mayoría de los animales se encuentran en fases tempranas del ciclo o de una disminución del efecto del tratamiento.
Determinación del ciclo estral mediante citologías
| ID Ratón | Tiempo (días) | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| −8 | −5 | −2 | −1 | 7 | 8 | 14 | 15 | 22 | |
| 1 | A | A | P | D | E | E-M | E | E | A |
| 2 | A | D | P | P | E | E-M | E-M | A | D |
| 3 | D-P | D | P | P | E | E | E-M | M | A |
| 5 | D | D | P | P | E | E | E-M | M | M |
| 8 | D | D | P | P | E-M | E-M | D | E | P |
| 9 | D | D | - | P | M | M | - | D | D |
Las fases del ciclo estral son las siguientes: A: anestro; D: diestro; P: proestro; E: estro; M: metaestro.
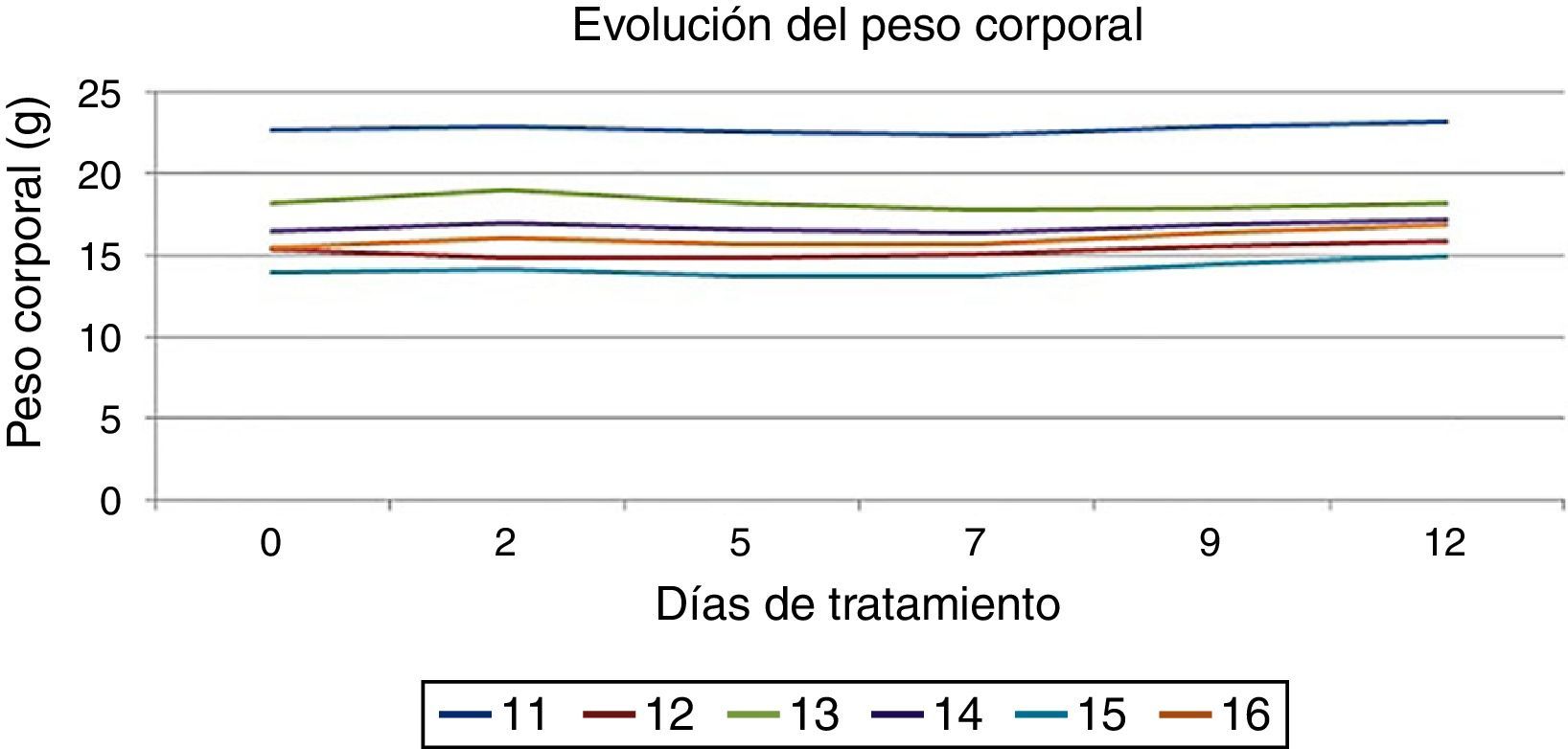
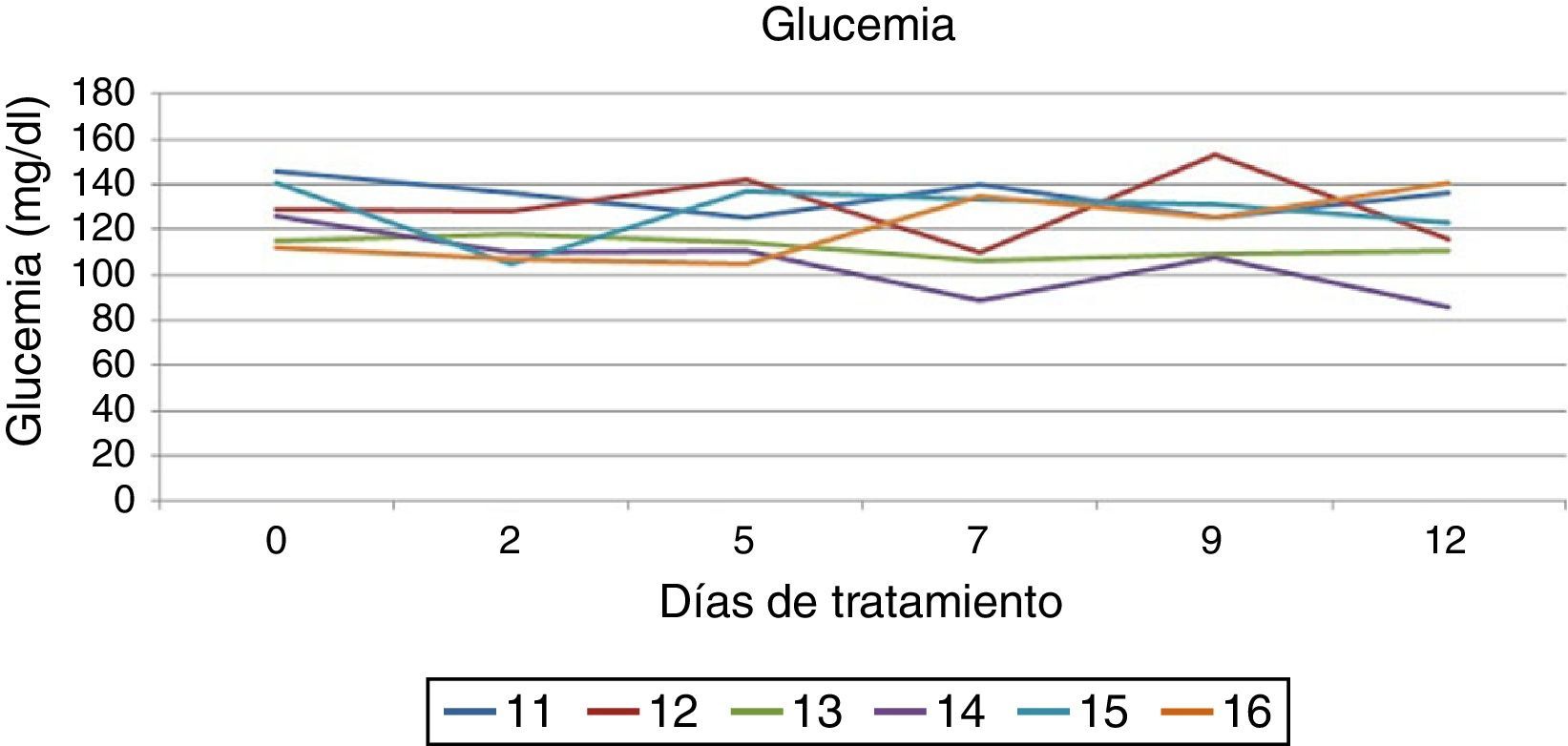
Se monitorizó la evolución de la ganancia ponderal en ratones hembra IRS-2−/− durante los primeros 12días de tratamiento con Na2WO4. En este periodo no se observaron cambios significativos en el peso corporal de los ratones (fig. 1). De la misma forma, se monitorizaron los niveles de glucosa en sangre en los mismos animales tras 6h de ayuno. Como previamente estaba descrito, los animales mostraron niveles de glucosa ligeramente superiores a los normales, pero en los márgenes de la euglucemia (fig. 2). Durante los primeros días de tratamiento no se observaron cambios en los niveles de glucosa en sangre.
El tungstato sódico recupera la fertilidad en ratones hembra IRS-2−/−Tras finalizar el periodo de cruces entre hembras IRS-2−/− y machos IRS-2wt, se sacrificaron las hembras que no habían parido y se biopsiaron en búsqueda de signos de embarazos. Cuatro hembras habían parido durante el periodo de estudio. En el momento del sacrificio 4 hembras estaban embarazadas en diferentes estadios de gestación. Así, un total de 8 de las 10 hembras tratadas (80%) estaban embarazadas o habían parido en el momento del sacrificio (tabla 2). Esta tasa de embarazo es muy superior al 9% descrito previamente en hembras IRS-2−/− no tratadas (Burks et al., 2000).
Tasas de embarazo y crías/embriones en ratones hembra IRS-2−/− tratados con Na2WO4
| N.° ratón | Embarazo | Número de embriones implantados o crías nacidas | Momento del parto o edad embrionaria en el momento del sacrificioa |
|---|---|---|---|
| 1 | Sí | 1 cría | Semana parto: 4 |
| 2 | Sí | 8 crías | Semana parto: 10 |
| 3 | Sí | 7 embriones | Embriones: E10-13 |
| 4 | Sí | 3 crías | Semana parto: 5 |
| 5 | Sí | 7 embriones | Embriones: E10-13 |
| 6 | No | − | − |
| 7 | Sí | 6 embriones | Embriones: E18-19 |
| 8 | Sí | 8 crías | Semana parto: 5 |
| 9 | No | − | − |
| 10 | Sí | 7 embriones | Embriones: E15 |
a El momento del parto se definió como semanas transcurridas desde el primer día de inicio de cruces con machos competentes.
El número medio de crías/embriones por hembra embarazada fue de 4,7 (mediana 6,5 crías/hembra). No se observaron anomalías a nivel macroscópico en los fetos ni en las crías nacidas.
Estos resultados sugieren que la administración de Na2WO4 mantiene la recuperación de la ovulación y permite la recuperación de la fertilidad en ratones hembra IRS-2−/−
DiscusiónEste estudio pretende hacer una primera aproximación experimental para determinar el efecto del Na2WO4 sobre la capacidad reproductiva un modelo animal, ratones hembra IRS-2−/−. Los resultados sugieren por primera vez, a nuestro conocimiento, los efectos directos del Na2WO4 en la fertilidad femenina. En estudios anteriores, Ballester et al. (2007) demostraron que la restauración parcial del metabolismo de la glucosa en ratas diabéticas tras la administración de Na2WO4 durante 11 semanas recupera parcialmente la capacidad fértil de las hembras. Sin embargo, nuestro estudio demuestra un efecto del Na2WO4 en la restauración del ciclo estral en tras solo 7días de tratamiento e independientemente de cambios en los niveles de glucosa y en la ganancia ponderal.
El modelo animal utilizado, IRS-2−/−, representa un modelo útil para estudiar las deficiencias en el sistema reproductivo, especialmente las relacionadas con la resistencia a la leptina. Las alteraciones en la función ovárica y en la señalización a nivel hipotalámico de estos animales presentan similitudes con diversas alteraciones en humanos, como el síndrome del ovario poliquístico o la obesidad, que tienen un importante impacto sobre la fertilidad (Burks et al., 2000). Así, los efectos del Na2WO4 aquí presentados podrían tener una traducción en posibles tratamientos en el manejo de la fertilidad en humanos.
El objetivo principal de esta prueba de concepto fue el estudio del ciclo ovárico en el modelo animal. En estudios anteriores con ratones hembras IRS-2−/− se ha observado una drástica disminución de folículos antrales frente a los animales wild-type, y la práctica ausencia de cuerpos lúteos, indicando la anovulación como causa de la infertilidad en estos animales (Burks et al., 2000). Una técnica clásica para el estudio del ciclo estral en roedores in vivo se basa en el análisis de citologías vaginales (Deb et al., 2006). Mediante esta técnica se pueden identificar las 4 fases del ciclo estral en roedores que ciclan normalmente, mientras que en animales anovuladores solo se pueden identificar las fases iniciales anestro/diestro y proestro. En nuestros resultados se observa que en las fases de pretratamiento ninguna de las citologías realizadas se encuentran en estadios tardíos del ciclo, indicando ausencia de ciclo estral y, por tanto, de ovulación. Sin embargo, tras solo 7días de tratamiento con Na2WO4 se observan citologías en los 4 estadios, indicando la recuperación del ciclo estral. En este experimento las citología se han realizado en días no consecutivos, lo que puede suponer una limitación del estudio, pero teniendo en consideración que la duración del ciclo estral en ratones es de 4-5días (Salvador, 2001), con la distribución de los días en que se realizan las medidas deberían identificarse estadios avanzados del ciclo en la fase de pretratamiento. Adicionalmente se observa que en el último día de recogida de las citologías hay una reducción en el número de hembras en estadios tardíos del ciclo (estro y metaestro). El diseño del estudio no permite determinar si se trata de un efecto aleatorio en el que la mayoría de los animales se encuentran en fases tempranas de un ciclo recuperado y normal, o de una disminución del efecto del tratamiento. Sin embargo, el hecho de que estas hembras se queden embarazadas en días posteriores nos sugiere que el Na2WO4 mantiene su actividad en la función ovárica a medio y largo plazo.
La recuperación de la ovulación es el paso previo para la restauración de la fertilidad en hembras IRS-2−/−. Estas presentan solo un 9% de tasa de embarazo al cruzarlos con machos wild-type competentes, mientras que en nuestro trabajo la tasa de embarazo se eleva hasta el 80% al tratar con Na2WO4. Estos resultados certifican que los ratones han recuperado la función ovárica, tal y como indicaban las citologías vaginales. Se ha observado una tardanza en el embarazo en varios de estos animales. Las causas de este retraso en conseguir el embarazo no quedan esclarecidas en nuestro trabajo. La ausencia de un grupo control y la ausencia de datos en la publicación de Burks et al. (2000) respecto al tiempo requerido por estos animales para conseguir un embarazo impiden evaluar si este efecto está relacionado con el tratamiento con Na2WO4 o si los tiempos se encuentran dentro de la normalidad. Este efecto se deberá estudiar en profundidad en futuros estudios controlados. Otro aspecto metodológico a discutir es la administración de Na2WO4 a los machos competentes y el efecto que puede producir en la capacidad fértil de estos. Sin embargo, trabajos anteriores han descartado cualquier efecto positivo o deletéreo del Na2WO4 sobre la fertilidad en ratones machos (Ballester et al., 2005), por lo que el efecto en este experimento es negligible.
No se han observado anomalías macroscópicas en las crías ni en los embriones, en concordancia con los estudios preclínicos de seguridad que se han realizado con el Na2WO4.
El estudio demuestra un efecto sistémico del Na2WO4 sobre la fertilidad mediante la restauración de la ovulación. En el modelo IRS-2−/− no se han descrito alteraciones a nivel uterino ni embriónico, pero no podemos descartar que el Na2WO4 tenga actividad directa en estos tejidos. De hecho, hay evidencias que indican que tanto la leptina como el receptor de leptina juegan un papel fundamental en la comunicación embrión-endometrio en el momento de la implantación (Ramos et al., 2005), y la vía de señalización JAK/STAT es crítica en este proceso (Gonzalez y Leavis, 2003; Catalano et al., 2005; Nakamura et al., 2006; Salamonsen et al., 2010). Además, la señal de leptina induce la secreción de factores de crecimiento vasculares endotelial (VEGF) en células endometriales, mecanismo por el que la leptina impactaría en el proceso de implantación. Diversos trabajos han demostrado el efecto del Na2WO4 sobre la expresión de VEGF (Bertinat et al., 2015) y sobre la modulación de la fosforilación de JAK-2 y STAT-3, principal mecanismo de modulación de la señal de leptina (Amigó-Correig et al., 2011). Adicionalmente, experimentos realizados en nuestro grupo de trabajo en colaboración con el Dr. Simón (FundaciónIVI) nos muestran un efecto directo del Na2WO4 sobre células endometriales (HEC-1A), aumentando hasta un 69% la tasa de adhesión de esferoides JEG-3, tras 24h de incubación con Na2WO4 (datos no publicados). Por tanto, el efecto del Na2WO4 sobre otros procesos clave en la fertilidad, como la implantación o la placentación, no pueden ser descartados y deben ser estudiados.
Como se ya se ha comentado, este trabajo pretende ser una primera aproximación experimental para determinar cuál es el papel del Na2WO4 en el manejo de la fertilidad en modelos con resistencia a la leptina. Las limitaciones experimentales son importantes, por lo que los resultados deben ser confirmados en estudios controlados y de diseño robusto. La ausencia de un grupo control o la realización de las citologías en días no consecutivos dificultan la interpretación de los datos. Sin embargo, la contundencia de los hallazgos en esta prueba de concepto nos sugiere una actividad relevante del Na2WO4 en el manejo de la fertilidad. Otras moléculas con actividad inhibidora de fosfatasas, como derivados del molibdeno, vanadio, cromo o selenio, o sales de tungsteno diferentes al Na2WO4 (Hsu y Goetz, 1992), también podrían ser efectivas en el tratamiento de la infertilidad o la mejora de la eficiencia reproductiva en mamíferos.
Los resultados de esta primera aproximación experimental indican que el Na2WO4 es capaz de recuperar el ciclo estral en ratones hembra IRS-2−/− anovuladoras, por lo menos en las primeras semanas de tratamiento, y conseguir altas tasas de embarazo. Estos resultados abren el interés hacia un estudio controlado y de diseño experimental más robusto que permita definir el efecto del Na2WO4 en la fertilidad en mamíferos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener conflicto de intereses en la elaboración de este trabajo.
Los autores agradecen a R. Gomis, F. Hanzu y J. Calaf por sus consejos durante el desarrollo del estudio y la revisión crítica de los resultados presentados en este manuscrito.
Ignasi Canals y Agnès Arbat han contribuido por igual en la elaboración de este trabajo.