Introducción: La analgesia multimodal preventiva consiste en la administración de fármacos analgésicos, para conseguir una disminución en la respuesta sensitiva al dolor. Con esto se pretende interrumpir el círculo inflamación-dolor-hiperalgesia. El objetivo de la analgesia multimodal preventiva es reducir los requerimientos analgésicos posoperatorios y el riesgo de hiperalgesia primaria o secundaria, y alodinia.
Objetivo: Evaluar la eficacia de la analgesia multimodal preventiva para dolor posoperatorio.
Material y métodos: Se efectuó un estudio experimental, longitudinal, comparativo, prospectivo, ciego, aleatorizado, que incluyó 26 pacientes divididos en dos grupos. El grupo uno consistió en 13 pacientes programados para colecistectomía abierta, en quienes se infiltró previo a la incisión quirúrgica, ropivacaína al 0.2%. El grupo dos también constaba de 13 pacientes programados para colecistectomía abierta, a éstos se les administró NaCl 0.9%. Se valoró la presión arterial, frecuencia cardiaca, frecuencia respiratoria y escala visual análoga a las dos, cuatro, seis, 12 y 24 horas posteriores al acto quirúrgico.
Resultados: No se observó una diferencia estadísticamente significativa en la presión arterial, frecuencia cardiaca y frecuencia respiratoria. Sin embargo, se observó una diferencia en la escala visual análoga, encontrándose una mayor puntuación en el grupo dos a las cuatro, seis y 12 horas. También hubo un mayor número de dosis de analgésico de rescate en el grupo dos.
Conclusiones: Encontramos una eficacia significativa de la analgesia multimodal, mejorando el manejo del dolor posoperatorio.
Introduction: Preventive multimodal analgesia consists of the administration of analgesic drugs to reduce response to pain. With this, we seek to interrupt the cycle of inflammation-pain-hyperalgesia. The objective of preventive multimodal analgesia is to reduce the need for postoperative analgesics and the risk of primary or secondary hyperalgesia, and allodynia.
Objective: Evaluate the efficacy of preventive multimodal analgesia for postoperative pain.
Material and methods: We performed an experimental, longitudinal, comparative, prospective, blind, randomized study that included 26 patients divided into two groups. Group one consisted of 13 patients programmed for open cholecystectomy in who 0.2% ropivacaine was infiltrated before surgical incision. Group two also consisted of 13 patients programmed for open cholecystectomy. In these, 0.9% NaCl was administered. Blood pressure, heart rate, respiratory rate, and visual analogue scale were evaluated two, four, six, 12, and 24 hours postoperatively.
Results: No statistically significant differences in blood pressure, heart rate, respiratory rate were observed. However, a difference in the visual analogue scale was found with a greater score in group two at four, six and 12 hours. Also, a greater number of additional rescue doses of analgesics were required in group two.
Conclusions: We found that preventive multimodal analgesia was significantly effective in improving postoperative pain.
Introducción
El anestesiólogo emplea una estrategia perioperatoria para brindar al paciente la mejor técnica analgésica desde la etapa preoperatoria. El tratamiento del dolor posoperatorio requiere una atención especializada, dadas las importantes repercusiones que tiene en la recuperación del paciente tras la intervención quirúrgica.
El objetivo principal de una buena analgesia posoperatoria en cirugía abdominal es proporcionar una analgesia profunda, en tanto se logra la recuperación funcional. Los componentes del dolor posoperatorio abdominal1 incluyen: dolor somático cutáneo, dolor somático profundo,2 sensibilización de nociceptores, dolor visceral,3 dolor referido.
Prevalencia del dolor posoperatorio
Unas 15 millones de personas sufren dolor posoperatorio en todo el mundo.4 Se caracteriza por ser agudo, previsible, de duración limitada, afecta el sueño, no tiene función biológica, surge en pacientes con estricto control médico y la mayoría de los enfermos carecen de antecedentes de enfermedades importantes.5 La American Association of Anesthesiologist define el dolor agudo posoperatorio como "el dolor que está presente en el paciente quirúrgico debido a la enfermedad, al procedimiento quirúrgico y a sus complicaciones o a una combinación de ambos".6
Chung y colaboradores en un estudio realizado en Canadá en 10 008 pacientes, encontraron que 5.3% de los pacientes tenían dolor severo en las primeras 24 horas del posoperatorio, las especialidades con mayor incidencia de dolor posoperatorio fueron Ortopedia (16.1%), Urología (13.4%), Cirugía General (11.5%) y Cirugía Plástica (10%).7,8
Los principales factores que influyen en la aparición, la intensidad, la cualidad y la duración del dolor posoperatorio dependen del paciente, de la intervención quirúrgica y de la técnica anestésica.9
Las repercusiones orgánicas del dolor posoperatorio pueden llegar a ocasionar importantes respuestas psicológicas. La situación puede complicarse, haciendo que el dolor posoperatorio no tratado llegue a desencadenar cuadros de dolor crónico rebeldes al tratamiento.9
El tratamiento efectivo permite disminuir la incidencia de complicaciones, así como la estancia media hospitalaria y el coste total del paciente posoperado, aumentando la satisfacción del paciente y la eficacia del tratamiento.4
Medición del dolor posoperatorio
Es importante aplicar las escalas de valoración del dolor en situación basal, es decir, antes de iniciar la intervención quirúrgica, pues hay pacientes afectados por diversas patologías (síndromes fribromiálgicos, síndrome miofascial, artrosis, entre otros), que pueden afectar los resultados obtenidos.4
El dolor consta de dos aspectos diferentes: afectivo y sensorial, que lo convierten en una experiencia única, subjetiva y multidimensional, lo que hace muy difícil su valoración y cuantificación.10,11
En 1976, Huskinsson presentó la Escala Visual Analógica (EVA), consiste en una línea horizontal o vertical de 10 cm, con los extremos marcados con dos líneas. El paciente debe indicar sobre una línea continua la intensidad de su dolor, en relación con los extremos de la misma. También se puede utilizar para evaluar el grado de alivio del dolor. Es un método simple, sólido, sensible, fiable y reproducible.10-12
Repercusiones del dolor posoperatorio
La respuesta autonómica como consecuencia del dolor da un incremento en la frecuencia cardiaca, resistencias vasculares periféricas, aumento de la presión arterial y la contractilidad miocárdica. Todas dan como consecuencia un incremento en el consumo de oxígeno miocárdico, por incremento del gasto cardiaco.13
Un control inadecuado del dolor, sobre todo después de la cirugía de abdomen alto, puede provocar disfunción pulmonar, incrementando de esta manera las complicaciones pulmonares posoperatorias.14 La respuesta espinal refleja, secundaria al estímulo nocivo, provoca espasmos musculares reflejos en la zona afectada y en el grupo de músculos de la región, disminuyendo la movilidad de los mismos, con la consecuente hipoventilación e hipoxemia. Como resultado de la disfunción diafragmática se da el deterioro de la ventilación, disminuyendo de esta manera la capacidad vital hasta en 40%.15
Al haber un incremento en la actividad simpática, hay un aumento en el tono del músculo liso, así como de las secreciones gastrointestinales, en tanto se disminuye la motilidad intestinal. Si a esto se agrega una analgesia opioide, se podría contribuir indirectamente a disminuir aún más la motilidad intestinal.16,17
Dolor posoperatorio persistente
Se define como aquel dolor que persiste al menos dos meses después del procedimiento quirúrgico, excluyendo obviamente la causa preoperatorio como condicionante del dolor.18,19
Las diferentes técnicas analgésicas pueden proporcionar diferencias en la calidad de la analgesia, de ésta manera las técnicas de analgesia regional han demostrado ser superiores cuando se comparan con la administración sistémica de opioides.20 El concepto de analgesia multimodal fue introducido para obtener estos resultados, combinando diferentes técnicas analgésicas con diferentes clases de analgésicos para mejorar los resultados posoperatorios.20 La efectividad individual de los analgésicos puede ampliarse combinando la acción de mecanismos diferentes.21
Anestésicos locales
Se han utilizado anestésicos locales para el manejo de dolor posoperatorio, y por muchos años la lidocaína y la bupivacaína han permanecido dentro del armamento del anestesiólogo.22
Existen reportes de efectos tóxicos, en particular los referidos de la bupivacaína, esto ha conducido a una serie de estudios que identifican la acción de la estéreo selectividad en el corazón, y subsecuentemente el descubrimiento de dos nuevos fármacos anestésicos: la ropivacaína y la levobupivacaína.23
Uno de los beneficios de los anestésicos locales es su acción moduladora en el proceso inflamatorio, lo cual ha sido demostrado en numerosos estudios. En cuanto a los beneficios de los anestésicos epidurales, consisten en que su absorción se lleva a cabo en el torrente sanguíneo, y este mismo efecto antiinflamatorio les concede a la vez, ser antitrombóticos.23,24
Analgesia para cirugía de abdomen alto
Los agentes antiinflamatorios no esteroideos (AINES) son los más usados como parte de la analgesia multimodal, desde el decenio de 1990.25 La ventaja principal es el ahorro del consumo de opioides, y con esto posiblemente disminuyen los efectos colaterales de los mismos. Las dosis recomendadas de estos en cirugía abdominal, son ya conocidas por todos: 60 mg de ketorolaco vs 40 mg de parecoxib.26
Ketorolaco trometamina es un potente analgésico, siendo uno de los pocos analgésicos no esteroideos en presentación parenteral así como enteral. Su actividad analgésica es mayor que su efecto antiinflamatorio. Es indicado para el manejo del dolor, solamente durante un corto plazo (menos de cinco días) y no es aconsejado su uso para dolor crónico.27
La analgesia epidural ofrece una mejor analgesia posoperatoria comparada con los opioides sistémicos.28 La localización del catéter puede afectar la eficacia, en un sitio congruente con el sitio dermatomérico de la incisión, lo cual mejora la calidad de la analgesia. Si se coloca a nivel torácico pudiera disminuir los efectos colaterales, ya que se evitará el bloqueo de fibras simpáticas T9-L1. Además, el catéter epidural torácico mejora el flujo sanguíneo coronario, disminuye las complicaciones pulmonares y reduce la inhibición del tono gastrointestinal, y de esta manera el retorno del peristaltismo intestinal es más rápido.29
Los anestésicos locales tienen la capacidad de bloquear las señales aferentes y eferentes de la medula espinal, con lo que se logra suprimir la respuesta quirúrgica al estrés.30 La absorción del anestésico local facilita el rápido retorno de los movimientos peristálticos, disminuye la inflamación y favorece la viscosidad de la sangre.31 Sin embargo, es recomendable su combinación con opioides para disminuir la concertación del anestésico local.
De ser posible, la duración de la analgesia debe ser de entre dos y cuatro días en casos de cirugía mayor, ya que se ha demostrado que una analgesia menor a 24 horas no proporciona el beneficio del retorno temprano de la motilidad gastrointestinal.
Aunque resulta claro que la analgesia multimodal mejora el dolor posoperatorio, no hay datos suficientes para dar un régimen multimodal óptimo, para una cirugía o paciente específico.32
Las técnicas de analgesia regional se están volviendo parte fundamental del abordaje multimodal. Los analgésicos no opioides deben ser utilizados con horario. Los opioides deben emplearse principalmente como analgésicos de rescate, con base en que sus efectos colaterales pudieran retrasar la evolución del paciente.
Analgesia multimodal
La escalera analgésica es la mejor demostración de la utilización multimodal de los analgésicos, la cual recomienda el manejo progresivo de los diferentes tipos, con una evaluación continua del dolor.33 La analgesia posoperatoria multimodal es la más empleada actualmente, y comprende la combinación de varias técnicas y analgésicos.
Material y métodos
Es un estudio realizado en el Hospital Universitario Dr. José Eleuterio González, de la Facultad de Medicina, de la Universidad Autónoma de Nuevo León. Estudio experimental, longitudinal, comparativo, prospectivo, ciego y aleatorizado. El Comité de ética de nuestra institución revisó y autorizó el proyecto. El estudio fue realizado durante el periodo comprendido de noviembre 2011 - febrero 2012. Los criterios de inclusión fueron: edad mayor de 18 años y menor de 65 años, pacientes ASA I y II programados para cirugía colecistectomía abierta, con técnica anestésica de anestesia general y bloqueo epidural torácico. Los criterios de exclusión fueron: paciente embarazada, fuera del rango de edad estimado, contraindicación para el bloqueo epidural torácico, alergia a los anestésicos locales, opioides y/o AINES. Los criterios de eliminación fueron: bloqueo epidural torácico fallido, hallazgos transquirúrgicos que amplíen la cirugía.
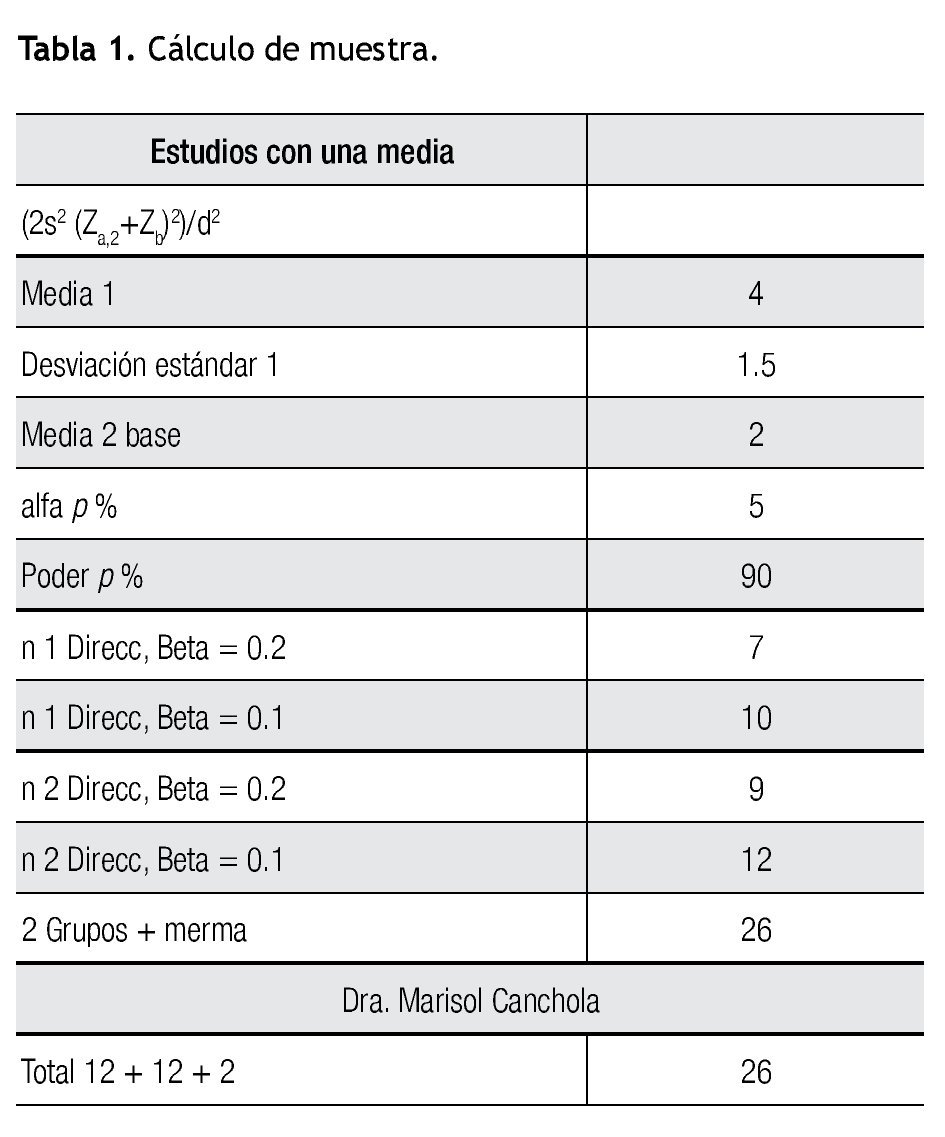
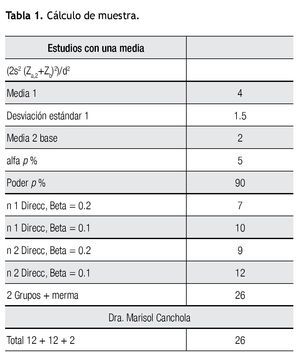
Se realizó el cálculo de la muestra en base al artículo publicado por Bisgaard Thue y colaboradores, en la revista Anesthesia & Analgesia en 1999, utilizando la siguiente fórmula: 2s2 (Za,2+Zb)2)/d. Con esto se obtuvo, una n de 26 pacientes, los cuales se dividieron en dos grupos de 13 pacientes cada uno (Tabla 1).
Nuestro objetivo general es valorar la eficacia analgésica de la infiltración local de ropivacaína vs solución fisiológica antes de la incisión quirúrgica, agregada a un AINE como ketorolaco 0.5 mg/Kg I.V. y un opioide débil como tramadol 0.5 mg/Kg I.V., ambos administrados 30 minutos antes de terminar el procedimiento quirúrgico, como tratamiento del dolor posoperatorio. Por medio de una tabla de números aleatorias, se determinó el grupo al que pertenecería cada paciente. Una vez en la sala quirúrgica, se realizó monitorización tipo uno. Posteriormente, todas las pacientes recibieron bloqueo epidural torácico y anestesia general como técnica anestésica, y previo a la incisión quirúrgica se infiltró el medicamento de estudio.
En el grupo uno, se administró al paciente ropivacaína al 0.2% y en el grupo dos, se NaCl 0.9%. Posteriormente se registró la tensión arterial, frecuencia cardiaca, frecuencia respiratoria, intensidad del dolor (a través del EVA, por medio de una regla graduada con números del cero al 10) a las dos, cuatro, seis, 12, 24 horas posoperatorias. Se administró tradol 1 mg/Kg I.V. como medicamento de rescate, si la paciente refería una EVA mayor de cinco.
Análisis estadístico
Se contrastaron los resultados de acuerdo a las distribuciones que presentaron los datos de los resultados, para distribuciones tipo normal (paramétricas) se usó la prueba de t de student, para distribuciones tipo no normal (no paramétricas) se usó prueba ji cuadrada.
El proceso electrónico de datos y métodos de estadística descriptiva e inferencial, se llevó a cabo con el programa STATA-IC-10-2008.
Resultados
Se obtuvo una n total de 26 pacientes, divididos en dos grupos, grupo uno y dos, cada uno con 13 pacientes.
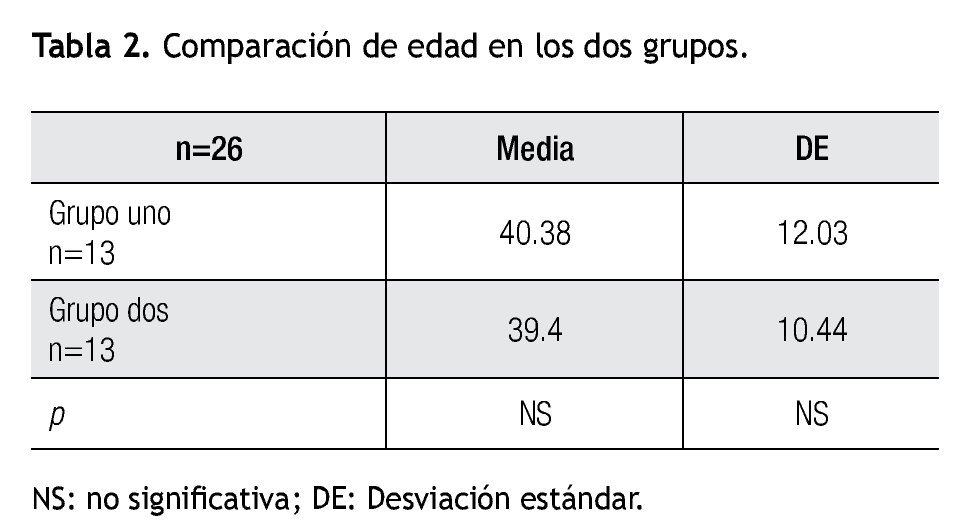
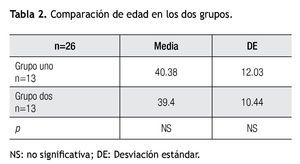
El grupo uno tiene el 69.23% de pacientes del sexo femenino y 30.76% del sexo masculino, mientras que el grupo dos tiene un 76.92% de pacientes del sexo femenino y 23.07% del sexo masculino. Se obtuvo una media de 40.38 ± 12.03 años de edad y 39.46 ± 10.44 años de edad, en el grupo uno y dos; respectivamente (p=No significativa NS) (Tabla 2).
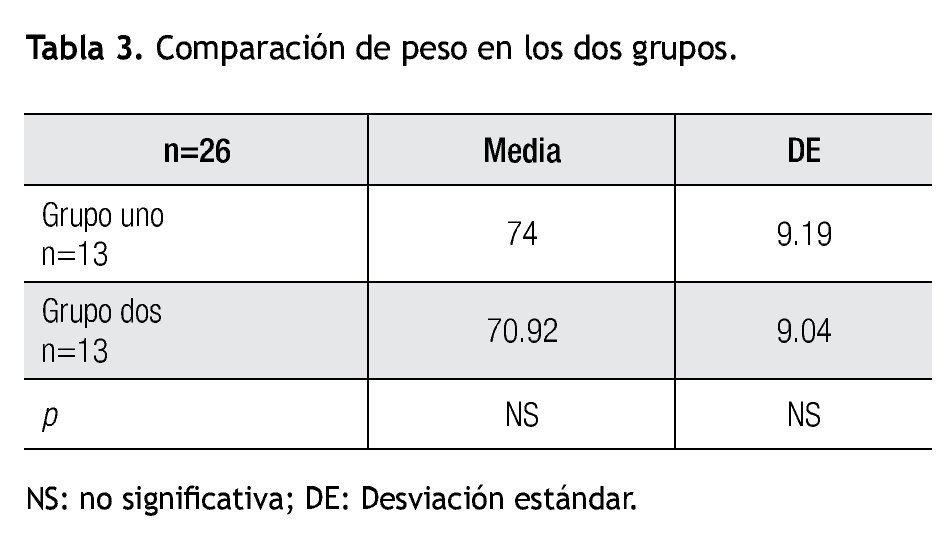
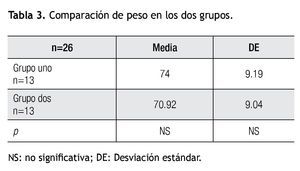
Con respecto al peso observamos una media de 74 ± 9.19 para el grupo uno, y 70.92 ± 9.0 para el grupo dos, con tendencia al sobrepeso, sin embargo, no fue significativa (p=NS) (Tabla 3).
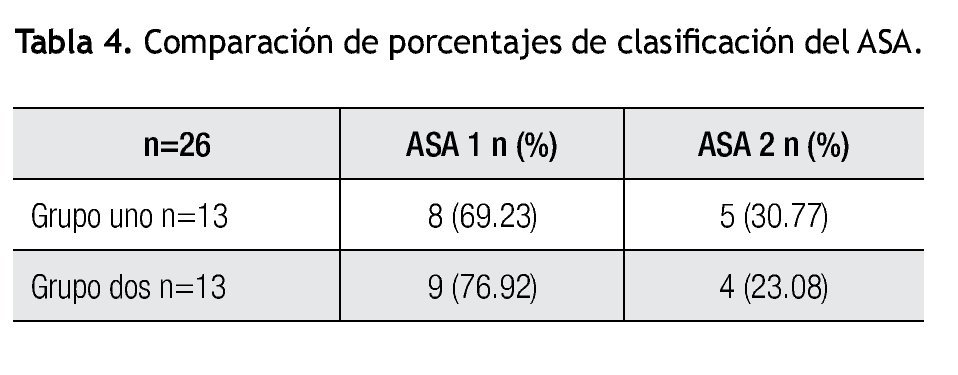
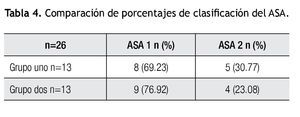
En la clasificación del ASA en ambos grupos, se observó un mayor porcentaje de ASA I 69.23% en el grupo uno y 76.92% el grupo dos, ASA II 30.77% en el grupo uno y 23.08% para el grupo dos (Tabla 4).
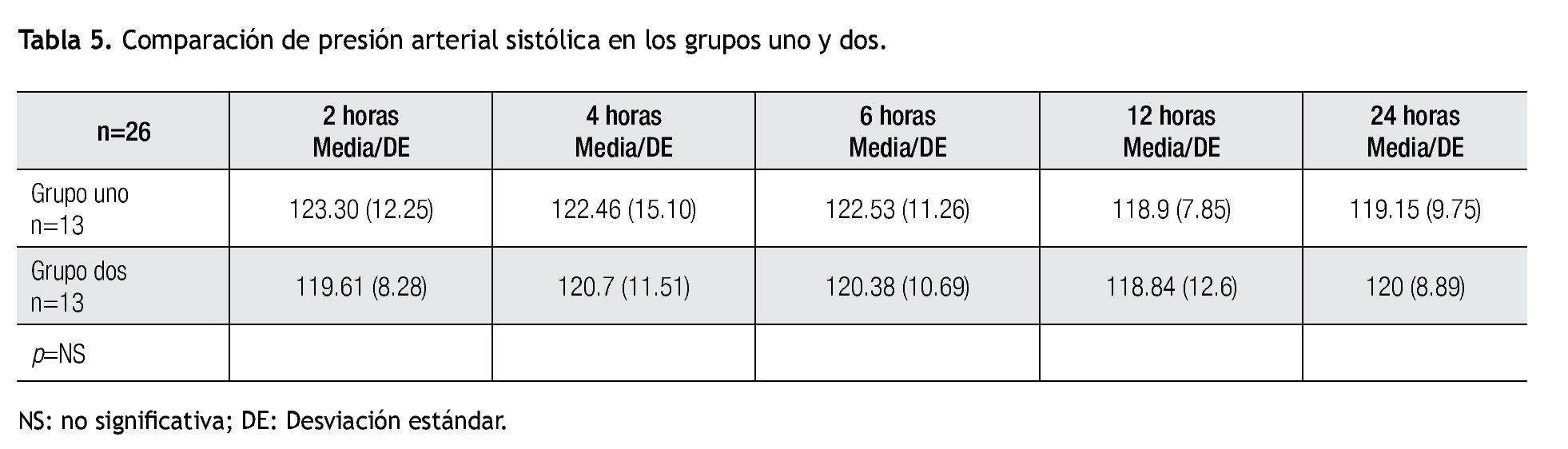
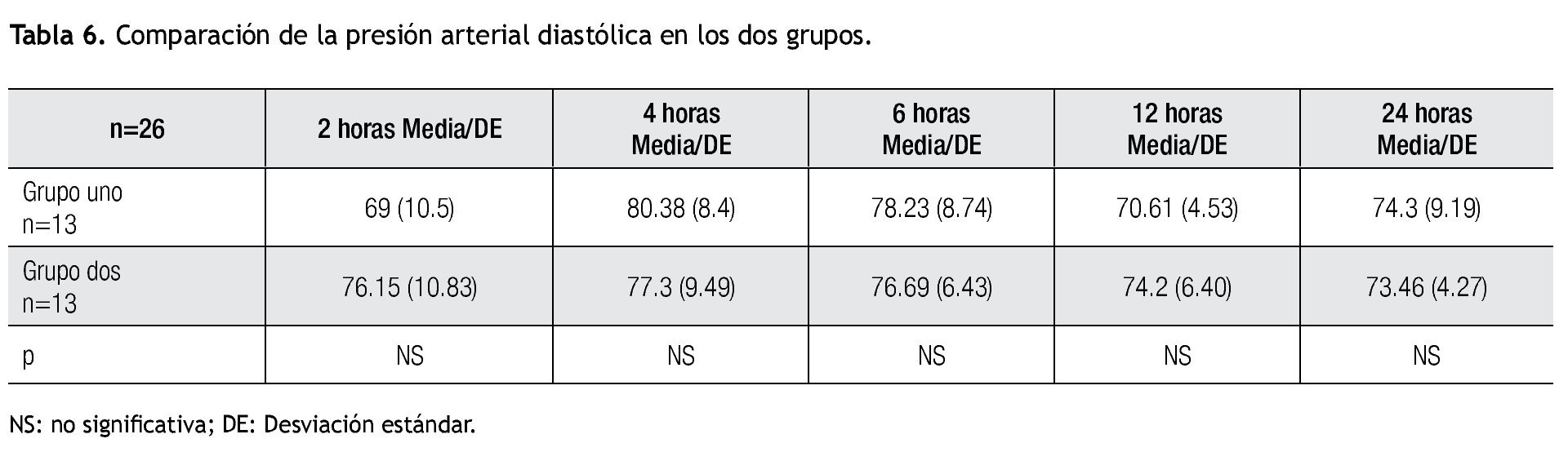
En la presión arterial sistólica/diastólica no se observó una diferencia significativa en las tomas posoperatorias a las dos, cuatro, seis, 12, 24 horas (p=NS) (Tablas 5 y 6).
No se observó una diferencia estadísticamente significativa en cuanto a los datos demográficos, ni los signos vitales (presión arterial sistólica, presión arterial diastólica, frecuencia cardiaca y frecuencia respiratoria) en el posoperatorio.
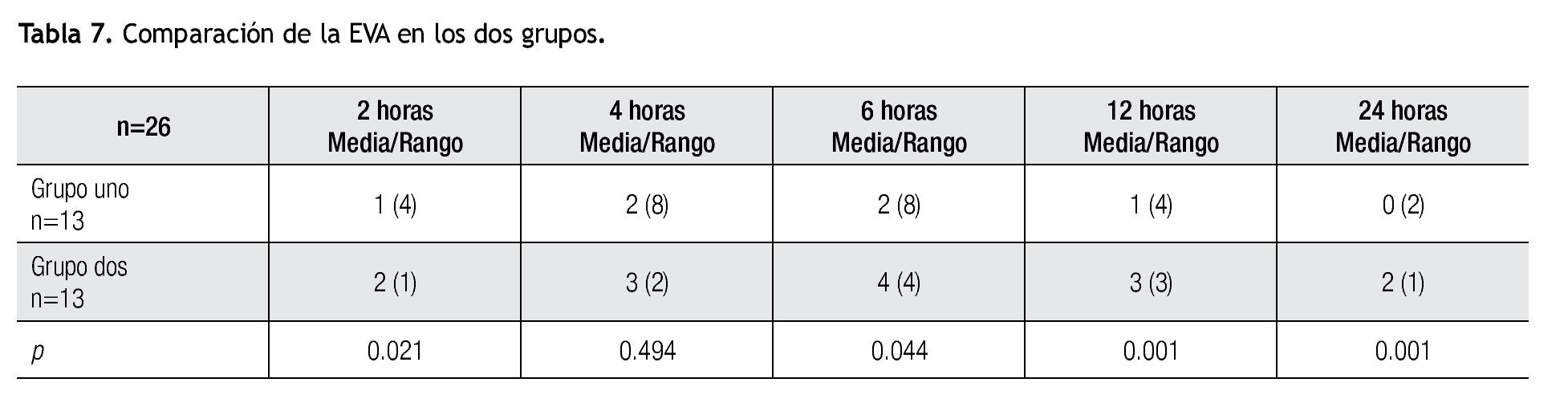
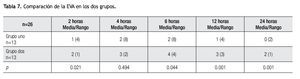
Se observó una diferencia significativa en la EVA a las dos horas (p=0.021), a las cuatro horas (p=0.494), a las seis horas (p=0.044), a las 12 horas (p=0.001) y a las 24 horas de (p=0.001) (Tabla 7).
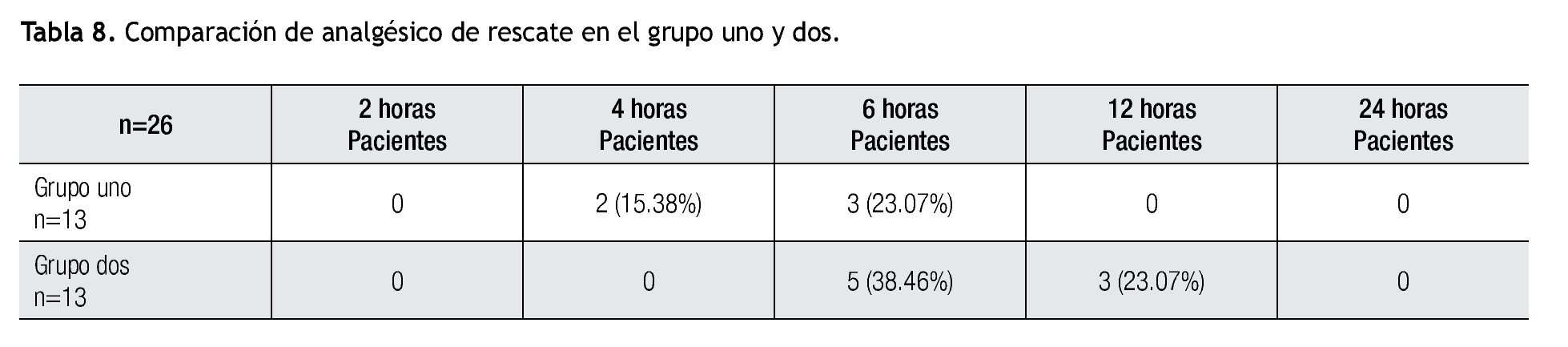
El requerimiento de analgésico de rescate (tradol 1 mg/Kg I.V.) a las dos horas fue cero para ambos grupos, a las cuatro horas fue de 15.38% para el grupo uno (dos pacientes), y de cero para el grupo dos; a las seis horas fue de 23.07% (tres pacientes) para el grupo uno y de 38.46% (cinco pacientes) para el grupo dos; a las 12 horas fue de cero en el grupo uno y 23.07% (tres pacientes) para el grupo dos; a las 24 horas, por último, fue de cero para ambos grupos (Tabla 8).
Discusión
El objetivo de la analgesia multimodal es la reducción de los requerimientos analgésicos posoperatorios y reducir el riesgo de hiperalgesia primaria o secundaria, y alodinia.34 Varios estudios han presentado informes sobre los anestésicos locales preventivos para aliviar el dolor posoperatorio, los cuales han mostrado resultados contradictorios.
La infiltración con ropivacaína previo a la incisión quirúrgica, además de un AINE y un opioide débil, administrados en el transoperatorio, mejora el control del dolor posoperatorio.
En nuestro estudio se comparó la infiltración con ropivacaína al 0.2% vs Na Cl 0.9% (placebo), ya que no se encontró literatura médica suficiente donde se demuestre la superioridad de la analgesia multimodal preventiva con anestésico local.
Se encontró un mejor manejo del dolor posoperatorio con la infiltración de ropivacaína, valorado por la EVA y el menor requerimiento de analgésico de rescate, comparado con el placebo. No se observó una diferencia significativa en cuanto a la modificación de los signos vitales.
Finalmente, encontramos que la infiltración de ropivacaína previo a la incisión quirúrgica es una alternativa para el tratamiento de dolor posoperatorio, con mínimos efectos adversos, además de que recomendamos una terapia analgésica multimodal.
Conclusiones
En este estudio se demostró una superioridad significativa de la analgesia multimodal, utilizando como anestésico local ropivacaína previo a la incisión quirúrgica, en base a los datos obtenidos en la EVA a las dos, cuatro, seis, 12, y 24 horas.
En cuanto a los signos vitales (presión arterial, frecuencia cardiaca, frecuencia respiratoria) no se observó diferencia. La analgesia es similar a las dos y 24 horas en ambos grupos.
Por lo anterior, podemos concluir que la administración del anestésico local ropivacaína al 0.2% por infiltración local, previo a la incisión quirúrgica como parte de la analgesia multimodal es eficaz para el manejo de dolor posoperatorio
Recibido: Febrero 2012. Aceptado: Marzo 2012
Correspondencia:
Dr. Gustavo González Cordero.
Servicio de Anestesiología, del Hospital Universitario José Eleuterio González de la Facultad de Medicina de la Universidad Autónoma de Nuevo León.
Av. Madero y Gonzalitos s/n,
Colonia Mitras Centro.
C.P. 64460. Monterrey, N. L., México.
Correo electrónico: ggcordero@yahoo.com