Evaluar la factibilidad de implementar un plan de actividad física en pacientes con enfermedad renal crónica en hemodiálisis crónica. Analizar beneficios aportados en calidad de vida, tolerancia al ejercicio, desarrollo de capacidad aeróbica y resistencia y fuerza muscular de la extremidad inferior así como los parámetros metabólicos y nutricionales, presión arterial y dosis de diálisis.
Material y métodosEstudio de intervención con diseño antes-después. Se consideró el porcentaje de adherencia y abandono. Se evaluó previo y al final del programa: calidad de vida, parámetros clínicos, pruebas de laboratorio, masa magra y agua corporal. Se evaluó capacidad aeróbica a través del test de marcha de 6minutos. También se evaluó fuerza muscular dinámica e isométrica mediante prueba de levantarse de la silla y dinamometría. Se llevó a cabo un plan de ejercicio aeróbico mediante una pedalera y de resistencia muscular mediante ejercicios contra una resistencia elástica.
ResultadosSetenta y siete pacientes cumplían criterios de inclusión, 34 (44%) iniciaron la actividad física y 3 (3,9%) abandonaron el programa. Se observó un aumento estadísticamente significativo (p<0,05) del test de marcha de 6minutos y del puntaje en las pruebas funcionales. También de la masa magra y del porcentaje de reducción de urea. Se observó una disminución significativa del agua corporal, la ganancia intradialítica y la presión arterial.
ConclusiónEs factible realizar un programa de actividad física intradialítica. La implementación y sustentación requieren la ponderación del paciente y estrategias para mejorar la adherencia al mismo y una dosis individualizada y adecuada de ejercicio para cada paciente.
To assess the feasibility of implementing an exercise programme in patients with end stage renal disease on haemodialysis treatment. To assess the impact on quality of life, exercise tolerance, development of aerobic capacity, as well as metabolic and nutritional parameters, blood pressure and dialysis dose.
Material and methodsInterventional study with a before and after design. Adherence and abandonment was established by percentage. Quality of life, clinical characteristics, laboratory tests, lean body mass, and total body water was evaluated before and after the programme. Aerobic capacity was tested using the 6minutes walking test. Dynamic and isometric muscle strength was also evaluated by the chair-stand test and dynamometry. An aerobic exercise plan was carried out using a pedal board and muscular endurance through exercises against elastic resistance.
ResultsA total of 77 patients met the inclusion criteria, 34 (44%) initiated physical activity and 3 (3.9%) abandoned the programme. A statistically significant increase (P<.05) was observed for 6minutes walking test, the functional test score, the lean body mass, and the urea reduction ratio. On the other hand, a significant decrease was observed in body water, intra-dialysis gain, and blood pressure.
ConclusionIt is feasible to carry out an intra-dialysis exercise programme. Implementation and sustainability require patient empowerment and strategies to improve adherence, such as an individualised exercise plan for each patient.
La prevalencia de enfermedad renal crónica (ERC) en terapia de reemplazo renal muestra un incremento significativo en Latinoamérica en los últimos años, desde 119 pacientes por millón de habitantes en 1991 a 601 pacientes por millón de habitantes en 2012 [1]. La hemodiálisis (HD) crónica es la terapia de reemplazo renal de mayor prevalencia en la región latinoamericana (82%) [1]. La Diabetes es la principal causa de ERC. La edad de la población en terapia de reemplazo renal muestra un incremento progresivo a lo largo de los últimos años [1]. Esta población presenta una mayor morbimortalidad cardiovascular, siendo que un paciente de 30 años de edad en HD crónica presenta la misma condición cardiovascular que en una persona de 70 años de edad sin ERC [2]. La Argentina muestra una situación similar al resto de los principales países de Latinoamérica [1,3].
En los pacientes con ERC las alteraciones musculares son factores limitantes de su capacidad funcional [4]. Además hay una declinación progresiva de la capacidad funcional después del inicio de programas de HD [5]. Se pueden atenuar algunas anormalidades metabólicas de la ERC durante la terapia de reemplazo renal, pero durante procedimientos dialíticos hay pérdida de aminoácidos y la liberación de citocinas lleva a un mayor catabolismo proteico muscular y síntesis de proteínas durante la fase aguda [6].
Los pacientes en HD tienen niveles bajos de actividad física diaria; si se compara con sujetos sanos como controles, se considera que un paciente de 30 años sometido a HD tiene menos actividad física diaria que un individuo sano y sedentario de 70 años de edad [7].
La atrofia muscular en los pacientes urémicos es consecuencia de una neuropatía urémica causada por degeneración axonal primaria con desmielinización segmentaria, o de una miopatía urémica debido a una estructura y funcionalidad anormal de las fibras musculares. Una HD efectiva puede corregir la neuropatía urémica pero la miopatía persiste [8].
No solo la inflamación urémica per se, sino también la acidosis metabólica, el estrés oxidativo, la malnutrición, la inactividad, la deficiencia de andrógenos, la resistencia a la insulina, los procedimientos de HD y las enfermedades concurrentes son todos factores que se relacionan con pérdida de la masa muscular. En los pacientes con ERC la pérdida de masa muscular se define como un «derroche de energía», que se caracteriza por el aumento de catabolismo de proteínas musculares con relación a la síntesis de proteína. El ejercicio es una medida preventiva para reducir la pérdida de proteína muscular y mantener la función muscular [9].
Existen programas que combinan ejercicio aeróbico y de resistencia muscular que pueden aumentar la fuerza y resistencia musculares, la capacidad funcional y la calidad de vida de pacientes en HD [10].
El ejercicio regular moderado puede modular la respuesta inflamatoria, lo que indicaría los beneficios en los pacientes con ERC. El entrenamiento aeróbico y de resistencia muscular durante la diálisis aumenta el flujo sanguíneo a nivel muscular, lo que dinamiza el flujo de urea y toxinas desde los tejidos hacia el compartimento vascular, lo que podría mejorar la eficacia de la diálisis [11,12].
La inactividad física representa un grave problema para los pacientes en HD. El desarrollo e implementación de un programa de actividad física podría tener importancia para mejorar la calidad de vida e inclusive tener una repercusión favorable en la morbimortalidad de estos pacientes [13].
Más allá de los beneficios atribuidos a los ejercicios físicos en esta población de riesgo, los programas sistematizados no constituyen aún una norma estandarizada de cuidado en los pacientes en HD en Latinoamérica.
Por lo tanto, nuestro objetivo principal fue evaluar la factibilidad de implementar un plan piloto de actividad física.
Como objetivos secundarios se propusieron analizar los posibles beneficios que puede aportar en la calidad de vida, la tolerancia al ejercicio, el desarrollo de su capacidad aeróbica y en el desarrollo de la resistencia y fuerza muscular de la extremidad inferior, los parámetros metabólicos y nutricionales, la presión arterial y la dosis de diálisis.
Material y métodoEstudio intervencionista con diseño antes-después sin grupo control. Se incluyeron pacientes con más de 3 meses en tratamiento en HD trisemanal, mayores de 18 años con una hemoglobina superior a 10mg/dl pertenecientes a una población de 140 pacientes del Hospital Italiano de Buenos Aires. La duración del estudio fue de 16 semanas. Tanto el protocolo de estudio como la información y el consentimiento informado para los participantes fueron aprobados por el Comité de protocolos de Investigación de dicho hospital.
Fueron motivos de exclusión, IAM en las 6 semanas previas, angina inestable durante el ejercicio o en reposo, alteraciones respiratorias o musculoesqueléticas que empeoran con el ejercicio, alteraciones neurológicas con déficit funcional, diabetes mellitus descompensada, amputados y pacientes con acceso vascular femoral. El protocolo del estudio se llevó a cabo bajo la supervisión de kinesiólogos, médicos, psicólogo, nutricionista y enfermeros de diálisis, con una frecuencia trisemanal. Se registró la edad de los pacientes, el sexo, el tiempo en diálisis, la causa de ingreso a diálisis, la presencia de diabetes o hipertensión, el tipo de acceso vascular y la duración del tratamiento dialítico.
Evaluación antes-despuésPara evaluar la factibilidad del ensayo se consideró el porcentaje de pacientes que se adhirieron al mismo, la cantidad que abandonaron y las causas que lo determinaron.
Para evaluar los objetivos secundarios, a los pacientes se le realizaron 2 evaluaciones, una previa al inicio del programa y la otra al finalizar. Las mismas incluían las siguientes variables: calidad de vida mediante 2 escalas, el EuroQol-5D [14,15] y el KDQuol [16]; parámetros clínicos como peso corporal, ganancia de peso interdialítica, presión arterial prediálisis; pruebas de laboratorio como hematocrito, creatininemia, albuminemia, transferrina sérica, calcemia, fosfatemia, ionograma, estado ácido base venoso, urea pre- y posdiálisis (para el cálculo de la dosis de diálisis); la masa magra y el agua corporal a través de bioimpedanciometría utilizando del BCM Fresenius; y por último las pruebas funcionales. Estas últimas fueron: el test de marcha de 6minutos [17] para evaluar la capacidad aeróbica, para evaluar la fuerza muscular dinámica se utilizó la prueba de levantarse de la silla [18], la fuerza muscular isométrica de cuádriceps y la fuerza del puño por dinamometría, con los equipos Nicholas manual tester y Jamar Hydraulic Hand Dynamometer respectivamente [19–21].
Programa de ejerciciosSe llevó a cabo un plan de ejercicio aeróbico y de resistencia muscular. La actividad fue intradialítica durante las 2 primeras horas de inicio de la diálisis. El paciente realizó ejercicio aeróbico utilizando una pedalera; comenzó con un tiempo mínimo de 15min de acuerdo a los resultados del test de marcha de 6minutos y aumentó progresivamente hasta llegar a 40min. Se controló la intensidad del trabajo mediante la frecuencia cardiaca de reserva y para este plan se estableció una intensidad del trabajo moderada entre un 40 a un 60% de la frecuencia cardiaca de reserva. Esta corresponde a [(220−edad)− frecuencia cardiaca de reposo)] × (60-90%)+frecuencia cardiaca de reposo [22]. Se interrumpió el ejercicio al presentarse una presión arterial>180/100 o <90/50mm Hg o caída brusca de la misma, o al mostrar síntomas tales como disnea, náuseas, palpitaciones o calambres. El plan de ejercicios para resistencia muscular consistió en ejercicios contra una resistencia elástica para cuádriceps, dorsiflexores del pie y glúteos. Se comenzó con 3 series de 6/8 repeticiones hasta llegar a 5 series de 10/12 repeticiones con bandas elásticas de baja densidad tipo «Theraband» con ambos miembros inferiores [23,24]. La sesión completa de ejercicio duró 30-60min; el tiempo se fue adecuando paulatinamente a cada paciente.
La negativa a la participación en el protocolo, así como también el abandono y los eventos adversos fueron documentados.
Análisis estadísticoLas variables continúas se expresaron en media y desviación estándar o mediana y rango, sean paramétricas o no respectivamente. Las variables categóricas se expresaron como frecuencia y porcentaje. Para el análisis de diferencias significativas se utilizó el test de Student o Wilcoxon test pareados, para las variables paramétricas o no paramétricas respectivamente.
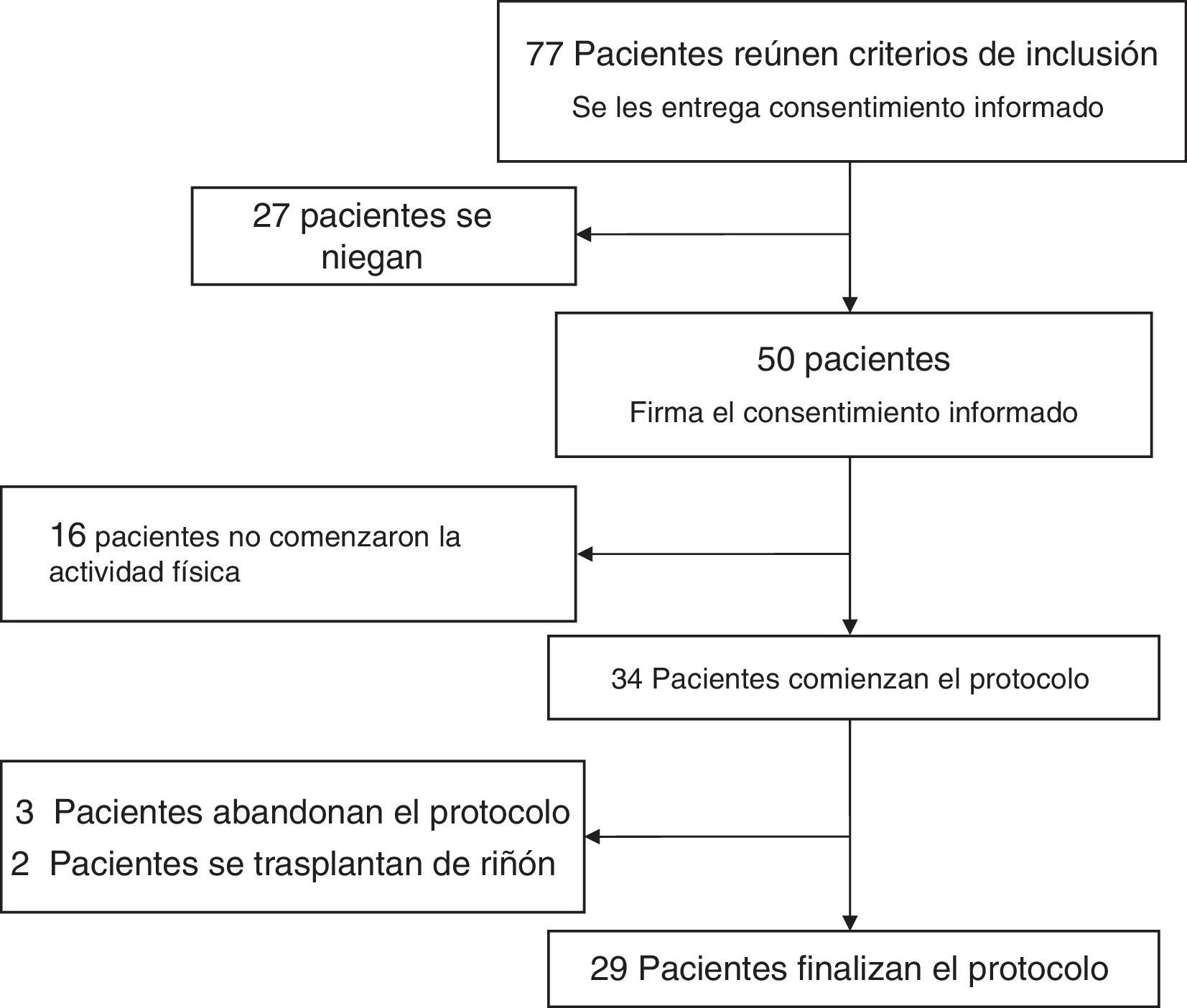
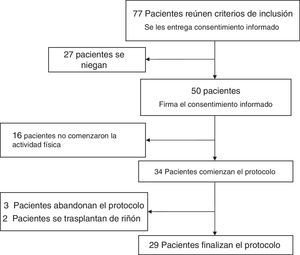
ResultadosLa figura 1 muestra que de una población existente de 140 pacientes adultos pertenecientes a la Sección de Hemodiálisis del Hospital Italiano de Buenos Aires, 77 (55%) reunían los criterios de inclusión. De esos 77 pacientes solo aceptaron participar 50 (el 65% de los pacientes con criterio de inclusión). De la población inicial de pacientes que aceptaron participar, 34 iniciaron finalmente la actividad física. La causa principal de negativa manifestada por los pacientes fue la preferencia a las actividades de ocio (lectura o TV) y descanso. Con respecto a los motivos por los cuales no iniciaron la actividad física aquellos pacientes que firmaron el consentimiento, se destaca la negativa a completar los test de evaluación (60%), la realización de trasplante renal (30%) y el traslado a otro centro de diálisis (10%).
Durante la primera semana de inicio del plan de ejercicio intradialítico, 3 pacientes abandonaron el protocolo. Treinta y un pacientes continuaron hasta la semana 12 del estudio ya que 2 de ellos fueron trasplantados entre la semana 13 y 14 del programa. Solo finalizaron el protocolo completo de actividad física 29 pacientes.
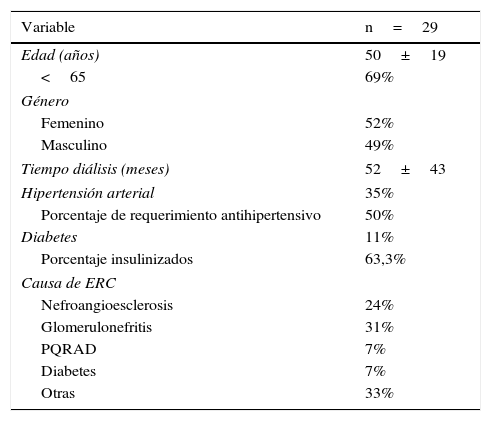
En la tabla 1 se describe las características clínicas de los 29 pacientes que finalizaron el estudio, y sobre los cuales se analizaron las variables incluidas en los objetivos secundarios.
Población en estudio, incluyendo comorbilidades (hipertensión arterial y diabetes) y causas de ingreso a diálisis
| Variable | n=29 |
|---|---|
| Edad (años) | 50±19 |
| <65 | 69% |
| Género | |
| Femenino | 52% |
| Masculino | 49% |
| Tiempo diálisis (meses) | 52±43 |
| Hipertensión arterial | 35% |
| Porcentaje de requerimiento antihipertensivo | 50% |
| Diabetes | 11% |
| Porcentaje insulinizados | 63,3% |
| Causa de ERC | |
| Nefroangioesclerosis | 24% |
| Glomerulonefritis | 31% |
| PQRAD | 7% |
| Diabetes | 7% |
| Otras | 33% |
ERC: enfermedad renal crónica; PQRAD: poliquistosis renal del adulto.
En las tablas 2–5 se muestran los resultados para todas las variables analizadas y en las figuras 2–4 los de algunas de las variables que resultaron significativas.
Pruebas funcionales realizadas antes y después del programa de ejercicio
| Variable | Antes | Después | Valor de p |
|---|---|---|---|
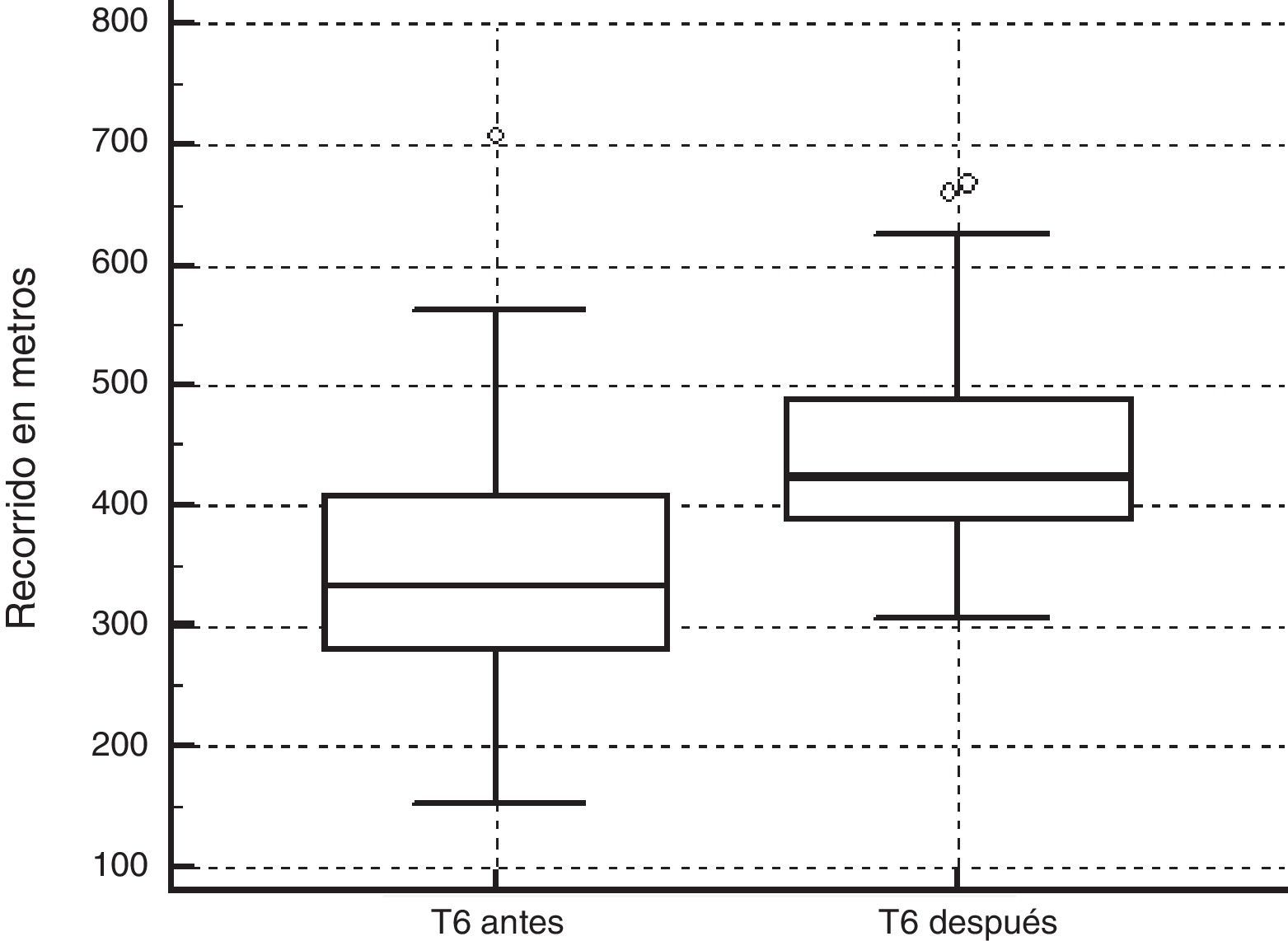
| Test de marcha (metros) | 357,5±115,6 | 444,7±99,3 | <0,0001 |
| Fuerza cuádriceps (kg) | 10,7±3,6 | 11,6±3,8 | 0,10 |
| Fuerza puño (kg) | 25,8±9,7 | 26,3±11 | 0,49 |
| Silla sentado parado (puntaje) | 3,34±1,11 | 3,7±0,84 | 0,0189 |
En negrita, hallazgos estadísticamente significativos.
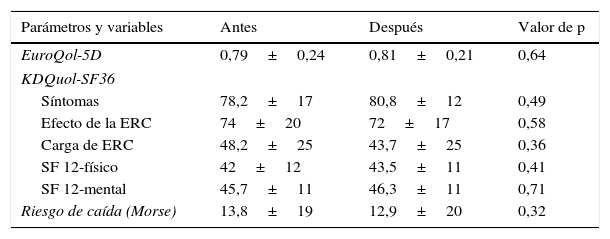
Test de calidad de vida y riesgo de caída, realizados antes y después del programa de ejercicio
| Parámetros y variables | Antes | Después | Valor de p |
|---|---|---|---|
| EuroQol-5D | 0,79±0,24 | 0,81±0,21 | 0,64 |
| KDQuol-SF36 | |||
| Síntomas | 78,2±17 | 80,8±12 | 0,49 |
| Efecto de la ERC | 74±20 | 72±17 | 0,58 |
| Carga de ERC | 48,2±25 | 43,7±25 | 0,36 |
| SF 12-físico | 42±12 | 43,5±11 | 0,41 |
| SF 12-mental | 45,7±11 | 46,3±11 | 0,71 |
| Riesgo de caída (Morse) | 13,8±19 | 12,9±20 | 0,32 |
ERC: enfermedad renal crónica.
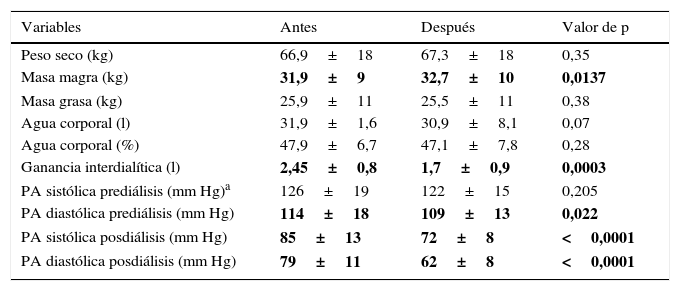
Composición corporal, ganancia interdialítica y presión arterial en diálisis, antes y después del programa de ejercicio
| Variables | Antes | Después | Valor de p |
|---|---|---|---|
| Peso seco (kg) | 66,9±18 | 67,3±18 | 0,35 |
| Masa magra (kg) | 31,9±9 | 32,7±10 | 0,0137 |
| Masa grasa (kg) | 25,9±11 | 25,5±11 | 0,38 |
| Agua corporal (l) | 31,9±1,6 | 30,9±8,1 | 0,07 |
| Agua corporal (%) | 47,9±6,7 | 47,1±7,8 | 0,28 |
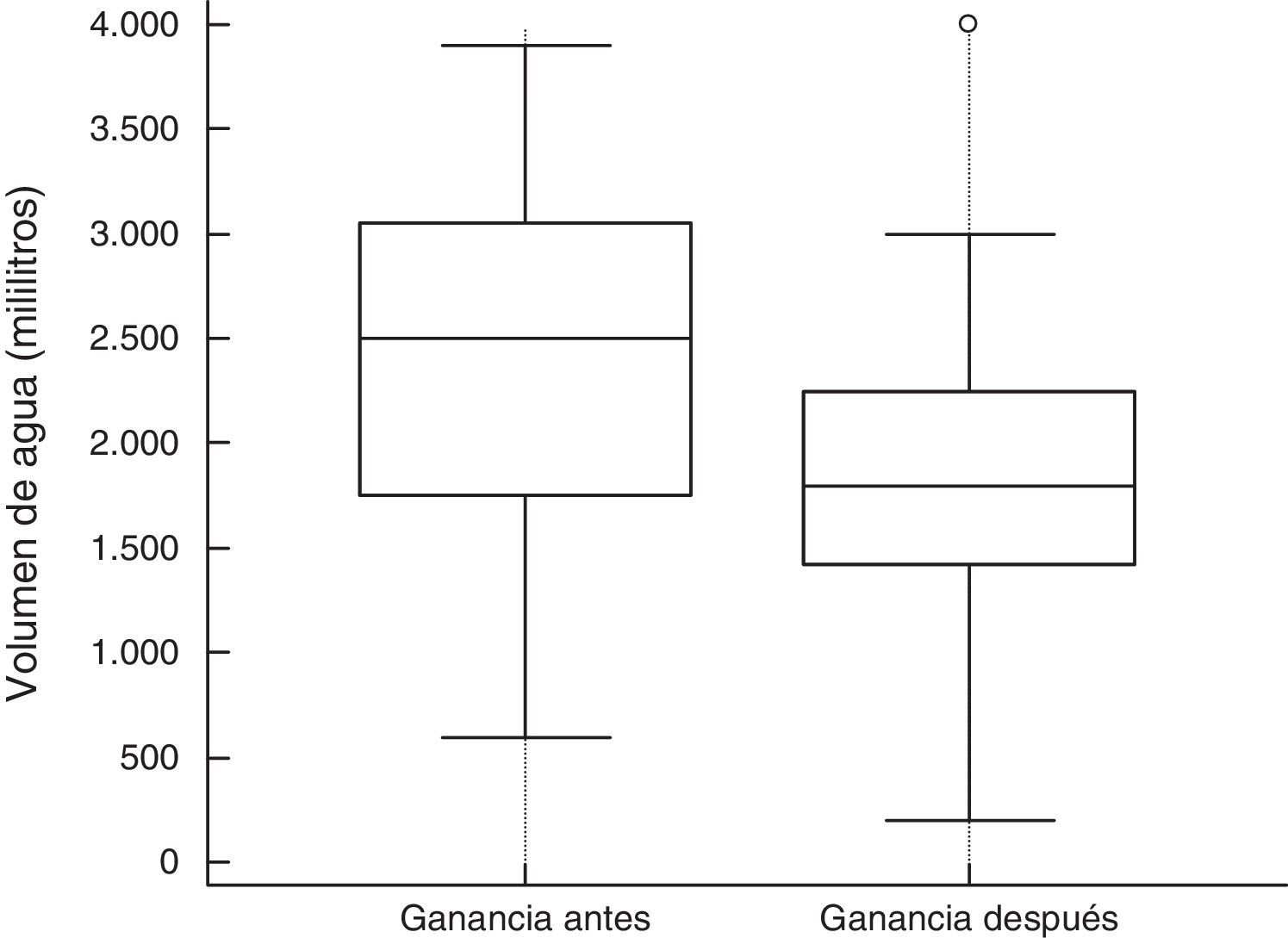
| Ganancia interdialítica (l) | 2,45±0,8 | 1,7±0,9 | 0,0003 |
| PA sistólica prediálisis (mm Hg)a | 126±19 | 122±15 | 0,205 |
| PA diastólica prediálisis (mm Hg) | 114±18 | 109±13 | 0,022 |
| PA sistólica posdiálisis (mm Hg) | 85±13 | 72±8 | <0,0001 |
| PA diastólica posdiálisis (mm Hg) | 79±11 | 62±8 | <0,0001 |
PA: presión arterial
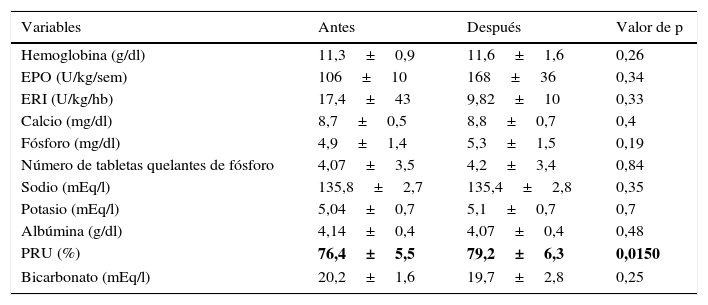
Parámetros de laboratorio, porcentaje de reducción de urea, ingesta de quelantes, dosis de eritropoyetina e índice de resistencia a la eritropoyetina, antes y después del programa de ejercicio
| Variables | Antes | Después | Valor de p |
|---|---|---|---|
| Hemoglobina (g/dl) | 11,3±0,9 | 11,6±1,6 | 0,26 |
| EPO (U/kg/sem) | 106±10 | 168±36 | 0,34 |
| ERI (U/kg/hb) | 17,4±43 | 9,82±10 | 0,33 |
| Calcio (mg/dl) | 8,7±0,5 | 8,8±0,7 | 0,4 |
| Fósforo (mg/dl) | 4,9±1,4 | 5,3±1,5 | 0,19 |
| Número de tabletas quelantes de fósforo | 4,07±3,5 | 4,2±3,4 | 0,84 |
| Sodio (mEq/l) | 135,8±2,7 | 135,4±2,8 | 0,35 |
| Potasio (mEq/l) | 5,04±0,7 | 5,1±0,7 | 0,7 |
| Albúmina (g/dl) | 4,14±0,4 | 4,07±0,4 | 0,48 |
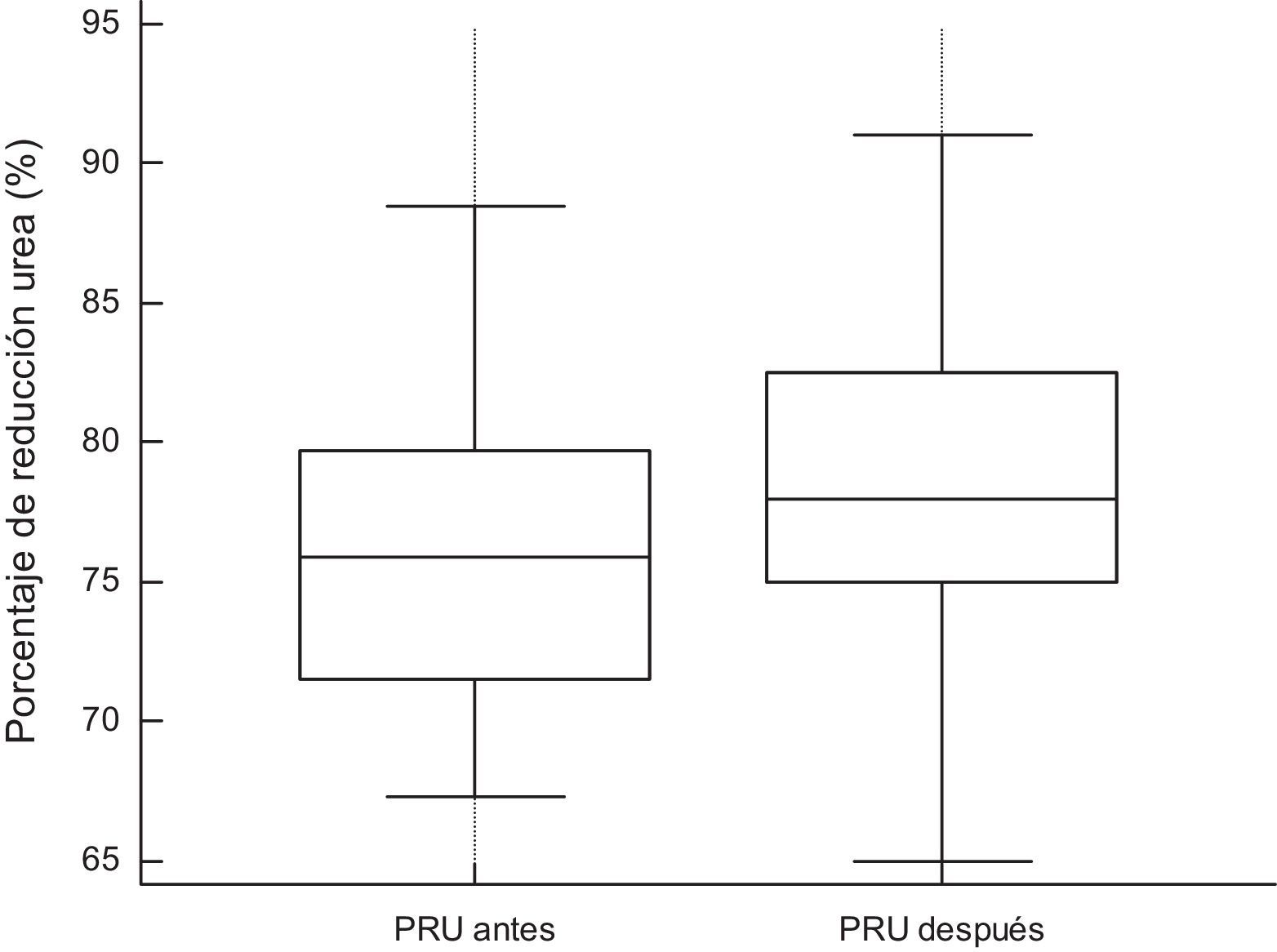
| PRU (%) | 76,4±5,5 | 79,2±6,3 | 0,0150 |
| Bicarbonato (mEq/l) | 20,2±1,6 | 19,7±2,8 | 0,25 |
EPO: eritropoyetina; ERI: índice de resistencia a la eritropoyetina; PRU: porcentaje de reducción de urea.
En negrita, hallazgos estadísticamente significativos.
Resultaron significativas las siguientes variables:
- •
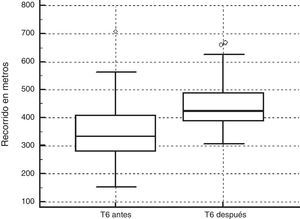
Aumento significativo del test de marcha de 6minutos (fig. 2) y del puntaje en las pruebas funcionales.
- •
Aumento significativo de la masa magra.
- •
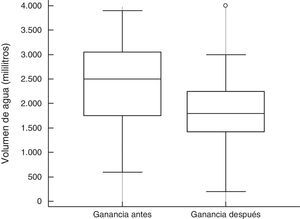
Reducción significativa del agua corporal, la ganancia interdialítica (fig. 3) y la presión arterial.
- •
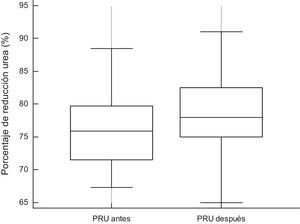
Aumento significativo del porcentaje de reducción de urea (fig. 4).
Este protocolo fue desarrollado por profesionales de la Sección de Hemodiálisis del Servicio de Nefrología y por profesionales del Servicio de Kinesiología. Para la realización del mismo fue necesario hacer varias modificaciones en los horarios habituales de los kinesiólogos intervinientes, para poder cubrir todos los turnos, incluyendo fines de semana y feriados. Respecto de los recursos tecnológicos, se debieron adaptar las pedaleras para el ejercicio aeróbico, con sujeción mecánica cada vez que el paciente iniciaba el ciclo de trabajo, lo cual generaba una carga mayor de trabajo.
DiscusiónEl presente estudio muestra que es factible la realización de un programa de actividad física intradiálisis en pacientes con ERC en HD.
Se logró una mejora en la capacidad aeróbica de los pacientes, evidenciada a través de un aumento significativo de la distancia recorrida en el test de marcha [25], así como en la fuerza dinámica de los cuádriceps demostrada en la prueba de sentarse y pararse. Con relación a los datos de fuerza muscular estática registrada con el handgrip y el músculo de cuádriceps, no se registraron diferencias estadísticamente significativas. Con referencia al handgrip cabe mencionar que los pacientes durante la sesión de diálisis no movilizan uno de los miembros, lo cual determinaría no incluir este test en futuros protocolos de estudio. Con respecto a la fuerza muscular estática de los cuádriceps, la ausencia de una respuesta significativa podríamos atribuirla a falta de tiempo necesaria o a una falta de dosificación individualizada para la condición de cada paciente dado que, en nuestro caso, la dosis fue estandarizada [24,26,27]. Nuevamente esta observación será considerada en futuros protocolos de estudio.
La falta de evidencia significativa en los cuestionarios de calidad de vida, así como también en el riesgo de caída de los pacientes evaluados, se atribuye a un escaso tiempo, solo 16 semanas de diferencia entre uno y otro cuestionario (antes-después) y al pequeño número de pacientes. Particularmente los cuestionarios de calidad de vida incluyen varios dominios, los cuales pueden modificar los resultados finales, especialmente si el número de pacientes estudiados es pequeño [15,16].
Se evidenció un aumento de la masa magra medida por bioimpedanciometría (tabla 4), la cual está asociada al aumento de la masa muscular [28].
Por otro lado, los pacientes mostraron una reducción de la ganancia de agua interdialítica, así como también de la presión arterial (tabla 4), 2 factores fundamentales, la sobrecarga hídrica y la hipertensión arterial, que son considerados factores de riesgo cardiovascular para los pacientes en HD [29]. A su vez, la reducción de la presión arterial observada podría ser atribuida en parte a la reducción de la ganancia de agua interdialítica.
El ejercicio durante la diálisis ha demostrado que mejora la eficiencia dialítica, aumentando la depuración de solutos tales como la urea [30]. Así, nuestros pacientes mostraron un mayor porcentaje de reducción de urea posdiálisis con el programa de ejercicio impuesto.
Con respecto al resto de las variables clínicas analizadas, consideramos que estas no fueron significativas en su mayor medida por el pequeño número de pacientes y el escaso tiempo de 16 semanas del programa de ejercicios, si bien las mismas no estaban contempladas en el objetivo principal.
Cabe destacar la negativa a la inclusión por parte de algunos pacientes así como el abandono por parte de otros. Esto no sorprende y ha sido descripto por otros autores, en el sentido de la adherencia de los pacientes con enfermedad crónica, y en particular los pacientes con ERC en diálisis [31–33]. Sin embargo, una vez iniciado nuestro protocolo de estudio, 10 pacientes solicitaron ser incluidos en el plan de ejercicio, los cuales fueron incluidos en el programa de ejercicio, pero no en el protocolo de estudio. Esto enfatiza la importancia de la estimulación y la educación, tanto para los pacientes como para el grupo terapéutico de asistencia diaria (médicos, enfermeros y técnicos de diálisis).
El programa que ha sido estudiado tiene algunas dificultades particularmente relacionadas con el aumento de la carga de trabajo de los profesionales y los recursos instrumentales. Para el desarrollo de futuros programas, se deberán considerar ambos aspectos para lograr mejorar la factibilidad de realización. Creemos necesario estudiar en una segunda etapa los resultados del programa autoadministrado por el paciente (similar a como si estuviese en su domicilio), pero con el control periódico de un profesional para la evaluación y/o modificación de las variables necesarias.
Con referencia a las fortalezas y debilidades del presente estudio, cabe destacar la descripción de los factores involucrados en el éxito de un programa de ejercicio intradialítico tanto del paciente como de los recursos humanos y técnicos requeridos, los cuales pueden ser tenidos en cuenta para el desarrollo de futuros programas. Dentro de las debilidades, se trata de un estudio unicéntrico, si bien los factores mencionados pueden ser aplicables a nivel regional.
ConclusiónEn este trabajo demostramos la factibilidad de realizar un programa de actividad física intradialítica en pacientes con HD. En el corto período de desarrollo se demuestran, además, beneficios en la funcionalidad así como en las variables clínicas de importancia de los pacientes en diálisis. La implementación y sustentación de un programa de ejercicio intradialítico requiere la ponderación del paciente para la autoadministración, así como también estrategias para mejorar la adherencia al mismo y una dosis individualizada y adecuada de ejercicio para cada paciente.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.