El síndrome de Brugada es una canalopatía de origen genético, autosómica dominante, que afecta a los canales de sodio de las membranas celulares de las células cardíacas. Es más común en jóvenes, y su diagnóstico se basa en criterios electrocardiográficos y antecedentes clínicos de síncope o historia familiar de muerte súbita debida a arritmias ventriculares malignas. Se han descrito 3 patrones electrocardiográficos distintos: a) patrón tipo I, caracterizado por una elevación descendente del segmento ST≥2mm en más de una derivación precordial derecha (V1-V3), seguida de ondas T negativas, el único diagnóstico de la enfermedad; b) patrón tipo II, caracterizado por elevación del segmento ST≥2mm en precordiales derechas seguida de ondas T positivas o isodifásicas, lo que confiere al electrocardiograma un aspecto de silla de montar, y c) patrón tipo III, definido como cualquiera de los 2 anteriores si la elevación del segmento ST es ≤1mm1,2.
Se han descrito, además, distintas situaciones o fármacos que pueden desencadenar un patrón electrocardiográfico de síndrome de Brugada.
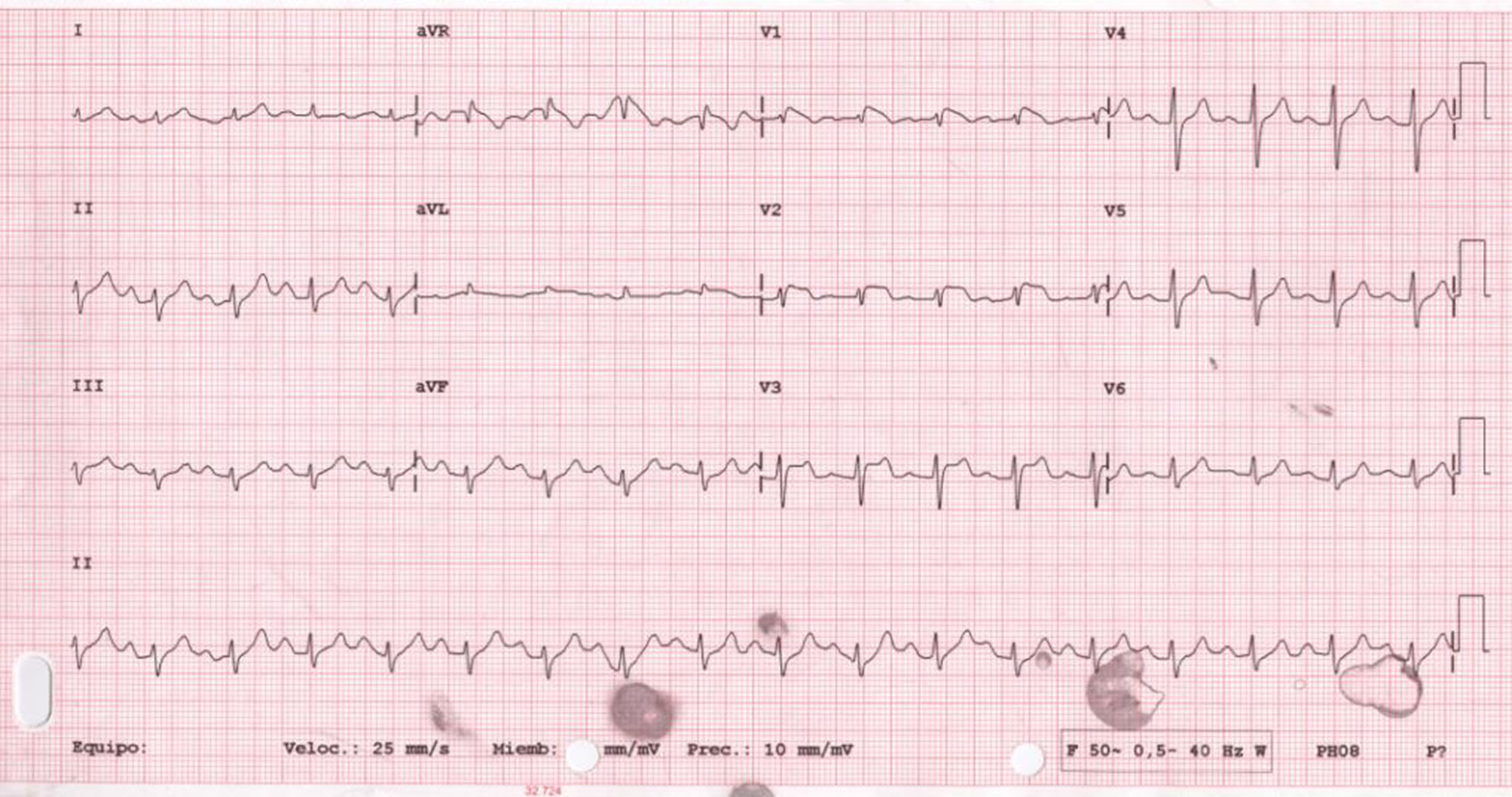
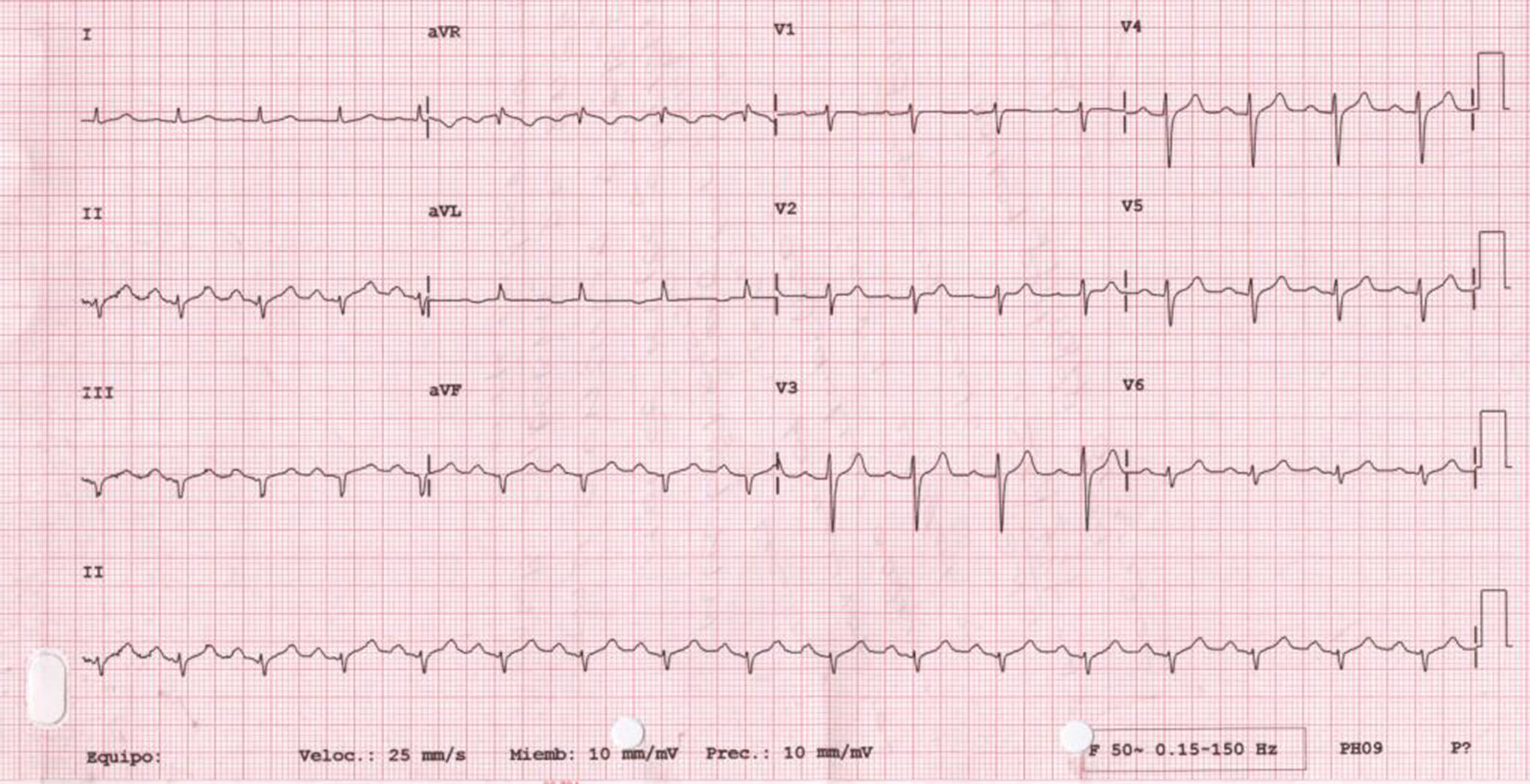
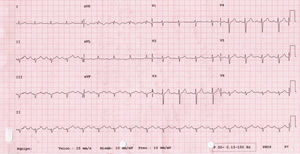
Presentamos el caso de una paciente de 56 años con antecedentes de tabaquismo, diabetes, hipertensión y dislipemia en tratamiento con insulina, metformina, valsartán/hidroclorotiazida y atorvastatina. Además, seguía tratamiento con topiramato y levetiracetam por epilepsia, y amitriptilina por depresión. Su situación basal era muy limitada por deterioro cognitivo moderado. No refería historia familiar de muerte súbita. Ingresó en nuestro hospital por episodio de síncope de perfil vasovagal en contexto de cuadro catarral sin fiebre termometrada superior a 38°C. El primer electrocardiograma mostró un ritmo sinusal con BAV de 1.er grado con elevación del segmento ST de 1mm de V1-V3 con onda T negativa de V1-V2 (fig. 1). La analítica inicial mostró: creatinina 2,2mg/dl; Na 136mEq/l; K 4,7mEq/l; Mg 1,2mEq/l; pH 7,32 y troponina I<0,01ng/ml. Por sospecha de infarto agudo de miocardio con elevación del segmento ST de localización anteroseptal se comentó el caso con el servicio de hemodinámica que recomendó ante la duda diagnóstica de síndrome coronario agudo y la limitación física y psíquica de la paciente realizar seriación enzimática que fue normal y completar estudio cardiológico. Se realizó un ecocardiograma que mostró hipertrofia ventricular izquierda con FEVI normal, sin alteraciones de la contractilidad segmentaria. La paciente evolucionó favorablemente con resolución del cuadro infeccioso y normalización de la función renal (creatinina al alta 0,78mg/dl). Se repitió el electrocardiograma 48h después del ingreso que mostró desaparición de las alteraciones del electrocardiograma previo (fig. 2). Se realizó estudio Holter-ECG sin objetivarse eventos arrítmicos significativos. La paciente fue dada de alta con el diagnóstico de fenocopia Brugada probablemente secundario a deterioro de la función renal, sin alteraciones electrolíticas asociadas en el contexto de toma de fármacos con capacidad de inducción de patrón de Brugada tipo 1 (amitriptilina). Dado el importante deterioro físico y psíquico de la paciente se decidió no realizar test de flecainida. Se comentó el caso con neurología para el ajuste de dosis o retirada de amitriptilina.
Las fenocopias Brugada (Fbr) se caracterizan por unos patrones electrocardiográficos que son idénticos a los patrones de Brugada de tipo 1 o 2, a pesar de la ausencia del síndrome de Brugada congénito verdadero. Tienen su causa en diversas circunstancias clínicas entre las que se encuentran la hiperpotasemia, la insuficiencia suprarrenal, la hipotermia, la compresión mecánica cardíaca, la miocarditis, la pericarditis o la isquemia. Los criterios diagnósticos actuales de las Fbr son: 1) el patrón del ECG tiene una morfología de Brugada de tipo 1 o 2; 2) el paciente presenta un trastorno subyacente que es identificable; 3) el patrón del ECG se resuelve tras la resolución del trastorno subyacente; 4) hay una probabilidad pre-test clínica baja de un síndrome de Brugada verdadero, determinado por la ausencia de síntomas, antecedentes médicos y/o familiares; 5) pruebas de provocación negativas con bloqueadores del canal del sodio (ajmalina, flecainida o procainamida); 6) pruebas de provocación no obligatorias si ha habido una manipulación quirúrgica del tracto de salida ventricular derecho en las últimas 96h, y 7) los resultados de las pruebas genéticas son negativos (no obligatorio, ya que la mutación de SCN5A se identifica solo en un 20-30% de los afectados por un síndrome de Brugada verdadero)3. Por otro lado, varios fármacos psicoactivos como litio, amitriptilina, nortriptilina, oxcarbazepina o clomipramina están contraindicados en pacientes con síndrome de Brugada por su potencial acción bloqueando los canales de sodio, lo que puede inducir la aparición de arritmias malignas, síncope y muerte súbita cardíaca4,5. Otros fármacos como el topiramato o el levetiracetam no están contraindicados en estos pacientes. Nuestro caso describe una posible Fbr en una paciente bajo tratamiento con amitriptilina, con un resultado de causalidad probable según el algoritmo de Karch y Lasagna modificado6, en el contexto de un deterioro transitorio de la función renal sin alteraciones electrolíticas objetivadas.