Una de las reacciones más graves de hipersensibilidad a fármacos es el síndrome de DRESS (reacción de sensibilidad a medicamentos con eosinofilia y síntomas sistémicos). Característicamente, se presenta con un extenso exantema, fiebre, adenopatías, eosinofilia periférica y puede afectar a órganos internos como el hígado o riñón. Los fármacos más frecuentemente implicados son los antibióticos, otros antiinfecciosos y los fármacos anti-crisis epilépticas, y con menor frecuencia otros. Dentro de los fármacos anti-crisis epilépticas, los que con mayor frecuencia pueden desencadenar el síndrome DRESS son los que poseen estructura con anillos aromáticos, tales como carbamazepina, oxcarbazepina, fenitoína, fenobarbital y lamotrigina, y con menor frecuencia otros como ácido valproico, etosuximida, levetiracetam y zonisamida1–4. En los pacientes con síndrome DRESS, el cambio del fármaco causante del síndrome por otro diferente puede causar reactivación de los síntomas. A esta segunda reacción de hipersensibilidad se denomina fenómeno de reactivación cruzada o flare-up, que ha sido descrito con antibióticos, paracetamol y antivirales, pero no con fármacos anti-crisis epilépticas. El diagnóstico de este fenómeno tiene gran importancia, ya que el segundo fármaco puede ser tolerado posteriormente5. El reconocimiento del medicamento implicado en el síndrome DRESS es vital porque la tasa de mortalidad puede ser de hasta un 20%6.
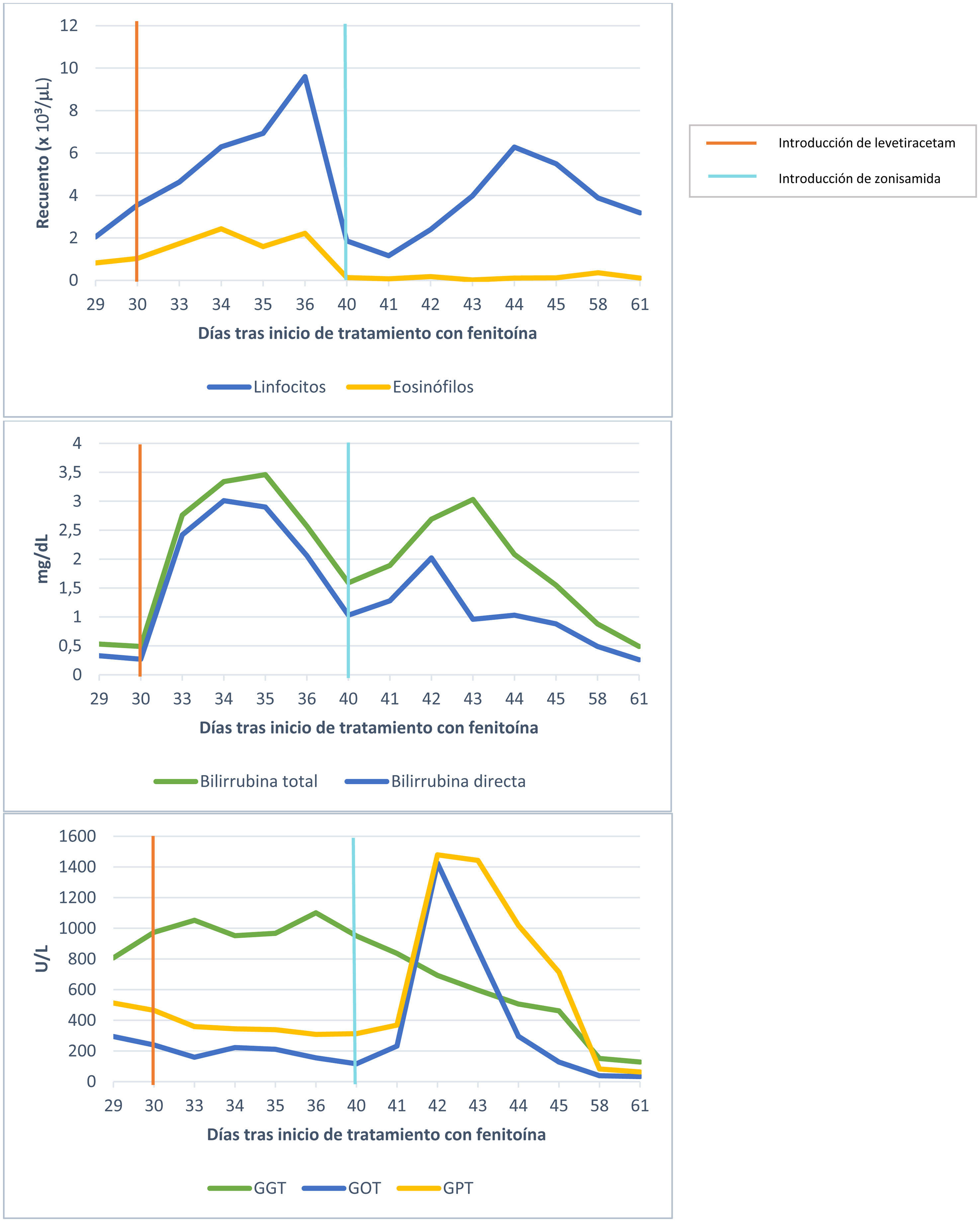
Describimos el caso de un hombre de 35 años con antecedente de cavernomatosis múltiple familiar sin tratamiento que comienza con crisis epilépticas y es tratado con fenitoína, valproato y levetiracetam, de forma escalonada, ante la falta de respuesta, y con los tres fármacos se obtiene el control. A los 10 días aparece fiebre de 39°C, convulsiones, exantema maculopapular progresivo que afecta a más del 50% de la superficie corporal con edemas de ojos y manos. El hemograma revela una eosinofilia (0,82 x 109/L) y la bioquímica, una elevación de las enzimas hepáticas (gama-glutamiltransferasa [GGT] 807 U/L, (glutámico-oxalacético transaminasa [GOT] 294 U/L, (glutámico-pirúvico transaminasa [GPT] 460 U/L). La función renal fue normal. El tratamiento fue retirado y el paciente mejoró en los siguientes tres días. El levetiracetam fue reintroducido y al tercer día el exantema se exacerba, aparece fiebre de 39°C y la analítica muestra leucocitosis de 21,99 x 10/μL, eosinofilia (2,43 x 109/L), GGT 952 U/L, GOT 222 U/L, GPT 344 U/L, bilirrubina total 3,44mg/dL, bilirrubina directa 3mg/dL con función renal normal. Se suspende levetiracetam, es tratado con corticoides (prednisona 30mg/12 h vo) y evoluciona favorablemente permaneciendo afebril. Cinco días después comienza tratamiento con zonisamida y a las 48 horas el estado general empeora, se acrecienta el rash, fiebre de 39°C, edema facial y la bioquímica muestra una elevación de GGT 693 U/L, GOT 1425 U/ y GPT 1479 U/L. Se suspende todo el tratamiento y los síntomas desaparecen en dos semanas con normalización de la analítica (fig. 1).
No se observó infección activa en la serología para hepatitis A, B y C, Epstein-Barr, citomegalovirus y herpes simplex.
A las ocho semanas se practicaron test epicutáneos (TE) con fenitoína, levetiracetam y valproato (puro, 1%, 10% y 20% en agua) así como con zonisamida (puro, 1%, 10% y 20% en vaselina), con lectura positiva a las 48-96 horas para la fenitoína pura y al 20%, siendo negativa para el resto de los fármacos.
Se siguió la técnica de Beeler et al7; se realizó un test de activación linfocitaria (TAL) que mide la expresión de CD69 en linfocitos T CD4+, usando citometría de flujo, cuando se expone al fármaco, que fue positivo para fenitoína y negativo con valproato, zonisamida y levetiracetam.
Los TE y el TAL han demostrado ser útiles para el diagnóstico de las reacciones tardías por fármacos mediadas por linfocitos7,8. Con ambos métodos positivos exclusivamente para la fenitoína y usando el sistema de puntuación RegiSCAR (registro de reacciones adversas cutáneas graves) para valorar el síndrome de DRESS obtuvimos una puntuación de 4, con lo que el diagnóstico del paciente en ese momento fue de probable síndrome DRESS por fenitoína1,6. Aunque el test de provocación controlada con fármacos es el gold standard para el diagnóstico de hipersensibilidad a medicamentos, está contraindicado en el síndrome DRESS por la posibilidad de provocar afectación de órganos internos9. Basándonos en el resultado del TAL y los TE y la necesidad de un tratamiento con fármacos anti-crisis epilépticas, se realizó un test de provocación controlada con levetiracetam, zonisamida y valproato (primero 25% de la dosis total, observación durante 60 minutos y luego la dosis restante) sin presentar reacción con ellos. Con lo que el diagnóstico definitivo fue de síndrome de DRESS por fenitoína y reactivación cruzada con levetiracetam, zonisamida y valproato.
Esta reacción podría explicarse con base en el p-i concept (interacción farmacológica con los receptores inmunitarios), la estimulación inmunitaria durante la hipersensibilidad al fármaco puede, de manera similar a las infecciones virales generalizadas, reducir el umbral de reactividad de las células T a los fármacos y provocar la aparición rápida de síntomas de hipersensibilidad al nuevo medicamento administrado que posteriormente puede ser tolerado si los cofactores están ausentes10.
Desde la resolución de los síntomas al diagnóstico de DRESS por fenitoína transcurrieron dos meses y el paciente no recibió ningún fármaco anti-crisis epiléptica. A partir de entonces está asintomático con levetiracetam 500mg/12 h.
El TAL y/o los TE pueden ser útiles para el diagnóstico de síndrome de DRESS con fenitoína y reactividad cruzada con levetiracetam, zonisamida y valproato.