El coste económico de las demencias es elevado. El perfil de deterioro cognitivo y neuropsiquiátrico puede predecir el gasto por demencia. Se desconoce en nuestro medio la diferencia entre los distintos subtipos de demencia.
ObjetivoComparar los costes directos de la enfermedad en los distintos subtipos de demencia.
Materiales y métodosFueron evaluados pacientes con diagnóstico de demencia tipo Alzheimer probable (DTA), frontotemporal (DFT) y vascular (DVASC) de acuerdo con criterios publicados (periodo 2002 a 2008). Se elaboró una entrevista estructurada sobre los gastos directos.
ResultadosSe seleccionaron 104 pacientes con demencia (DTA = 44, DFT = 34 y DVASC = 26) y fueron apareados con 29 controles normales. En las variables demográficas no se presentaron diferencias significativas (Kruskall-Wallis). El coste directo anual fue de 4.625 dólares para DTA, 4.924 dólares para la DFT y para la DVASC 5.112 dólares (p > 0,05 entre los grupos). En el análisis post hoc la DVASC presentó mayor coste por internaciones que la DTA (p < 0,001). La DVASC presentó menos gasto en medicamentos que la DFT (p < 0,001), la DTA mayor gasto por antidemenciales y la DFT mayor gasto por psicotrópicos. En el análisis multivariado la sobrecarga del cuidador, las actividades de vida diaria, la depresión y la educación se correlacionaron con el gasto trimestral (r2 = 0,76).
ConclusionesEl coste entre los distintos tipos de demencia ha sido diferente. El derivado de los pacientes se vio incrementado con la presencia de depresión, la institucionalización y con el número de medicamentos suministrados.
Economic costs in dementia are important. The profile of cognitive and behavioral impairment can predict costs in dementia. Differences between the subtypes of dementia are not well known in our country.
ObjectiveTo compare direct costs in the different subtypes of dementia.
Materials and methodsPatients with diagnosis of probable Alzheimer's disease (AD), frontotemporal (FTD) and vascular dementia (VD) were evaluated according to published criteria (2002 to 2008). A structured interview on direct cost was elaborated.
Results104 patients with dementia were selected (AD = 44, FTD = 34 and VD = 26) and matched with 29 normal controls. It did not appear significant differences in the demographic variables (Kruskall-Wallis analysis). Annual direct cost was 4,625 dollars for AD, 4,924 dollars for FTD and VD 5,112 dollars (p > 0.05 between the groups). In a posthoc analysis VD presented more cost for hospitalization than AD (p < 0.001). VD showed less cost in drugs than FTD (p < 0.001). AD had more cost for antidemential drugs and FTD more in psychotropics. In the multivariate analysis caregiver's burden, activities of daily life, depression and education were correlated with direct cost (r2 = 0.76).
ConclusionsCost between the different subtypes of dementia has been different. It increased with the presence of depression, the institutionalization and with the number of provided drugs.
Las demencias constituyen en la actualidad una de las problemáticas que más repercuten en la salud pública. De ellas, la enfermedad de Alzheimer es la más frecuente. En la República Argentina se estima en mayores de 65 años una tasa de prevalencia global de la demencia del 12,18% (tipo Alzheimer de 5,85% y demencia vascular de 3,86%)1. No se encuentran publicados estudios de prevalencia en demencia frontotemporal de nuestro país. En un estudio epidemiológico poblacional realizado en Cañuelas (piloto de la primera fase del Estudio Ceibo) en mayores de 60 años se encontró una prevalencia de deterioro cognitivo del 23,3%, con un rango de 16,9% en los 60–69 años hasta 42,5% en mayores de 80 años2.
Los costes generados por demencia son elevados para el sistema de salud. Existen escasos estudios publicados de costes en demencias en nuestro país, solamente dirigidos a enfermedad de Alzheimer3. En la Argentina los costes directos anuales de la demencia tipo Alzheimer para el año 2001 iban desde 3.420 dólares en los casos leves a 9.657 en los graves. El coste directo correspondiente al tratamiento farmacológico en la enfermedad de Alzheimer fue de 450 dólares en un periodo de tres meses3. En EE.UU. se estima un coste anual por paciente con demencia tipo Alzheimer de grado leve en 14.408 dólares, ascendiendo a 36.132 en aquellos con deterioro grave. Esto supone un coste nacional de 50 billones de dólares4.
Pocos estudios han examinado predictores clínicos del aumento del coste en la demencia5–7. No obstante, no han sido comparados los costes de los subtipos de demencia por separado, ni tampoco se ha incluido en el análisis la demencia frontemporal.
HipótesisLos costes económicos de las demencias son diferentes entre los distintos subtipos. El perfil cognitivo y neuropsiquiátrico puede predecir el gasto por demencia.
ObjetivosEl objetivo primario fue comparar los costes directos de la enfermedad en los distintos subtipos de demencia. Los objetivos secundarios fueron discriminar aquellas variables demográficas, cognitivas, sociales y neuropsiquiátricas que mejor predicen el coste directo final de las demencias, así como evaluar la influencia de los gastos en medicamentos sobre el coste directo total.
Materiales y métodosPoblaciónFueron evaluados pacientes con diagnóstico de demencia (según criterios DSM IV). Se seleccionaron para el análisis la enfermedad de Alzheimer probable (criterio NINCDS ADRDA8), demencia frontotemporal (según Consenso de los Grupos Lund y Manchester9) y demencia vascular probable (según criterios NINDS AIREN10). Los pacientes habían con sultado en el periodo comprendido desde enero de 2002 hasta abril del año 2008. En la muestra participaron pacientes derivados a un sistema público de salud (Centro de Investigación de la Memoria del Hospital Abel Zubizarreta del Gobierno de la Ciudad de Buenos Aires). Fueron seleccionados un grupo de sujetos normales para facilitar la comparación cualitativa de los costes específicamente derivados de la demencia.
Se incluyeron datos de los cuidadores primarios, definidos como aquellas personas que no recibían remuneración económica y que tenían la responsabilidad de ayudar al paciente en sus actividades de la vida diaria (AVD) y actividades instrumentales de la vida diaria (AIVD). Estas personas eran las que dedicaban más horas al paciente.
Todo el trabajo clínico estuvo sujeto a las Reglas ICH de Buenas Prácticas Clínicas, a la última revisión de las declaraciones de Helsinki (1964, c/ enmiendas Tokio, 1975; Venecia, 1983; Hong Kong, 1989) así como a las regulaciones de las Autoridades de Salud del GCBA.
ProcedimientoSe realizó un estudio de observación, retrospectivo de corte transversal, encuestando al grupo de pacientes y sus cuidadores en un punto del tiempo y midiendo información clínica en dicho momento y datos económicos en el pasado (tres meses).
Todos los gastos e ingresos fueron calculados con el valor del dólar (un dólar equivalente a 3 pesos argentinos en el año 2008).
InstrumentosLa entrevista incluyó los siguientes cuestionarios:
- 1.
Formulario de consentimiento informado: previamente al inicio de la entrevista, se explicó a todos los pacientes y sus cuidadores los alcances del estudio, se les entregó un texto de lectura y firmaron un formulario preestablecido de consentimiento informado.
- 2.
Datos sociodemográficos de los pacientes y sus cuidadores incluyendo la edad, el sexo, la educación, la ocupación, la nacionalidad, el estado civil, los ingresos económicos (tipo y cantidad mensual) y residencia (tipo y gastos).
- 3.
Evaluación cognitiva: Mini Mental State Examination (MMSE)11.
- 4.
Estadio evolutivo / gravedad del deterioro: Clinical dementia rating (CDR)12.
- 5.
Sobrecarga del cuidador: cuestionario de Zarit13.
- 6.
Inventario neuropsiquiátrico NPI14.
- 7.
Inventario de depresión de Beck15.
- 8.
Cuestionario de AIVD: cuestionario de Lawton16.
- 9.
Cuestionario estructurado de evaluación de costes directos, modificación del utilizado en el grupo 10/66 con permiso de M. Prince17.
Los costes directos son erogaciones relacionadas con el cuidado del paciente. Los costes considerados por el sistema de salud son los costes médicos directos. Los derivados de las visitas médicas programadas y no programadas, las visitas por auxiliares médicos, exámenes complementarios, Hospital de día y el ingreso hospitalario fueron calculados de acuerdo con el coste del Sistema de Seguridad Social. Los costes no médicos directos son los relacionados con gastos de la enfermedad, a cargo de la familia. El coste de los medicamentos de rutina fue calculado al 100% del valor del precio de venta al público (a fecha 1 de marzo de 2009) para cada uno de los principios activos registrados. La información fue recopilada de los precios publicados en Alfabeta®. El coste por cuidador y materiales sanitarios se calculó según información del coste mensual reportado de familiares.
Anólisis estadísticoSe obtuvieron la media y los desviación estándar para las variables cuantitativas, y la distribución de frecuencias para las cualitativas. Las diferencias entre las demencias fueron calculadas con ANOVA y Kruskal-Wallis (para datos no gaussianos). Se utilizaron los post hoc de Bonferroni y post hoc Mann–Whitney según correspondiese. El sexo y el estado civil fueron evaluados con Chi cuadrado. En aquellos datos con distribución de modo a la izquierda se realizó una transformación a logarítmica normal para la utilización de test paramétricos.
Para el análisis de predictores se seleccionó como variable dependiente el “coste total directo en 3 meses” y se realizó un análisis multivariado. Las covariables incluidas en el modelo fueron edad, educación, estado cognitivo (CDR, MMSE, CI global), compromiso neuropsiquiátrico (NPI e inventario de Beck), estado funcional (AVD y sobrecarga del cuidador). Ya que la variable costes presenta una distribución con modo a derecha, también se realizó el cálculo con su logaritmo natural (costes log-transformada). Ecuación del modelo de regresión lineal:
Costes log-transformada = B (+ CDR — MMSE — CI global + NPI + Beck + AVD + sobrecarga), siendo B: coeficientes de regresión estandarizados.
En todos los análisis una p < 0,05 fue considerada significativa.
Los resultados se analizaron con los paquetes estadísticos SPSS versión 13 y Medcalc.
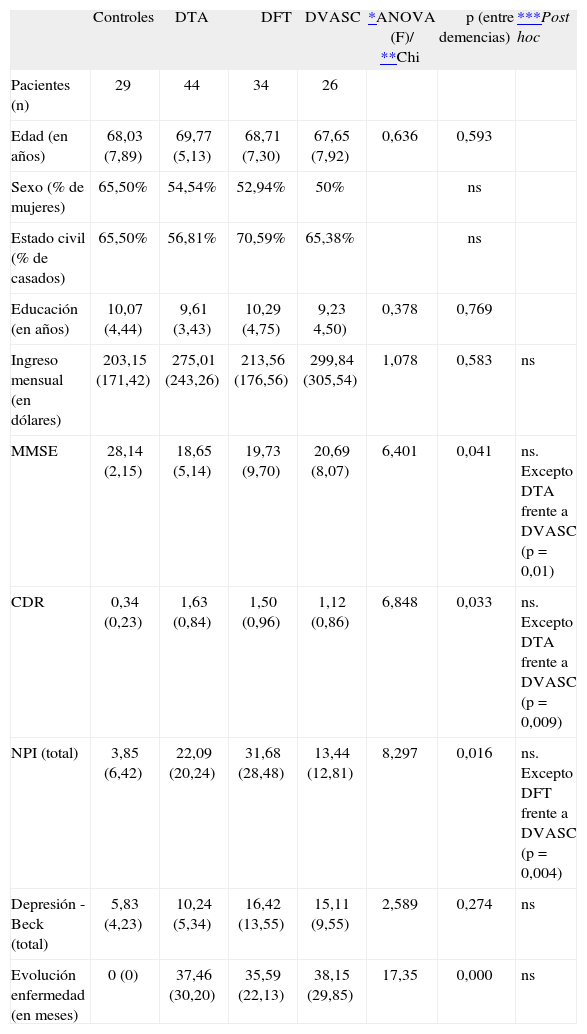
ResultadosPoblación en estudio y perfil sociosanitario de los pacientes con demenciaFueron evaluados 104 pacientes que presentaron diagnóstico de enfermedad de Alzheimer probable (DTA) 44, demencia frontotemporal (DFT) 34, demencia vascular (DVASC) 26 y apareados con 29 sujetos normales. No se encontraron diferencias significativas en edad, sexo, escolaridad y tiempo de evolución entre las demencias. En los test globales (CDR y MMSE) existieron leves diferencias entre DTA y DVASC. No obstante, la mayoría de los pacientes presentaron cuadros leves. Los pacientes con DFT presentaron mayor carga neuropsiquiátrica que la DVASC. Las características demográficas y clínicas de la población se presentan en la tabla 1.
Datos demográficos de los pacientes
| Controles | DTA | DFT | DVASC | *ANOVA (F)/ **Chi | p (entre demencias) | ***Post hoc | |
| Pacientes (n) | 29 | 44 | 34 | 26 | |||
| Edad (en años) | 68,03 (7,89) | 69,77 (5,13) | 68,71 (7,30) | 67,65 (7,92) | 0,636 | 0,593 | |
| Sexo (% de mujeres) | 65,50% | 54,54% | 52,94% | 50% | ns | ||
| Estado civil (% de casados) | 65,50% | 56,81% | 70,59% | 65,38% | ns | ||
| Educación (en años) | 10,07 (4,44) | 9,61 (3,43) | 10,29 (4,75) | 9,23 4,50) | 0,378 | 0,769 | |
| Ingreso mensual (en dólares) | 203,15 (171,42) | 275,01 (243,26) | 213,56 (176,56) | 299,84 (305,54) | 1,078 | 0,583 | ns |
| MMSE | 28,14 (2,15) | 18,65 (5,14) | 19,73 (9,70) | 20,69 (8,07) | 6,401 | 0,041 | ns. Excepto DTA frente a DVASC (p = 0,01) |
| CDR | 0,34 (0,23) | 1,63 (0,84) | 1,50 (0,96) | 1,12 (0,86) | 6,848 | 0,033 | ns. Excepto DTA frente a DVASC (p = 0,009) |
| NPI (total) | 3,85 (6,42) | 22,09 (20,24) | 31,68 (28,48) | 13,44 (12,81) | 8,297 | 0,016 | ns. Excepto DFT frente a DVASC (p = 0,004) |
| Depresión - Beck (total) | 5,83 (4,23) | 10,24 (5,34) | 16,42 (13,55) | 15,11 (9,55) | 2,589 | 0,274 | ns |
| Evolución enfermedad (en meses) | 0 (0) | 37,46 (30,20) | 35,59 (22,13) | 38,15 (29,85) | 17,35 | 0,000 | ns |
Salvo el sexo y el estado civil, el resto de los valores están expresados en medias (desviación estándar). Diferencias entre demencias con
CDR: Clinical Dementia Rating; DFT: demencia frontotemporal; DTA: demencia tipo Alzheimer; DVASC: demencia vascular; MMSE: Mini Mental State Exam; NPI: Neuropsychiatric Inventory; ns: no significativo.
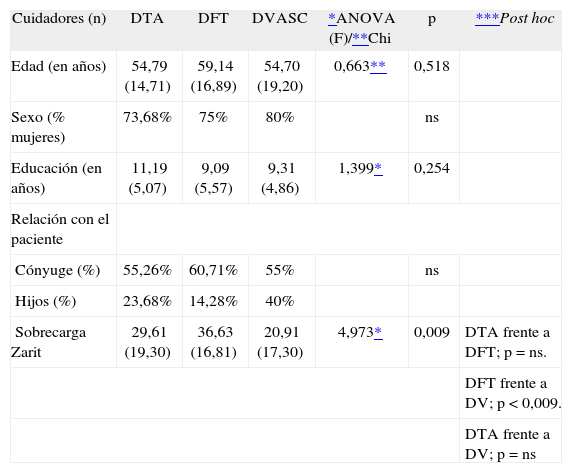
Entre las demencias no hubo diferencias significativas en edad y sexo (porcentaje de mujeres), educación (en años) y relación con el paciente. Los cuidadores de pacientes con DFT presentaron mayor índice de sobrecarga que los pacientes con DVASC (F = 4,97; p = 0,009). No hubo diferencias entre el resto de las demencias (tabla 2).
Datos demográficos de los cuidadores
| Cuidadores (n) | DTA | DFT | DVASC | *ANOVA (F)/**Chi | p | ***Post hoc |
| Edad (en años) | 54,79 (14,71) | 59,14 (16,89) | 54,70 (19,20) | 0,663** | 0,518 | |
| Sexo (% mujeres) | 73,68% | 75% | 80% | ns | ||
| Educación (en años) | 11,19 (5,07) | 9,09 (5,57) | 9,31 (4,86) | 1,399* | 0,254 | |
| Relación con el paciente | ||||||
| Cónyuge (%) | 55,26% | 60,71% | 55% | ns | ||
| Hijos (%) | 23,68% | 14,28% | 40% | |||
| Sobrecarga Zarit | 29,61 (19,30) | 36,63 (16,81) | 20,91 (17,30) | 4,973* | 0,009 | DTA frente a DFT; p = ns. |
| DFT frente a DV; p < 0,009. | ||||||
| DTA frente a DV; p = ns | ||||||
Salvo sexo y relación con el paciente, el resto de los valores están expresados en medias (desviación estándar). Diferencias entre demencias con
DTA: demencia tipo Alzheimer; DFT: demencia frontotemporal; DVASC: demencia vascular; ns: no significativo.
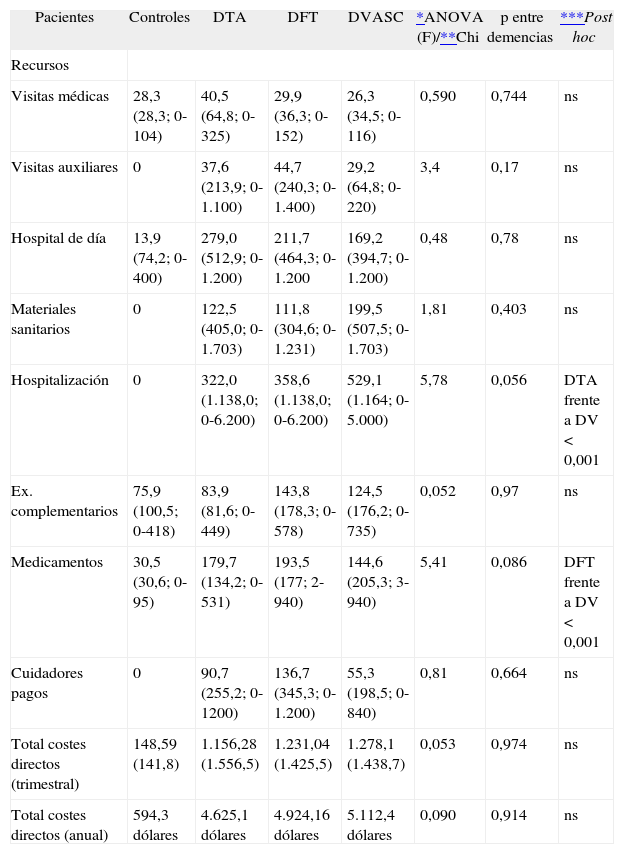
En tabla 3 se muestran las medias de coste por subtipo de demencias en lo que respecta a la utilización de recursos. El coste directo anual fue de 4.625 dólares para DTA, 4.924 para DFT y para DVASC 5.112 (p > 0,05 entre los grupos). En el análisis post hoc entre DTA y DFT no se presentaron diferencias significativas. Los pacientes con DVASC mostraron mayor coste por ingresos hospitalarios que las DTA (p < 0,001). Los pacientes con DVASC tuvieron un menor gasto en medicamentos que las DFT (p < 0,001). No hubo diferencias significativas en los costes directos trimestrales.
Utilización de recursos por trimestre
| Pacientes | Controles | DTA | DFT | DVASC | *ANOVA (F)/**Chi | p entre demencias | ***Post hoc |
| Recursos | |||||||
| Visitas médicas | 28,3 (28,3; 0-104) | 40,5 (64,8; 0-325) | 29,9 (36,3; 0-152) | 26,3 (34,5; 0-116) | 0,590 | 0,744 | ns |
| Visitas auxiliares | 0 | 37,6 (213,9; 0-1.100) | 44,7 (240,3; 0-1.400) | 29,2 (64,8; 0-220) | 3,4 | 0,17 | ns |
| Hospital de día | 13,9 (74,2; 0-400) | 279,0 (512,9; 0-1.200) | 211,7 (464,3; 0-1.200 | 169,2 (394,7; 0-1.200) | 0,48 | 0,78 | ns |
| Materiales sanitarios | 0 | 122,5 (405,0; 0-1.703) | 111,8 (304,6; 0-1.231) | 199,5 (507,5; 0-1.703) | 1,81 | 0,403 | ns |
| Hospitalización | 0 | 322,0 (1.138,0; 0-6.200) | 358,6 (1.138,0; 0-6.200) | 529,1 (1.164; 0-5.000) | 5,78 | 0,056 | DTA frente a DV < 0,001 |
| Ex. complementarios | 75,9 (100,5; 0-418) | 83,9 (81,6; 0-449) | 143,8 (178,3; 0-578) | 124,5 (176,2; 0-735) | 0,052 | 0,97 | ns |
| Medicamentos | 30,5 (30,6; 0-95) | 179,7 (134,2; 0-531) | 193,5 (177; 2-940) | 144,6 (205,3; 3-940) | 5,41 | 0,086 | DFT frente a DV < 0,001 |
| Cuidadores pagos | 0 | 90,7 (255,2; 0-1200) | 136,7 (345,3; 0-1.200) | 55,3 (198,5; 0-840) | 0,81 | 0,664 | ns |
| Total costes directos (trimestral) | 148,59 (141,8) | 1.156,28 (1.556,5) | 1.231,04 (1.425,5) | 1.278,1 (1.438,7) | 0,053 | 0,974 | ns |
| Total costes directos (anual) | 594,3 dólares | 4.625,1 dólares | 4.924,16 dólares | 5.112,4 dólares | 0,090 | 0,914 | ns |
Los valores están expresados en medias (desviación estándar; rango) a valor del dólar (1 dólar = 3 dólares argentinos a fecha de noviembre de 2008). Diferencias entre demencias con
DFT: demencia frontotemporal; DTA: demencia tipo Alzheimer; DVASC: demencia vascular; ns: no significativo.
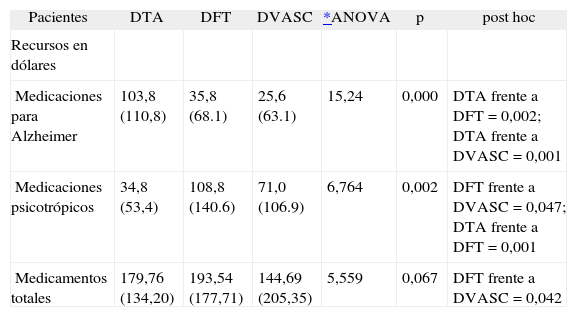
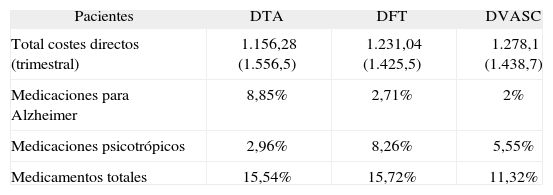
En la tabla 4 se muestra el análisis estadístico del coste de medicamentos entre las demencias. Los pacientes con DTA presentaron mayor gasto en antidemenciales que el resto de las demencias, los sujetos con DFT mayor gasto de psicotrópicos que el resto de las demencias y los que padecían DVASC menor gasto en medicamentos que otras demencias. El gasto trimestral en fármacos representó del total trimestral un 15,54% en DTA, 15,72% en DFT y 11,32% en DVASC (tabla 5).
Utilización de medicamentos (valores trimestrales)
| Pacientes | DTA | DFT | DVASC | *ANOVA | p | post hoc |
| Recursos en dólares | ||||||
| Medicaciones para Alzheimer | 103,8 (110,8) | 35,8 (68.1) | 25,6 (63.1) | 15,24 | 0,000 | DTA frente a DFT = 0,002; DTA frente a DVASC = 0,001 |
| Medicaciones psicotrópicos | 34,8 (53,4) | 108,8 (140.6) | 71,0 (106.9) | 6,764 | 0,002 | DFT frente a DVASC = 0,047; DTA frente a DFT = 0,001 |
| Medicamentos totales | 179,76 (134,20) | 193,54 (177,71) | 144,69 (205,35) | 5,559 | 0,067 | DFT frente a DVASC = 0,042 |
Los valores están expresados en medias (desviación estándar) a valor del dólar (1 dólar = 3 dólares argentinos a fecha de noviembre de 2008).
DFT: demencia frontotemporal; DTA: demencia tipo Alzheimer; DVASC demencia vascular.
Porcentajes de gasto en medicamentos sobre el coste total trimestral
| Pacientes | DTA | DFT | DVASC |
| Total costes directos (trimestral) | 1.156,28 (1.556,5) | 1.231,04 (1.425,5) | 1.278,1 (1.438,7) |
| Medicaciones para Alzheimer | 8,85% | 2,71% | 2% |
| Medicaciones psicotrópicos | 2,96% | 8,26% | 5,55% |
| Medicamentos totales | 15,54% | 15,72% | 11,32% |
DFT: demencia frontotemporal; DTA: demencia tipo Alzheimer; DVASC demencia vascular.
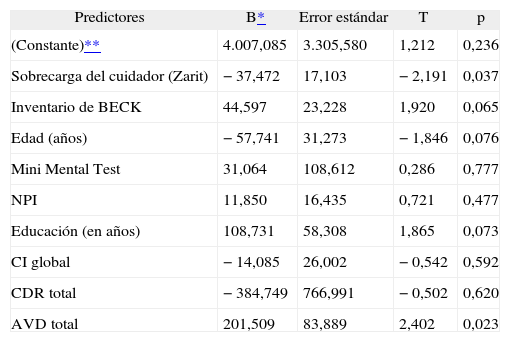
Para el primer análisis se realizó un análisis multivariado en el total de las demencias. En la tabla 6 se presenta el análisis de regresión (r2 = 0,76). Se demostró que las covariables que significativamente incrementaron el coste fueron: sobrecarga del cuidador (Zarit) (p = 0,037) y AIVD total (p = 0,023). La depresión demostró una tendencia (p = 0,065). El análisis de sensibilidad usando la variable costes log-transformada retiró del modelo la sobrecarga del cuidador (p = 0,23), pero aumentó la significación de la depresión (p = 0,027) y el nivel de educación (p = 0,04). Por cada punto del inventario de Beck los costes se incrementaron 44 dólares por trimestre y por cada punto en AIVD 201 dólares.
Ecuación de regresión lineal múltiple para todas las demencias
| Predictores | B* | Error estándar | T | p |
| (Constante)** | 4.007,085 | 3.305,580 | 1,212 | 0,236 |
| Sobrecarga del cuidador (Zarit) | −37,472 | 17,103 | −2,191 | 0,037 |
| Inventario de BECK | 44,597 | 23,228 | 1,920 | 0,065 |
| Edad (años) | −57,741 | 31,273 | −1,846 | 0,076 |
| Mini Mental Test | 31,064 | 108,612 | 0,286 | 0,777 |
| NPI | 11,850 | 16,435 | 0,721 | 0,477 |
| Educación (en años) | 108,731 | 58,308 | 1,865 | 0,073 |
| CI global | −14,085 | 26,002 | −0,542 | 0,592 |
| CDR total | −384,749 | 766,991 | −0,502 | 0,620 |
| AVD total | 201,509 | 83,889 | 2,402 | 0,023 |
AVD: actividades de la vida diaria; CDR: Clinical Dementia Rating.
Posteriormente se realizó el mismo análisis para cada una de las demencias. Con respecto a la DTA se destaca en este grupo una asociación significativa con el compromiso en las AIVD (B = 62,519; p = 0,020) y educación (B = 81,900; p = 0,008). Por cada punto en AIVD los costes se incrementaron 62 dólares por trimestre.
En la DFT se presentó asociación con la depresión (B = 74,408; p = 0,034) y la edad (B-222,195; p = 0,048). Con la variable costes log-transformada se demostró significación con el CDR (B= −1800,357; p = 0,048), Beck (B = 74,408,357; p = 0,01) y Minimental Test (B = −128,728; p = 0,028).
Con respecto a la DVASC no se demostró significación en los coeficientes de regresión lineal y tampoco con la variable costes log-transformada.
DiscusiónEste es el primer estudio en Argentina que registra los costes discriminados por tipo de demencia. A principios del año 2007 Allegri et al3 publicaron un estudio de costes en DTA, siendo el coste directo anual referido al año 2001 de 3.189 dólares. En el presente trabajo el coste para DTA fue de 4.625 dólares, además se añadió el gasto para DFT, que fue de 4.924 dólares y para DVASC que fue de 5.112 (valores desconocidos hasta el momento). Fue ligeramente mayor para DVASC probablemente porque este subgrupo tiene más coste por ingreso hospitalario. Se ha reportado que el coste de la DVASC es mayor que el de la DTA18. En nuestro estudio no hemos encontrado diferencias significativas en el coste directo anual.
El ingreso y la consulta en el hospital de día representaron el mayor gasto en todos los subtipos. En el presente trabajo no se discriminó el coste en los pacientes ingresados, ya que ese no era el objetivo. Es por ello que, a diferencia del estudio de Allegri et al donde el gasto por medicamentos representaba un 56,4% del gasto trimestral, en este estudio, en DTA, representó sólo un 15,4% del gasto total en todas las demencias.
El mayor gasto por medicamentos lo presentó la DFT, dado que este tipo de patología suele asociarse con una mayor prescripción de psicotrópicos, más trastornos de conducta (mayor NPI) y mayor sobrecarga por parte de los cuidadores. Lógicamente el subgrupo DTA tuvo más gasto por antidemenciales, aunque en la tabla 4 se observa que también se utilizaron de forma off label en DFT y DVASC. La DVASC implicó un menor gasto en medicamentos (menos psicotrópicos y antidemenciales).
Pocos estudios han examinado predictores clínicos del aumento del coste en demencia5–7. Se ha publicado que un punto de incremento en el NPI aumenta el coste en 30 dólares al mes19. En nuestra muestra no se demostró una correlación significativa en ninguno de los subtipos de demencia con el NPI. Sin embargo, se presentó como hallazgo una correlación con el inventario de Beck no reportado previamente en demencias. Por cada punto del inventario de Beck los costes de las demencias se incrementan 44 dólares por trimestre, y por cada punto en AIDV los costes aumentaban (201 en demencias y 62 dólares sólo en Alzheimer por trimestre).
A diferencia de otros estudios6 los test de rendimiento global (MMSE y CDR) no contribuyeron significativamente al incremento de costes en este modelo, salvo en la DFT, probablemente debido al tamaño de la muestra y a que la mayoría de los casos eran de grado leve.
Se destaca la importancia de la evaluación neuropsicológica en la toma de decisiones para orientar a estos pacientes y sus familias. Otros test cognitivos más específicos (como por ejemplo Fluencias, Listas de palabras, test ejecutivos) no fueron evaluados.
Debe destacarse que la mayoría de los pacientes presentaban grados leves de demencia, y el coste de estas aumenta según el grado de gravedad3.
En función de lo referido previamente se puede concluir que las acciones y los tratamientos dirigidos a retrasar o evitar la institucionalización y mejorar la cobertura de medicamentos (principalmente psicotrópicos) de los pacientes es de capital importancia para poder generar ahorros en el sistema de salud. Así mismo, resulta crucial el control de la depresión y el mantenimiento de los pacientes en estadios leves.
Se puede inferir que el control de estas variables podría ayudar en los costes indirectos a través de la disminución del tiempo necesario para cuidar a los pacientes.
El factor limitante de este trabajo es que no representa a la población de todo el país, ya que no se discriminó el análisis en pacientes internados y ambulatorios, y depende de la tasa de cambio de peso a dólar del momento, que si bien en el periodo evaluado (2002–2008) se mantuvo en aproximadamente 3 a 1, los costes básicos aumentaron en pesos argentinos en este periodo.
En resumen, este es el primer trabajo que compara los costes directos en enfermedad de Alzheimer, DFT y vascular en la República Argentina. Con el crecimiento de la población añosa en nuestro país se vuelve indispensable el análisis de la distribución de recursos sanitarios en pacientes con demencias, y las políticas sanitarias que de ello deriven, costes que por el momento están a cargo sólo de familiares, personas por lo demás golpeadas en cuanto a la distribución entre ingresos y costes.
AgradecimientosEl presente trabajo de investigación ha podido realizarse gracias al apoyo económico de subsidios de investigación del Ministerio de Salud de la Nación (Becas “Ramón Carrillo- Arturo Oñativia” [GR, CD, LB] y CONICET [RFA, GR y CD]) y del Ministerio de Salud del Gobierno de la Ciudad Autónoma de Buenos Aires (RFA, CMS). Las opiniones expresadas en este artículo pertenecen a los autores y no necesariamente a los Ministerios de Salud o los centros de trabajo de cada participante.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.