Evaluar el coste-efectividad del ácido 5-aminolevulínico (5-ALA, Gliolan®) en pacientes intervenidos quirúrgicamente de glioma maligno, en condiciones de práctica médica habitual en España.
Material y métodosSe determinaron las ratios de coste incremental por resección completa (RC) y de coste incremental por año de vida ajustado por calidad (AVAC) ganado, sobre la base de los datos recogidos en el estudio observacional VISIONA.
ResultadosEl coste incremental con 5-ALA frente a la cirugía convencional con luz blanca asciende a 4.550 € por RC adicional conseguida y a 9.021 € por AVAC ganado. Estos resultados se muestran consistentes en un análisis de sensibilidad.
ConclusiónLa cirugía del glioma maligno guiada por fluorescencia con 5-ALA conlleva un incremento de costes moderado respecto a la práctica quirúrgica actual y muestra una relación coste-efectividad favorable.
This study evaluates the cost-effectiveness of 5-aminolevulinic acid (5-ALA, Gliolan®) in patients undergoing surgery for malignant glioma, in standard clinical practice conditions in Spain.
Material and methodsCost-effectiveness ratios were determined in terms of incremental cost per complete resection (CR) and incremental cost per additional quality-adjusted life year (QALY), based on data collected in the VISIONA observational study.
ResultsIncremental cost with 5-ALA versus conventional surgery using white light only amounts to € 4550 per additional CR achieved and € 9021 per QALY gained. A sensitivity analysis shows these results to be robust.
ConclusionMalignant glioma surgery guided by 5-ALA fluorescence entails a moderate increase in hospital costs compared to current surgical practice and can be considered a cost-effective innovation.
Con una incidencia anual de en torno a 6 casos por cada 100.000 habitantes, los gliomas malignos (grados iii y iv de la escala de la Organización Mundial de la Salud) constituyen un tipo de neoplasia relativamente poco frecuente. No obstante, son tumores cerebrales de muy mal pronóstico, para los que hoy por hoy no existe tratamiento curativo1–3. El tratamiento estándar consiste actualmente en una resección del tumor lo más amplia posible sin afectar zonas elocuentes del cerebro, seguida de radioterapia y quimioterapia4.
Se ha observado que la resección quirúrgica completa (RC) de toda la parte del tumor captante de contraste en la resonancia magnética (RM) se asocia a un beneficio en la supervivencia5–9. Una dificultad importante durante la intervención quirúrgica, no obstante, es identificar los márgenes del tumor, por lo que actualmente en muchos pacientes no se logra una RC5.
La fluorescencia inducida con 5-aminolevulínico (5-ALA; Gliolan®), un medicamento que se administra por vía oral aproximadamente 3 h antes de la anestesia, permite delimitar de forma más clara esos márgenes y mejorar así sustancialmente los resultados de la intervención6,7. Su uso fue respaldado por el Grupo de Trabajo de Neurooncología de la Sociedad Española de Neurocirugía en un documento de consenso reciente10. No obstante, este nuevo abordaje terapéutico requiere el uso de recursos sanitarios adicionales, por lo que cabe plantearse si se trata de una opción coste-efectiva. En el análisis que se presenta en este artículo, se estudia esta cuestión en el contexto del sistema sanitario español, determinando el coste-efectividad incremental de la tecnología en términos del coste por RC adicionalmente conseguida en comparación con la práctica actual y determinando el coste-utilidad en términos del coste por año de vida ajustado por calidad ganado.
Material y métodosCoste-efectividadSe definió la ratio de coste-efectividad incremental de la cirugía con 5-ALA como sigue:
El análisis de coste-utilidad es una variante del análisis coste-efectividad, donde la efectividad conseguida se expresa en años de vida ganados ajustados por calidad de vida (AVAC). En este trabajo en particular, se definió la ratio de coste-utilidad incremental como:
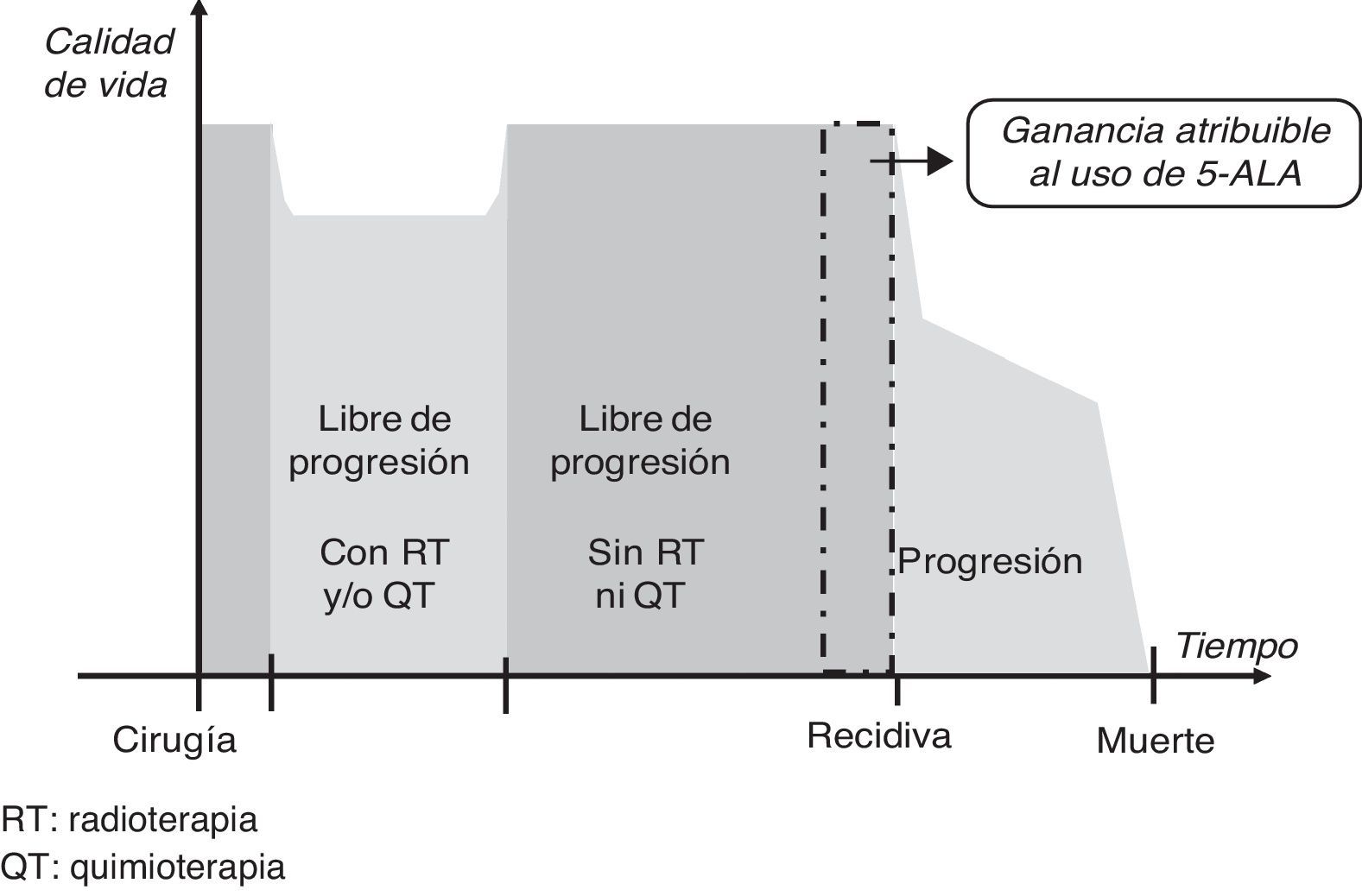
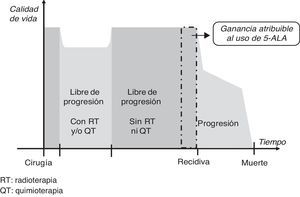
La ganancia en AVAC se entendió como la prolongación de la supervivencia libre de progresión (SLP) obtenida en la intervención con 5-ALA de gliomas malignos de grado iv respecto a la conseguida con luz blanca, ajustada por la calidad de vida de pacientes libres de progresión después de haber sido operados y de haber recibido radioterapia y quimioterapia. Esta definición se basa en la modelización del curso de la enfermedad y su tratamiento que muestra la figura 1, que diferencia 3 fases después del postoperatorio, en que los niveles de calidad de vida podrían ser sustancialmente diferentes11: una fase de tratamiento con radio y/o quimioterapia, una fase libre de progresión y sin tratamiento con radio y/o quimioterapia, y una fase final a partir de la recidiva.
Se consideró que una mayor tasa de RC podría resultar en una prolongación de la SLP de los pacientes operados bajo fluorescencia, pero ya no afectaría a la esperanza ni a la calidad de vida a partir del momento de la recidiva. Por esa razón, se tomó como hipótesis de trabajo que no habría diferencias entre los dos grupos de análisis en los parámetros clínicos y el consumo de recursos sanitarios en el periodo entre la cirugía y la finalización de la radioterapia y la quimioterapia, y que tampoco las habría en el periodo entre el momento de la constatación de la progresión de la enfermedad y el fallecimiento del paciente. Por tanto, se consideró que la única diferencia entre los dos grupos de pacientes sería un tiempo adicional libre de progresión para aquellos que fueron operados con 5-ALA.
Fuente de datos clínicosLos datos clínicos utilizados en el presente análisis se obtuvieron de la base de datos del estudio VISIONA, un reciente estudio observacional retrospectivo que comparó, en el contexto de la práctica clínica española, la resección de gliomas malignos guiada por fluorescencia con 5-ALA con la resección realizada de forma convencional bajo luz blanca. Los detalles de este estudio se han descrito recientemente en otra publicación12. De forma resumida, se seleccionó un grupo de centros hospitalarios españoles con un servicio de neurocirugía donde la técnica quirúrgica de extirpación con 5-ALA se usaba habitualmente y un grupo comparador de centros donde esta técnica no estaba disponible. Se recogieron datos de 251 pacientes evaluables, operados a partir de julio del 2008, fecha en la que se empezó a disponer de 5-ALA en España a través de su solicitud a las Autoridades Sanitarias mediante el procedimiento de uso compasivo. Se formularon los criterios de inclusión y exclusión de tal manera que solamente fueron elegibles pacientes que cumplían con los criterios de indicación clínica para el uso de 5-ALA, de modo que el hecho de ser intervenido con una técnica u otra no dependía de las características del paciente. Es decir, los pacientes operados sin 5-ALA habrían sido operados con 5-ALA si el centro en el que se operaron hubiera implantado esa técnica.
Efectividad ganadaLos datos sobre el impacto clínico de la tecnología, necesarios para el análisis económico planteado, eran la tasa de RC y el tiempo de SLP. La tasa de RC se definió como la proporción de pacientes con glioma de grados iii y iv operados con 5-ALA u operados con la microcirugía tradicional con luz blanca, que no presentaban captación de contraste en la RM postoperatoria de control previa a la radioterapia. Los casos en que la valoración de si había o no tumor residual en la RM fue dudosa se consideraron como resecciones incompletas.
Para el análisis de la SLP solo se incluyó a los pacientes con gliomas de grado IV, dado que la supervivencia es muy distinta para los pacientes con gliomas de grado iii. El tiempo de SLP se definió como el número de meses tras la cirugía hasta producirse progresión de la enfermedad o muerte por cualquier causa. A este efecto, se definió como progresión, la aparición de nuevas lesiones captantes de contraste mayores de 1cm, el incremento en la extensión del tumor de un 25% o más, según la tomografía computarizada o la RM, empeoramiento en la condición clínica/neurológica o necesidad de incrementar los corticoides. El tiempo de SLP se analizó mediante el método Kaplan-Meier, estimando la media restringida de tiempo en cada grupo de análisis.
Las utilidades de estados de salud después de una cirugía de glioma, necesarias para el ajuste por calidad de vida del tiempo de SLP ganado, se obtuvieron de una publicación reciente de Rogers et al.11, que las determinaron mediante el llamado método del «juego estándar»13.
Costes incrementalesRespecto a los costes adicionales de la cirugía con 5-ALA, estos se limitan, en principio, al empleo de Gliolan®, cuyo precio por vial de 1,5g es de 980 € (PVL), de acuerdo con la base de datos del medicamento del Consejo General de Colegios Oficiales de Farmacéuticos. Cabe señalar que este fármaco solo puede ser utilizado por neurocirujanos experimentados, familiarizados con la cirugía de los gliomas malignos, que tengan un exhaustivo conocimiento de la anatomía funcional del cerebro y que hayan completado un curso de formación sobre cirugía guiada por fluorescencia, de acuerdo con los actuales requisitos establecidos por la Agencia Europea del Medicamento para el uso del fármaco. No obstante, teniendo en cuenta que la empresa comercializadora, siguiendo lo establecido en el Plan de Gestión de Riesgos del medicamento, se encarga de organizar esta formación en España, su coste no recae sobre el sistema sanitario y no se ha tenido en cuenta en el presente análisis.
Dado que el desembolso de los costes incrementales se produce al inicio del periodo de análisis (el momento de la cirugía), no se ha llevado a cabo ningún tipo de descuento.
Análisis de sensibilidadTeniendo en cuenta que algunos de los parámetros clave utilizados en el presente análisis económico no se conocen con certeza, se llevó a cabo un análisis de sensibilidad en el que se recalcularon las ratios de coste-efectividad y coste-utilidad, introduciendo variaciones en los valores de estos parámetros. En primer lugar, se determinaron las ratios que hubiesen resultado de utilizar los resultados del análisis principal del único ensayo clínico controlado con 5-ALA, reportado por Stummer et al.6. También se variaron los parámetros claves en un rango de –40% a +40%, considerando que este intervalo engloba ampliamente los resultados observados en todos los subgrupos analizados en el estudio VISIONA, así como los reportados por Stummer et al.
Además, para tener en cuenta que no todos los centros de neurocirugía españoles disponen en la actualidad de un microscopio quirúrgico preparado para el uso de fluorescencia, se realizó otro análisis adicional para este escenario. Para poder utilizar 5-ALA, estos centros deberían primero adaptar sus equipos mediante el acoplamiento de un módulo específico, incurriendo en un importante coste adicional. Se consideró que, en el caso de tener que instalar un módulo de este tipo, el coste por intervención se incrementaría en un importe dependiendo del precio del módulo escogido, del periodo en que se amortiza y del número de pacientes que se intervienen en el centro. En concreto, se determinó el importe en cada caso mediante la siguiente fórmula:
Finalmente, se determinaron los resultados para el hipotético caso en que todos los parámetros tomaran los valores de los escenarios anteriores menos ventajosos para el uso de 5-ALA.
ResultadosEn el estudio VISIONA se obtuvieron datos evaluables de 131 pacientes operados con 5-ALA (de estos, 8 con glioma de grado iii y 123 de grado iv) y 120 pacientes operados bajo luz blanca (15 de grado iii y 105 de grado iv). En las características basales hubo algunas diferencias estadísticamente significativas entre los dos grupos: en el grupo de pacientes operados bajo luz blanca, había un número mayor de pacientes en grupos de estado funcional bueno (KPS 90-100) y un porcentaje mayor de pacientes con dudosa afectación de un área elocuente. En el grupo de pacientes operados con 5-ALA, el volumen preoperatorio del tumor fue algo mayor y hubo más tumores con infiltración del epéndimo12.
No hubo diferencias estadísticamente significativas respecto al momento de inicio y la duración de la radioterapia y la quimioterapia, aunque la dosis total de radioterapia era ligeramente superior en el grupo de pacientes con luz blanca. En ambos grupos, el 90% de los pacientes con glioma de grado iv recibió quimioterapia con temozolomida.
El porcentaje de pacientes operados con fluorescencia con 5-ALA en los que se alcanzó una RC fue del 67% frente al 45% del grupo operado bajo luz blanca (p=0,001, prueba de la chi al cuadrado). Durante los primeros 24 meses después de la cirugía, el porcentaje de pacientes con glioma grado iv libres de progresión fue en todo momento mayor en el grupo operado con 5-ALA (p=0,034, prueba de Breslow) y se consiguió una media de 1,5 meses adicionales de SLP (p=0,067, prueba de Student); la diferencia entre las medianas era de 2,1 meses. El 22% de las observaciones fueron censuradas y solo 10 pacientes constaban como vivos y libres de progresión a los 24 meses. La proporción de pacientes libres de progresión a los 6 meses, la variable principal en el estudio VISIONA determinante para su tamaño muestral, fue del 69% frente al 48% (p=0,002, prueba de la chi al cuadrado).
Respecto a la calidad de vida, se determinó la utilidad para el estado libre de progresión (sin recibir radioterapia ni quimioterapia) en 0,887, en una escala de 0 (equivalente a muerte) a 1 (equivalente a un estado de salud perfecta), por lo que se ganaron en promedio 0,11 AVAC (= 0,887×1,5/12) con la cirugía guiada mediante fluorescencia con 5-ALA frente a la cirugía convencional con luz blanca.
En el 97% de los pacientes operados con 5-ALA se empleó un vial de Gliolan® 1,5g, ya que contenía la dosis suficiente, utilizándose un segundo vial de Gliolan® solo en el 3% de pacientes restantes. Dado que el precio de un vial asciende a 980 €, en promedio el coste farmacológico adicional frente a los pacientes operados con luz blanca ascendía por tanto a 1.010 €.
La ratio de coste-efectividad incremental ascendía por consiguiente a 4.550 € por RC adicional frente a la cirugía convencional con luz blanca, y la ratio de coste-utilidad incremental a 9.021 € por AVAC ganado.
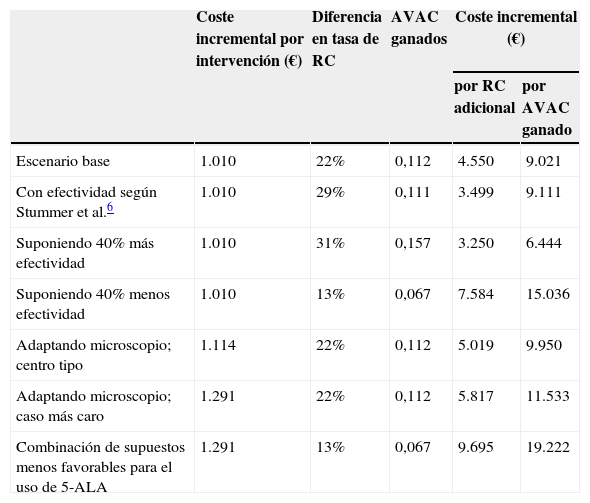
Análisis de sensibilidadSi se efectúan otros supuestos alternativos para los parámetros de efectividad, los resultados se modifican de manera proporcional, tal como muestran los datos en la tabla 1. En particular, si en lugar de los resultados obtenidos en el estudio VISIONA se realizara el análisis con los datos reportados en el ensayo clínico de Stummer et al6, la ratio de coste-efectividad incremental sería de 3.499 € por RC adicional y la ratio de coste-utilidad incremental de 9.111 € por AVAC ganado.
Análisis de sensibilidad
| Coste incremental por intervención (€) | Diferencia en tasa de RC | AVAC ganados | Coste incremental (€) | ||
|---|---|---|---|---|---|
| por RC adicional | por AVAC ganado | ||||
| Escenario base | 1.010 | 22% | 0,112 | 4.550 | 9.021 |
| Con efectividad según Stummer et al.6 | 1.010 | 29% | 0,111 | 3.499 | 9.111 |
| Suponiendo 40% más efectividad | 1.010 | 31% | 0,157 | 3.250 | 6.444 |
| Suponiendo 40% menos efectividad | 1.010 | 13% | 0,067 | 7.584 | 15.036 |
| Adaptando microscopio; centro tipo | 1.114 | 22% | 0,112 | 5.019 | 9.950 |
| Adaptando microscopio; caso más caro | 1.291 | 22% | 0,112 | 5.817 | 11.533 |
| Combinación de supuestos menos favorables para el uso de 5-ALA | 1.291 | 13% | 0,067 | 9.695 | 19.222 |
Para conocer el precio del módulo que sería necesario instalar en caso de que un centro no dispusiera de un microscopio quirúrgico preparado para fluorescencia, se solicitó su precio a los principales proveedores. Así se pudo saber que este recurso adicional tiene un precio orientativo de entre 30.000 € y 45.000 €. Respecto a su periodo de amortización, se supuso que en ningún caso sería inferior a 8 años. Finalmente, teniendo en cuenta las exigencias de la práctica mínima del procedimiento quirúrgico, el número de intervenciones en un centro no debería ser inferior a 20 al año. De ello se desprende que el coste adicional por intervención no superaría los 281 € (= 45.000 €/[8 años × 20 intervenciones por año]), con lo que incluso en el centro con menor actividad imaginable el coste total no superaría en promedio los 1.291 € por intervención, incluyendo el coste farmacológico. Para este caso extremo, la ratio de coste-efectividad incremental ascendería a 5.817 € por RC adicional frente a la cirugía convencional con luz blanca, mientras el coste-utilidad incremental se situaría en 11.533 € por AVAC ganado.
Por otro lado, en un centro tipo, que adquiere el módulo adicional a un precio intermedio, lo amortiza en un plazo de 12 años y opera 30 pacientes al año, las dos ratios serían de 5.019 € por RC adicional y 9.950 € por AVAC ganado, respectivamente.
Finalmente, la tabla 1 incluye un escenario que refleja los resultados que se obtendrían suponiendo que, de entre los todos escenarios anteriores, se tomaran los parámetros menos ventajosos para el uso de 5-ALA.
DiscusiónLa utilización de la fluorescencia con 5-ALA supone esencialmente una innovación en el procedimiento quirúrgico del glioma maligno. En coherencia con ello, en este trabajo se ha determinado en primer lugar el coste-efectividad de esta nueva tecnología en términos del objetivo inmediato de la intervención, que es la extirpación del tumor más radical posible, mediante la ratio de coste incremental por RC adicionalmente conseguida frente a la cirugía convencional con luz blanca. No obstante, teniendo en cuenta que el objetivo último de la cirugía es la mejora en la supervivencia y calidad de vida del paciente, también se ha considerado de interés conocer el coste-utilidad en términos de coste incremental por AVAC ganado.
Los resultados en ambos indicadores indican una eficiencia económica notable de la nueva tecnología. Para apreciar que el importe de 4.550 € por RC adicionalmente conseguida con 5-ALA no es muy elevado, puede ser útil tener como punto de referencia el coste de los procesos con hospitalización correspondientes a la cirugía de glioma. Según datos publicados por el Fondo de Cohesión Sanitaria, el coste del Grupo Relacionado con el Diagnóstico más frecuentemente asociado a las craneotomías asciende a aproximadamente 18.000 €14. Teniendo en cuenta que según el estudio VISIONA la tasa de RC alcanzada sin 5-ALA es del 45%, el coste medio por RC conseguida estaría actualmente en torno de los 40.000 € (≈ 18.000€/0,45).
En cuanto al coste por AVAC ganado, se puede apreciar que el valor calculado en este trabajo, de unos 9.000 €, queda muy debajo de los umbrales de coste-utilidad habitualmente considerados aceptables en España15. Otro punto de referencia aquí es el Instituto Nacional de Excelencia Clínica británico, que normalmente sitúa el umbral para la financiación pública de nuevos fármacos en 30.000 £ por AVAC, pero precisamente en el contexto del tratamiento de gliomas malignos ha aplicado un criterio más flexible en el pasado reciente.
Los resultados del análisis principal han mostrado ser robustos en el análisis de sensibilidad, a pesar de que este refleja el impacto de variaciones más amplias de lo que razonablemente sería de esperar sobre la base de los datos clínicos conocidos. Así el rango de valores estudiados engloba ampliamente los resultados observados en todos los subgrupos analizados en el estudio VISIONA, así como los reportados por Stummer et al. La referencia a este último trabajo es obligada, ya que se trata del único estudio fase iii, multicéntrico, controlado, aleatorizado y prospectivo que comparó la resección de gliomas malignos guiada por fluorescencia con 5-ALA con la resección realizada de forma convencional. Es de destacar también que los resultados observados en el estudio VISIONA están en concordancia con este ensayo en cuanto a las ganancias terapéuticas en RC y SLP.
Para atender a la variabilidad en los niveles de actividad y dotación de equipamientos existentes en el sistema sanitario español, el análisis de sensibilidad también contempla la casuística de los centros hospitalarios que actualmente no disponen de un microscopio quirúrgico preparado para la microcirugía guiada por fluorescencia. Se ha podido ver que incluso en el caso menos favorable para el uso de 5-ALA, los costes adicionales por intervención que se derivan de la necesaria adaptación de los equipos existentes en estos centros, no son muy elevados y no alteran de manera sustancial las ratios de coste-efectividad y coste-utilidad obtenidas.
La mayor debilidad del análisis llevado a cabo en este trabajo está directamente relacionada con las debilidades de la fuente de los datos clínicos, el estudio VISIONA. Siendo un estudio observacional y retrospectivo, los datos obtenidos están sujetos a la calidad y cantidad de la información que se haya recogido, siempre menor a lo que se podría alcanzar con un estudio prospectivo controlado. También se ha visto que los dos grupos de pacientes no eran del todo homogéneos en algunos factores que podrían tener efecto sobre las variables de resultado. No obstante, en la medida que estas diferencias estaban presentes, suponían un sesgo en contra de la cirugía con 5-ALA.
Por otro lado, el interés añadido del estudio VISIONA respecto al ensayo de Stummer et al. radica, en primer lugar, en que los datos se han obtenido de la práctica clínica real en el contexto del sistema sanitario español y, por tanto, son una mejor base para hacer proyecciones sobre el impacto económico que comportan. En segundo lugar, desde que se llevó a cabo el ensayo de Stummer et al., se ha producido un cambio en el tratamiento de los pacientes, consistente actualmente en la administración, después de la cirugía, de radioterapia y quimioterapia con temozolomida, mientras los pacientes incluidos en el estudio de Stummer et al. recibieron solo cirugía y radioterapia. La proporción de pacientes con SLP 6 meses después de la cirugía observada en los pacientes tratados con 5-ALA en el estudio VISIONA supera la del trabajo sobre la eficacia de temozolomida de Stupp et al.16, que definieron el actual estándar. Este hallazgo es especialmente importante para confirmar la aplicabilidad de los resultados del beneficio del 5-ALA a la situación actual, ya que contribuye a clarificar que la utilidad de la resección completa no disminuye al utilizar una quimioterapia eficaz.
Respecto al análisis estadístico utilizado en este trabajo, hay que destacar que la diferencia en SLP entre pacientes operados con y sin 5-ALA fue estimada utilizando solamente las observaciones empíricas del estudio VISIONA. No se llevó a cabo ningún tipo de extrapolación de las curvas de supervivencia, por lo que implícitamente se supuso que no habría más ventaja en SLP por el uso de 5-ALA en pacientes con una SLP superior a los 2 años. Se trata, por tanto, de un supuesto muy conservador17.
Finalmente, hay que señalar que para transformar la ganancia en SLP conseguida con 5-ALA en AVAC ganados, el tiempo ganado fue ponderado por utilidades procedentes de un estudio de calidad de vida llevado a cabo en el Reino Unido. Aparte de que la metodología utilizada para determinar las utilidades no está fuera de debate, estos datos no se corresponden necesariamente con las preferencias de la población española por los correspondientes estados de salud. Aunque el análisis de sensibilidad ha mostrado que eventuales divergencias nacionales difícilmente podrían tener un impacto relevante en los resultados del presente análisis farmacoeconómico, sería de interés que futuros trabajos estudiaran la calidad de vida en pacientes españoles en las distintas fases del tratamiento del glioma maligno.
Como conclusión, se puede afirmar que la cirugía del glioma maligno guiada por fluorescencia con 5-ALA conlleva un incremento de costes moderado respecto a la práctica quirúrgica actual y muestra una relación coste-efectividad favorable.
FinanciaciónEste trabajo ha sido financiado por Laboratorios Gebro Pharma S.A.
Conflicto de interesesJordi Galván es empleado de Laboratorios Gebro Pharma, S.A. John Slof y Ricardo Díez Valle han recibido honorarios de Laboratorios Gebro Pharma, S.A.