El ictus es la principal causa de ingreso en los servicios de Neurología, siendo el infarto cerebral cardioembólico (ICE) de los subtipos más frecuentes.
MétodosEstudio observacional, multicéntrico, prospectivo, realizado en 5 hospitales públicos de la Comunidad de Madrid, cuyo objetivo fue estimar la utilización de recursos sanitarios y costes en el manejo del ICE agudo. Se incluyeron pacientes con ICE agudo de evolución<48h. Se registraron datos sociodemográficos, clínicos y los recursos sanitarios utilizados durante el ingreso y al alta hasta 30 días desde el ingreso, incluyendo el tratamiento rehabilitador al alta.
ResultadosSe seleccionaron 128 pacientes durante 8 meses, de 75,3±11,25 años, siendo un 46,9% mujeres, con una mortalidad del 4,7%. El 100% cumplía los criterios diagnósticos del GEENCV-SEN por antecedentes o el estudio realizado. Como antecedentes clínicos, el 50% presentó fibrilación auricular, y el 18,8%, otras fuentes mayores embolígenas. La fibrilación auricular no valvular fue la causa más frecuente de ICE (33,6%). Consumo de recursos: estancia media, 10,3±9,3 días; rehabilitación durante el ingreso, 46,9%, media 4,5 días, y al alta, 56,3%, media 26,8 días; complicaciones, 32%; intervenciones hospitalarias específicas, 19,5%; pruebas diagnósticas y analíticas sanguíneas, 100%, siendo la TAC craneal (98,4%), el dúplex TSA (87,5%) y el electrocardiograma (85,9%), las diagnósticas más frecuentes. El coste total medio por paciente en la fase aguda y rehabilitación por ICE fue de 13.139€, siendo la estancia hospitalaria (45,0%) y la rehabilitación al alta (29,2%) los recursos más importantes.
ConclusionesEl manejo agudo del ICE en la Comunidad de Madrid generó un importante consumo de recursos (13.139€) debido a la asistencia hospitalaria y la rehabilitación.
Stroke is the main cause of admission to Neurology departments and cardioembolic stroke (CS) is one of the most common subtypes of stroke.
MethodsA multicentre prospective observational study was performed in 5 Neurology departments in public hospitals in the Region of Madrid (Spain). The objective was to estimate the use of healthcare resources and costs of acute CS management. Patients with acute CS at<48h from onset were recruited. Patients’ socio-demographic, clinical, and healthcare resource use data were collected during hospitalisation and at discharge up to 30 days after admission, including data for rehabilitation treatment after discharge.
ResultsDuring an 8-month recruitment period, 128 patients were recruited: mean age, 75.3±11.25; 46.9% women; mortality rate, 4.7%. All patients met the CS diagnostic criteria established by GEENCV-SEN, based on medical history or diagnostic tests. Fifty per cent of the patients had a history of atrial fibrillation and 18.8% presented other major cardioembolic sources. Non-valvular atrial fibrillation was the most frequent cause of CS (33.6%). Data for healthcare resource use, given a mean total hospital stay of 10.3±9.3 days, are as follows: rehabilitation therapy during hospital stay (46.9%, mean 4.5 days) and after discharge (56.3%, mean 26.8 days), complications (32%), specific interventions (19.5%), and laboratory and diagnostic tests (100%). Head CT (98.4%), duplex ultrasound of supra-aortic trunks (87.5%), and electrocardiogram (85.9%) were the most frequently performed diagnostic procedures. Average total cost per patient during acute-phase management and rehabilitation was €13,139. Hospital stay (45.0%) and rehabilitation at discharge (29.2%) accounted for the largest part of resources used.
ConclusionsAcute CS management in the Region of Madrid resulted consumes large amounts of resources (€13,139), mainly due to hospital stays and rehabilitation.
El infarto cerebral de origen cardioembólico (ICE) se produce por la oclusión total o parcial de una arteria cerebral o precerebral por material embólico proveniente del corazón producido por arritmias, liberación de material desde superficies anormales valvulares o miocárdicas o por embolismo paradójico1. Son infartos generalmente de tamaño medio o grande, de topografía habitualmente cortical, con un inicio frecuente de la sintomatología en vigilia, una instauración habitualmente instantánea (minutos) o aguda (horas) de la focalidad neurológica, y generalmente con un máximo déficit neurológico desde el inicio de la enfermedad. Es imprescindible para su diagnóstico la presencia de una cardiopatía embolígena demostrada y la ausencia de oclusión o estenosis arterial significativa concomitantemente2.
El ICE representa entre el 14-30% de los infartos cerebrales3. En un reciente estudio observacional en España con más de 6.000 pacientes con ictus, un 87,6% presentó infarto cerebral, de los cuales el 26,2% eran cardioembólicos4–6. Este tipo de infarto cerebral presenta una tasa de incidencia bruta estimada de 28 casos/100.000 habitantes-año, y una tasa de prevalencia bruta en la población anciana de unos 8 casos por 1.000 habitantes7.
Las enfermedades cerebrovasculares son la primera causa de defunción en las mujeres y la segunda en hombres en España8. El ictus supone la cuarta causa de años de vida perdidos por discapacidad, la primera causa de discapacidad o invalidez a largo plazo en adultos, y la segunda causa de demencia9. Más del 18% de las muertes prematuras se deben a ictus, lo que conlleva una pérdida de unos 12 años potenciales de vida por cada 10.000 habitantes, siendo esta mayor en hombres9,10. Los ICE son infartos más extensos, en ocasiones múltiples, y con mayor probabilidad de recurrencia. Además, presentan peor pronóstico respecto a los de etiología aterotrombótica, con una supervivencia global del ICE a los 10 años inferior al 45%11.
En los servicios de Neurología, el ictus es la causa más frecuente de ingreso y de prolongación de la estancia hospitalaria. Además, las técnicas requeridas para su diagnóstico son costosas12. Los costes sanitarios en el primer año tras el diagnóstico son considerablemente elevados debido al ingreso hospitalario y a la rehabilitación, suponiendo la estancia hospitalaria hasta el 50% del coste total en ese primer año. Dentro de la atención ambulatoria, la necesidad de rehabilitación y transporte tras el alta supone el coste más importante13,14.
Para la prevención del ICE, los nuevos anticoagulantes orales aportan una nueva perspectiva terapéutica, pero presentan un mayor coste directo de tratamiento que las alternativas disponibles.
Considerando la elevada incidencia de ictus, especialmente en población anciana, el mayor envejecimiento de la población, y sobre todo, el coste de las nuevas terapias disponibles y la mayor gravedad del ICE que conllevaría un mayor consumo de recursos sanitarios, conocer el coste del manejo de los pacientes con ICE será de utilidad para racionalizar los recursos económicos y permitir una adecuada distribución de estos, y servirá de base para posibles estudios de costes o estrategias de prevención disponibles en el futuro.
El objetivo principal del Estudio COstes Directos del Infarto cerebral CardioEmbólico (CODICE) fue establecer los recursos sanitarios consumidos y los costes directos asociados al proceso asistencial de los pacientes con ICE agudo hospitalizados en centros públicos de la Comunidad de Madrid, desde la perspectiva del Sistema Nacional de Salud.
Pacientes y métodosEl Estudio CODICE es observacional, multicéntrico, de seguimiento prospectivo, realizado según la práctica clínica habitual. Se llevó a cabo en 5 servicios de Neurología, con o sin Unidad de Ictus, de centros hospitalarios de la red sanitaria pública de la Comunidad de Madrid: Hospital Universitario de La Princesa, Hospital General Universitario Gregorio Marañón, Hospital Universitario Príncipe de Asturias, Hospital Universitario Fundación Alcorcón y Hospital Universitario Infanta Sofía.
El estudio fue autorizado por la Dirección General de Ordenación e Inspección de la Consejería de Sanidad de la Comunidad de Madrid y por el Comité Ético de Investigación Clínica del Hospital Universitario de La Princesa, como centro de referencia, tras su clasificación por la Agencia Española de Medicamentos y Productos Sanitarios. Todos los pacientes incluidos en el Estudio CODICE, o sus cuidadores en representación de estos, firmaron un consentimiento informado previo.
Población del estudioEl estudio incluyó pacientes≥18 años con diagnóstico de ICE, según la clasificación de la Sociedad Española de Neurología2, con evidencia, en ausencia de otra etiología, de cardiopatía embolígena como trombo/tumor intracardíaco, estenosis mitral reumática, prótesis aórtica o mitral, endocarditis, fibrilación auricular, enfermedad del nodo sinusal, aneurisma ventricular izquierdo o acinesia tras infarto agudo de miocardio, infarto agudo de miocardio reciente (<3 meses), hipocinesia cardíaca global o discinesia, ingresados con menos de 48h de evolución en servicios de Neurología. Se excluyeron aquellos pacientes que presentaron un diagnóstico de ictus distinto de ICE o de ataque isquémico transitorio, así como los ictus intrahospitalarios en razón a una fuente cardioembólica inusual como, por ejemplo, embolismos durante procedimientos cardiológicos.
Los pacientes fueron seleccionados de forma consecutiva y competitiva durante un periodo de 8 meses (diciembre 2011-julio 2012). Se calculó un tamaño muestral de 140 pacientes mediante la aplicación GRANMO v. 7.10, a partir de la estimación de los pacientes con un nuevo episodio de ictus en la Comunidad de Madrid (1.625), según la incidencia bruta de ictus y la proporción de ictus cardioembólico1,15, con un valor riesgo alfa igual a 0,05, para una precisión de ±0,165 unidades en un contraste bilateral, asumiendo una pérdida de seguimiento del 7%.
Diseño y variables del estudioLos datos del estudio se recogieron prospectivamente mediante un cuaderno de recogida de datos cumplimentado por el investigador. El estudio se estructuró en 2 fases: una visita basal, coincidente con el ingreso del paciente, y el seguimiento de este tras el alta hospitalaria, mediante llamada telefónica al paciente y/o cuidador a los 30 días de la fecha de ingreso.
En la visita basal se recogió información sobre datos sociodemográficos, aspectos clínicos y consumo de recursos durante el ingreso hospitalario, a partir de sistemas informáticos, registros, historias clínicas e informes de alta. Además, se incluyó información sobre el tratamiento farmacológico crónico prescrito y la estimación del tratamiento de rehabilitación necesario al alta hospitalaria, considerando el tipo y la duración prevista. El grado de discapacidad física tras el episodio de ICE se midió mediante la Escala de Rankin modificada, en la que una mayor puntuación supone un aumento en el grado de discapacidad (máximo 6 puntos: muerte)16.
En la llamada telefónica de seguimiento se recogió información referente a la situación clínica del paciente tras el alta hospitalaria y el consumo de recursos durante ese periodo (exitus, complicaciones, reingresos y visitas a Urgencias), así como el tratamiento de rehabilitación al alta finalmente prescrito.
Análisis estadísticoCon los datos recogidos en el cuaderno de recogida de datos se elaboró una base de datos que se analizó con el programa estadístico PASW Statistics® 18.0 (Predictive Analytics Software). Se realizó un análisis descriptivo de las variables clínicas, de la enfermedad y de su manejo. Para las variables cuantitativas se calculó: media, desviación estándar (DE), intervalos de confianza al 95%, varianza, error típico, media recortada al 5%, mediana, mínimo y máximo. Para las variables cualitativas se calcularon las distribuciones de frecuencias y sus porcentajes. Además, se realizó un análisis de costes del consumo de recursos realizado por paciente.
Estimación de costesLos costes directos del manejo de pacientes con ICE agudo en la Comunidad de Madrid obtenidos en el Estudio CODICE comprenden el coste del consumo de recursos durante la estancia hospitalaria, el coste del tratamiento de rehabilitación prescrito al alta hospitalaria y el coste de los recursos sanitarios consumidos tras el alta hasta los 30 días desde la fecha de ingreso (reingresos, visitas a Urgencias y tratamiento farmacológico crónico durante ese periodo).
La estimación del coste por paciente se calculó mediante el consumo de recursos sanitarios individual de cada paciente en función del coste unitario asociado a cada uno de los recursos.
Los costes unitarios de los recursos sanitarios se obtuvieron a partir de los precios de mercado procedentes de la Base de Datos de Costes Sanitarios e-Salud (Oblikue Consulting)17. El coste de los tratamientos farmacológicos (PVP−IVA) se obtuvo a partir de los precios del Catálogo de Medicamentos del Consejo General de Colegios Oficiales de Farmacéuticos de España18. Todos los costes se presentaron en euros de 2012.
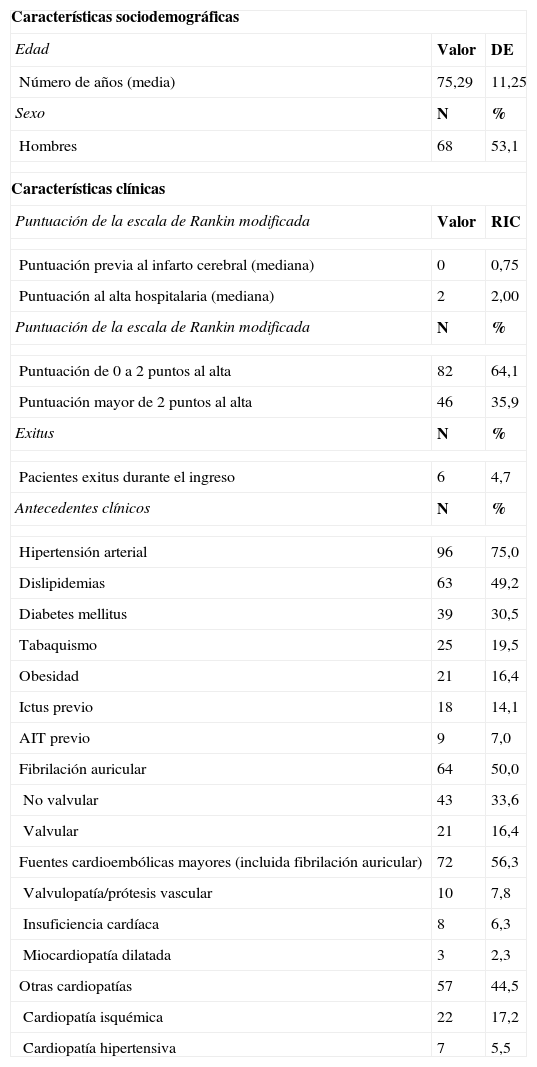
ResultadosCaracterísticas basales de los pacientesUn total de 128 pacientes fue seleccionado para el estudio. Las características clínicas y sociodemográficas de los pacientes se detallan en la tabla 1.
Características sociodemográficas y clínicas de los pacientes (n=128)
| Características sociodemográficas | ||
| Edad | Valor | DE |
| Número de años (media) | 75,29 | 11,25 |
| Sexo | N | % |
| Hombres | 68 | 53,1 |
| Características clínicas | ||
| Puntuación de la escala de Rankin modificada | Valor | RIC |
| Puntuación previa al infarto cerebral (mediana) | 0 | 0,75 |
| Puntuación al alta hospitalaria (mediana) | 2 | 2,00 |
| Puntuación de la escala de Rankin modificada | N | % |
| Puntuación de 0 a 2 puntos al alta | 82 | 64,1 |
| Puntuación mayor de 2 puntos al alta | 46 | 35,9 |
| Exitus | N | % |
| Pacientes exitus durante el ingreso | 6 | 4,7 |
| Antecedentes clínicos | N | % |
| Hipertensión arterial | 96 | 75,0 |
| Dislipidemias | 63 | 49,2 |
| Diabetes mellitus | 39 | 30,5 |
| Tabaquismo | 25 | 19,5 |
| Obesidad | 21 | 16,4 |
| Ictus previo | 18 | 14,1 |
| AIT previo | 9 | 7,0 |
| Fibrilación auricular | 64 | 50,0 |
| No valvular | 43 | 33,6 |
| Valvular | 21 | 16,4 |
| Fuentes cardioembólicas mayores (incluida fibrilación auricular) | 72 | 56,3 |
| Valvulopatía/prótesis vascular | 10 | 7,8 |
| Insuficiencia cardíaca | 8 | 6,3 |
| Miocardiopatía dilatada | 3 | 2,3 |
| Otras cardiopatías | 57 | 44,5 |
| Cardiopatía isquémica | 22 | 17,2 |
| Cardiopatía hipertensiva | 7 | 5,5 |
AIT: ataque isquémico transitorio; DE: desviación estándar; RIC: rango intercuartílico.
La edad media fue de 75,29 años (DE 11,25), con un rango entre 30 y 95 años. El 53,1% de los pacientes fueron hombres. Un 4,7% falleció durante el ingreso hospitalario. La puntuación de la Escala de Rankin modificada al alta hospitalaria obtuvo una mediana de 2 puntos (rango intercuartílico: 2,0), correspondiendo esta a un grado de discapacidad leve, en la que el paciente mantiene su independencia funcional. En la situación basal previa al infarto cerebral la puntuación obtenida fue una mediana de 0 puntos (rango intercuartílico: 0,75). El incremento medio en la puntuación de la Escala de Rankin modificada al alta hospitalaria frente a la situación basal previa al infarto cerebral fue de 1,57 puntos. Al recibir el alta hospitalaria, el 35,9% de los pacientes presentaba una puntuación mayor a 2 puntos.
Todos los pacientes cumplieron los criterios diagnósticos del Grupo de Estudio de Enfermedades Cerebrovasculares de la Sociedad Española de Neurología para ICE, debido a antecedentes clínicos o a través del estudio diagnóstico realizado durante el ingreso. Las potenciales fuentes embolígenas fueron los factores de riesgo vascular más frecuentes (57%), estando presente la fibrilación auricular en el 50% de los pacientes, y otras fuentes mayores en el 18,8%. Destacan también la hipertensión arterial y la dislipidemia. Según el juicio clínico al alta, el 100% de los pacientes presentó al menos una causa de ICE, siendo la más frecuente del episodio de ICE la fibrilación auricular no valvular, con un 33,6% de los pacientes (50% considerando todos los tipos de fibrilación auricular). Otras causas de ICE fueron miocardiopatía dilatada (FEVI<30%)/insuficiencia cardíaca congestiva reciente (5,5%) o valvulopatías (4,7%).
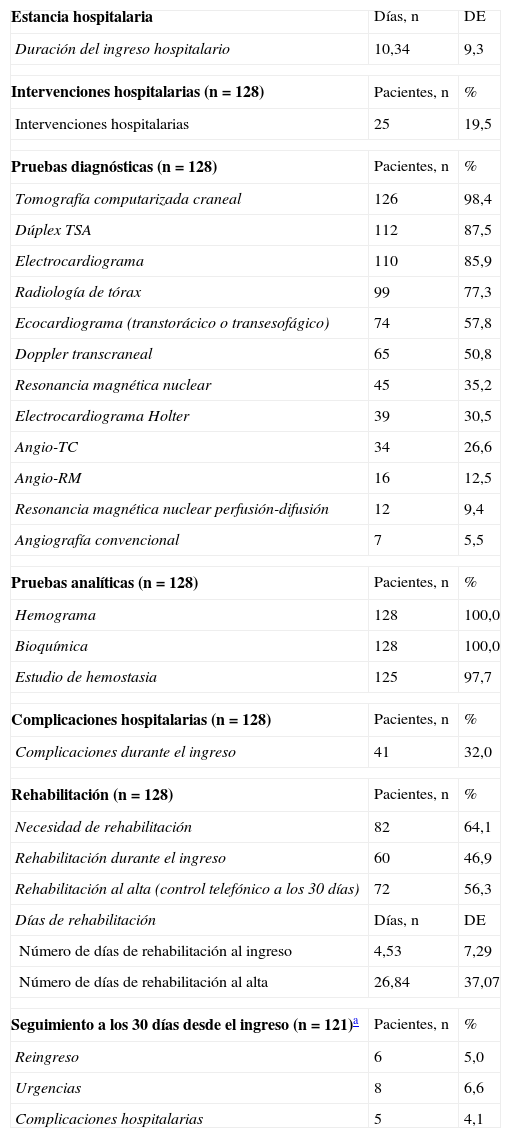
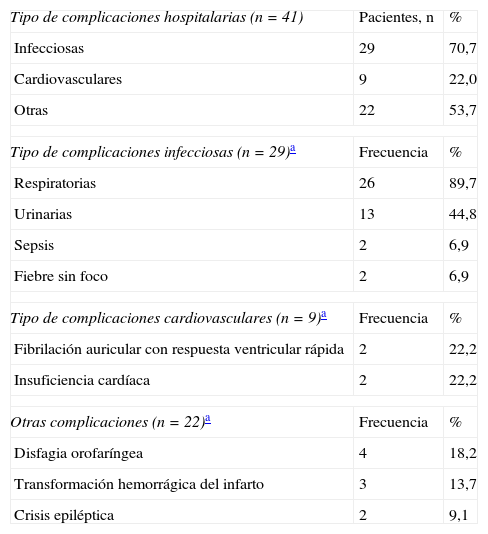
Utilización de los recursos sanitariosEl consumo de recursos realizado por los pacientes seleccionados se describe en la tabla 2. Los pacientes presentaron una estancia media hospitalaria de 10,34 días (DE 9,30). Durante el ingreso hospitalario, el 32% de los pacientes presentó alguna complicación, siendo más frecuentes las de etiología infecciosa (tabla 3).
Consumo de recursos sanitarios (n=128)
| Estancia hospitalaria | Días, n | DE |
| Duración del ingreso hospitalario | 10,34 | 9,3 |
| Intervenciones hospitalarias (n=128) | Pacientes, n | % |
| Intervenciones hospitalarias | 25 | 19,5 |
| Pruebas diagnósticas (n=128) | Pacientes, n | % |
| Tomografía computarizada craneal | 126 | 98,4 |
| Dúplex TSA | 112 | 87,5 |
| Electrocardiograma | 110 | 85,9 |
| Radiología de tórax | 99 | 77,3 |
| Ecocardiograma (transtorácico o transesofágico) | 74 | 57,8 |
| Doppler transcraneal | 65 | 50,8 |
| Resonancia magnética nuclear | 45 | 35,2 |
| Electrocardiograma Holter | 39 | 30,5 |
| Angio-TC | 34 | 26,6 |
| Angio-RM | 16 | 12,5 |
| Resonancia magnética nuclear perfusión-difusión | 12 | 9,4 |
| Angiografía convencional | 7 | 5,5 |
| Pruebas analíticas (n=128) | Pacientes, n | % |
| Hemograma | 128 | 100,0 |
| Bioquímica | 128 | 100,0 |
| Estudio de hemostasia | 125 | 97,7 |
| Complicaciones hospitalarias (n=128) | Pacientes, n | % |
| Complicaciones durante el ingreso | 41 | 32,0 |
| Rehabilitación (n=128) | Pacientes, n | % |
| Necesidad de rehabilitación | 82 | 64,1 |
| Rehabilitación durante el ingreso | 60 | 46,9 |
| Rehabilitación al alta (control telefónico a los 30 días) | 72 | 56,3 |
| Días de rehabilitación | Días, n | DE |
| Número de días de rehabilitación al ingreso | 4,53 | 7,29 |
| Número de días de rehabilitación al alta | 26,84 | 37,07 |
| Seguimiento a los 30 días desde el ingreso (n=121)a | Pacientes, n | % |
| Reingreso | 6 | 5,0 |
| Urgencias | 8 | 6,6 |
| Complicaciones hospitalarias | 5 | 4,1 |
DE: desviación estándar; RM: resonancia magnética; TC: tomografía computarizada; TSA: troncos supraaórticos.
Complicaciones hospitalarias durante el ingreso (n=41)
| Tipo de complicaciones hospitalarias (n=41) | Pacientes, n | % |
| Infecciosas | 29 | 70,7 |
| Cardiovasculares | 9 | 22,0 |
| Otras | 22 | 53,7 |
| Tipo de complicaciones infecciosas (n=29)a | Frecuencia | % |
| Respiratorias | 26 | 89,7 |
| Urinarias | 13 | 44,8 |
| Sepsis | 2 | 6,9 |
| Fiebre sin foco | 2 | 6,9 |
| Tipo de complicaciones cardiovasculares (n=9)a | Frecuencia | % |
| Fibrilación auricular con respuesta ventricular rápida | 2 | 22,2 |
| Insuficiencia cardíaca | 2 | 22,2 |
| Otras complicaciones (n=22)a | Frecuencia | % |
| Disfagia orofaríngea | 4 | 18,2 |
| Transformación hemorrágica del infarto | 3 | 13,7 |
| Crisis epiléptica | 2 | 9,1 |
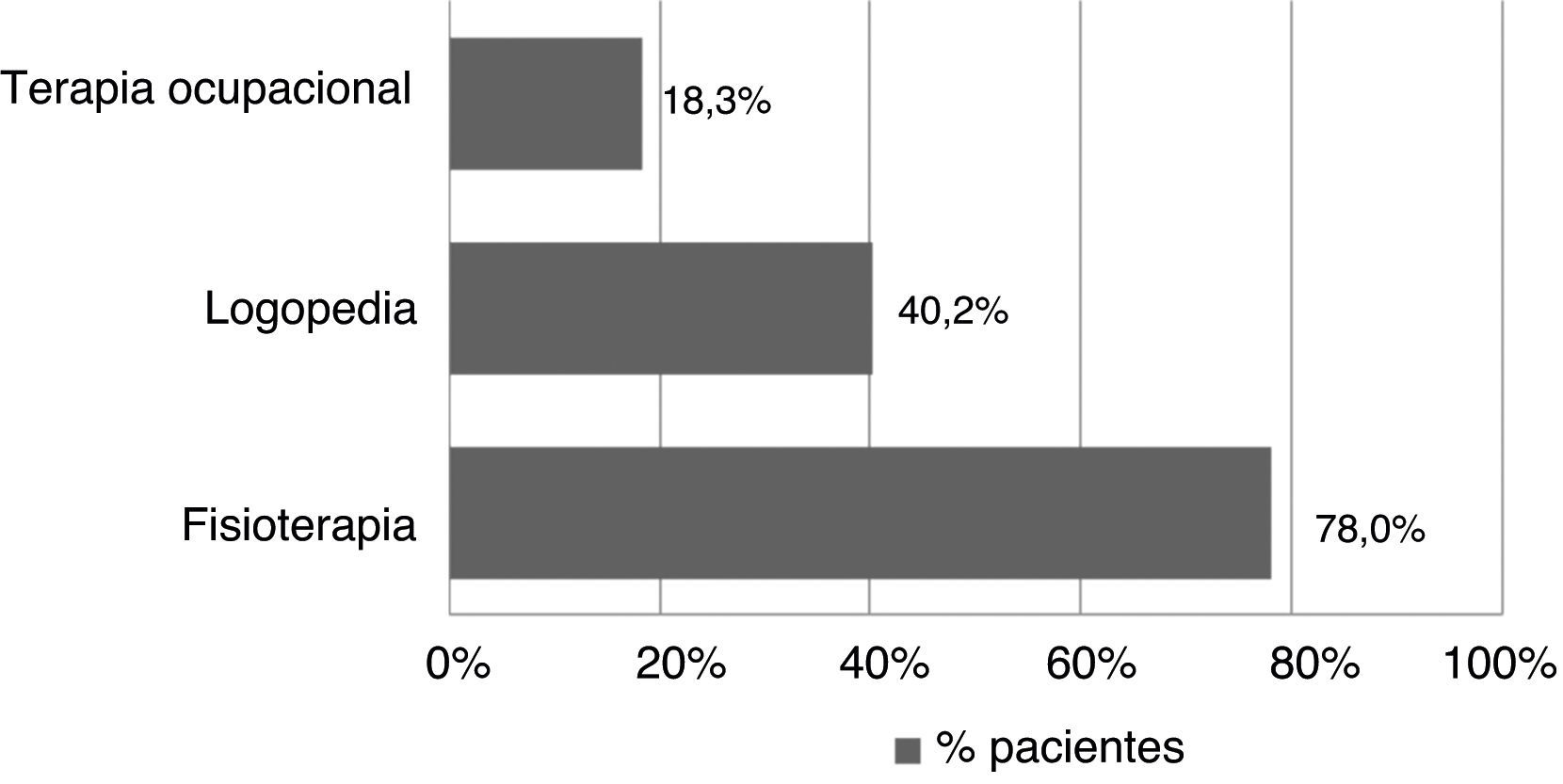
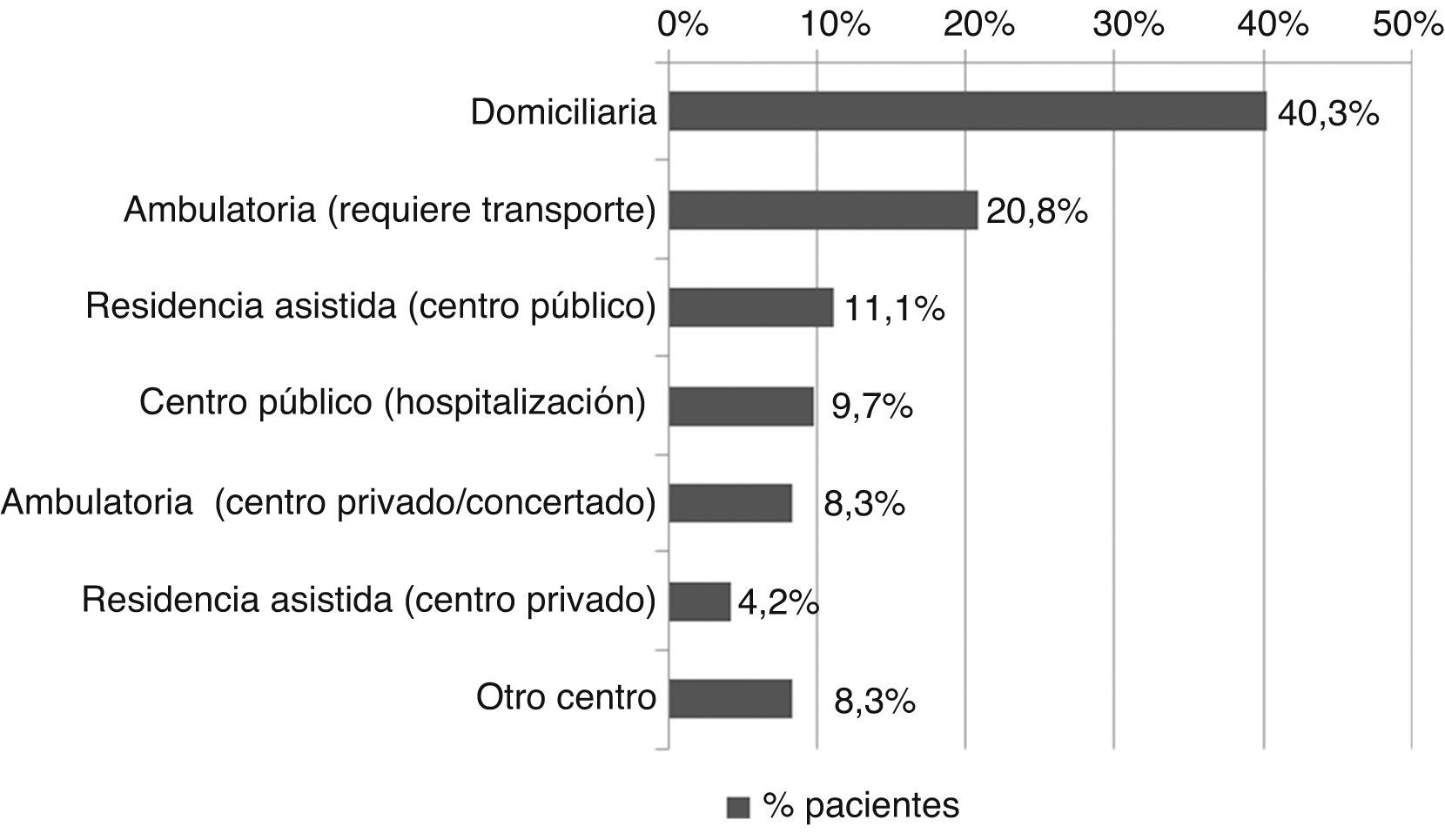
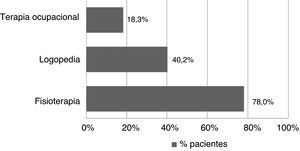
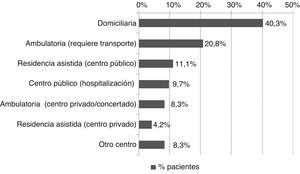
Todos los pacientes recibieron tratamiento farmacológico durante el ingreso y al alta y a todos se les realizó alguna prueba diagnóstica o analítica. Para confirmar el diagnóstico de ICE, todos los pacientes se sometieron a pruebas de imagen cerebral, presentaron estudio carotídeo negativo y presencia de fuente cardioembólica como antecedente o detectada mediante electrocardiograma/ecocardiograma. La prueba diagnóstica más frecuente fue la tomografía computarizada craneal (98,4%), seguida por dúplex TSA (87,5%), electrocardiograma (85,9%) y radiología de tórax (77,3%). Las pruebas analíticas más realizadas fueron el hemograma y la bioquímica sanguínea, llevadas a cabo en todos los pacientes, y el estudio de hemostasia (97,7%). Del total de pacientes, 82 requirieron tratamiento rehabilitador (64,1%), siendo la fisioterapia y la logopedia las terapias más recibidas. Durante el ingreso hospitalario, un 46,9% de los pacientes recibió rehabilitación, mientras que al alta ascendió hasta el 56,3%. La duración total promedio de rehabilitación fue de 31,37 días por paciente (DE 40,01). Según la localización, la mayoría de los pacientes recibió rehabilitación domiciliaria al alta (40,3%), seguida por un 20,8% en el que esta fue ambulatoria (figs. 1 y 2).
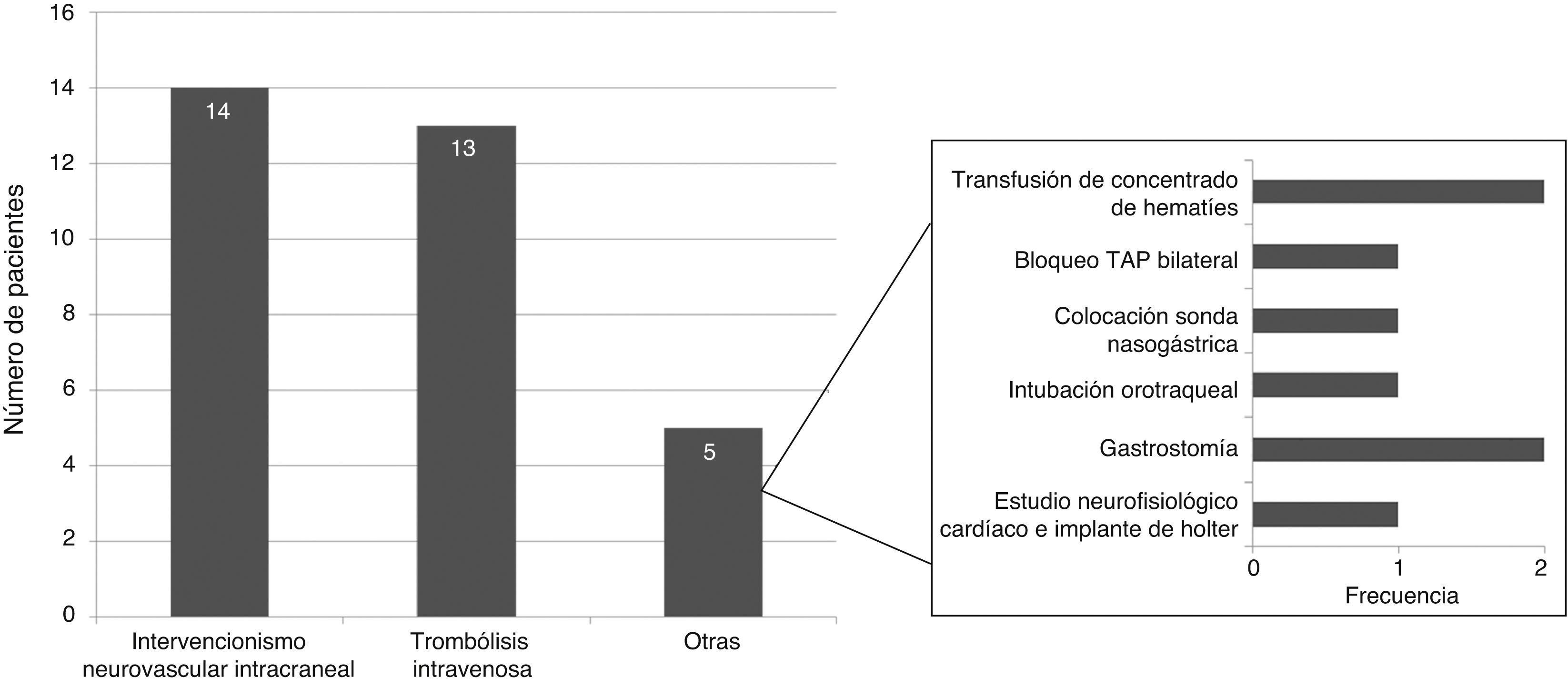
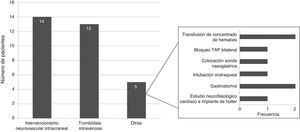
El 19,5% se sometió a intervenciones hospitalarias específicas, siendo las más frecuentes el intervencionismo neurovascular intracraneal (56%) y la trombólisis intravenosa (52%) (fig. 3).
Seguimiento a los 30 días desde el ingresoTras el alta hospitalaria, a 121 (94,5%) de los pacientes se les realizó seguimiento vía telefónica a los 30 días del ingreso. El 6,6% de los pacientes permanecía aún hospitalizado, y el 11,6% se encontraba institucionalizado en centros sociosanitarios. Un 5% de los pacientes precisó reingreso hospitalario, siendo en un tercio de ellos debido a complicaciones del infarto cerebral previo. En este periodo, un 6,6% acudió a Urgencias y un 4,1% presentó complicaciones.
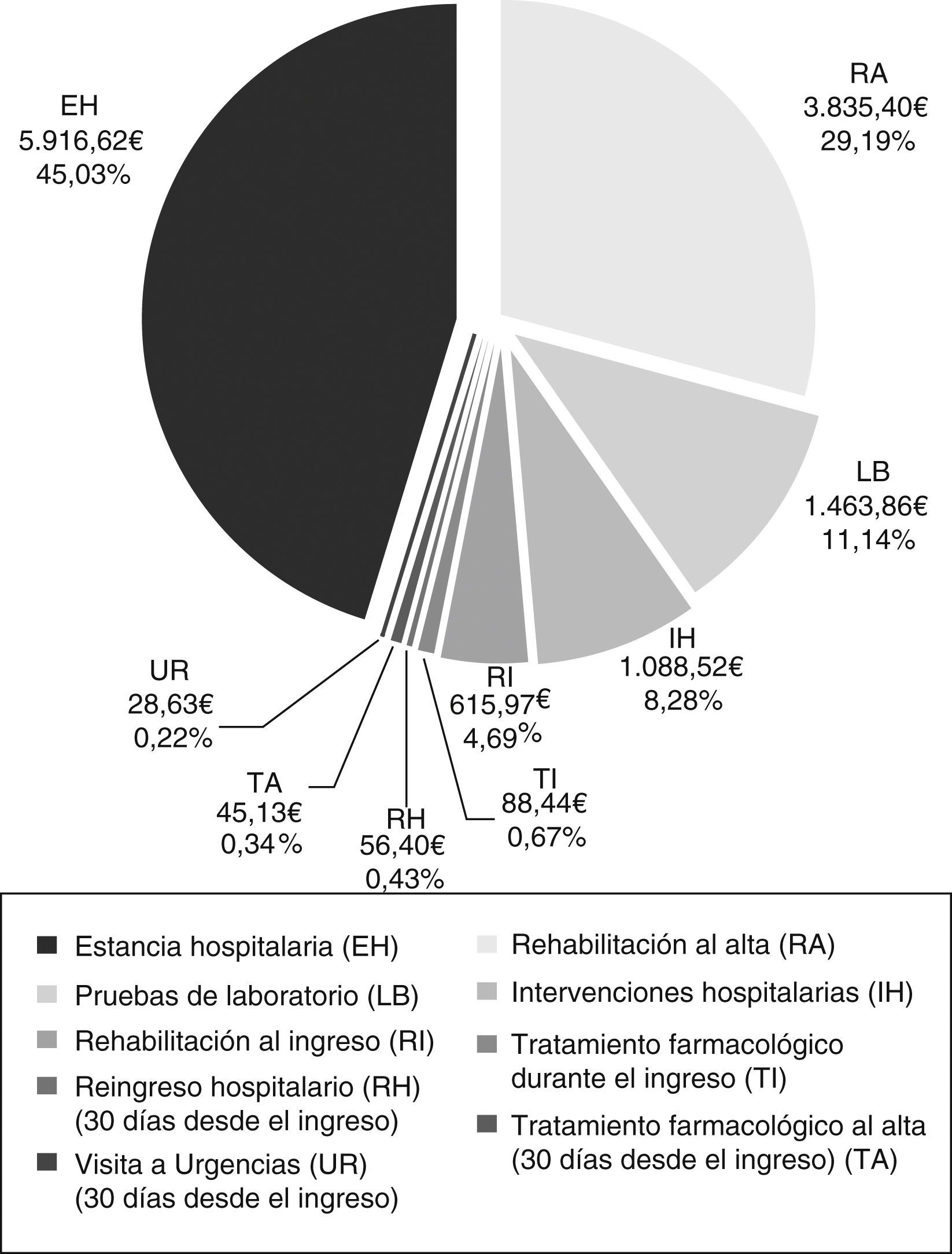
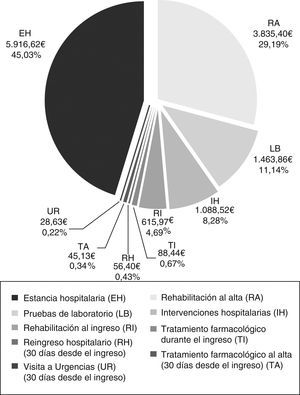
CostesEl coste total medio por paciente del manejo del ICE agudo en la Comunidad de Madrid fue de 13.138,97€. La estancia hospitalaria (5.916,62€) y la rehabilitación al alta (3.835,40€) fueron los recursos que más contribuyeron a este coste total (fig. 4). El coste hospitalario medio por paciente durante el ingreso fue de 9.173,42€.
DiscusiónEl manejo de los pacientes con ICE requiere una mayor inversión en el periodo inicial tras el episodio, siendo de especial relevancia el coste del primer año en comparación con los posteriores13,19. Debido a este hecho, es importante identificar el coste generado en los primeros meses tras el episodio, especialmente en la fase aguda durante la hospitalización y en la recuperación funcional del paciente mediante la rehabilitación, al ser los componentes que más inciden en el coste total. En el coste global del ICE se considerarían, además, otros costes, como los sociales y los derivados de la asistencia sanitaria y la rehabilitación necesarias a más largo plazo, que no se incluyen dentro de los objetivos del presente estudio.
El coste del manejo del ICE agudo en la Comunidad de Madrid alcanzó los 13.139€, donde el 70% de los costes correspondió al manejo de los pacientes durante la estancia hospitalaria. El coste de la estancia hospitalaria, con 5.917€, fue el más importante dentro del consumo de recursos hospitalarios. Además, los pacientes con ICE pueden requerir intervenciones hospitalarias específicas que conllevan un aumento del consumo de recursos durante la hospitalización, realizadas en un 19,5% de los pacientes del estudio, entre ellas, el intervencionismo neurovascular y la trombólisis intravenosa, llevadas a cabo en más de la mitad de los pacientes con intervenciones hospitalarias. Casi un tercio del total de los pacientes (32%) sufrió complicaciones hospitalarias, mayoritariamente infecciosas. La rehabilitación, fundamentalmente al alta (3.835€), fue otra variable importante dentro del manejo de los pacientes con ICE.
Los centros participantes pertenecen al Servicio Madrileño de Salud, que presentó en 2008 un Plan Asistencial que aborda de manera integral la asistencia a los pacientes que padecen un ictus, estableciendo procedimientos de actuación específicos y una adecuada distribución de los recursos20. Los datos obtenidos en el Estudio CODICE aportan información de gran relevancia sobre las características específicas actuales del manejo de estos pacientes y del consumo de recursos generados tras su aplicación en el ámbito de la Comunidad de Madrid.
Diferentes estudios realizados en España presentan datos de costes del manejo de pacientes con ictus13,19,21–27, sin embargo, no se presenta información específica sobre los costes directos del manejo del ICE, por lo que son difícilmente comparables con los recogidos en el Estudio CODICE.
Un estudio de costes socioeconómicos del ictus se desarrolló en España con el objetivo de comparar los costes del ictus en pacientes con y sin FANV26. Las diferencias respecto al presente estudio son la realización del estudio únicamente en servicios de Neurología con Unidad de Ictus y la obtención de los costes desde una perspectiva social. Los datos preliminares presentados mostraron un coste hospitalario del episodio de ictus de 6.428€21. Otro estudio realizado en España estimó la carga económica de los ictus y la calidad de vida de los supervivientes en los 3 primeros años tras sufrir un ictus. Los costes directos sanitarios durante el primer año correspondieron a 5.007€ (año 2004)19. Estos datos hospitalarios, a diferencia de la metodología del Estudio CODICE, fueron obtenidos mediante costes medios de Grupos Relacionados por el Diagnóstico de 18 centros españoles. En otro estudio, el coste medio por Grupo Relacionado por el Diagnóstico (2008) para el ictus con infarto en el Hospital General Universitario de Valencia correspondió a 4.227,15€23. El estudio realizado por Fernández de Bobadilla et al. estimó el coste anual bruto medio por paciente (2006) asociado al ictus en práctica clínica habitual a nivel nacional en 2.590,36€, incluyendo costes directos en atención primaria (1.630,06€)25. Los costes directos sanitarios medios de atención hospitalaria para el primer año tras el ictus fueron de 2.990,70€ en 2004, y para la rehabilitación y transporte, de 80,50€ y 466,10€, respectivamente, obtenidos mediante un estudio retrospectivo a 3 años desde una perspectiva social13. Un estudio de costes realizado en el País Vasco estimó los costes sanitarios medios de transición para el infarto cerebral en 2.587,30€ (año 2002) para la hospitalización en fase aguda, y en 256,80€ los debidos a reingresos posteriores. Los costes debidos a la rehabilitación hospitalaria y ambulatoria fueron 925,40€ y 488,70€, respectivamente22. La diferente metodología utilizada, año de realización y selección de pacientes de estos estudios impide la comparación directa de estos resultados con los obtenidos en el Estudio CODICE.
La calidad de los datos obtenidos depende fundamentalmente del diseño del estudio. Si es observacional de seguimiento prospectivo aporta la evidencia científica óptima para este tipo de datos, ya que la información es más precisa al recogerse simultáneamente durante el manejo del paciente, evitando las pérdidas que podrían acontecer en otros estudios, como los de seguimiento retrospectivo28. Además, al requerir una clasificación previa por la Agencia Española de Medicamentos y Productos Sanitarios y la aprobación por un Comité Ético de Investigación Clínica acreditado, aportan mayor fiabilidad en la calidad del diseño del estudio29. Otra ventaja de los estudios longitudinales prospectivos se debe a que permite la recogida de información en la práctica clínica habitual, por lo que aporta información real del manejo de los pacientes en cada centro, que dependerá de la gravedad del paciente y las necesidades terapéuticas que requiera cada caso.
En cualquier caso, el presente estudio no está exento de limitaciones. El consumo de recursos en los días posteriores al alta hospitalaria se determinó mediante entrevista telefónica al paciente o cuidador, con la probabilidad de omitirse algún recurso, a pesar del corto periodo de tiempo considerado. La duración de la rehabilitación prescrita tras el alta del paciente se calculó mediante el tiempo estimado prescrito por el médico rehabilitador durante el ingreso, y fue confirmado a los 30 días tras la fecha de ingreso mediante control telefónico.
No se dispuso de información sobre la evaluación neurológica mediante la escala NIHSS en todos los centros debido a que en algunos de ellos no determinan esta puntuación al ingreso por no disponer de neurólogo de guardia. Según los datos disponibles, se presume que la gravedad al alta es menor a la reflejada habitualmente, pudiéndose atribuir por el mayor porcentaje de terapias de reperfusión en fase aguda realizadas.
El estudio se limita a 5 centros públicos de la Comunidad de Madrid, pudiendo presentar diferencias respecto a otras comunidades autónomas, dada la disparidad en recursos asistenciales utilizados en el ictus en cada comunidad30.
El presente análisis no considera la comparación de costes entre los servicios de Neurología con o sin Unidad de Ictus, aunque resultará de interés su consideración para el desarrollo de futuros análisis del Estudio CODICE y otras posibles investigaciones.
El importante consumo de recursos generado en el manejo de los pacientes con ICE agudo, con un coste total medio por paciente de 13.139€, derivó, en gran medida, de la asistencia hospitalaria. Esto fue, en parte, debido a la alta especialización requerida y a las técnicas de diagnóstico e intervenciones terapéuticas específicas necesarias. Además del manejo en fase aguda, las secuelas producidas en los pacientes tras el episodio de ICE requirieron tratamientos de rehabilitación que incrementaron también la utilización de los recursos económicos por el Servicio Madrileño de Salud.
FinanciaciónEste estudio ha sido financiado conjuntamente por Pfizer S. L. U. y Bristol-Myers Squibb S. A.
Conflicto de interesesLos investigadores coordinadores (José Vivancos Mora y Antonio Gil Núñez) han recibido honorarios por parte de Pfizer S. L. U., resultantes de la asesoría y coordinación científica del estudio. Los investigadores participantes del estudio han recibido honorarios por parte de Pfizer S. L. U., resultantes de su participación en el estudio. Miguel Ángel Casado Gómez, Covadonga Torres González y Fernando de Andrés Nogales, responsables del seguimiento y análisis del estudio, desarrollan su actividad profesional en PORIB. Marina de Salas Cansado y Javier Soto Álvarez son empleados de Pfizer S. L. U.
Francisco Javier Barriga Hernández, Laura Izquierdo Esteban, Fernando Díaz Otero, José Vivancos Mora, M. Ángeles Ortega Casarrubios, Laura Castillo Moreno, Teresa Montojo Villasanta, Mónica Álvarez Moreno, Pablo Bandres Hernández, Carlos Ignacio Gómez-Escalonilla Escobar, Inmaculada Puertas Muñoz, Alicia Parra Santiago, M. Paz Martín Torres, Álvaro Ximénez-Carrillo, Gemma Reig Roselló.
Datos preliminares de este estudio se presentaron previamente en el 15.o Congreso Anual Europeo de la Sociedad Internacional de Farmacoeconomía e Investigación de Resultados (ISPOR) con el título «Health care resource utilization and costs of cardioembolic stroke in the region of Madrid, Spain: Preliminary results of CODICE study» (Berlín, 3-7 noviembre 2012) y en las XXXIII Jornadas de Economía de la Salud (Santander, 18-21 junio 2013) con el título «Utilización de recursos sanitarios y costes asociados al manejo de los pacientes con infarto cerebral cardioembólico agudo hospitalizados en la Comunidad de Madrid: Estudio CODICE».
Los nombres de los componentes del Grupo de Investigación Estudio CODICE están relacionados en el anexo.