La enfermedad trofoblástica persistente puede ser diagnosticada después de cualquier tipo de gestación, pero su frecuencia aumenta tras el hallazgo de un embarazo molar, con lo que su adecuado diagnóstico y seguimiento es vital para un tratamiento temprano y eficaz.
Presentamos un caso de un aborto diferido, en el que se diagnosticó mola completa y tras la confirmación de persistencia de esta, precisó de tratamiento poliquimioterápico para lograr su curación.
Persistent trophoblastic disease can be diagnosed after any type of pregnancy, but the frequency of this entity increases after molar pregnancies and consequently early diagnosis and follow-up is vital for prompt and effective treatment. We present a case of missed abortion, with diagnosis of a complete hydatiform mole. Persistent trophoblastic disease was subsequently diagnosed, requiring treatment with multiple drug therapy to achieve complete resolution.
La incidencia del aborto diferido es muy alta en nuestro medio (hasta el 30% de todas gestaciones clínicas) gracias al diagnóstico cada vez más temprano del embarazo, tanto con los test de orina, con detección de niveles muy bajos de β-hCG, como por el diagnóstico por imagen, al que las pacientes acuden con rapidez en cuanto tienen noticia de su estado gestacional. Es gracias al análisis anatomopatológico de los restos coriales de estos abortos que en la actualidad se diagnostican la mayoría de las gestaciones molares que surgen, ya que la clínica tan sugestiva de esta enfermedad que principalmente aparece a lo largo del segundo y el tercer trimestres, en contadas ocasiones se llega a producir, y se queda en una metrorragia, ausencia de embrión o de latido cardiaco.
Presentamos un caso en que esto fue así y nos llevó a una enfermedad trofoblástica persistente de difícil y complicado abordaje.
Caso clínicoMujer de 30 años, que acude a consulta en la novena semana de su tercera gestación, para iniciar el seguimiento de esta. Como antecedentes personales y familiares de interés presenta una poliquistosis renal familiar, con dos trasplantados renales cercanos, ella sin tratamiento en la actualidad y con función renal dentro de la normalidad; amigdalectomizada y con intolerancia al ácido acetilsalicílico. Grupo sanguíneo A+. Dentro de su historia ginecoobstétrica contaba con una citología normal hacía 2 años, ciclos regulares, un parto eutócico hacía 2 años y una interrupción legal de su segundo embarazo tras haber recibido una dosis de vacuna triple vírica, desconociendo su estado gestacional.
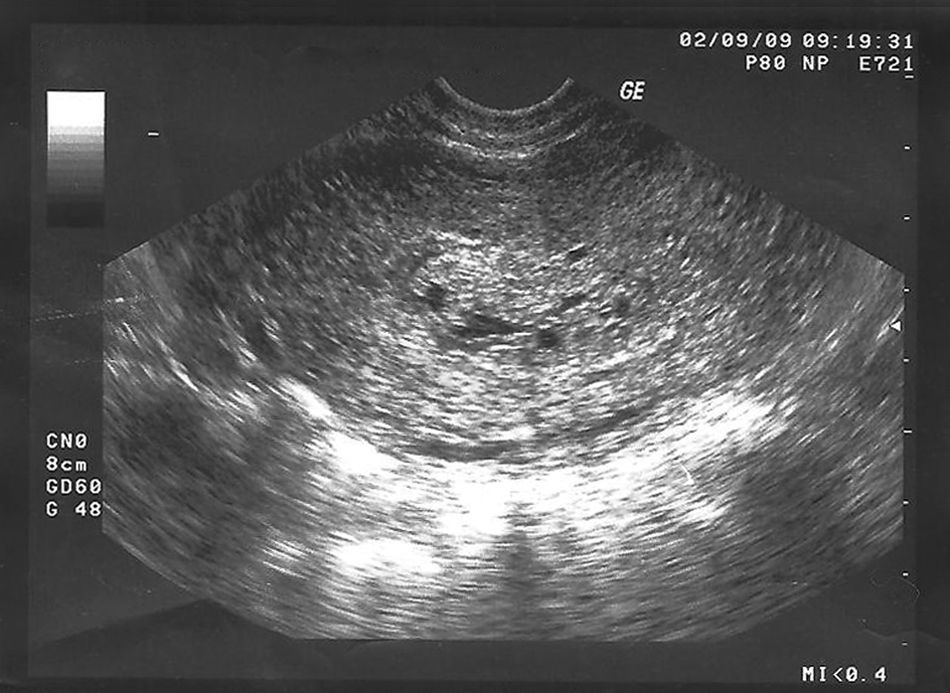
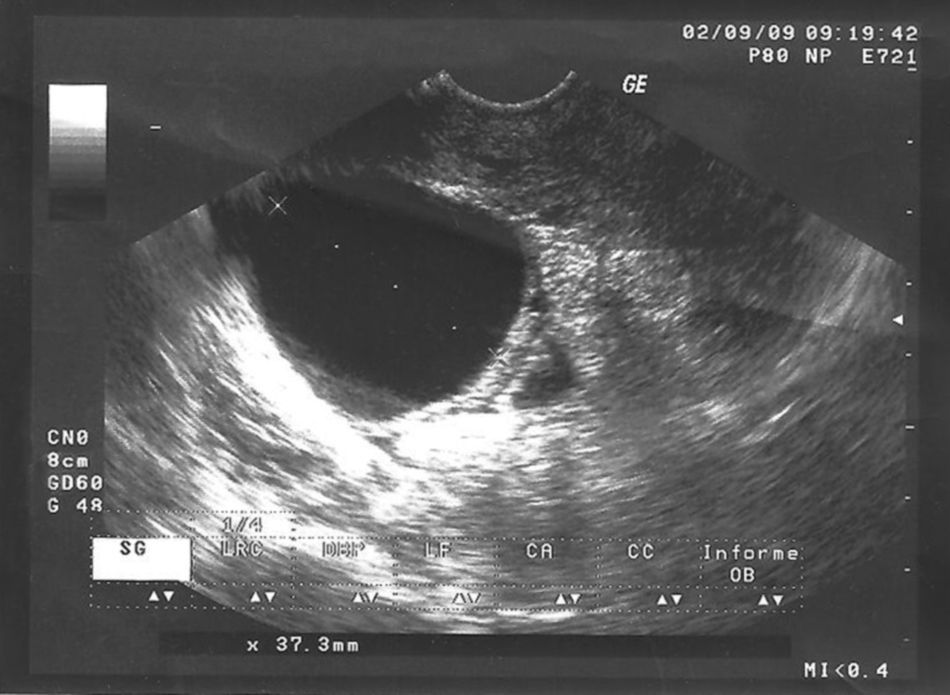
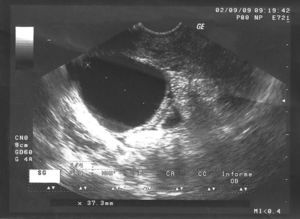
Con el diagnóstico de aborto diferido tras la realización de una ecografía (figs. 1 y 2), se ingresa en nuestro servicio para la realización de un legrado evacuador. Después de la preparación del cuello con prostaglandinas, se lleva a cabo este sin incidencias.
Cuatro semanas después se cita de nuevo a la paciente para la revisión habitual tras legrado, encontrándose entonces el resultado de la anatomía patológica de mola hidatidiforme completa. Se le realiza a la paciente una radiografía de tórax, que es informada como normal, y un control de β-hCG, que resulta un valor de 134 mU/ml. Se cita a la semana para nuevo análisis, cuando la β-hCG se encuentra inferior a 2 mU/ml. En los siguientes 7 días la hormona sube a 316 mU/ml, persistiendo elevada en los controles semanales posteriores (190-181-242), por lo que se inicia estudio complementario al considerarse ya una enfermedad trofoblástica persistente (ETGP)1. Clínicamente, la paciente refiere manchado escaso intermitente desde el legrado, y una menstruación abundante al mes del mismo, que persiste al iniciar el estudio. En la exploración presenta un útero en anteversión, móvil, blando, discretamente doloroso, vagina sin alteraciones. Se realiza una ecografía que es informada como normal con endometrio lineal. Se solicita una histeroscopia por la metrorragia escasa persistente, donde se visualiza una pared anterior uterina de aspecto polipoideo, con biopsia que se informa como mucosa endometrial escasa, de tipo proliferativo, sin elementos coriales presentes. La TC abdomino-pélvica informa de una imagen subpleural en lóbulo inferior izquierdo que podría ser un granuloma, sin descartarse metástasis; riñones poliquísticos, y en la pelvis un aumento de densidad en área de parametrios y en torno a la vagina, que interpretan como inflamación versus infiltración; sin adenopatías. Pasa entonces al servicio de oncología de nuestro hospital, para tratamiento y control de la enfermedad neoplásica.
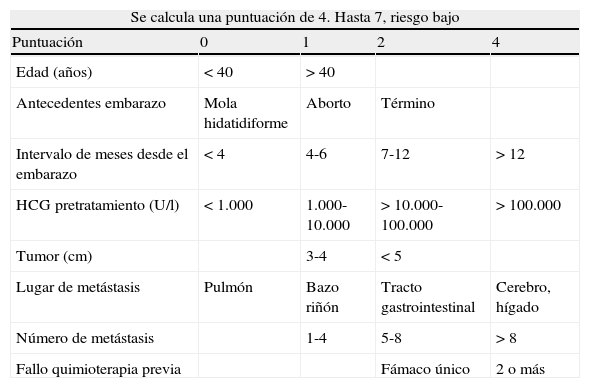
Es etiquetada como ETGP en estadio II vs III y con un índice pronóstico según la puntuación de la FIGO de 4 (tabla 1), de riesgo bajo, por lo que se opta por el esquema de 8 días con metotrexato 1mg/kg por vía intramuscular más ácido fólico2. Comienza el tratamiento al mes y medio de la realización del legrado, con un nivel de β-hCG de 153 mU/ml, finalizando este primer ciclo con buena tolerancia al este y 58,79 mU/ml, manteniéndose estos niveles en las 2 semanas posteriores de control (36,5-41,6), por lo que se indica un segundo ciclo de tratamiento al mes del primero. Tras este, los niveles de hormona no se negativizan (35,2-18,11-46), por lo que recibe un tercer ciclo, manteniéndose positiva la β-hCG en 52,5 mU/ml al finalizar este. Se solicita una TC de control, donde se detecta una disminución de tamaño del nódulo pulmonar. Ante la falta de respuesta completa al tratamiento de primera línea, se propone tratamiento poliquimioterápico de segunda línea3 con el esquema EMA-CO: día 1.° con etopósido-actinomicina D-metotrexato; 2.° día con etopósido-actinomicina D-leucovorín, y el 8.° día con vincristina-ciclosporina. Se inicia el tratamiento con una β-hCG de 35,44 mU/ml, finalizándolo con 8,2 mU/ml; al comienzo del segundo ciclo los niveles ya se han negativizado (2,87), por lo que este ciclo se da como consolidación y un tercero con el que la β-hCG se encuentra en 0,86 mU/ml y se da por finalizado el tratamiento quimioterápico. Los siguientes controles semanales, y posteriormente mensuales, continúan en valores negativos de hormona. En la TC de control persiste la imagen inespecífica de nódulo subpleural, por lo que se propone vigilarlo y, si no se modifica, considerar la exéresis. A los 4 meses desaparece esta imagen de la TC y los controles persisten negativos en el momento de la realización de este artículo, 6 meses después de su negativización.
Puntuación pronóstica FIGO 2000
| Se calcula una puntuación de 4. Hasta 7, riesgo bajo | ||||
| Puntuación | 0 | 1 | 2 | 4 |
| Edad (años) | < 40 | > 40 | ||
| Antecedentes embarazo | Mola hidatidiforme | Aborto | Término | |
| Intervalo de meses desde el embarazo | < 4 | 4-6 | 7-12 | > 12 |
| HCG pretratamiento (U/l) | < 1.000 | 1.000-10.000 | > 10.000-100.000 | > 100.000 |
| Tumor (cm) | 3-4 | < 5 | ||
| Lugar de metástasis | Pulmón | Bazo riñón | Tracto gastrointestinal | Cerebro, hígado |
| Número de metástasis | 1-4 | 5-8 | > 8 | |
| Fallo quimioterapia previa | Fámaco único | 2 o más | ||
La incidencia del embarazo molar en Norteamérica y Europa es de 1 de cada 1.000-2.000 embarazos, mucho menor que en Asia, donde es de 1 cada 250, a pesar del descenso de incidencia observado en la última década en esta zona, posiblemente debido a la mejora de las condiciones socioeconómicas y cambios en la dieta4. La incidencia de la enfermedad trofoblástica persistente es menos conocida, ya que esta puede aparecer después de cualquier tipo de embarazo.
La causa de esta alteración es genética, en la mola completa con contribución exclusiva paterna, al estar el óvulo sin cromosomas fecundado por un espermatozoide que se duplica, o bien por dos espermatozoides, y en la parcial con carga triploide, por un óvulo fecundado por dos espermatozoides5.
El diagnóstico morfológico en gestaciones tempranas puede ser dificultoso en ocasiones, necesitando técnicas auxiliares que no siempre se emplean, con lo que la medición de la β-hCG es la clave para el diagnóstico en todos los casos. El diagnóstico ecográfico durante el primer trimestre no siempre es posible (40-60% de los casos), por lo que se etiquetan como gestaciones no evolutivas y es el estudio histológico de los restos evacuados el que da el diagnóstico de embarazo molar, como ocurrió en el caso que nos ocupa.
Otro problema para su diagnóstico lo encontramos en los abortos completos espontáneos o en aquellos que han tenido tratamiento médico, donde el retraso en el diagnóstico nos lleva a un incremento de la morbilidad, por lo que la recomendación es un control de las concentraciones de β-hCG a las 3-4 o semanas postratamiento para asegurar su retorno al rango normal4.
El tratamiento de elección es el legrado por aspiración, sin empleo de prostaglandinas para la preparación del cuello porque favorecen la embolización de material trofoblástico. En nuestra paciente, sí se utilizó previo a la realización del legrado instrumental, ante la falta de sospecha de la mola, lo cual pudo facilitar su trasformación a enfermedad trofoblástica persistente.
La ETGP se diagnostica1 cuando en el seguimiento que se debe hacer a toda gestación molar aparecen unos niveles de β-hCG con una subida mayor del 10% en tres valores durante 2 semanas, unos niveles en meseta +/–10% durante 3 semanas, con la detección de esta 6 meses después de la evacuación uterina y con el diagnóstico anatomopatológico de coriocarcinoma. Los niveles mantenidos en meseta nos llevaron al diagnóstico en nuestro caso, precisando entonces tratamiento quimioterápico. Las metástasis más frecuentes son las pulmonares, por lo que la radiografía de tórax es obligada, pero cerca del 95% de las pacientes están en el estadio I de la FIGO6,7, y con un riesgo bajo según la clasificación pronóstica, en que el tratamiento de primera elección es el pautado en el caso que nos ocupa, aunque se clasificó en el estadio II (invasión fuera del útero) vs III (pulmonar), se trató con metotrexato, que alcanza una efectividad de hasta del 90% de los casos2,8.
Se precisan niveles de β-hCG < 5 para considerar la curación del proceso; aunque tenía niveles bajos de β-hCG, nuestra paciente precisó de tratamiento de segunda línea, y no se optó por cambiar de fármaco, medida indicada en distintos protocolos9, sino por usar el régimen poliquimioterápico más ampliamente utilizado a nivel mundial por su efectividad y fácil control de los efectos secundarios: EMA-CO3. La supervivencia a los 5 años de las pacientes que recibieron este tratamiento está entre el 75 y el 90%, pero en la mayoría de estos casos había enfermedad metastásica en el hígado o el cerebro, siendo por tanto casos de riesgo alto, que no coinciden con el nuestro, donde la sospecha de metástasis era vaginal o pulmonar.
Tras la negativización de la hormona es preciso un seguimiento de esta durante un año, evitando en cualquier caso una nueva gestación, que no nos permitiera reconocer una recidiva.
En definitiva, este caso debe hacernos recordar la necesidad de un diagnóstico ante las gestaciones no evolutivas de embarazo molar, seguimiento adecuado de este y el tratamiento oportuno.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.