ANTECEDENTES
La preeclampsia-eclampsia fue descrita hace más de 100 años y a pesar del interés mundial por esta entidad aún no tenemos conocimiento de su etiología y fisiopatología. La preeclampsia/eclampsia es un término utilizado para describir una enfermedad de la mujer embarazada que se caracteriza por el desarrollo secuencial de: a) acumulación de líquido en el tejido intersticial; b) hipertensión arterial, y c) excreción de grandes cantidades de proteína por la orina; se presenta después de la semana 24 de gestación o en el puerperio. La preeclampsia-eclampsia (o enfermedad hipertensiva aguda del embarazo), junto con la hemorragia y los procesos infecciosos, son la causa más común de muerte materna en el embarazo tardío, particularmente en países en vías de desarrollo(1,2). La prevalencia de esta patología a nivel mundial se estima en un 5 a 7% de todos los embarazos: en nuestro país se calculó entre un 8 a 10% en un estudio retrospectivo de 1.800 pacientes efectuado en la Ciudad de México por Díaz de León et al(3,4).
En 1889, Lazard describe el primer caso de hemorragia cerebral diagnosticado por autopsia en un puerperio postparto distócico, y desde entonces se reconocen las graves complicaciones vasculares neurológicas que durante el embarazo se pueden presentar distinguiendo claramente dos eventos causales: los oclusivos y los hemorrágicos (trombosis, embolismo, vasculitis, ruptura de aneurismas o malformaciones arteriovenosas, respectivamente) o los casos de hemorragia secundarios a la hipertensión del embarazo con la característica de que ésta es de tipo parenquimatoso, sobre todo hacia núcleos basales y tallo cerebral a diferencia de la hemorragia subaracnoidea observada en los eventos vasculares. Desde el punto de vista clínico a estas pacientes se les ha documentado a través de estudios angiográficos, angiorresonancia magnética o tomografía computarizada de casos reportados en puerperio con preeclampsia-eclampsia: encefalopatía hipertensiva, microhemorragias, isquemia, vasoespasmo y edema cerebral de magnitud variable, dependiendo de la serie analizada, con la limitante que impone la misma gestación por ser estudios invasivos potencialmente nocivos para el feto(5-8).
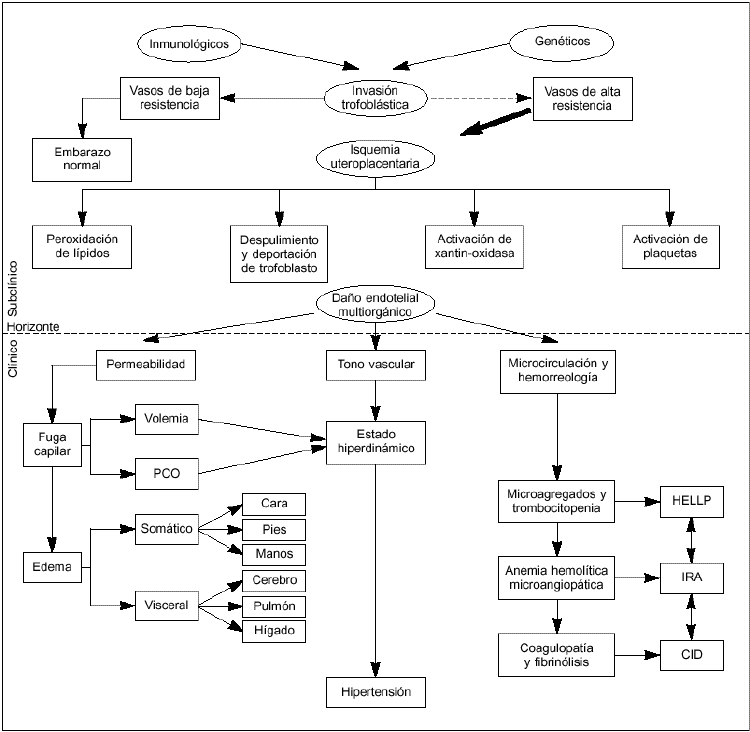
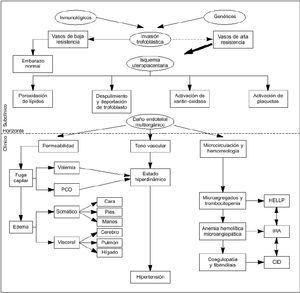
La patogénesis de las manifestaciones neurológicas de la paciente con preeclampsia-eclampsia no se conoce; sin embargo, se admite la similitud de las manifestaciones clínicas entre el vasoespasmo y la encefalopatía hipertensiva. El mecanismo de autorregulación cerebral y su participación en esta patología, hasta hoy no conocida, reconociendo que las cefaleas y las convulsiones pueden presentarse en el puerperio. Se han implicado alteraciones endoteliales como la disminución en la síntesis de prostaciclina (PgI2), lo que favorece la agregación plaquetaria contribuyendo a fenómenos de isquemia cerebral transitoria o bien a que las mismas alteraciones panendoteliales favorecen la fuga de líquido y el edema cerebral(9-13) (Fig. 1).
Figura 1. Fisiopatología de la toxemia (Briones y Díaz de León).
ANATOMÍA Y FISIOLOGÍA
El cerebro se irriga por un sistema arterial anastomótico formado por las carótidas y las vertebrales (círculo arterial o polígono de Willis). La finalidad del circuito arterial cerebral es asegurar una circulación anastomótica; se ha demostrado que la arteria carótida interna y la arteria basilar se distribuyen por los hemisferio cerebrales de tal forma que normalmente no existe mezcla de sangre entre ellas; las corrientes opuestas derivadas de las dos arterias se encuentran en la arteria comunicante posterior en un punto muerto, en la cual la presión de ambas arterias es idéntica; de modo similar los territorios de las arterias carótidas encuentran un punto muerto en la mitad de la arteria comunicante anterior; sin embargo, si ambas arterias carótidas internas o ambas vertebrales están ocluidas, la sangre se dirige hacia adelante o hacia atrás, respectivamente, del par que todavía permanece libre, entrando en función una anastomosis anteroposterior a través de cada arteria comunicante posterior; esta arteria también llega desde la arteria carótida interna opuesta a través de la arteria comunicante anterior, lo cual ha quedado confirmado durante el curso de una angiografía si se inyecta el medio opaco en una carótida, mientras la opuesta se comprime; éste normalmente cruza la línea media a través de la arteria comunicante anterior, pero cuando se permite circular libremente a la sangre ésta vuelve a sus causas normales y sólo en una proporción reducida, sobre todo en personas jóvenes, se aprecia llenado de los dos lados. Además existe en el cerebro otra circulación no anastomótica, situada más distalmente a nivel de los campos de irrigación de la corteza cerebral, constituida principalmente por las tres arterias cerebrales de más volumen que son extracerebrales y se convierten en intracerebrales cuando penetran en la sustancia cerebral, pero una vez en ella cada una de las arterias conserva su individualidad(14,15).
El cerebro posee un mecanismo de autorregulación, su flujo sanguíneo se mantiene constante, así como la concentración de oxígeno, en contraste con las variaciones de la presión sistémica arterial a través de dos factores: el primero se basa en la dilatación y contracción de las paredes arteriolares ante los cambios de la presión intravascular (dentro de ciertos límites), de tal manera que se contrae al elevarse y se dilata al disminuir ésta.
El segundo factor es bioquímico; depende principalmente del nivel sanguíneo del bióxido de carbono y de oxígeno. Al incrementarse el primero o al disminuir el segundo, los capilares y arteriolas se dilatan y se vasoconstriñen cuando sucede lo contrario. La concentración de ácido láctico resultante de la glucólisis anaerobia es la responsable de la dilatación. Actualmente es posible medir en los pacientes el flujo sanguíneo cerebral mediante inyección intracarotídea de kriptón o xenón radioactivo; su valor fisiológico es de 50 a 60 ml por 100 gramos de tejido cerebral por minuto, siendo constante esta cantidad gracias al fenómeno de autorregulación, salvo que la tensión arterial descienda a menos de 50 mmHg; la autorregulación también resuelve la isquémia cerebral local por la dilatación de los vasos sanguíneos vecinos al área isquémica o infartada, así como a través de la circulación colateral dirigida a la referida zona patológica cerebral.
VASOESPASMO CEREBRAL
Éste continúa siendo la complicación más temida de la hemorragia secundaria a la ruptura de un aneurisma cerebral y puede ser causa de secuelas importantes y de mortalidad; se considera un fenómeno común que ocurre aproximadamente en el 50% de los pacientes durante el curso clínico posterior al sangrado; se han postulado varios mediadores químicos bajo consideraciones hipotéticas para explicar este evento, por ejemplo: 5-hidroxitriptamina, catecolaminas, prostaglandinas, incremento en los endo e hidroxiperóxidos en ácidos poliinsaturados, etc., es un factor invariablemente asociado a la hemorragia que se desarrolla cuando la sangre se pone en contacto con la pared externa de los vasos sanguíneos cerebrales y que conduce a la contracción segmentaria y sostenida de ciertos territorios vasculares cerebrales, pero que en la mayor parte de las veces se encuentran adyacentes al evento hemorrágico; en la preeclampsia-eclampsia sólo se ha documentado mediante angiografía durante el puerperio inmediato(16-20).
DOPPLER TRASCRANEAL
El efecto Doppler fue descrito por el matemático Chistian Andreas Doppler en 1842, quien postuló la relación entre frecuencia óptica y acústica dependiente del movimiento entre emisor y receptor. El ultrasonido emite ondas sonoras con frecuencias superiores a las del rango audible para el oído humano que es de 20 MHz (en espectro de frecuencia con el que operan los equipos de ultrasonido y Doppler es de 1 a 10 MHz); si se disminuye la frecuencia del transductor aumenta la longitud de onda y el haz ultrasónico disminuye la resolución tanto lateral como axial. En 1982, Aaslid publica un método no invasivo de Doppler transcraneal que permite conocer las velocidades de flujo sanguíneo cerebral; posteriormente en 1984 aparece otro estudio donde utiliza Doppler transcraneal para el diagnóstico de vasoespasmo secundario a hemorragia subaracnoidea. Estudios comparativos entre arteriografía y Doppler han demostrado una relación inversa entre el diámetro de los vasos cerebrales y la velocidad de flujo sanguíneo apoyando con esto la utilidad de la técnica Doppler para el diagnóstico de vasoespasmo(21-23).
El Doppler transcraneal es una técnica capaz de registrar las velocidades de flujo sanguíneo cerebral en las arterias intracraneales y por tanto permite comprender los cambios en la circulación cerebral bajo condiciones normales y patológicas; es un estudio no invasivo de ultrasonografía que permite evaluar la circulación cerebral, determinando diversos parámetros de flujo sanguíneo en las principales arterias cerebrales. El Doppler transcraneal utiliza un sistema Doppler pulsado que emite ondas de muy baja frecuencia (1-2 MHz), logrando penetración a través de estructuras óseas craneales seleccionadas denominadas «ventanas ultrasónicas»; la interpretación de los resultados requiere integración entre las mediciones Doppler con el estado clínico del paciente; debido a su carácter no invasivo se puede hacer seguimiento las veces que se quiera; se estima que aproximadamente en un 15% de los casos, por razones técnicas o por variaciones anatómicas en la circulación, no se logra hacer el registro a través de la ventana temporal. A diferencia de los estudios angiográficos que básicamente proporcionan información sobre configuración anatómica, el Doppler transcraneal brinda información sobre aspectos fisiológicos de la circulación cerebral; en la literatura médica encontramos reportes de pacientes con preeclampsia-eclampsia con vasoespasmo documentado mediante Doppler transcraneal con casuísticas pobres que no permiten conclusiones clínicas valederas(24,25).
El diagnóstico de vasoespasmo cerebral mediante Doppler transcraneal se debe practicar desde el momento en que se sospecha el evento hemorrágico para contar con un registro basal y se repite con la finalidad de detectar el incremento en la velocidad de flujo sanguíneo cerebral indicativo del vasoespasmo. El Doppler transcraneal es sobre todo eficaz para detectar vasoespasmo en la arteria cerebral media (se considera que existe vasoespasmo cuando se detectan velocidades medias superiores a 120 cm/segundo). Por su situación y variaciones anatómicas es menos probable detectar vasoespasmo en la arteria comunicante anterior y la arteria comunicante posterior, así como en las ramas distales.
Se ha encontrado una correlación entre la magnitud del incremento en las velocidades de flujo y el desarrollo de vasoespasmo sintomático, y por lo general el aumento en las velocidades precede a las manifestaciones clínicas de isquemia o vasoespasmo; se considera la posibilidad de isquemia cerebral cuando las velocidades exceden de 200 cm/segundo; en estudios comparativos con angiografía cerebral, la especificidad del Doppler transcraneal para detectar vasoespasmo es del 98 al 100%, mientras que su sensibilidad es del 65 al 70%. Cabe mencionar que cuando estudiamos dinámica de flujo vascular se mencionan dos metodos: uno basado en el ángulo de incidencia. En algunas situaciones clínicas los datos de desplazamiento Doppler no son transformados en velocidades de flujo real, ello ha hecho que se definan índices Doppler que denotan las mediciones de segmentos en las ondas de velocidad de flujo Doppler, que son proporciones basadas en cifras promedio; uno de estos índices es el de pulsatilidad (IP) y se obtiene como cociente entre las cifras sistólica menos la diastólica y entre la media(26-30).
METODOLOGÍA
Es una encuesta comparativa.
Se seleccionaron pacientes con embarazo igual o mayor a 24 semanas de gestación a las que se les practicará medición de la velocidad de flujo sanguíneo cerebral mediante Doppler pulsado.
Las mediciones de la velocidad de flujo sanguíneo cerebral se hicieron directamente por el investigador principal utilizando un equipo: Tran Doppler pulsado 2 MHz (Trans-Scan EME 3-D Transcranial Doppler Scanner), registrando las velocidades promedio de flujo y el índice de pulsatilidad en los principales vasos cerebrales (arteria cerebral media, sifón carotídeo, arteria vertebral derechas e izquierdas, respectivamente; así como el tronco de la arteria basilar) a través de las ventanas ultrasónicas convencionales (temporal, orbitaria y occipital), asimismo se hicieron los registros de la velocidad de flujo sanguíneo y del índice de pulsatilidad.
El método de muestreo fue aleatorio simple.
El tamaño de la muestra se calculó mediante diferencia de medias (considerando un estudio piloto de 92 pacientes(32).
Dividimos a las pacientes en dos grupos de trabajo de la siguiente forma:
-- Grupo A (grupo comparativo): 76 pacientes con embarazo igual o mayor a 24 semanas de gestación sin patología previa o concomitante al embarazo.
-- Grupo B (grupo en estudio): 40 pacientes con embarazo igual o mayor a 24 semanas de gestación con diagnóstico de preeclampsia- eclampsia.
Análisis estadístico
Se calculó sesgo y kurtosis que permitió seleccionar la estadística utilizada (mediante el paquete estadístico SPSS versión 97) la prueba de ajuste de bondad de Kolmogorov-Smirnov y la prueba no paramétrica de Mann-Whitney.
RESULTADOS
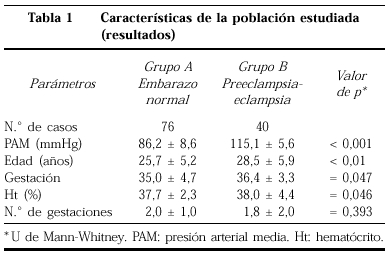
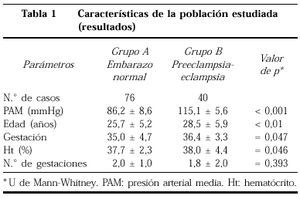
En la tabla 1 expresamos las características generales de nuestra población estudiada; mostramos diferencias mínimas en las variables de presión arterial media (PAM), semanas de gestación y valor del hematócrito; la edad de las pacientes en cambio sí muestra diferencia importante, siendo esto dado porque en el grupo de preeclampsia-eclampsia son de mayor edad que el grupo control, aparentemente sin una explicación clínica específica y como cabría esperar con un valor de p dependiente del tamaño de la muestra.
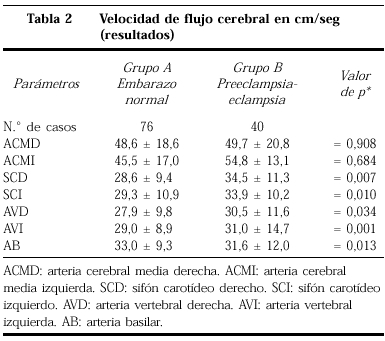
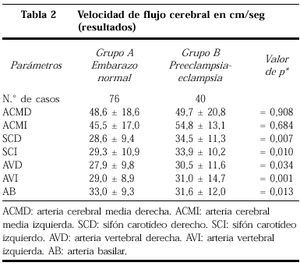
En la tabla 2 mostramos la velocidad de flujo sanguíneo cerebral, con diferencias en el sifón de ambas carótidas internas y la vertebral izquierda de acuerdo a los valores de p.
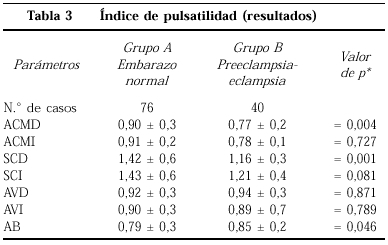
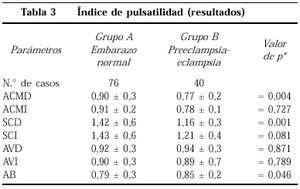
La tabla 3 muestra los valores en el índice de pulsatilidad que coinciden las diferencias en ambos sifones carotídeos, mostrados en el cuadro previo. También encontramos diferencias en la arteria cerebral media derecha.
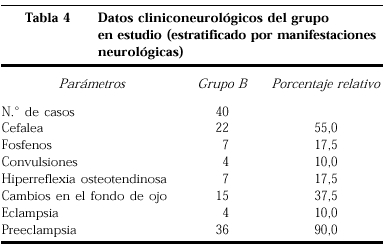
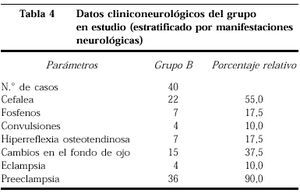
En la tabla 4 estratificamos el grupo B en función de las principales manifestaciones clínicas neurológicas; incluimos número de pacientes y su porcentaje relativo, destacando la cefalea como la principal manifestación (55%), seguida de los cambios en el fondo de ojo (37%), y en tercer lugar los fosfenos y la hiperreflexia osteotendinosa (17,5%). En nuestra población estudiada, el 90% representado con pacientes con preeclampsia y el 10% con eclampsia.
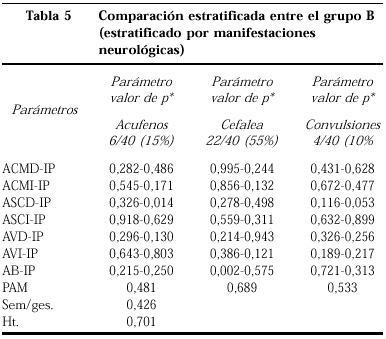
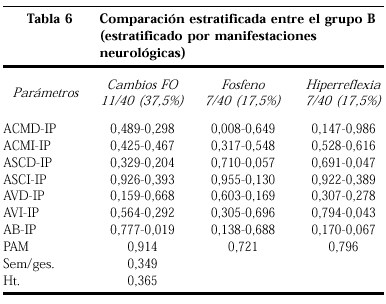
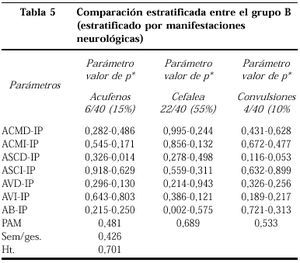
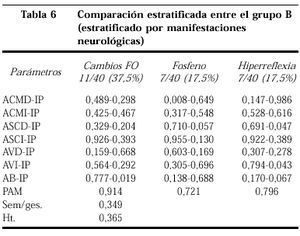
En las tablas 5 y 6 mostramos los valores de p al comparar entre sí las pacientes con y sin sintomatología neurológica y que muestra diferencias mínimas.
CONCLUSIONES
-- Los resultados encontrados en las 76 pacientes estudiadas con embarazo normal permiten decir que tanto la velocidad de flujo sanguíneo cerebral como el índice de pulsatilidad se modifican durante el embarazo con respecto a los valores reportados en pacientes sin embarazo.
-- Podemos concluir con 40 pacientes estudiadas con preeclampsia-eclampsia que en nuestra población existen modificaciones en la velocidad de flujo sanguíneo cerebral y en el índice de pulsatilidad por efecto de esta patología.
-- Tiene el presente estudio la limitante de tratarse de un diseño transversal y por tanto no tener un seguimiento de la evolución de estas pacientes.
-- Se describe la velocidad de flujo sanguíneo cerebral en troncos arteriales principales y no en arterias terminales.
-- Comparando entre sí el grupo de estudio (estratificado por sintoma neurológico) no mostró diferencias con significancia estadística.
-- Podemos inferir que el vasoespasmo es un evento secundario al daño vascular y a los cambios microcirculatorios y hemorreológicos y no la causa como se ha postulado hasta ahora.
DISCUSIÓN
En nuestro país la mortalidad materna es muy alta (se estima entre 29 a 90 * 100.000) comparada con la mortalidad reportada en países desarrollados, que es de 9 a 30 * 100.000 nacidos vivos(43,44,50,51). La preeclampsia-eclampsia representa alrededor del 36% de las defunciones, de las cuales la hemorragia cerebral, la anemia hemolítica microangiopática y la coagulación intravascular diseminada son los principales caminos fisiopatológicos que conducen a estas mujeres hacia su muerte(4,9,45,50,51). Conocemos algunos aspectos de esta fisiopatología, como el tipo de hemorragia que es predominantemente parenquimatoso, localizada comúnmente en núcleos basales y tallo cerebral, zonas descritas como de «vulnerabilidad vascular selectiva»; probablemente el mecanismo de la hemorragia en estas arteriolas terminales está relacionado con el daño microangiopático, en el cual el daño endotelial permite el contacto directo de la sangre con el subendotelio, lo que inicia activación de plaquetas formándose microtrombos que obstruyen parcialmente el lumen vascular e incrementando la presión hidrostática que finaliza con la ruptura microvascular, el contacto directo de la sangre genera vasoespasmo y coagulación intravascular diseminada(31,35,46); otro mecanismo involucrado es el edema cerebral, inicialmente del tipo vasogénico y posteriormente citotóxico de magnitud variable, ambas entidades bien documentadas mediante tomografía axial computarizada y resonancia magnética nuclear(36,48); cabe mencionar que la eclampsia (la forma más grave de este padecimiento) se puede presentar prácticamente con la misma prevalencia en casos de hemorragia cerebral, como en los casos sin hemorragia cerebral, como lo muestra un estudio multicéntrico realizado en Francia(37), lo que apoya precisamente nuestra idea previamente planteada sobre el mecanismo fisiopatologico; la anemia hemolítica microangiopática antecede y propicia el síndrome intermedio de coagulación intravascular diseminado que autores internacionales refieren bajo el término novedoso de síndrome de HELLP (H: hemólisis; EL: elevación de enzimas hepáticas, LP: plaquetopenia)(4,9,45); el daño endotelial multisistémico que presentan estas pacientes nos hace plantear la interrogante sobre ¿cuál es el lugar que tiene el vasoespasmo en la fisiopatología de la preeclampsia-eclampsia? Para contestar esta pregunta encontramos en la literatura médica reportes con arteriografía cerebral en donde se describen espasmos arteriales multisegmentarios de mujeres con eclampsia durante el puerperio o que el vasoespasmo predomina en la microvasculatura de arterias terminales. Con la aplicación del Doppler transcraneal en la evaluación de estas pacientes se han descrito estudios longitudinales, con aumento en las velocidades de flujo sanguíneo cerebral en las principales arterias del encéfalo, con incremento significativo entre 24 y 48 horas del puerperio, en arterias terminales como la central de la retina, lo que contrasta con los hallazgos clínicos señalados al examinar el fondo de ojo de algunas pacientes como rectificación y adelgazamiento vascular, hallazgos con los que se ha especulado sobre la causalidad del vasoespasmo durante el evento agudo(38-42). En nuestro trabajo determinamos velocidad de flujo sanguíneo cerebral e índice de pulsatilidad en siete vasos principales del polígono de Willis y dividimos en dos grupos comparativamente; encontramos aumento en la velocidad de flujo sanguíneo cerebral y en el índice de pulsatilidad con significacia en los sifones de ambas arterias carótidas, cerebral media y vertebrales, pero la velocidad media no sugiere vasoespasmo, ya que en ningún caso se alcanzó la cifra aceptada en la literatura (120 ml/segundo); tampoco al comparar los grupos por estratos de acuerdo a los datos clínicos neurológicos.
Aceptamos que la presente comunicación tiene dos limitaciones importantes, la primera es de diseño al tratarse de un estudio transversal y no tener seguimiento de los casos y el segundo es técnico, ya que al no acceder a los vasos de menor calibre no podemos descartar la posibilidad de vasoespasmo arteriolar (vasos terminales) como lo sugiere el examen del fondo de ojo que observamos en 15 pacientes (37%). Consideramos que nuestros resultados apoyan la hipótesis de que el punto de mayor conflicto fisiopatológico en estas pacientes se encuentra en la microvasculatura intracerebral con un evidente compromiso circulatorio y hemorreológico, traducido clínicamente con microangiopatía y hemólisis intravscular, y que el vasoespasmo es un evento secundario, por lo que las manifestaciones clínicas neurológicas son el resultado de este compromiso hemodinámico-hematológico y no directamente el vasoespasmo como se ha considerado hasta ahora.
Teniendo en mente el concepto de vasoespasmo como evento aislado no puede ser explicado en su contexto el mecanismo de la hemorragia y la muerte misma, pero si consideramos que el vasoespasmo no es un evento aislado y además no es el elemento primario, sino una consecuencia de los cambios hemorreológicos microvasculares, podremos adoptar como postura académica este concepto y así explicar esta fisiopatología, ya que la velocidad de flujo en un capilar depende directamente del gradiente de presión y del diámetro del vaso, e inversamente de la longitud del mismo y de la viscosidad del líquido, de tal manera que la microcirculación en pacientes con preeclampsia-eclampsia se encuentra alterada; sabemos que el daño endotelial multisistémico causa disminución de oxido nítrico y prostaciclina e incremento en la síntesis de tromboxano A2 y endotelinas, causando vasoconstriccion, exposición del subendotelio que propicia adhesión y activación plaquetaria con liberacion de serotonina que magnifica el fenómeno de agregación plaquetaria, activación de trombina y formación de fibrina, formando microtrombos de plaqueta-fibrina que se deposita sobre el endotelio dañado, dismunuyendo consecuentemente el lumen de vaso, constituyendo una microiangiopatía trombótica, causando anemia hemolítica al fragmentarse los eritrocitos en forma mecánica, liberando hemoglobina y detritus celulares que contribuyen a la suboclusión microvascular. Esto incrementa la presión microvascular y puede ser la causa de la ruptura, produciendo hemorragia cerebral, hepática o en cualquier otro órgano blanco(54-56).