Introducción
La introducción de nuevos materiales con propiedades biológicas cuestionables y la correspondiente aparición de una creciente conciencia de los pacientes con respecto a los peligros para la salud de los materiales odontológicos constituyen dos importantes problemas de la odontología clínica moderna25,54. Así, en los últimos años se ha observado un incremento de las molestias subjetivas y objetivas que fueron directa o indirectamente relacionadas con la prótesis dental utilizada42,43.
A menudo, el paciente, el médico o el odontólogo, en buena medida como consecuencia de una influencia persistente por parte de los medios94, sospechan reacciones alérgicas o tóxicas debidas a los materiales99. Éstas desencadenan con frecuencia múltiples medidas diagnósticas y terapéuticas con resultados habitualmente insatisfactorios19,44. Dado que la composición exacta de los materiales es considerada por los diversos fabricantes como secreto de producción y se distribuyen materiales de composición modificada con el nombre antiguo y materiales idénticos con nombres comerciales distintos, no es del todo posible un ensayo preciso de los materiales. En relación con el derecho del paciente a la integridad física y a un tratamiento conforme al estado de la ciencia, reviste especial importancia el hecho de que, tras la colocación de la reposición dental, recae sobre el odontólogo la responsabilidad exclusiva ante el paciente57.
Pese a los esfuerzos por lograr una profilaxis intensa y al desarrollo de nuevos métodos de tratamiento, en el creciente grupo de pacientes de edad avanzada se observa un predominio de la rehabilitación mediante prótesis parciales o completas realizadas en resina46,64. Aunque las resinas protésicas no se encuentran en el foco del interés de la ciencia de materiales, se cuentan entre los materiales odontológicos más frecuentemente utilizados, con más de 400 toneladas anuales sólo en Europa51. En este contexto, las resinas del grupo de los metacrilatos, pese a la búsqueda intensiva de materiales alternativos, ocupan desde hace décadas una posición de liderazgo indiscutido49. Teniendo en cuenta la expectativa de vida creciente y el consiguiente desplazamiento de la edentación hasta edades avanzadas56,76, las cada vez más duras medidas de ahorro en políticas de salud, el descenso del poder adquisitivo y, no menos importante, la enorme demanda acumulada de los países en vías de desarrollo en el ámbito odontológico, las resinas protésicas continuarán siendo también en el futuro uno de los materiales más importantes en la odontología51.
Reacciones de intolerancia a las prótesis de resina
La colocación de una prótesis, con la carga sobre el tejido de sostén, el recubrimiento de la mucosa oral y el contacto directo con el material, produce en muchos aspectos una situación no fisiológica110. Por regla general, los tejidos orales toleran esta situación. Sin embargo, en algunos casos aparecen reacciones de intolerancia a la prótesis. En su desencadenamiento y en la aparición de posibles trastornos de la mucosa intervienen o interactúan diversos factores43. Debido a la complejidad etiológica y patogénica, la bibliografía no refleja una opinión unánime en cuanto a la definición, la clasificación y la aparición de este cuadro clínico26. No obstante, es posible restringir las causas a unos pocos grupos de factores exógenos y endógenos7. Así, se mencionan como causas las irritaciones macromecánicas y micromecánicas y la influencia del ajuste de la prótesis y la calidad de la resina79,81,108,110,113, una eventual acumulación de calor bajo la placa de resina3,44, infecciones microbianas10,14, dolencias previas generales e internas14,26 y factores del ámbito psiquiátrico-neurológico44,74,78. Junto a todos estos factores, también las reacciones tóxicas o alérgicas a componentes de la resina pueden dar lugar a molestias relacionadas con una intolerancia a la prótesis20,54.
Pese a que, en la opinión de numerosos autores24,40,43,44,71,74,97,109, las reacciones alérgicas sólo constituyen en pocos casos la causa de intolerancias a la prótesis, odontólogos y médicos, pero sobre todo los pacientes, identifican con frecuencia como reacción alérgica los efectos secundarios indeseados y las molestias relacionados con prótesis de resina. Esta sospecha se refuerza cuando las molestias no son explicables claramente o diagnosticables inequívocamente, o resulta difícil influir terapéuticamente en los síntomas clínicos43.
Resinas protésicas
Pese a los más diversos desarrollos químicos y físico-técnicos en el ámbito de los materiales para bases de prótesis, el polimetilmetacrilato (PPMA) y sus modificaciones conservan a día de hoy su posición dominante como materiales protésicos odontológicos. Los metacrilatos para prótesis odontológicas se ofrecen habitualmente como monómero (líquido) y como material prepolimerizado (polvo). El material de base o monómero es el éster metílico del ácido metacrílico (MMA), un líquido incoloro con un punto de ebullición de 100,3 ºC58. Dado que tienden a la polimerización ya bajo la acción de la luz o el calentamiento débil, a los monómeros se les añaden estabilizadores. Uno de estos estabilizadores, utilizado con frecuencia, es la hidroquinona. Pero también se utilizan ácido ascórbico, fenol, resorcina, pirogalol, piridina, ácido benzoico, pirocatecol o sales metálicas para mejorar la estabilidad de almacenamiento85. En el caso de los materiales autopolimerizables, además se encuentran activadores o aceleradores adicionales en el líquido monómero. El componente en forma de polvo contiene el éster metílico de ácido polimetacrilo (PMMA) prepolimerizado en forma de astillas o perlas con un diámetro aproximado de 0,001 a 0,2 mm. El PMMA es un material termoplástico. Por debajo de la temperatura de transición vítrea de aproximadamente 130 ºC, la resina es dura y quebradiza. Por encima de esta temperatura, el PMMA es deformable plásticamente. A partir de una temperatura de 250 ºC empieza a despolimerizarse irreversiblemente. El PMMA es relativamente resistente a ácidos, lejías, gasolina y agua, pero en un medio húmedo absorbe hasta un 2,5 l % vol. de agua. En cambio, es soluble en diversos disolventes orgánicos y en el monómero propio. Además, en el componente en polvo se encuentran catalizadores e iniciadores como el peróxido de dibenzoilo (DBPO). Además, contiene en pequeñas cantidades colorantes y aditivos, como óxido de hierro, cromato de cinc, sulfuro de mercurio y dióxido de titanio, o fibras de nylon o acrílicas sintéticas coloreadas. Actualmente, el sulfuro férrico de cadmio o el seleniuro de cadmio ya sólo se utilizan con poca frecuencia como colorantes13. A fin de mejorar la dureza y la transparencia, y para reducir la contracción de polimerización, se añaden materiales de relleno tales como perlas y astillas de vidrio, silicato de aluminio o litio, cuarzo e hidroxilapatita. Otros materiales de relleno son otras resinas o ceras naturales o sintéticas, talco y óxido de cinc32.
Además del PMMA se han utilizado y se siguen utilizando otras resinas como materiales de base para prótesis. Así, por ejemplo, se han utilizado policarbonatos, poliamidas, poliuretanos, poliacetales, polímeros mixtos PVC-PMMA u otras resinas de metacrilato, como diuretandimetacrilatos. Sin embargo, debido a las tecnologías de fabricación más costosas en comparación con el procesamiento de resinas PMMA convencionales, a las propiedades materiales a menudo limitadas y a los costes generalmente elevados, en el pasado estas resinas protésicas no lograron imponerse en una medida significativa91.
Alergias a resinas protésicas odontológicas
La tolerabilidad biológica es un requisito determinante planteado a los materiales odontológicos que se introducen en la cavidad oral para su presencia provisional o permanente44. Los polimetilmetacrilatos biológicamente inertes satisfacen en gran medida este requisito en cuanto a posibilidades de daños a la mucosa oral y al organismo en su conjunto debido al contacto y a la reabsorción19. Así, esta resina, además de su aplicación en todos los ámbitos odontológicos, se utiliza también en la epitética, para la restauración neuroquirúrgica de defectos craneales, como material para lentes intraoculares o de contacto y como cemento óseo para la fijación de endoprótesis ortopédicas60. Sin embargo, un gran número de los componentes y las sustancias residuales de la reacción de polimerización se hallan bajo sospecha de desencadenar reacciones alérgicas en la mucosa oral o en la piel44. A excepción del polimetilmetacrilato, además del monómero residual también todos los demás componentes de los materiales protésicos a base de metacrilato presentan propiedades alergénicas en diversos grados de potencial. Entre éstos se cuentan los iniciadores de la polimerización, los reticulantes, los inhibidores de la oxidación, los aceleradores, los materiales de relleno, los antiestáticos, los colorantes, los estabilizadores UV y los ablandadores18,43,77,109. Se cree que algunos otros componentes de diversos polímeros más modernos, como las resinas protésicas fotopolimerizables, también desencadenan alergias y poseen un potencial de sensibilización superior incluso al del MMA55.
Si bien en principio las alergias son específicas de cada sustancia, es posible la aparición de alergias cruzadas o de grupo clínicamente relevantes. Para la aparición de alergias son importantes para el riesgo de sensibilización tanto el potencial alergizante de la sustancia como la forma, el intervalo y la cantidad de aplicación. Pese a que en principio es independiente de la dosis, para el desencadenamiento de una reacción alérgica la cantidad incorporada de la sustancia en cuestión debe exceder un valor umbral individual determinado104.
Según Coombs y Gell17, cabe distinguir entre cuatro formas distintas de reacción alérgica. En este contexto se ha observado la reacción tardía mediada por células del tipo IV, la cual se desarrolla como reacción de contacto, y en algunos casos la acción inmediata anafiláctica medida por Ig-E del tipo I en relación con alergias a reposiciones dentales41. En el caso de la acción retardada (tipo dermatitis de contacto), observada con mayor frecuencia, la sustancia en cuestión actúa como un hapteno durante el contacto primario. Mediante el enlace a una proteína portadora se forma un antígeno que es asociado por las células de Langerhans existentes en la piel y en la mucosa oral. Dichas células migran hasta los nodos linfáticos regionales, donde se estimulan linfocitos T sensibilizados específicamente. A continuación, éstos circulan por el organismo y llegan a zonas periféricas, sobre todo a la piel. Esta fase de sensibilización dura un mínimo de cinco días. A este respecto es importante un tiempo de contacto lo suficientemente largo y una concentración suficientemente elevada de la sustancia en cuestión11,97.
En caso de un nuevo contacto con la sustancia en cuestión, el alérgeno es presentado nuevamente por células de Langerhans locales a linfocitos T específicos, los cuales son estimulados a producir linfoquinas. Mediante la liberación de estos mediadores de la inflamación se atraen otras células T específicas, las cuales incrementan la liberación local de mediadores y conducen gradualmente a intensificar la reacción inflamatoria linfohistiocitaria al cabo de un máximo de 18 a 48 h43. En casos infrecuentes, ésta puede ir asociada a una reacción del tipo I. Después de una sensibilización así completada, la reacción alérgica es reproducible en cualquier momento. No existen disposiciones genéticas en cuanto al patomecanismo. El momento de la manifestación de la dolencia a causa de la sensibilización alérgica depende tanto del potencial alergénico, de la concentración y del tiempo de actuación de la sustancia como del estado inmunitario celular del organismo en su conjunto10.
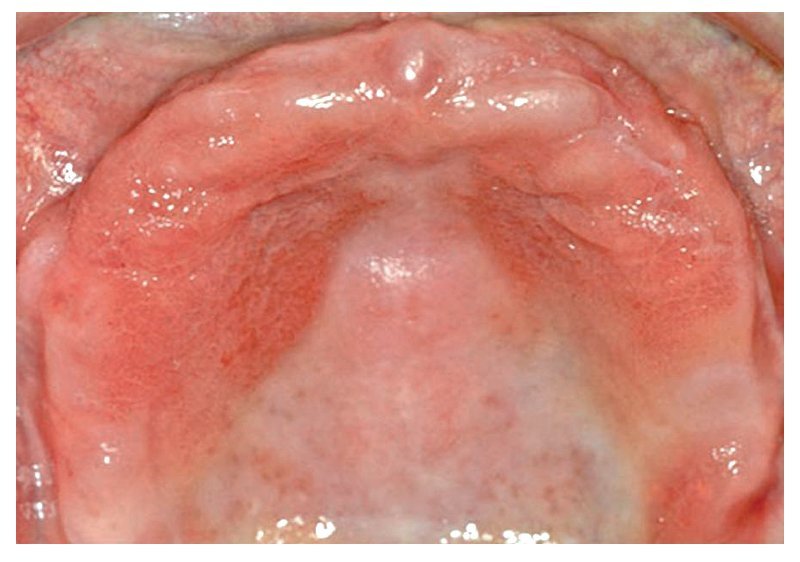
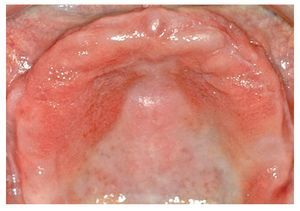
En una reacción del tipo IV (reacción tardía), los primeros síntomas inflamatorios no se observan hasta después de transcurridos horas o días. Empiezan con un enrojecimiento localizado, sobre todo en zonas de contacto íntimo con la sustancia desencadenante. En el caso de una alergia a componentes de una resina protésica, este enrojecimiento se limita generalmente a una zona inflamada que se corresponde con la extensión de la placa de la prótesis30 (fig. 1). Las inflamaciones son difíciles de identificar en la boca. Más allá de la mucositis o la dermatitis de contacto, en casos infrecuentes puede llegarse a la formación de vesículas, pápulas o papulovesículas, descamaciones epiteliales con placas fibrinosas, hemorragias puntiformes y úlceras44,84. También se han observado pérdida del sentido del gusto en caso de afectación acusada de la lengua e incremento de la salivación. Como síntomas subjetivos, los cuales en ocasiones impresionan más que los factores objetivos, se han descrito prurito, dolores, sensación de herida y calor y una merma general del bienestar84,93. La irritación de la mucosa por sí sola, sin síntomas de inflamación, no se considera típica de la alergia43,44. Así pues, si bien no puede excluirse por completo la existencia de una reacción alérgica sin ninguna correlación clínica, sí se considera improbable5. También pueden verse afectadas zonas más alejadas, como la lengua, los labios y regiones cutáneas periorales. Así, las queilitis angulares se cuentan entre los síntomas iniciales de una alergia a resinas protésicas84. Sólo en contadas excepciones debe contarse además con casos ocasionales de reacciones sistémicas6.
Fig. 1. Cuadro clínico en el diagnóstico de sospecha de una reacción de intolerancia a componentes de la resina protésica.
En comparación con las reacciones cutáneas, el cuadro clínico de los enantemas en la mucosa oral es mucho menos impactante104. También las reacciones de las pruebas en la mucosa son más débiles y habitualmente sólo alcanzan el estadio de eritema80. Las causas de las distintas intensidades de reacción de la piel y de la mucosa oral son múltiples111,112. Sin embargo, estos síntomas objetivos y subjetivos por sí solos no constituyen en modo alguno la demostración de una estomatitis de contacto alérgica, sino que también pueden observarse en muchas otras dolencias11.
Después de examinar la bibliografía, diversos autores han llegado a la conclusión de que el número de casos de alergia que aparecieron en relación con reacciones de intolerancia a la prótesis no se diferencia del grado de alergización general de la población normal79. En consecuencia, las reacciones de intolerancia especialmente a prótesis dentales de resina constituyen una complicación muy infrecuente que se da sólo esporádicamente11,14,62,89,104,107. La frecuencia de tales reacciones de hipersensibilidad se sitúa en la población entre el 0,2 y el 5 por mil73,109,113. Después de examinar la bibliografía desde 1940 hasta 1980, Kaaber54 estima para este período en un total de no más de 150 a 200 casos el número de presuntas alergias a componentes de prótesis. En dichos casos se veían afectados sobre todo pacientes con sensibilización múltiples18. Así pues, la alergia a las resinas dentales no parece revestir cuantitativamente una importancia determinante para la aparición de la intolerancia a la prótesis24,40,43,44,71,74,97,109. Sin embargo, el diagnóstico de sospecha de una sensibilización alérgica por resinas se produce presumiblemente con mayor frecuencia de lo que es realmente demostrable57. En la mayoría de los casos de diagnóstico de una alergia a la resina protésica se trataría simplemente de la no identificación de otros factores tales como estímulos mecánicos o la constitución física en relación con causas endógenas70,78. Además, en opinión de Weaver y Goebel108, una irritación química directa en la boca es mucho más probable que la aparición de una reacción alérgica.
Algunos autores defienden la postura de que un producto final totalmente polimerizado ya no es capaz de ejercer una acción sensibilizante o desencadenar una reacción alérgica10,27,28. En consecuencia, las prótesis polimerizadas de forma incompleta o incorrecta serían la principal causa de reacciones de intolerancia a materiales1,47,77. Sin embargo, sólo aparecen estímulos de contacto si también concurren otros factores mecánicos, bacteriológicos, locales y generales adversos37. Tras una nueva reposición con prótesis polimerizadas de forma óptima o una polimerización ulterior, en la mayoría de los casos no aparecieron otras molestias37,106.
Debido a las grandes diferencias en cuanto a los criterios de estudio, grupos de pacientes, métodos de ensayo y concentraciones de las sustancias sospechosas, resulta imposible una comparación fiable de los resultados de estudio disponibles en la bibliografía. También en la bibliografía más antigua, muchas observaciones no constituyen demostración de un proceso alérgico. La existencia de un gran número de casuísticas, las cuales a menudo describen únicamente casos aislados, subraya la infrecuencia descrita de este tipo de casos y las incertidumbres que continúan existiendo a la hora de demostrar inequívocamente una causa en principio alérgica43.
Posibilidades terapéuticas en caso de reacciones de intolerancia a resinas protésicas
En caso de existir una intolerancia a la prótesis de resina presente, en primer lugar debería pensarse en la presencia de, por ejemplo, causas mecánicas, microbianas, internas o incluso psiquiátricas y neurológicas. Debido a la etiología frecuentemente incierta, la gran variedad de factores, algunos de ellos controvertidos, requiere un procedimiento diferenciado para descartar todas las causas posibles. En este contexto debería otorgarse prioridad a la eliminación de cualquier tipo de causa de irritación mecánica o debida a la confección de la prótesis y a una mejora de la higiene de la prótesis, combinadas con un eventual tratamiento antimicrobiano94.
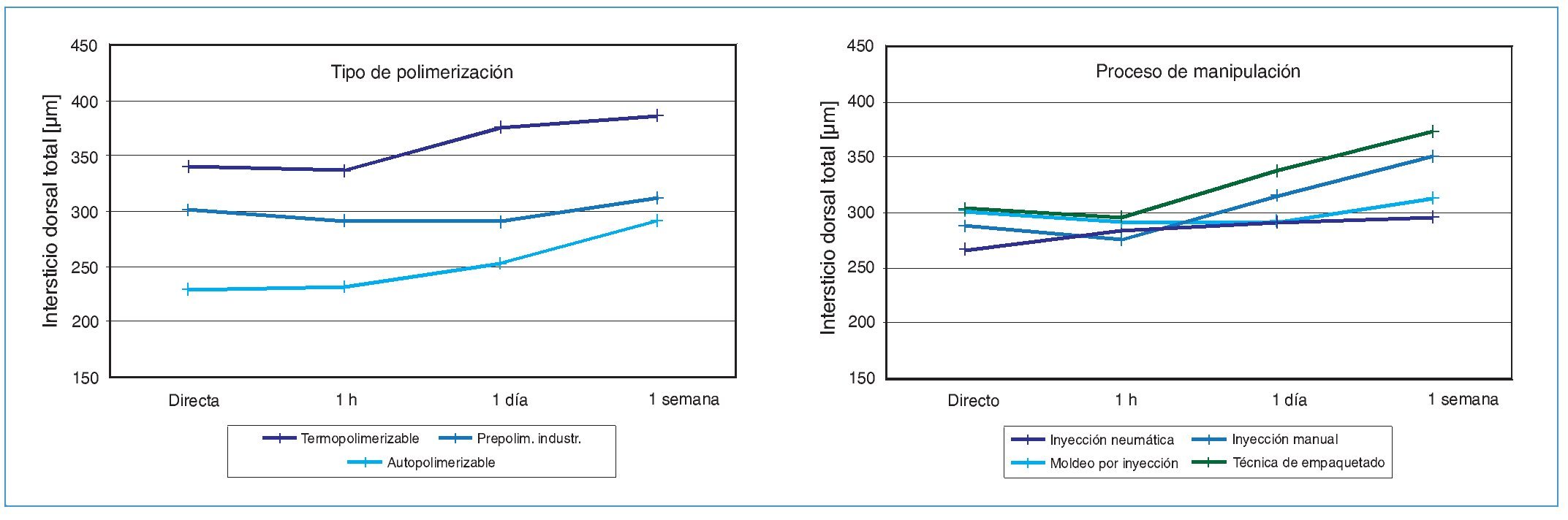
En este contexto desempeña un papel esencial la precisión del ajuste entre la base de la prótesis y el tegumento. Según Körber59, a partir de una formación de intersticio marginal dorsal de aproximadamente 250 µm es probable que surjan problemas de ajuste de la prótesis. Con frecuencia, este problema mecánico se manifiesta clínicamente como estomatitis protésica. Sus causas pueden ser diversas. Así, además de la contracción de polimerización específica de la resina, tanto las tensiones internas en la resina provocadas por el enfriamiento y por el desmuflado como el hinchamiento en caso de almacenamiento húmedo ejercen una influencia sobre el ajuste de la prótesis. Los estudios experimentales continuaron mostrando una influencia significativa del método protésico de manipulación de la resina sobre el ajuste de la prótesis82,83. Así, una vez realizada la polimerización conforme a las indicaciones del fabricante, se comparó en diferentes momentos la medida del intersticio dorsal de siete resinas protésicas (materiales polimerizables en frío, en caliente y termoplásticos) trabajadas utilizando cuatro tecnologías distintas. Se demostró que, en comparación con la tecnología de procesamiento, el tipo de polimerización ejerce una influencia significativamente mayor sobre la formación del intersticio dorsal de las bases protésicas de PMMA83 (fig. 2). Una breve ausencia de la prótesis o el uso de los denominados «Tissue Conditioner» o «Soft Liner» conducen en casi todos los casos a la curación de la mucosa inflamada4. Hennicke37 y Reitz et al94 recomiendan descartar primero todos los demás factores a los que pudiera atribuirse un estímulo por contacto y a continuación llevar a cabo la prueba con una segunda prótesis polimerizada impecablemente. Si después de esto no se observara ninguna mejora de los síntomas objetivos en el área de contacto, debe considerarse la prueba alergológica mediante métodos establecidos por parte de un médico especializado98. Sin embargo, si sólo existen molestias subjetivas, en casos justificados debería procederse a una consulta multidisciplinaria psicosomática. Debe rechazarse considerar la remisión de las molestias al retirar temporalmente la prótesis como demostración exclusiva de una alergia de contacto94.
Fig. 2. La influencia del tipo de polimerización y del proceso de manipulación sobre la formación de intersticio dorsal de diversas resinas de base de prótesis basada en PMMA.
Como ya se ha explicado, la alergia a un componente de una resina protésica constituye un hecho relativamente infrecuente. Sólo después de descartar todos los demás factores posibles debería partirse de la premisa de la existencia de una posible causa alérgica de la intolerancia a la prótesis. No obstante, si pueden garantizarse un procesamiento y unas propiedades impecables de la resina, en opinión de diferentes autores no debería sustituirse precipitadamente el material de la prótesis39,95. Y es que durante el tratamiento posterior no es determinante la composición química del material protésico presente, sino la liberación real de cantidades suficientes de sustancias alérgenas en las condiciones clínicas concretas. Si bien se han detectado analíticamente sustancias irritantes todavía potencialmente alérgenas incluso en prótesis utilizadas durante hasta 29 años77, en un estudio in vitro se logró demostrar que en condiciones similares a las del medio oral no se produce necesariamente también la liberación de sustancias de riesgo alergológico por parte de resinas de base de prótesis8. No obstante, en casos clínicos concretos se da la dificultad de demostrar clínicamente la inexistencia de dicha liberación. En consecuencia, en primer lugar debería intentarse reducir o incluso eliminar el contenido en sustancias potencialmente sospechosas de alergia en la prótesis dental ya existente. Según la bibliografía, a este respecto se atribuye la mayor importancia al denominado monómero residual MMA. Para la reducción de su contenido residual, en el pasado se han descrito distintos métodos. Sin embargo, por regla general su aplicación se refiere a prótesis de nueva confección antes de su colocación en boca del paciente. Tampoco está clara la eficacia de tales métodos para la reducción de otros monómeros. Así, el almacenamiento de la prótesis en agua conduce a una eliminación posterior de componentes de monómero de la resina72. Las especificaciones para la duración de este tratamiento ulterior oscilan entre algunas horas y días51,69,75,99. En cualquier caso, la eficacia de este método está cuestionada12,34,99.
Otro método consiste en el almacenamiento durante hasta cuatro horas de la prótesis en una solución 0,1 normal de permanganato potásico descrita por diversos autores38,69,73,100,101,103. A continuación se lava la prótesis con ácido sulfúrico y agua y se somete a un secado en varias etapas.
La polimerización ulterior de la prótesis de resina debería conducir a una transformación más completa del monómero residual aún no polimerizado47,52,73. En este contexto se prefiere la polimerización ulterior en el armario de secado sobre la polimerización en baño de agua47. De todos modos, los autores no coinciden en las especificaciones para la ejecución concreta. Así, a temperaturas de entre 70 y 100 ºC se recomiendan tiempos de polimerización ulterior de entre 15 min y 8 h. Faltan datos sobre el alcance de la reducción.
Por motivos profilácticos, por parte protésica deben observarse estrictamente los tiempos y las temperaturas de polimerización especificados por el fabricante. Si bien la polimerización que tiene lugar durante un tiempo más largo que el indicado en las instrucciones de uso no debería aportar ventaja alguna59, diferentes autores opinan que mediante una polimerización más alargada que acortada con respecto a las indicaciones del fabricante se minimiza eficazmente el peligro de sensibilización por prótesis de resina1,38,47.
Además de los monómeros residuales MMA, habitualmente se asocia el peróxido de dibenzoilo (DBPO) con reacciones de intolerancia18,22,29,35,45,72. El DBPO forma parte del sistema de polimerización en la mayoría de los materiales fotopolimerizables presentes en el mercado o está presente en la resina como residuo de la producción del prepolímero en forma de polvo31. Sin embargo, son muy pocos los casos en los que se conoce la cantidad real de DBPO en la resina de prótesis polimerizadas12,20,47.
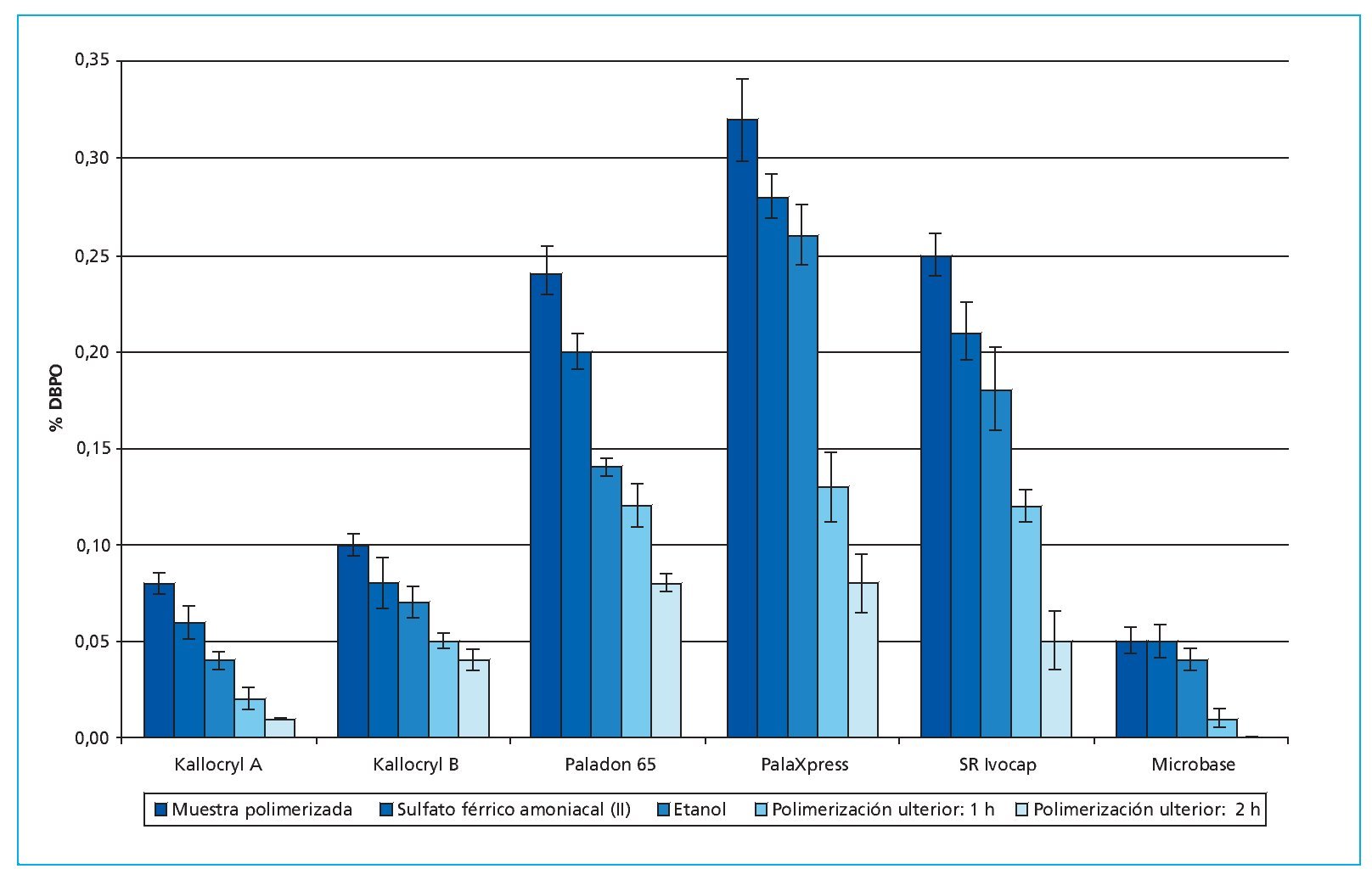
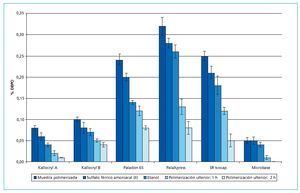
La eficacia de diversos métodos para la reducción del contenido residual de DBPO se probó en varios estudios in vitro8. El almacenamiento de muestras de resina de PPMA y dimetacrilato de diuretano en agua destilada no resultó en una reducción del contenido en DBPO. Tampoco el almacenamiento en solución de permanganato potásico se tradujo en una reducción significativa en ninguna de las resinas. Los almacenamientos en etanol y solución de sulfato férrico amoniacal (II) tuvieron un efecto considerablemente más reductor sobre el contenido residual de DBPO. Sin embargo, la reducción significativamente mayor se logró mediante la polimerización ulterior en el armario de secado (fig. 3).
Fig. 3. La eficacia de diversos métodos para la reducción del contenido residual de DBPO en distintas resinas de base de prótesis. DBPO: peróxido de dibenzoilo.
Así pues, el tratamiento térmico posterior de la resina posibilita, además de una mejora del grado de polimerización, una degradación más completa del iniciador remanente, conduciendo así a una mejora de la biocompatibilidad de la resina protésica. En este proceso, los componentes potencialmente dañinos se reducen tanto más cuanto más elevada es la temperatura y más tiempo dura el tratamiento posterior térmico.
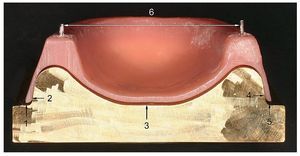
Sin embargo, existe el problema de que una polimerización prolongada podría ejercer una influencia sobre la estabilidad dimensional de la prótesis así tratada82. A este respecto, además de la contracción de polimerización quimioplástica se debe considerar también una posible deformación termoplástica de la base de la prótesis. Como ya se ha mencionado anteriormente, esto podría favorecer a su vez la aparición de una estomatitis protésica de origen mecánico. En un estudio experimental de diversas resinas protésicas convencionales se analizó ejemplarmente este efecto mediante medición de los intersticios marginales lateral y dorsal y la determinación de la dimensión transversal en diversos cuerpos de muestra similares a prótesis sometidos a distintos métodos de polimerización ulterior9 (fig. 4). Se constató que para evitar alteraciones dimensionales clínicamente relevantes debían escogerse individualmente tanto la temperatura (36 ºC a 95 ºC) y el tiempo (2 a 12 h) de polimerización ulterior como la puesta en recubrimiento para cada resina.
Fig. 4. Ejemplo de determinación experimental de la dimensión transversal y del intersticio total dorsal en cuerpos de muestra similares a prótesis.
Así pues, en caso de aparecer una alergia, suficientemente demostrada mediante métodos reconocidos, al monómero residual MMA o a restos de DBPO de la prótesis de resina utilizada en ese momento y en caso de existir un cuadro de molestias alérgicas típico, en el primer paso debería procederse a una polimerización ulterior de la prótesis dental durante varias horas. En este contexto, el tipo de ejecución protésica óptima de la polimerización ulterior debe ser adaptado a la resina concreta. De este modo parece posible una reducción del contenido en sustancias sospechosas de alergia hasta cantidades apenas detectables.
Resinas alternativas para bases de prótesis
A diferencia de los métodos descritos, para la reposición protésica de un paciente ya sensibilizado demostrablemente mediante una prueba reconocida a un componente de resinas protésicas convencionales, debe escogerse un producto que contenga la menor cantidad posible de la sustancia en cuestión. Este procedimiento consecuente para la elección de material se corresponde también con las recomendaciones de la Asociación de Información de Clínicas Dermatológicas (IVDK), así como con las del Grupo de Alergias de Contacto Alemán (DKG) de la Sociedad Dermatológica Alemana95,96. Según dichas recomendaciones, en el futuro debe evitarse consecuentemente una sustancia confirmada mediante métodos reconocidos como desencadenante de alergia. Naturalmente también existen numerosos pacientes de eccema de contacto con alergia a la resina comprobada que sin embargo toleran sin problemas estos materiales en la boca95. No obstante, se le plantea al responsable del tratamiento el problema forense de la obligación de demostración de que no existe relación directa entre las posibles molestias del paciente y la aplicación clínica de materiales dentales que contengan la sustancia sospechosa de alergia. Así pues, en estos casos resulta necesaria la reposición con una prótesis dental alternativa23. Para ello, durante décadas se utilizaron prótesis de caucho18 o prótesis con lámina de oro basal23. Junto a la posibilidad básica de prescindir de una prótesis dental de resina extraíble mediante el uso de una restauración puramente implantosoportada, se describió también el empleo de prótesis completas metalocerámicas sin resina61. No obstante, por regla general en tales casos se persigue la restauración mediante una prótesis completa realizada en una resina protésica alternativa sin sustancias sospechosas de alergia. En caso de una alergia a los pigmentos colorantes de óxido metálico contenidos en la resina protésica, existe la posibilidad de confeccionar una prótesis en una resina transparente sin pigmentos90. En caso de existir sensibilización a otros componentes de resinas de base de prótesis basadas en PMMA convencionales, diversos fabricantes ofrecen resinas de base alternativas que no contienen sustancias irritantes potenciales o presentan una concentración considerablemente reducida de dichas sustancias. Estos productos alternativos se denominan frecuentemente resinas protésicas «hipoalergénicas».
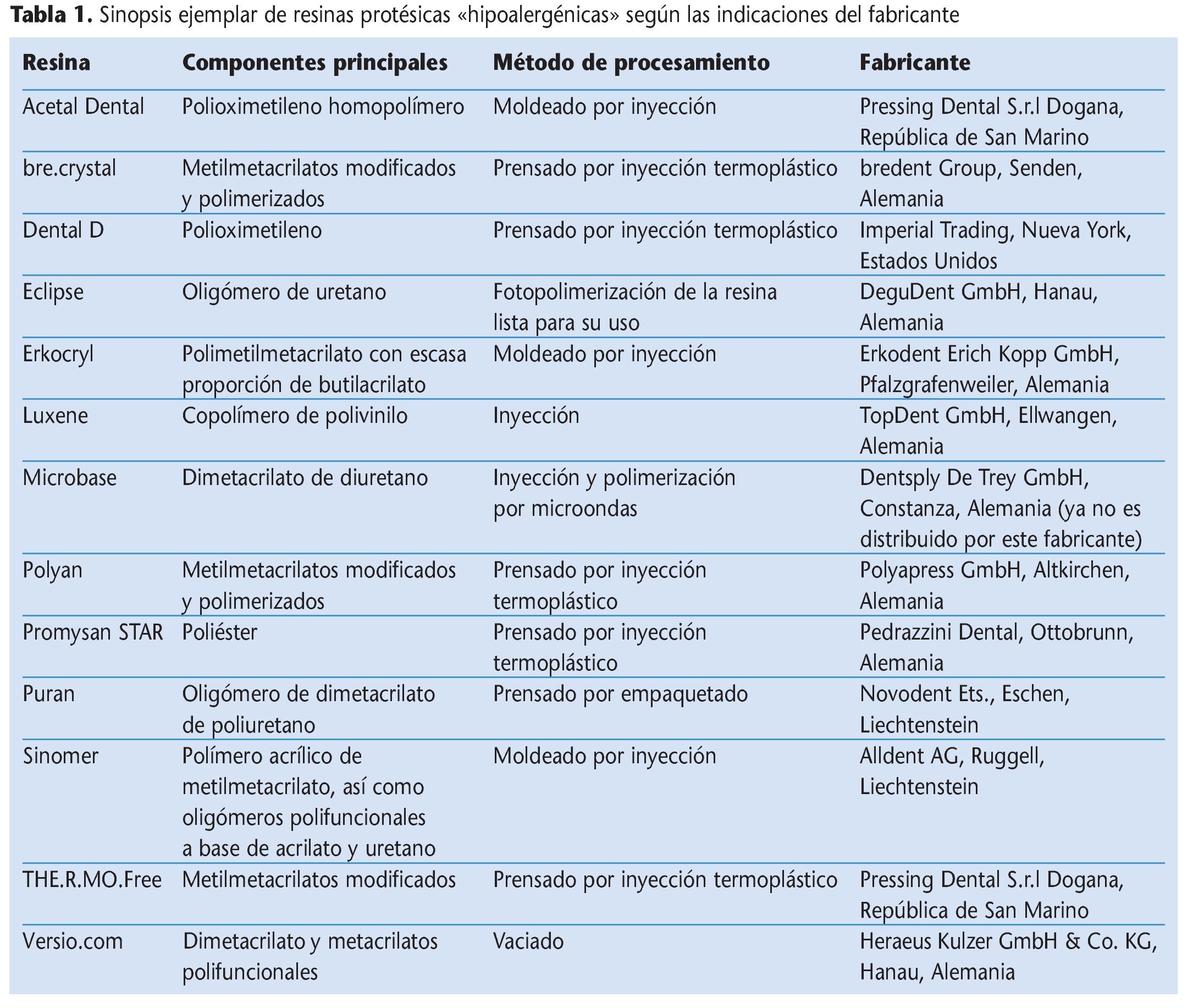
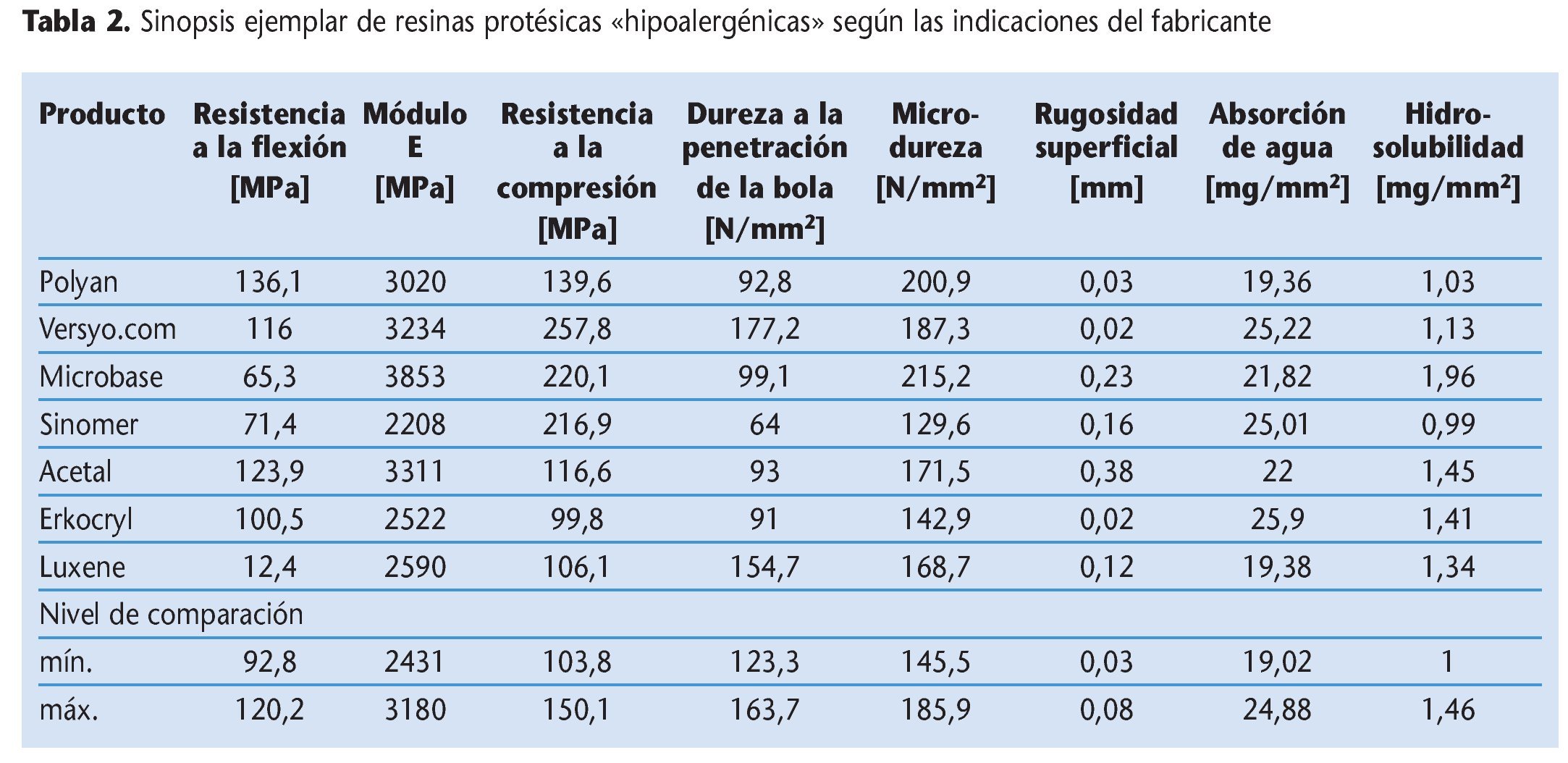
En el «Dental Vademekum»15, conforme a la tipificación de resinas protésicas según la norma DIN-ISO 1567:2000, se distingue entre resinas de polimerización en frío, en caliente, fotopolimerizables y polimerizables por microondas, así como deformables termoplásticamente. No existe una clasificación formal en resinas convencionales y alternativas o hipoalergénicas. El concepto de las resinas «alternativas» o «hipoalergénicas» se refiere particularmente a la ausencia o reducción de sustancias residuales potencialmente alergénicas, como éster metílico del ácido metacrílico (MMA), peróxido de dibenzoilo o hidroquinona en el producto de resina terminado. Bajo el concepto genérico de las resinas protésicas alternativas se engloban, así pues, una serie de productos de resina heterogéneos, los cuales se diferencian sobre todo químicamente, pero en algunos casos también por su procesamiento protésico, de las resinas PPM convencionales y de los sistemas de polimerización habituales (tabla 1).
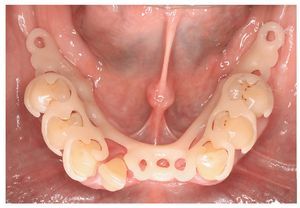
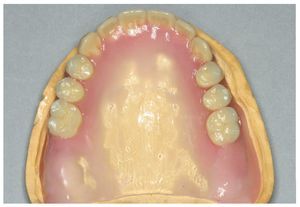
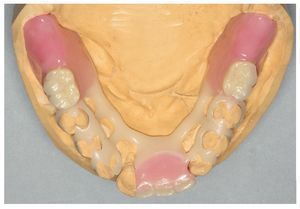
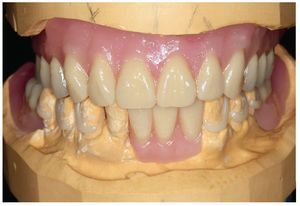
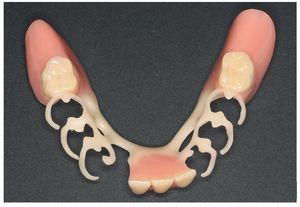
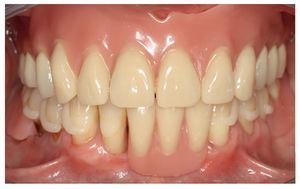
Por un lado, existe la posibilidad de influir, mediante modificaciones del sistema de polimerización de resinas PMMA, sobre las sustancias residuales que provocan la alergia. Así, se recomendó la utilización de resinas de polimerización por microondas para prevenir reacciones alérgicas16. Así mismo existe la posibilidad de prescindir en gran parte, mediante la prepolimerización y métodos de procesamiento especiales de las resinas PMMA, de las sustancias residuales críticas de los sistemas de reacción. Un ejemplo lo constituye la utilización de los denominados materiales termoplásticos (las figuras 5 a 26 muestran la restauración protésica de una paciente con intolerancia dermatológicamente comprobada al DBPO y diversas aleaciones dentales mediante resinas termoplásticas alternativas). Por regla general se trata de resinas PMMA polimerizadas. Estos polímeros constan de moléculas filiformes macromoleculares que, a diferencia de los polímeros reticulados, sólo interactúan entre sí mediante fuerzas de semivalencia.
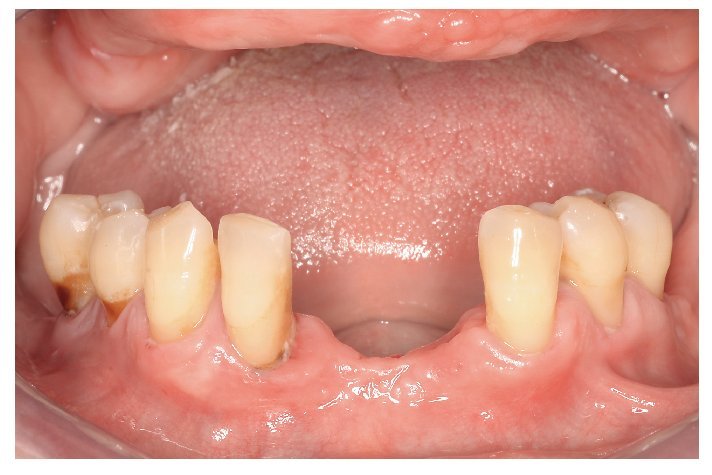
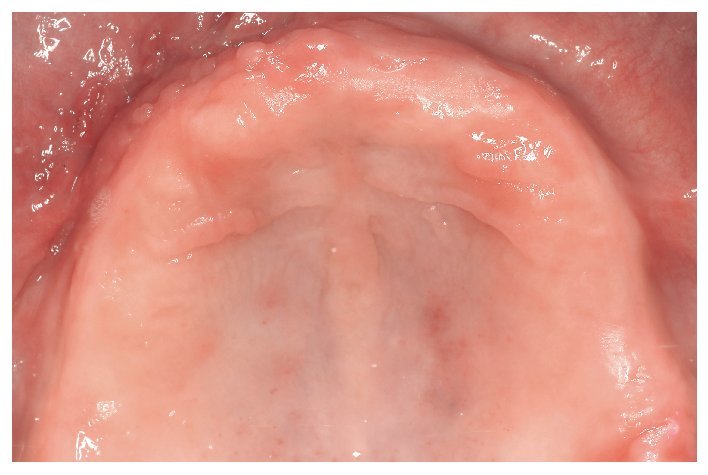
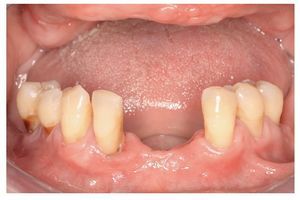
Fig. 5. La situación de partida antes de la nueva restauración protésica con alergia al DBPO demostrada y diversas aleaciones dentales.
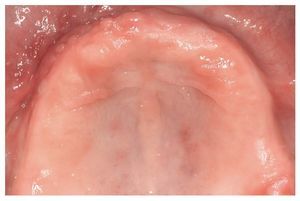
Fig. 6. Vista del estado edéntulo del maxilar superior tres semanas después de la excisión de un fibroma en la región del antiguo diente 13.
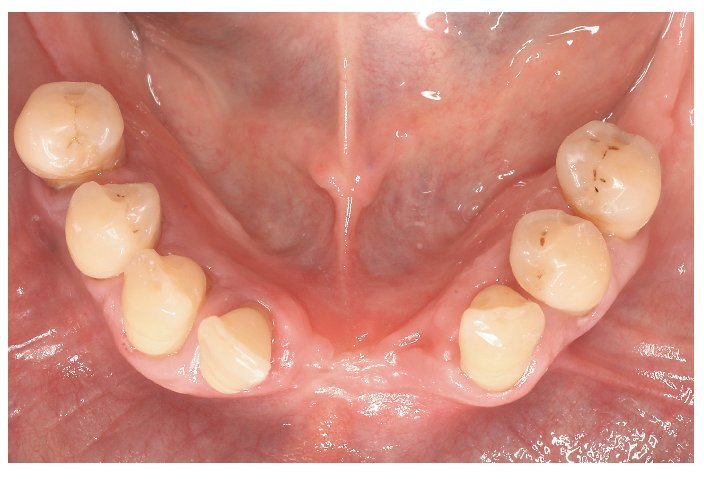
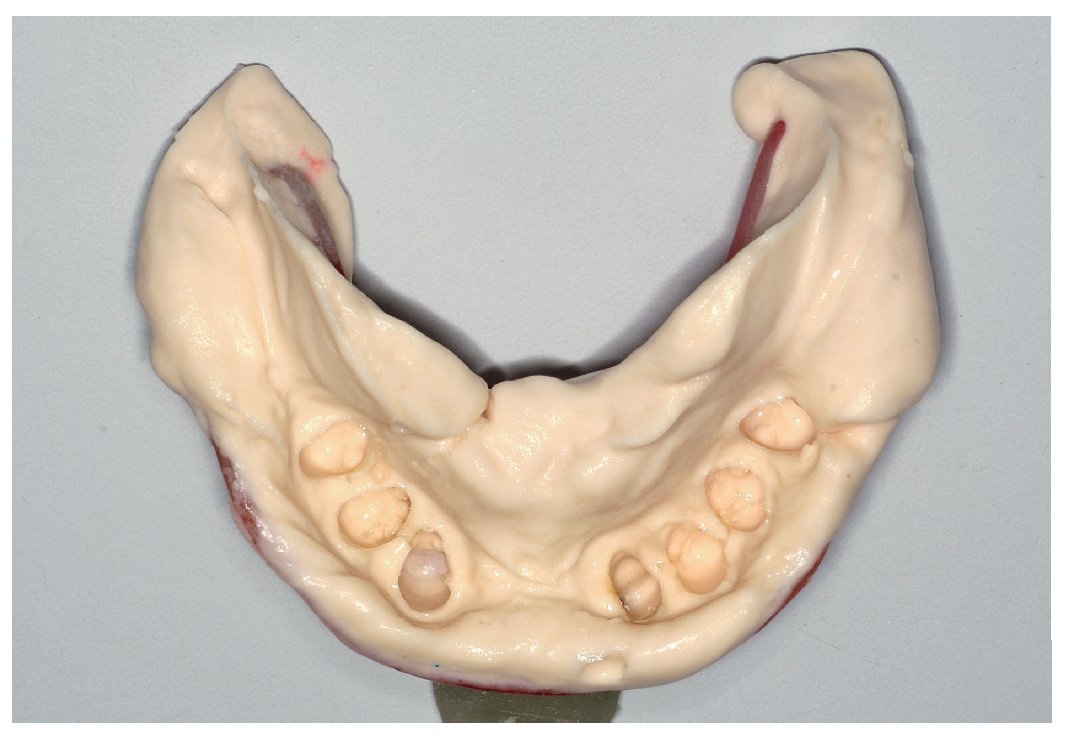
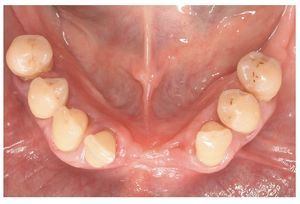
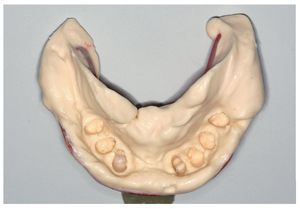
Fig. 7. Vista del estado parcialmente dentado del maxilar inferior tras el tratamiento previo periodontal y aflojamiento residual aún existente de dientes individuales.
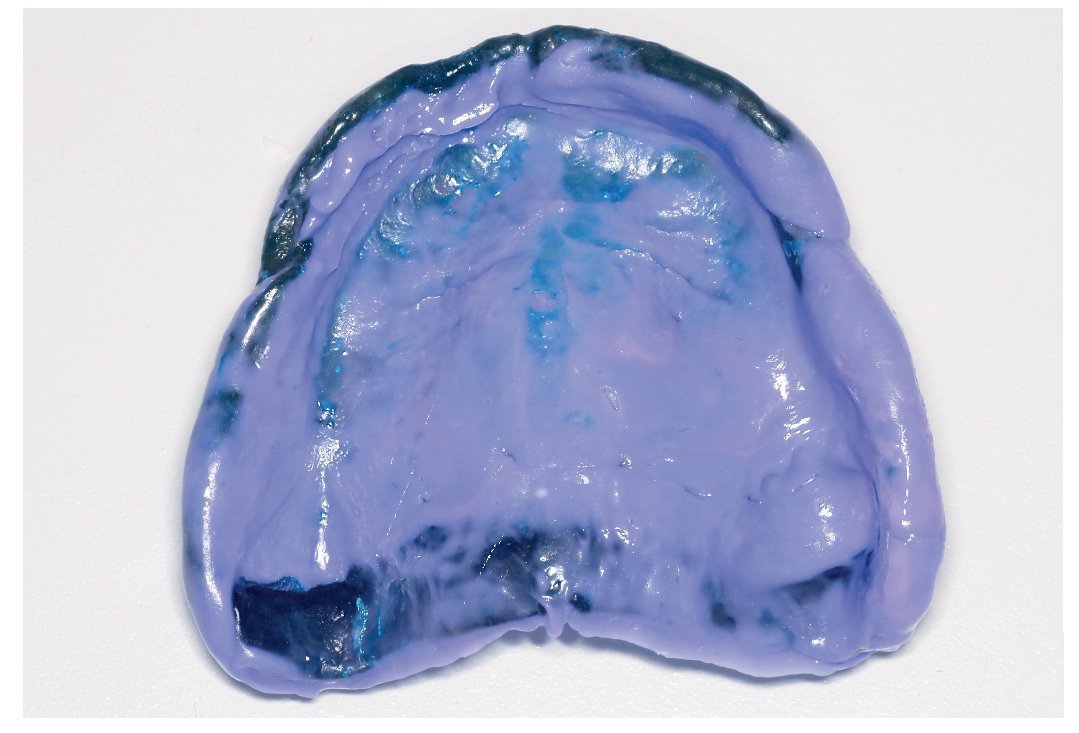
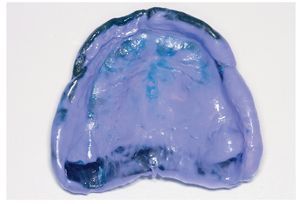
Fig. 8. Impresión funcional mediante cubeta individual y masa de poliéter.
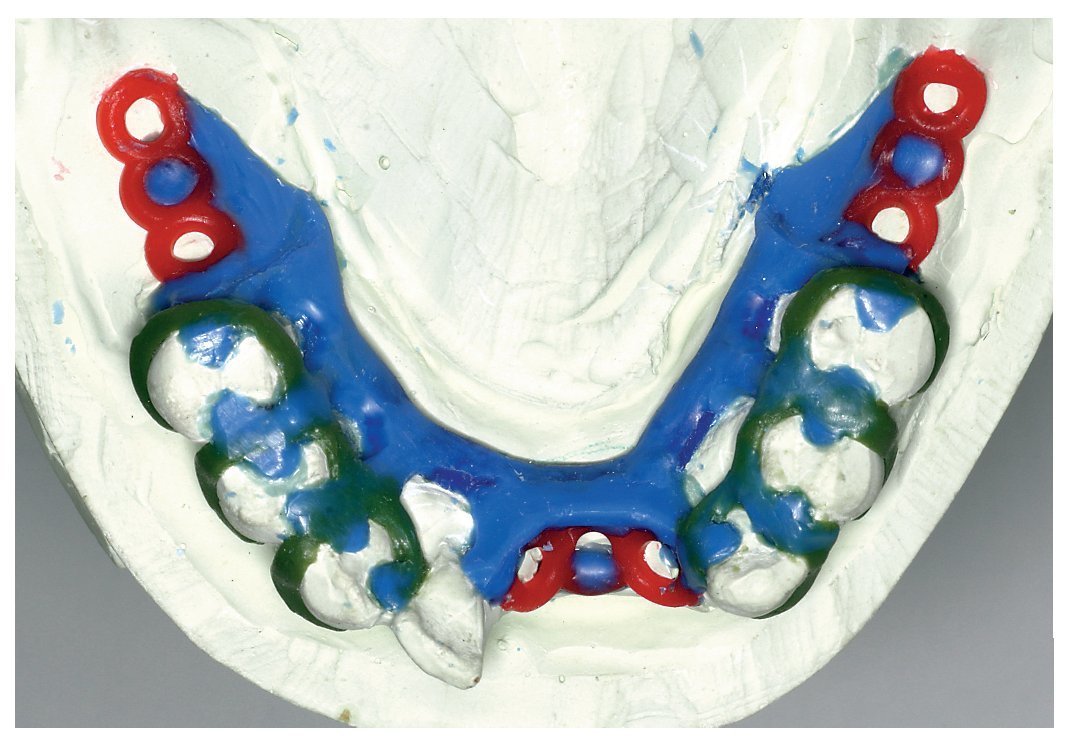
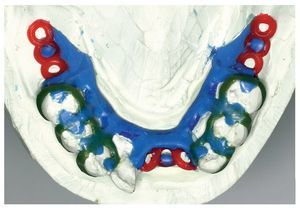
Fig. 9. Toma de impresión del maxilar inferior realizada mediante alginato tras la preparación de los apoyos de los ganchos.
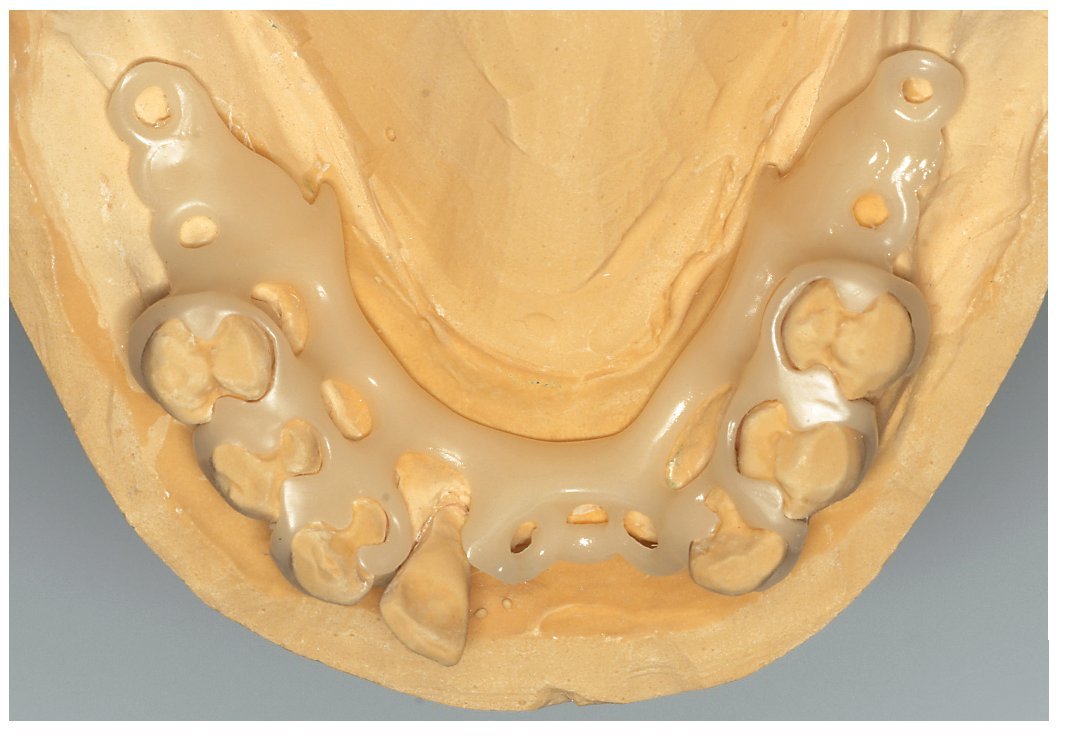
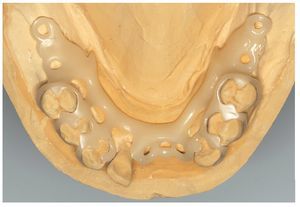
Fig. 10. Estructura encerada para una prótesis de ganchos sin metal.
Fig. 11. Estructura de ganchos prensada y ajustada, realizada en un copolímero de poliacetal (Polyamid Flexiplast, Polyapress, Altkirchen, Alemania).
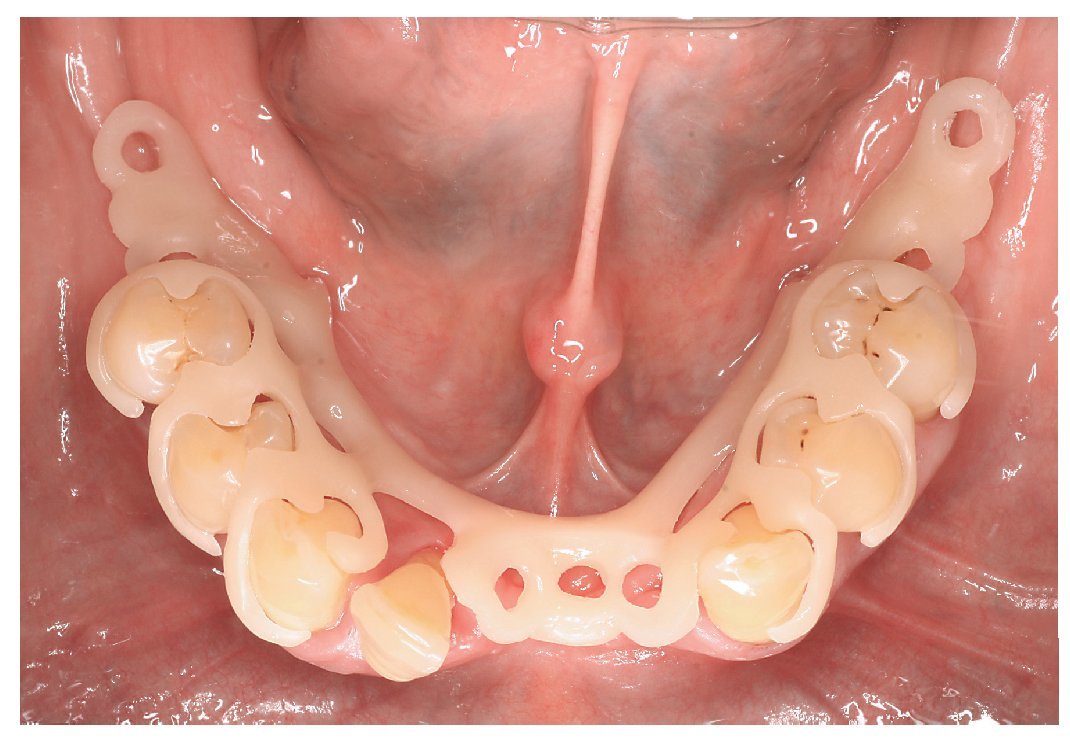
Fig. 12. La prueba en boca de la estructura de la prótesis en el maxilar inferior; la configuración maciza de los conectores y los hombros de los ganchos, típica del material, puede representar un problema higiénico potencial.
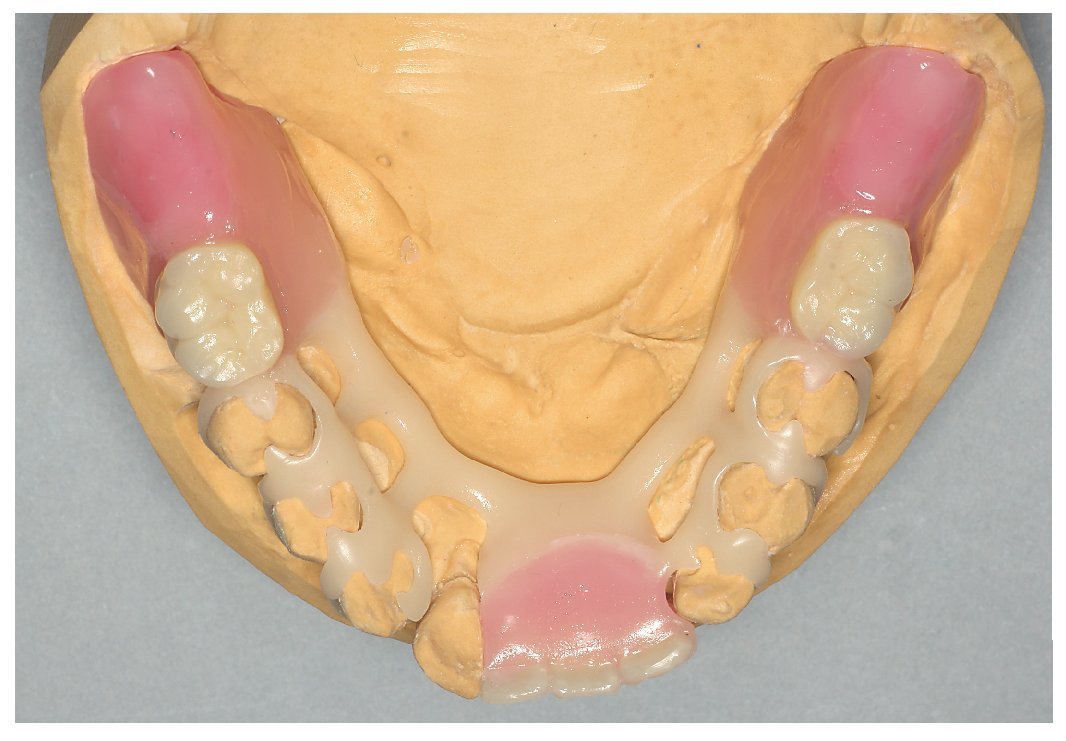
Fig. 13. El montaje en cera de la prótesis superior.
Fig. 14. El montaje en cera sobre la estructura de ganchos.
Fig. 15. Vista general del montaje en cera.
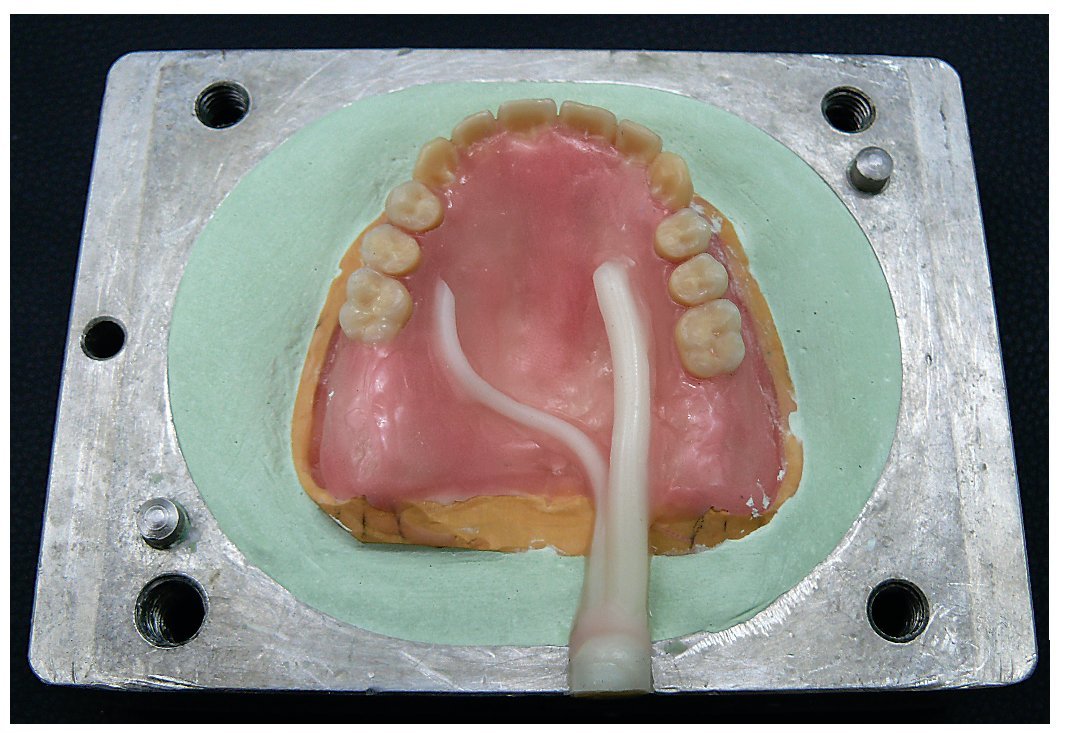
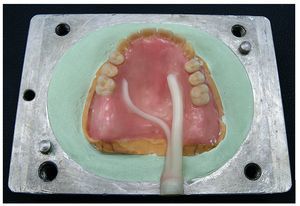
Fig. 16. La preparación de la prótesis superior para completar con una resina termoplástica.
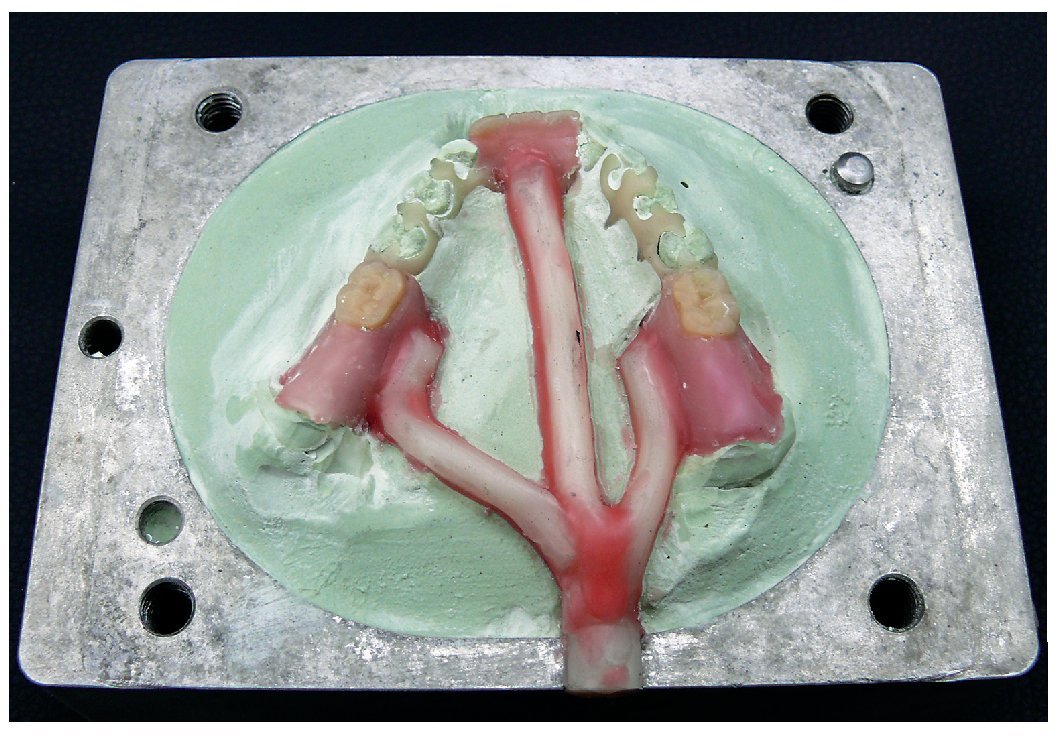
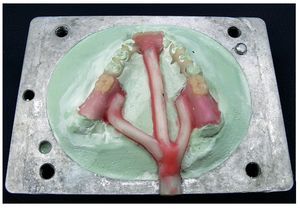
Fig. 17. La prótesis parcial inferior con canales de inyección encerados.
Fig. 19. La colocación del cartucho y la cubeta en el aparato de moldeo por inyección.
Fig. 18. Resina termoplástica en cartucho metálico (Polyan, Polyapress).
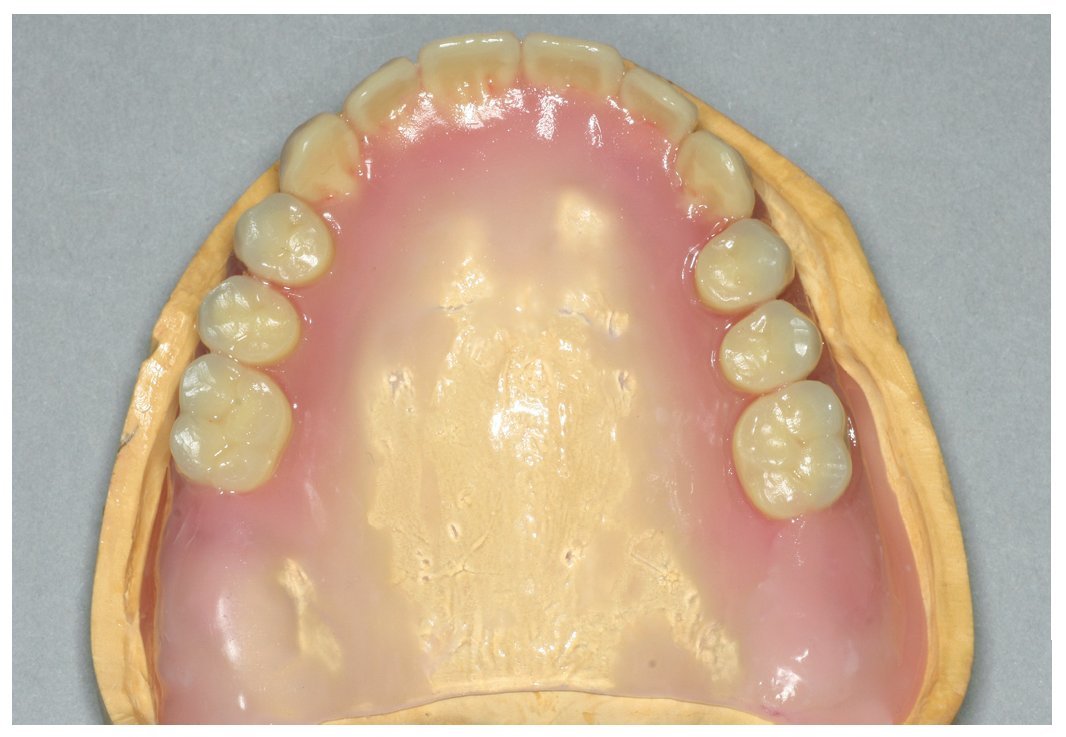
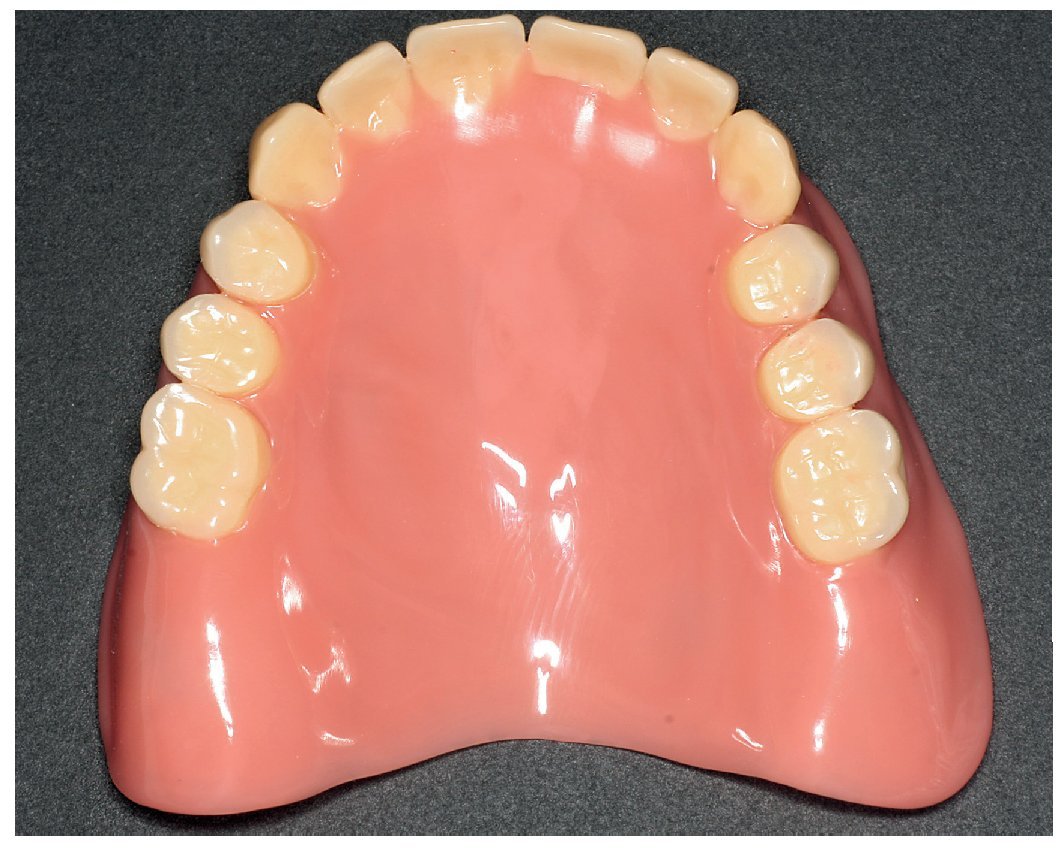
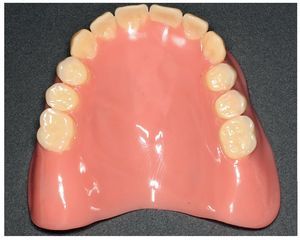
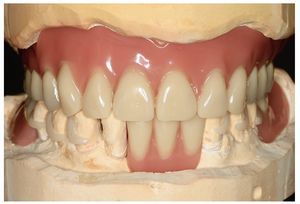
Fig. 20. La prótesis superior acabada, realizada en PMMA trabajado termoplásticamente.
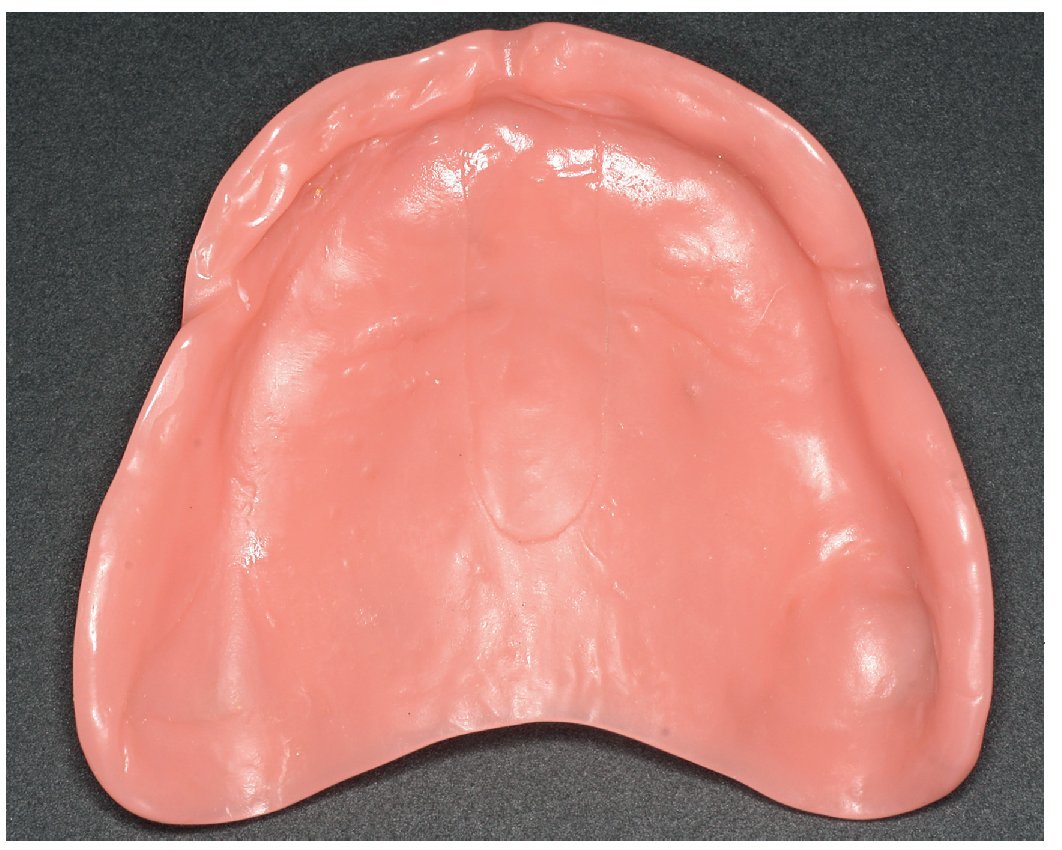
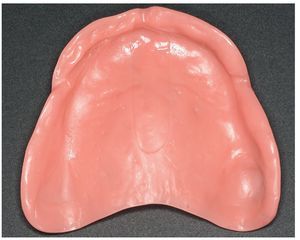
Fig. 21. La parte inferior de la prótesis cuidadosamente desperfilada para prevenir irritaciones mecánicas (torus palatinus expuesto localmente).
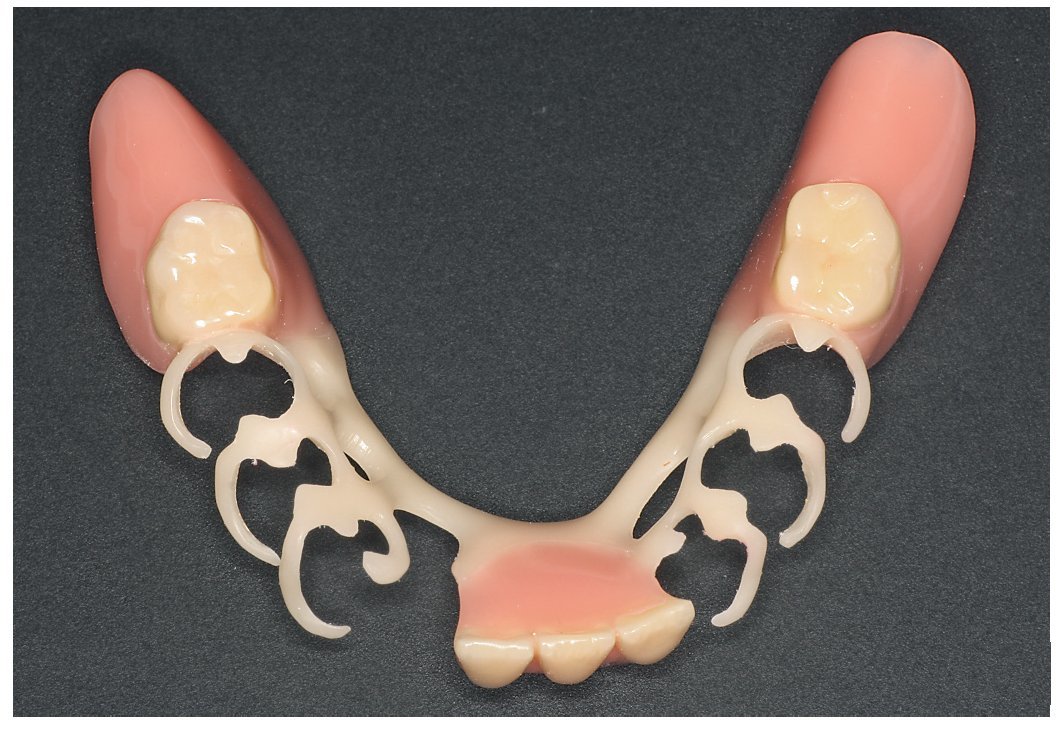
Fig. 22. La prótesis de ganchos inferior sin metal.
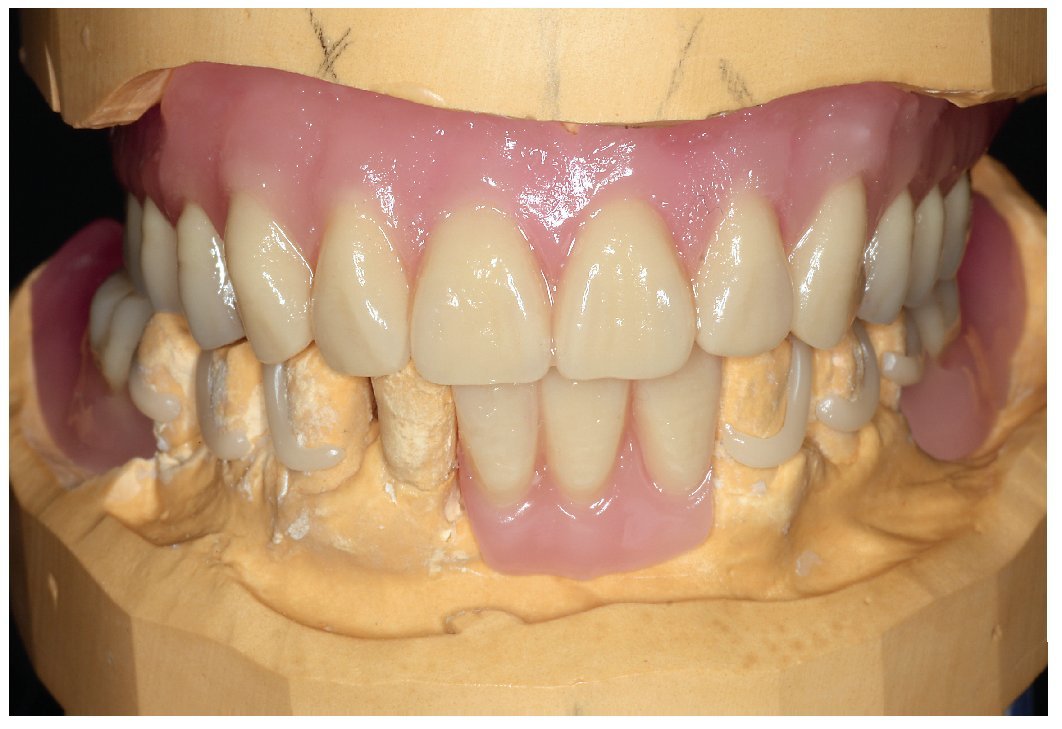
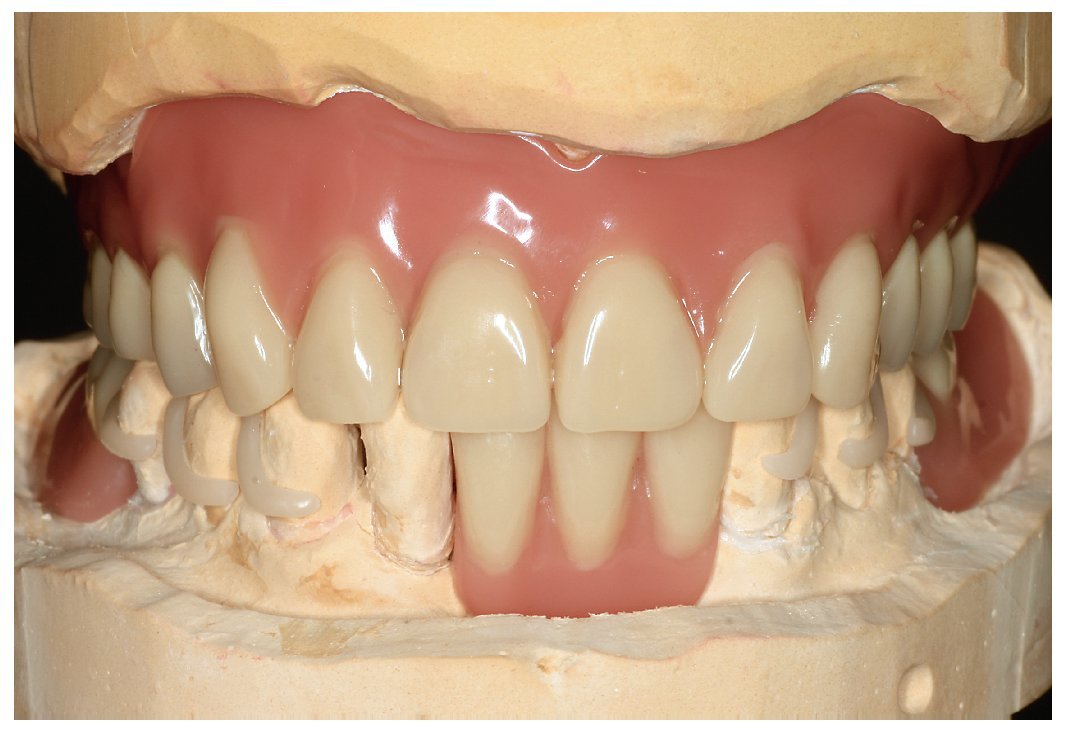
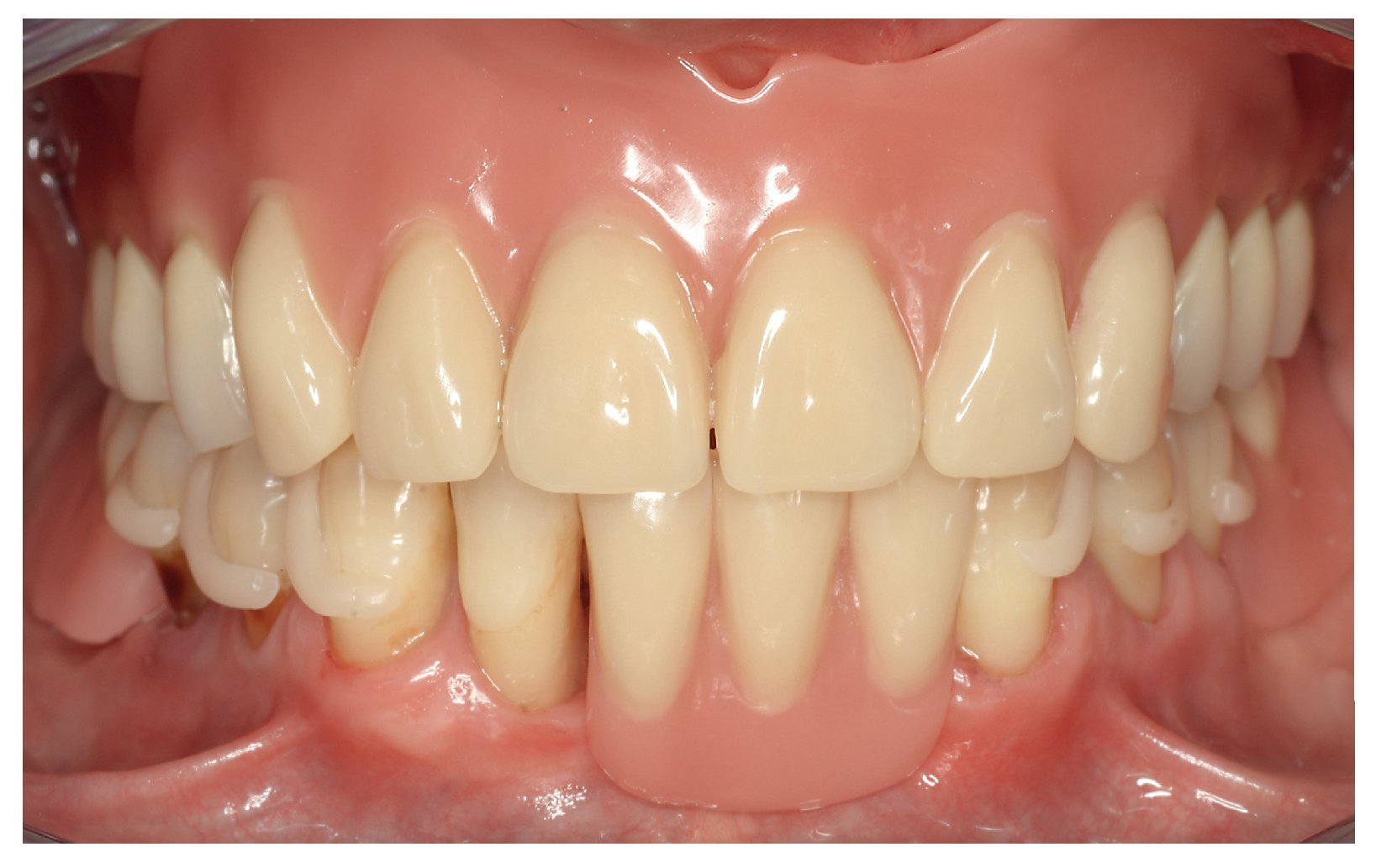
Fig. 23. La prótesis dental «hipoalergénica» antes de la colocación.
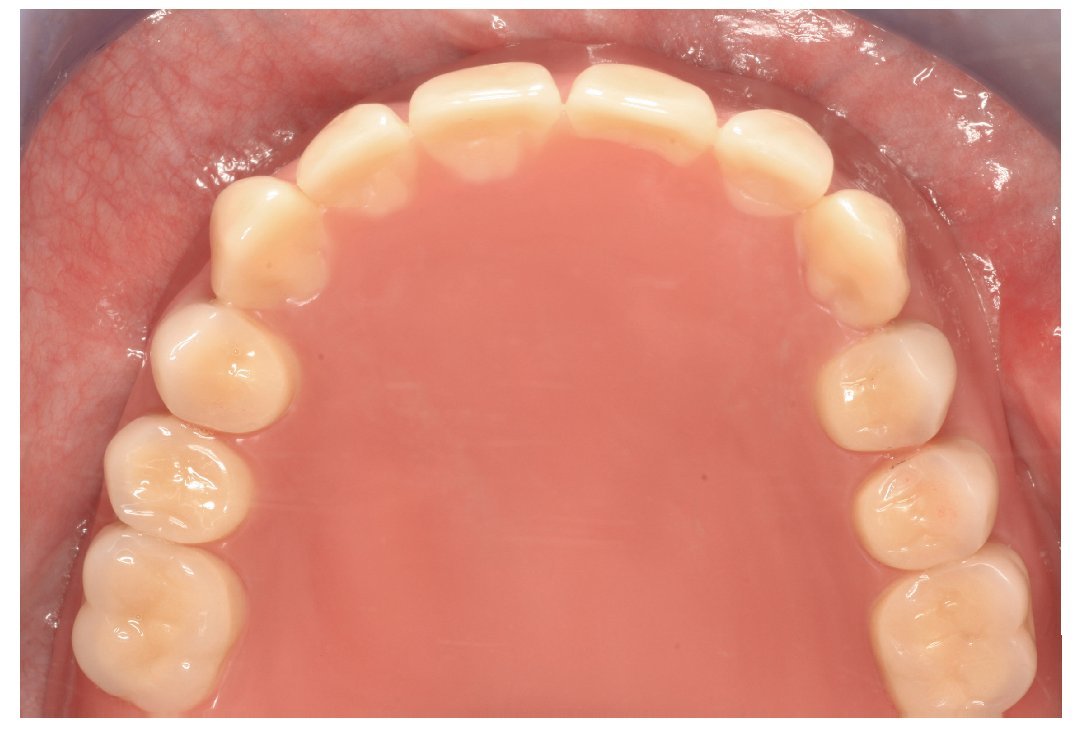
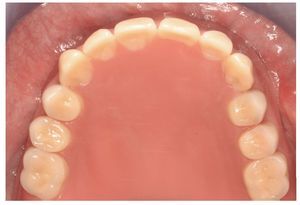
Fig. 24. El maxilar superior con la nueva prótesis.
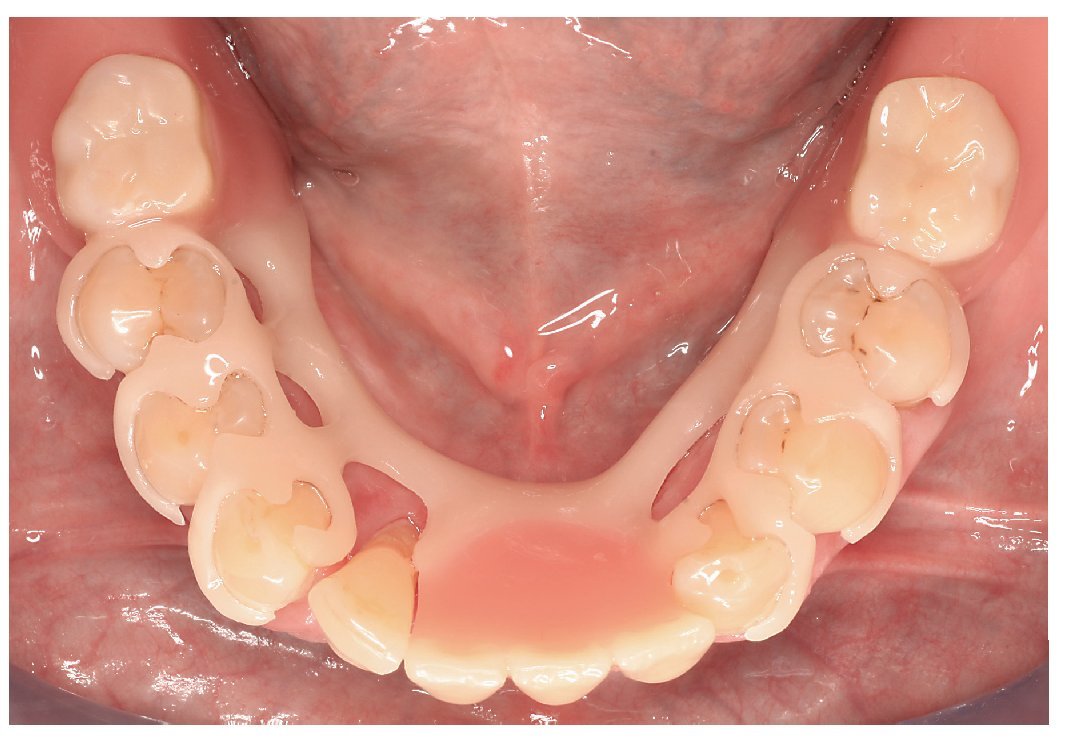
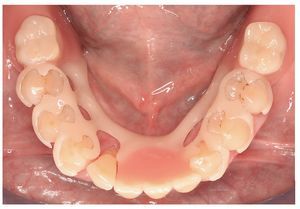
Fig. 25. La prótesis parcial con efecto de ferulización en el maxilar inferior pretratado periodontalmente.
Fig. 26. Incluso seis meses después de la colocación no se observan indicios de reacciones de intolerancia, además de constatarse una buena función y una estética satisfactoria.
Mediante el incremento de la temperatura hasta aproximadamente 260 ºC se aumentan dichas valencias, en un primer momento de forma reversible. El material se vuelve fluido y puede inyectarse bajo presión en un molde hueco preparado114. Dado que el material ya ha sido polimerizado industrialmente durante su procesamiento, puede mantenerse en su composición libre de posibles sustancias alergénicas del sistema de reacción, como peróxido de dibenzoilo o derivados del formaldehído. De todos modos, durante el calentamiento del material hasta el rango de manipulación termoplástica también puede producirse en algunos casos una despolimerización de las moléculas, de modo que en la resina terminada puede estar presente un cierto contenido residual de MMA libre de hasta el 0,3%115.
Otra posibilidad para evitar las sustancias de riesgo alergénico conocidas es la utilización de resinas de base no basadas en el PMMA convencional. Desde hace ya algunos años existen en el mercado diversos materiales alternativos. En los últimos años se han desarrollado nuevas resinas de metacrilato sin MMA. Se trata de resinas de composite con más de un 50% de sustancias de relleno en forma de partículas de polvo polímero, polvo vítreo microfino y fibras orgánicas. La base química está formada por dimetacrilato de diuretano. A diferencia del MMA convencional, este monómero de diacrilato posee dos enlaces dobles reactivos. Por regla general, la polimerización tiene lugar en el microondas50. Hasta ahora todavía no existían resultados de ensayos a largo plazo clínicos y de higiene laboral112. Sin embargo, tampoco estas resinas basadas en monómeros de diacrilato parecen ser completamente irrelevantes alergológicamente. Así, Kanerva et al55 han demostrado en un odontólogo una alergia laboral al dimetacrilato. Básicamente, a la hora de escoger el producto en un caso clínico concreto debería tenerse en cuenta que una resina denominada «hipoalergénica» no está necesariamente completamente libre de sustancias irritantes alergénicas.
A fin de garantizar su uso clínico sin problemas, además de sus propiedades hipoalergénicas, los productos alternativos no sólo deben corresponderse con las resinas PMMA reconocidas en cuanto a sus propiedades físico-mecánicas, sino que deben ofrecer unas propiedades y ventajas mejoradas lo más posible87. De ahí que fuera preciso esclarecer si las resinas hipoalergénicas alternativas presentan propiedades mecánicas equiparables en comparación con las resinas protésicas convencionales y establecidas y por consiguiente constituyen una alternativa desde puntos de vista mecánicos del material68,87.
Propiedades mecánicas de las resinas para base de prótesis hipoalergénicas
En la norma DIN EN ISO 1567 «Resinas para bases de prótesis» en su versión más actualizada del año 2000 se describen propiedades mecánicas seleccionadas de resinas protésicas, entre ellas la resistencia a la flexión, el módulo de elasticidad, la absorción y la solubilidad en agua. Paralelamente se establecen también requisitos mínimos en cuanto a las propiedades mecánicas del material. Estas especificaciones son aplicables así mismo a las resinas hipoalergénicas y deben ser satisfechas por cada uno de estos productos.
Algunas de las principales propiedades mecánicas materiales de las resinas protésicas son su resistencia a la flexión y su módulo de elasticidad. Para el respeto de la zona de apoyo de la prótesis, además de la precisión de ajuste de la prótesis, es determinante sobre todo la resistencia a la flexión de la resina112. El valor característico de material de la resistencia a la flexión es el módulo de elasticidad. Así pues, un módulo de elasticidad elevado, y por ende una resistencia a la flexión elevada, contribuyen decisivamente a respetar la zona de apoyo de la prótesis.
Otra propiedad mecánica importante de las resinas de base de prótesis es la microdureza. Ésta proporciona, además de información sobre la dureza superficial, información sobre la estructura de la superficie de una muestra. En consecuencia, la medición de la microdureza permite extraer indirectamente conclusiones sobre el contenido en monómero residual o el peso molecular. De este modo se conoce que, por ejemplo, los metacrilatos termopolimerizables presentan unos valores de microdureza más elevados que los autopolimerizables21,66,67.
La calidad de la superficie reviste un especial interés para la evaluación cualitativa de una resina de base de prótesis. Depende en gran medida de los métodos de polimerización y procesamiento previos y del acabado y el pulido posteriores65,102. Una superficie de resina rugosa y porosa conduce a decoloraciones intraorales y a la retención de placa. Así pues, una calidad insuficiente de las superficies de resina en contacto con la mucosa puede contribuir a la aparición de reacciones inflamatorias36,92. En cambio, una superficie de la prótesis lisa y brillante resiste las decoloraciones y la acumulación de placa33. Se demostró que la rugosidad de la superficie de las resinas protésicas depende del tipo de polimerización117.
Otros indicadores que influyen en las propiedades clínicas de los materiales de base de prótesis son la absorción de agua y solubilidad en agua2. Éstas vienen determinadas por las estructuras químicas de los monómeros y polímeros, así como por el grado de cristalinidad y reticulación50. Idealmente, las resinas protésicas no deberían absorber agua ni otros líquidos, dado que este proceso conduce siempre tanto a fluctuaciones dimensionales y dificultades de ajuste116 como a alteraciones de las propiedades mecánicas y la estabilidad del material105. El monómero residual remanente en la resina protésica puede conducir a un incremento de la absorción de agua y la solubilidad48. Así, los estudios han demostrado que los valores de hidrosolubilidad y absorción de agua en materiales de base de prótesis termopolimerizables son más bajos que los de los metacrilatos autopolimerizables63. A su vez, en comparación con un material termopolimerizable se constató en una resina termoplástica una absorción de agua significativamente menor88.
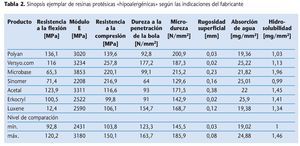
En el pasado, los estudios de las propiedades mecánicas materiales de las resinas protésicas hipoalergénicas se realizaron centrándose en algunos parámetros seleccionados63,86-88. En un estudio propio debía esclarecerse si las resinas de base de prótesis alternativas en comparación con las resinas protésicas convencionales y consolidadas desde hace muchos años satisfacen los requisitos mínimos en los ámbitos de la resistencia a la flexión, el módulo de elasticidad, la resistencia a la compresión, la dureza a la penetración de la bola, la microdureza, la rugosidad de la superficie, la hidrosolubilidad y la absorción de agua53. Así, se estudiaron y compararon ejemplarmente siete productos distintos hipoalergénicos según las indicaciones del fabricante con tres resinas de base de prótesis convencionales mediante un programa de ensayo físico-mecánico. En la comparación descriptiva de materiales se constató que tres productos presentaban déficits manifiestos. En la contraposición al nivel de comparación determinado a partir de las resinas convencionales, estos materiales requieren una optimización selectiva del material (tabla 2). En virtud de los niveles de propiedades mecánicas medidos, los materiales Polyan, Versyo.com y Luxene cumplieron en mayor medida los requisitos derivados de los valores característicos de los materiales termopolimerizables y autopolimerizables convencionales. Sin embargo, ninguna de las resinas hipoalergénicas ensayadas satisfizo todos los parámetros de comparación estudiados, de modo que serían deseables mejoras adicionales de estos productos en cuanto a la mecánica del material.
Agradecimientos
Llegados a este punto, el autor desea expresar su agradecimiento al Prof. Karl-Ernst Dette, director del área de Propedéutica Odontológica, por la amable cesión de la fotografía reproducida en la figura 1. El agradecimiento se extiende al laboratorio HAL-Dent Zahntechnik GmbH, Halle (Saale), Alemania, por la realización de la restauración protésica mostrada. Correspondencia
Dr. med. dent. Arne F. Boeckler, Oberarzt.
Martin-Luther-Universität Halle-Wittenberg. Department für Zahn-, Mund- und Kieferheilkunde. Poliklinik für Zahnärztliche Prothetik (Direktor Prof. Dr. Jürgen M. Setz).
Große Steinstraße 19, 06108 Halle (Saale), Alemania.
Correo electrónico: arne.boeckler@medizin.uni-halle.de