El dolor torácico en urgencias supone un reto asistencial. A pesar de los avances en el diagnóstico clínico, todavía existen muchos pacientes con dolor torácico atípico que son hospitalizados de manera innecesaria y pacientes dados de alta erróneamente. Ante la situación clínica concreta de pacientes con dolor torácico, electrocardiograma (ECG) inicial normal o no diagnóstico y biomarcadores cardiacos normales, la tomografía computarizada multicorte (TCMC), ha demostrado ser una técnica que puede ayudar a descartar las patologías de mayor morbimortalidad y establecer la causa del dolor. En este trabajo se revisa el estado actual de la utilidad de la TCMC en el diagnóstico del paciente que acude al Servicio de Urgencias por dolor torácico, se repasa el desarrollo de la técnica, se define la población de estudio más apropiada, se describen los protocolos de adquisición y se discuten las ventajas e inconvenientes de cada protocolo de estudio.
Chest pain is a challenging clinical problem in the emergency department. Despite advances in clinical diagnosis, many patients with atypical chest pain are needlessly hospitalized and others are mistakenly discharged. Faced with the specific clinical situation in which a patient has chest pain, an initially normal or inconclusive electrocardiogram, and normal cardiac biomarkers, multislice CT has proven useful for ruling out the conditions that involve the greatest morbidity and mortality and for establishing the cause of pain. This article reviews the current usefulness of multislice CT in the diagnostic workup of patients presenting at the emergency department with chest pain. We review the technique, define the most appropriate population, describe the acquisition protocols, and discuss the advantages and disadvantages of each study protocol.
La valoración del paciente con dolor torácico representa un desafío para la asistencia sanitaria y economía actual. Se estima que el 5-20% de los motivos de consulta en los Servicios de Urgencias en España se debe a dolor torácico no traumático1. Las causas potencialmente más letales de dolor torácico son el tromboembolismo pulmonar, la disección aórtica y la enfermedad coronaria. A pesar de que el 50% de estos pacientes presenta un cuadro clínico sugestivo de síndrome coronario agudo (SCA), únicamente en la mitad de los casos se llega al diagnóstico2,3. Aproximadamente un 15% es diagnosticado de SCA demostrable por la clínica y el ECG al inicio, incrementándose esta cifra en un 35% adicional si se consideran los SCA con ECG inicial normal4. Si bien la mayoría de los pacientes con dolor torácico no presenta una causa potencialmente letal, un gran número de estos pacientes permanece en observación o es hospitalizado de manera innecesaria5,6. Con objeto de optimizar los recursos7, optimizar la asistencia y manejar apropiadamente este grupo de pacientes se han creado las unidades de dolor torácico (UDT)8. No obstante, a pesar de los avances en el diagnóstico clínico, la sensibilidad y especificidad de las exploraciones que se realizan como primera aproximación al dolor torácico (historia clínica, niveles de enzimas cardiacos, ECG y radiografía de tórax) pueden resultar insuficientes para establecer la causa del dolor9,10. De hecho, existe un número de pacientes con SCA no correctamente diagnosticados que son dados de alta de manera errónea11–13, con la consiguiente problemática legal que esto conlleva14–17.
La tomografía computarizada multicorte (TCMC) es la técnica de primera elección para el despistaje del tromboembolismo pulmonar (TEP)18–20 y la patología aórtica21,22. Estudios recientes señalan, además, que la TCMC-64 es útil para descartar la enfermedad coronaria23. Por tanto, al permitir valorar la aorta, la arteria pulmonar y sus ramas y las arterias coronarias, una única exploración mediante TCMC podría ser útil para estudiar los pacientes que acuden por dolor torácico al Servicio de Urgencias24,25 y descartar así las causas de mayor morbimortalidad.
Desarrollo tecnológico: ¿cómo ha evolucionado la TC?La TC cardiotorácica está sufriendo una evolución constante. En la década de los 80 se diseñó el primer equipo específico para estudiar el corazón (TC de haz de electrones, electron beam CT)26. Más adelante, a finales de la década de los 90, la imagen cardiaca sufrió un avance significativo al comercializarse los equipos multicorte de cuatro coronas de detectores que, además de suponer un gran progreso en la adquisición de estudios de cualquier órgano del cuerpo, permitieron estudiar el corazón con sincronización con el ECG y elevada resolución espacial y temporal27. Con esta técnica de imagen se demostró que era posible cuantificar la calcificación coronaria y evaluar las arterias coronarias con suficiente calidad de imagen28. Más adelante, fue con la introducción de los equipos de TCMC-16 y, sobre todo, TCMC-64 cuando se generalizó la imagen cardiaca no invasiva. Estos últimos equipos permiten estudiar el corazón con un tiempo de rotación de gantry de 330ms (resolución temporal de 165ms) y resolución espacial de 0,4mm en una apnea corta29. Hoy en día, según las recomendaciones clínicas más actuales, se considera que el estándar de referencia en equipos TCMC utilizados para imagen cardiaca deben ser sistemas de al menos 64 cortes30.
En los dos últimos años, con objeto de superar las limitaciones de estos equipos, que se deben fundamentalmente a su resolución temporal y espacial, se han desarrollado dos tipos de sistemas de TC. Los equipos de TC dual o de doble fuente permiten obtener estudios con una resolución temporal de 83 o 75ms, dado que utilizan los dos tubos de rayos X disponibles para adquirir las imágenes. Este avance tecnológico ha facilitado la obtención de estudios coronarios de calidad diagnóstica en pacientes con frecuencia cardiaca elevada y/o ritmo cardiaco irregular31–33, sin necesidad administrar fármacos que controlen la frecuencia cardiaca (habitualmente fármacos betabloqueantes). Además, con este tipo de equipos se ha reintroducido el concepto de «técnica de doble energía» que mejora la caracterización tisular, con resultados prometedores34. Entre las potenciales limitaciones de estos equipos destaca la dosis de radiación administrada a los pacientes con frecuencia cardiaca lenta, que podría resultar ligeramente superior a la aplicada con equipos de TC multicorte convencionales en el mismo grupo de sujetos, según un trabajo experimental35. No obstante, estudios recientes demuestran que la diferencia en la dosis de radiación administrada con estos equipos no es estadísticamente significativa; más aún, en pacientes con frecuencia cardiaca elevada, las dosis de radiación es menor con los equipos de TC dual35,36. Por otra parte, con la idea de incrementar la resolución espacial en el eje-Z (eje longitudinal), se han diseñado equipos de TC volumétricos (hasta 320 detectores), que permiten obtener imágenes del corazón completamente isofásicas37 en un único latido, con un tiempo de rotación mínimo de 350ms38 reduciendo, por tanto, los artefactos. En este sentido, la nueva técnica de adquisición de «pitch-alto» implementada en los equipos de TC-dual más recientes también permite adquirir el estudio cardiaco en un único latido, reduciendo a menos de 1 mSv la dosis de radiación si se utilizan protocolos específicos39 o estudiar todo el tórax en menos de 1 segundo40.
Entre los avances en protocolos de adquisición de TC cardiaco destaca la adquisición de estudios con sincronización con el ECG prospectiva (prospective ECG-triggering)41, la cual permite disminuir de manera significativa la cantidad de radiación que se administra a los pacientes (2,8-4,2 mSv), muy por debajo de la que supone la sincronización con el ECG retrospectiva convencional (8-18 mSv)42–46. La mayor limitación de esta técnica de adquisición es que impide cuantificar los parámetros de función ventricular, excepto si se utilizan los protocolos de adquisición desarrollados más recientemente (flex padding).
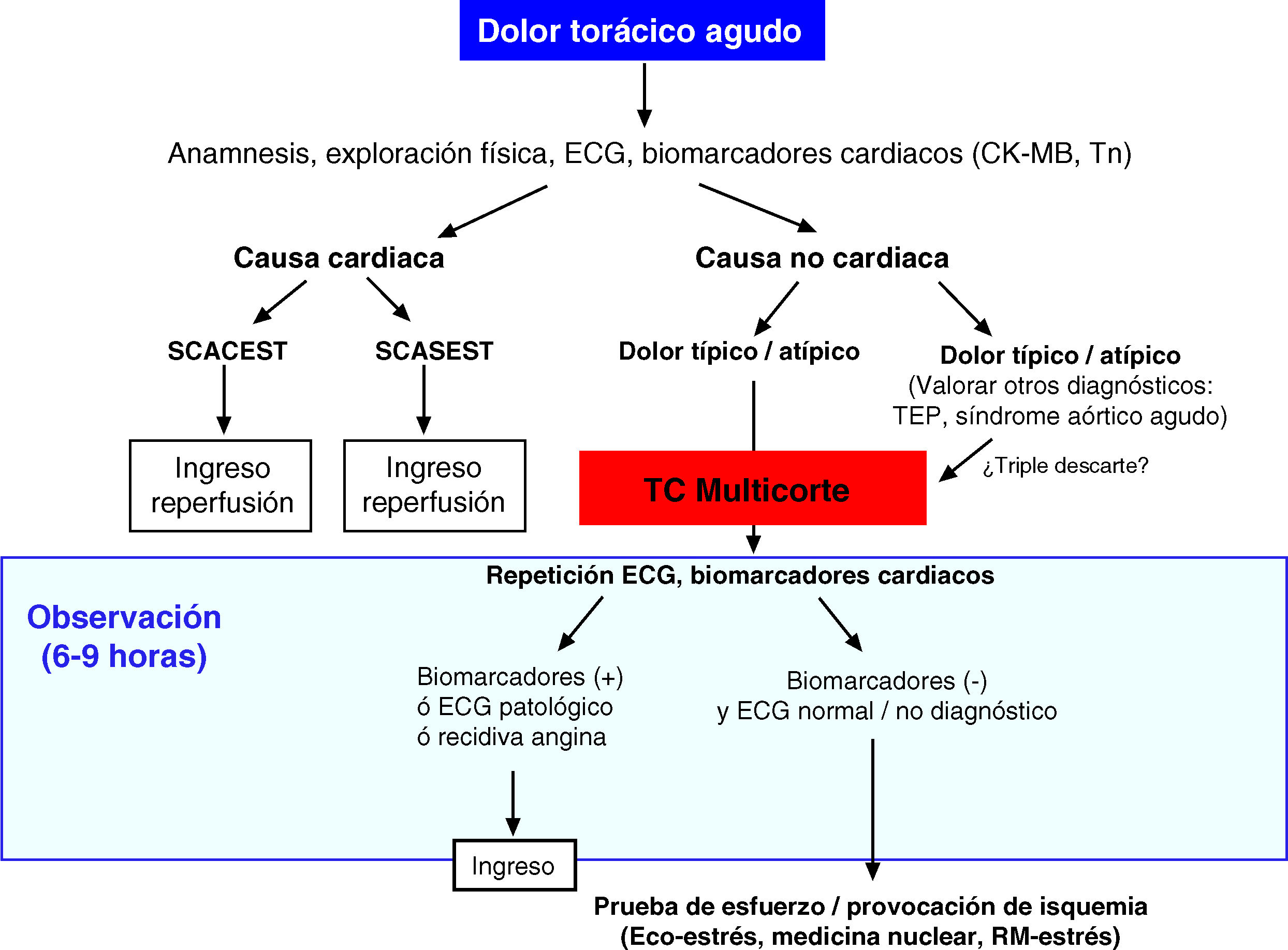
Población de estudio: ¿qué paciente con dolor torácico debemos estudiar mediante TC?Entre el grupo de pacientes que acuden al Servicio de Urgencias por dolor torácico atípico, todavía no se conoce cuál es la población concreta que más se puede beneficiar de un estudio de TCMC. En la práctica clínica habitual, además de la anamnesis, la primera medida que se toma en los pacientes que se presentan en urgencias por dolor torácico es monitorizar su ECG y analizar los biomarcadores cardiacos (troponina [Tn], creatinfosfocinasa [CPK] y creatincinasa MB [CK-MB]). Según sus resultados y de acuerdo con otros parámetros clínicos, se pueden utilizar diferentes algoritmos de estratificación del SCA, entre los que se incluye la escala TIMI (Thrombosis in Myocardial Infarction)47. Según esta escala de riesgo, los pacientes se pueden estratificar en pacientes de alto riesgo (TIMI 5-7), quienes habitualmente son dirigidos al laboratorio de hemodinámica para cateterismo urgente, pacientes de riesgo intermedio (TIMI 3-4) y pacientes de riesgo bajo (TIMI 0-2). En estos dos últimos grupos de pacientes el resultado del ECG y de los biomarcadores suele ser negativo o indeterminado, de manera que estos individuos suelen permanecer en observación durante un periodo de unas 6-9 horas, momento en el que se obtiene un nuevo ECG y se analizan nuevamente los biomarcadores cardiacos para establecer si el dolor torácico se debe o no a una causa cardiaca1. De acuerdo con lo publicado hasta la fecha, es durante ese periodo de observación cuando se propugna la realización del estudio de TCMC (fig. 1), con objeto de reducir o acortar al máximo el tiempo de «incertidumbre diagnóstica». Según los trabajos llevados a cabo en este sentido, realizar un estudio TCMC en el período comprendido entre las dos actuaciones permite reducir el coste derivado del periodo de observación y disminuir el número de ingresos innecesarios. Por supuesto, el éxito del procedimiento depende de la elección apropiada de los pacientes30,48,49 y la adecuada realización de los protocolos de estudio, adaptados a la sospecha clínica y características propias de cada individuo. En la tabla 1 se especifican las contraindicaciones para realizar un estudio cardiaco o de triple descarte por TCMC en pacientes que acuden al Servicio de Urgencias por dolor torácico.
Protocolo de actuación clínica ante el paciente que acude al Servicio de Urgencias por dolor torácico. Los estudios más recientes sugieren realizar un estudio de TCMC a pacientes de riesgo bajo o intermedio con resultado de ECG inicial normal o indeterminado y biomarcadores cardiacos negativos.
Fuente: modificado de Bayón Fernández J et al1.
Contraindicaciones para realizar un estudio cardiaco o de triple descarte con TCMC en pacientes que acuden al Servicio de Urgencias por dolor torácico
| Clínicas: |
| – Elevación de biomarcadores cardiacos (troponina, creatincinasa MB) en la muestra de sangre inicial |
| – Cambios en el ECG sugestivos de síndrome coronario agudo |
| Técnicas: |
| – Antecedentes de reacción alérgica o hipersensibilidad a los agentes yodados |
| – Contraindicaciones relativas: |
| • Embarazo |
| • Edad<40 años |
| • Insuficiencia renal (creatinina sérica>1,5 mg/dl) |
| • Fibrilación auricular o extrasistolia frecuente |
| • Inestabilidad hemodinámica |
| • Contraindicaciones para la administración de beta-bloqueantes (metoprolol) |
| • Contraindicación para la administración de nitroglicerina sublingual |
| • Incapacidad de apnea>15 segundos |
Desde el punto de vista de la valoración del paciente con dolor torácico utilizando la TCMC como técnica de imagen, se ha analizado tres abordajes distintos: la cuantificación de la calcificación coronaria, la coronariografía por TCMC y el estudio de triple descarte o «triple-rule-out». La obtención de estudios cardiacos específicos implica acotar el rango de la exploración al corazón, de manera que si bien es posible estudiar los vasos pulmonares centrales y parte de la aorta ascendente y descendente, un protocolo de estas características no es capaz de detectar émbolos periféricos en los ápices y bases pulmonares. Por el contrario, realizar un estudio torácico completo con sincronización con el ECG implica incrementar de manera significativa la dosis de radiación, administrar más contraste yodado y aumentar la presencia y número de artefactos, sobre todo en pacientes hemodinámicamente inestables o poco colaboradores50.
Por tanto, siguiendo las recomendaciones establecidas, es aconsejable establecer la sospecha clínica con la mayor concreción posible, de manera que se optimice el protocolo de estudio en cada paciente a «su medida». Así, en los pacientes en los que claramente se sospecha una etiología coronaria, es recomendable realizar un estudio cardiaco dirigido, dado que el protocolo de adquisición de este tipo de estudios se encuentra bien establecido y el número de exploraciones no diagnósticas por mala calidad técnica es reducido. Sin embargo, en aquellos pacientes en los que el dolor no sugiera una etiología concreta y se quiera descartar además de la enfermedad coronaria, tromboembolismo pulmonar, patología aórtica u otras posibles causas torácicas, es más recomendable realizar un protocolo que incluya toda la caja torácica. En las tablas 2 y 3 se proponen protocolos de TCMC-64 para cada tipo de estudio. Se trata de protocolos generales, que deberán ser adaptados a cada máquina, a la experiencia de cada centro y a la situación clínica del paciente. Los protocolos para TC-dual se pueden consultar en Bastarrika G et al51 y Arraiza M et al52. Los protocolos de inyección de contraste que se describen son orientativos y deben ajustarse a las características de cada paciente, teniendo en cuenta que la atenuación mínima para el diagnóstico en las arterias coronarias debe ser de 250 UH53.
Protocolo de estudio de coronariografía mediante TCMC-64. Parámetros de adquisición
| Estudio | |
| Rango | Carina-diafragma |
| Dirección | Cráneo-caudal |
| Tiempo | ∼9-12 s |
| Radiación | |
| Voltaje | 120 kVp |
| Corriente | 500-800 mAs |
| Modulación de la dosis | Modulación de la corriente del tubo |
| Adquisición | |
| Colimación | 32×0,6 mm |
| Grosor de corte | 64×0,6 mm |
| Tiempo de rotación | 330 ms |
| Pitch | 0,2 |
| Modo | Secuencial (sincr. ECG-prospectiva)Helicoidal (sincr. ECG-retrospectiva) |
| Medicación | |
| Betabloquantes | Si FC>65 lpm |
| Nitroglicerina | 0,4mg sublingual (comprimido/spray) |
| Contrastea | |
| Vía | Vena antecubital derecha |
| Tamaño de la aguja | 18-20 G |
| Técnica | Bolus tracking |
| Región de interés | Aorta ascendente |
| Umbral | 100 UH |
| Retardo | 6 s |
| Concentración de contraste | 400mg I/ml |
| Cantidad | 80 ml |
| Bolo de suero | 50 ml |
| Flujo | 4-5 ml/s |
| Reconstrucción | |
| Arterias coronarias (GC/IR) | 0,75 mm/0,4 mm |
| Ventana de reconstrucción | Si FC<80 lpm, 70% del ciclo cardiacoSi FC>80 lpm, 40% del ciclo cardiaco |
| Parénquima pulmonar (GC/IR) | 3 mm/3 mm |
| Postproceso | |
| Imágenes axiales | |
| MIP | |
| MPR (curvo) | |
| VR | |
FC: frecuencia cardiaca; G: gauge; GC/IR: grosor de corte/incremento de reconstrucción; kVp: pico de voltaje; lpm: latidos por minuto; mAs: miliamperio segundo; mg: miligramo; mgI: miligramos de yodo; mGy: miliGray; MIP: proyección de máxima intensidad; ml: mililitro; mm: milímetro; MPR: reconstrucción multiplanar; ms: milisegundo; s: segundos; sincr.: sincronización; UH: unidades Hounsfield; VR: reconstrucción volumétrica.
Una variación de este protocolo de administración de contraste, si se quiere administrar menor cantidad, es utilizar un protocolo trifásico con 80ml de contraste (400mg I/ml)+50ml mezcla (30% contraste/70% suero salino)+50ml de suero salino con el ROI en la arteria pulmonar, umbral de 100 UH y retardo de 10 segundos en adquisición cráneo-caudal.
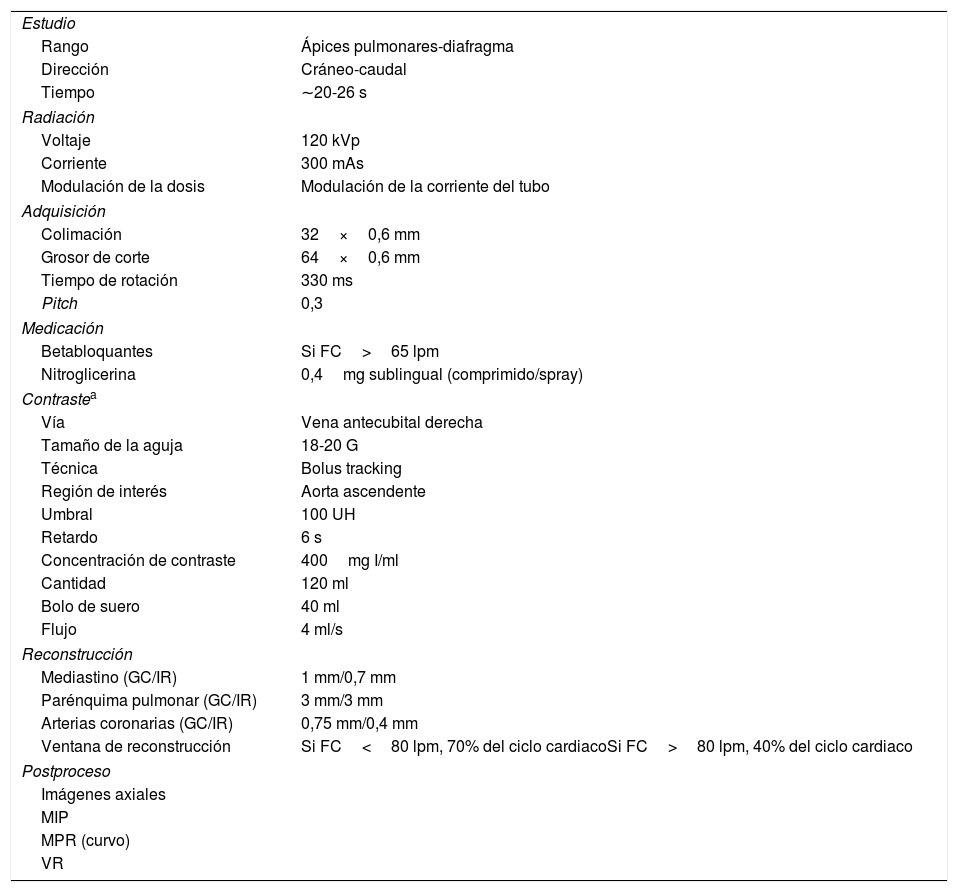
Protocolo de estudio de triple descarte («Triple-rule-out»). Parámetros de adquisición
| Estudio | |
| Rango | Ápices pulmonares-diafragma |
| Dirección | Cráneo-caudal |
| Tiempo | ∼20-26 s |
| Radiación | |
| Voltaje | 120 kVp |
| Corriente | 300 mAs |
| Modulación de la dosis | Modulación de la corriente del tubo |
| Adquisición | |
| Colimación | 32×0,6 mm |
| Grosor de corte | 64×0,6 mm |
| Tiempo de rotación | 330 ms |
| Pitch | 0,3 |
| Medicación | |
| Betabloquantes | Si FC>65 lpm |
| Nitroglicerina | 0,4mg sublingual (comprimido/spray) |
| Contrastea | |
| Vía | Vena antecubital derecha |
| Tamaño de la aguja | 18-20 G |
| Técnica | Bolus tracking |
| Región de interés | Aorta ascendente |
| Umbral | 100 UH |
| Retardo | 6 s |
| Concentración de contraste | 400mg I/ml |
| Cantidad | 120 ml |
| Bolo de suero | 40 ml |
| Flujo | 4 ml/s |
| Reconstrucción | |
| Mediastino (GC/IR) | 1 mm/0,7 mm |
| Parénquima pulmonar (GC/IR) | 3 mm/3 mm |
| Arterias coronarias (GC/IR) | 0,75 mm/0,4 mm |
| Ventana de reconstrucción | Si FC<80 lpm, 70% del ciclo cardiacoSi FC>80 lpm, 40% del ciclo cardiaco |
| Postproceso | |
| Imágenes axiales | |
| MIP | |
| MPR (curvo) | |
| VR | |
FC: frecuencia cardiaca; G: gauge; GC/IR: grosor de corte/incremento de reconstrucción; kVp: pico de voltaje; lpm: latidos por minuto; mAs: miliamperio segundo; mg: miligramo; mgI: miligramos de yodo; mGy: miliGray; MIP: proyección de máxima intensidad; ml: mililitro; mm: milímetro; MPR: reconstrucción multiplanar; ms: milisegundo; s: segundos; sincr.: sincronización; UH: Unidades Hounsfield; VR: reconstrucción volumétrica.
Una variación de este protocolo de administración de contraste, si se quiere administrar menor cantidad, es utilizar un protocolo trifásico con 80ml de contraste (400mg I/ml)+50ml mezcla (30% contraste/70% suero salino)+50ml de suero salino con el ROI en la arteria pulmonar, umbral de 100 UH y retardo de 10 segundos en adquisición cráneo-caudal.
Por supuesto, asumiendo que la dosis de radiación administrada en los estudios de TC es la gran limitación de este tipo de exploraciones, se deben tomar todas las medidas disponibles para mantener la dosis de radiación en el mínimo razonable que permita obtener estudios de calidad diagnóstica. En este sentido, se deben aplicar todas las estrategias disponibles para reducir la dosis de radiación. El requisito más importante es seleccionar apropiadamente el paciente que se va a beneficiar de dicho tipo de estudio30. El protocolo de adquisición, sobre todo en cuanto a los parámetros de exploración, se debe adaptar a las características propias de cada paciente, ajustando el kilovoltaje (kV) y el miliamperaje (mAs) en función de su hábito corporal. Como norma general se suelen emplear 120kV, aunque en sujetos con índice de masa corporal menor de 25kg/m2 se obtienen estudios de buena calidad diagnóstica utilizando protocolos con 100kV, consiguiendo una reducción de la dosis de radiación de aproximadamente un 40-50%. Además, los sistemas de TCMC vienen equipados con técnicas de adquisición específicas que permiten reducir la dosis de radiación. La técnica más ampliamente difundida es la modulación de la corriente del tubo. Con esta técnica se administra la máxima dosis de radiación en la fase del ciclo cardiaco donde es esperable obtener la mejor calidad de imagen de los vasos a estudio, en este caso las arterias coronarias, y se reduce (generalmente al 25% de la corriente nominal del tubo) la dosis de radiación administrada en el resto de las fases del ciclo cardiaco. En general, aunque los rangos pueden variar en función del equipo de TC disponible, se recomienda aplicar máxima dosis de radiación durante el 60-70% del ciclo cardiaco en pacientes con frecuencia cardiaca menor de 60 latidos por minuto (lpm), durante el 50-80% del ciclo cardiaco en pacientes con frecuencia cardiaca comprendida entre 60 y 70 lpm y durante el 35-80% del ciclo cardiaco en pacientes con frecuencia cardiaca superior a 70 lpm. Con esta técnica, se puede obtener estudios cardiacos con unos 9 mSv utilizando equipos de TCMC-6449. La dosis de radiación en estudios cardiotorácicos de triple descarte es significativamente superior (16-17 mSv)54, aunque se sitúa en el rango de la dosis de radiación administrada en otras aplicaciones de TC. De modo comparativo, la dosis de radiación aplicada en una angio-TC convencional (sin sincronización con el ECG), es de aproximadamente 5-7 mSv45. Por tanto, es imprescindible establecer el beneficio/riesgo de este tipo de exploraciones, particularmente en el caso de los estudios de triple descarte. Por último, trabajos recientes subrayan la posibilidad de adquirir los estudios con sincronización con el ECG prospectiva55 o en un único latido40, reduciendo de manera drástica la dosis de radiación administrada.
TC en el paciente con dolor torácico: ¿qué aportan los distintos protocolos de estudio?Cuantificación del calcio coronarioLa calcificación coronaria es un marcador de arteriosclerosis. Se ha demostrado que su cantidad refleja la carga total de placa de ateroma56 pero no posee correlación con la gravedad de la estenosis coronaria57. De acuerdo con los trabajos realizados en la década de los 90, la cuantificación de la calcificación coronaria, medida en la escala de Agatston («Agatston Score»)58, ha sido propuesta como técnica de estratificación del riesgo cardiovascular59,60, habiéndose demostrado que posee valor pronóstico tanto en pacientes sintomáticos como en sujetos asintomáticos61–69. Se conoce que en individuos sintomáticos, una puntuación de calcio coronario de cero posee un elevado valor predictivo negativo para descartar estenosis coronaria hemodinámicamente significativa70. En el contexto clínico concreto de los pacientes con dolor torácico que acuden al Servicio de Urgencias, los estudios realizados con TC de haz de electrones demostraron que la cuantificación de la calcificación coronaria puede ser un método útil de cribado de enfermedad coronaria. En diversos estudios se ha llegado a conclusiones similares: los pacientes con dolor torácico, ECG normal o no diagnóstico y ausencia de calcio coronario (Agatston Score=0) pueden ser dados de alta del Servicio de Urgencias con gran fiabilidad71. Laudon et al72 llevaron a cabo un estudio observacional prospectivo en 105 pacientes consecutivos con dolor torácico a los que se les cuantificó la calcificación coronaria y se les realizó una prueba de esfuerzo según criterio clínico. Estos autores concluyeron que no es necesario realizar exploraciones complementarias a pacientes con enzimas cardiacos iniciales normales, hallazgos de ECG normales o indeterminados y una puntuación de calcio nula. En un estudio prospectivo realizado en 192 pacientes con dolor torácico, Georgiou et al62 demostraron un incremento en la tasa de eventos anuales en sujetos con puntuaciones elevadas de calcio coronario respecto a pacientes sin calcificación coronaria, concluyendo que en esta población la ausencia de calcio coronario implica un riesgo bajo de eventos cardiacos futuros (< 1% anual).
Actualmente, el estudio para cuantificar la calcificación coronaria forma parte de la mayoría de los protocolos de cardio-TC. Por una parte, permite afinar en la estratificación del riesgo cardiovascular de los pacientes y, por otra, aporta información para planificar la coronariografía por TCMC. La decisión acerca de realizar o no el estudio con contraste en función de la cantidad de calcio coronario que se encuentre en el paciente, es controvertida73. Por una parte, en pacientes con elevada cantidad de calcio, la coronariografía por TCMC puede diagnosticar lesiones significativas en segmentos coronarios no calcificados; sin embargo, la calcificación extensa supone una gran limitación para visualizar la luz vascular. En general, se considera como mayor determinante la localización y extensión de las placas calcificadas en el árbol coronario, más que la propia puntuación de Agatston. Como recomendación, ante cada paciente individual, si se presupone que la calcificación detectada va a impedir una valoración adecuada de los segmentos arteriales más importantes o de mayor calibre, se debe plantear el beneficio/riesgo de realizar el estudio cardiaco con contraste (coronariografía por TCMC).
Estudio cardiaco por TCEn el año 2005, Sato et al74 publicaron uno de los primeros estudios de evaluación de la eficacia de la TCMC-4 y TCMC-16 para diagnosticar un SCA en el Servicio de Urgencias, definido como estenosis coronaria ≥ 75% asociada a placas de ateroma de baja atenuación y/o defectos de perfusión miocárdicos, concluyendo que la TCMC posee una sensibilidad del 95,5% y una especificidad del 88,9% para diagnosticar esta entidad. En su estudio preliminar, Hoffmann et al75 incluyeron 40 pacientes con dolor torácico, enzimas cardiacos normales y ECG sin cambios sugestivos de isquemia a los que se realizó una coronariografía por TCMC durante el periodo de observación, previo al ingreso. Los autores concluyeron que el empleo de la TCMC en este contexto puede disminuir el número de pacientes que son ingresados de forma innecesaria. Posteriormente, el mismo grupo de trabajo realizó un estudio prospectivo en 103 pacientes, observando que la ausencia de estenosis coronaria significativa predice la ausencia de SCA durante la hospitalización y durante un periodo de seguimiento de 5 años76 (fig. 2). En un estudio aleatorio realizado en sujetos con dolor torácico y bajo riesgo, Goldstein et al77 compararon el rendimiento de la TCMC (99 pacientes) frente al estándar clínico habitual (98 pacientes) (ECG seriado, biomarcadores cardiacos y estudio de perfusión miocárdica el mismo día) demostrando que en pacientes con dolor torácico y bajo riesgo, la TCMC posee una exactitud similar al estándar clínico habitual para diagnosticar un SCA, con el valor añadido de que acorta el tiempo de observación y reduce costes. Rubinstein et al78 evaluaron la utilidad de la TCMC para el despistaje inicial de 58 pacientes con sospecha de SCA y estudiaron su evolución durante 15 meses. El hallazgo principal de este trabajo fue que no ocurrió ningún fallecimiento en sujetos que fueron dados de alta en base a un estudio cardiaco por TCMC normal. En un trabajo más reciente realizado en 568 pacientes con dolor torácico y bajo riesgo de SCA los autores observaron que del 84% de los pacientes dados de alta de acuerdo con un resultado negativo en la TCMC, ninguno experimentó un evento cardiaco en los siguientes 30 días79. Recientemente, se ha llevado a cabo el estudio observacional ROMICAT (Rule Out Myocardial Infarction using Computer Assisted Tomography) en 368 pacientes con troponinas iniciales normales y ECG no sugestivo de isquemia con objeto de detectar estenosis coronaria > 50% y placas de ateroma80. En este estudio, la sensibilidad y el valor predictivo de la prueba para SCA fue del 100% en ausencia de enfermedad coronaria y del 77 y 98% en caso de que existiera estenosis coronaria significativa. De acuerdo con sus resultados, los autores concluyeron que tanto la cantidad de placas de ateroma como la presencia de estenosis coronaria por TCMC predicen el SCA de manera independiente y añadida a la escala de riesgo TIMI (áreas bajo la curva de 0,88; 0,82; frente a 0,63, respectivamente)80.
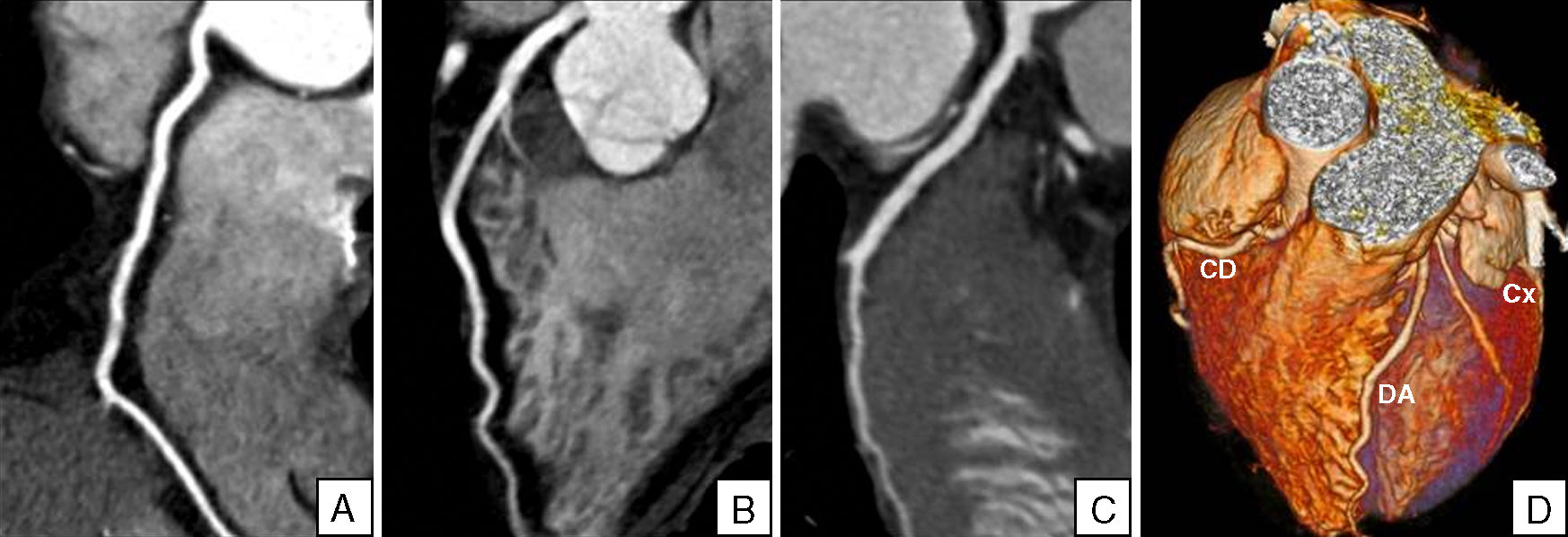
Coronariografía por TCMC en mujer de 56 años que acudió al Servicio de Urgencias por dolor torácico. A, B, C) Reconstrucciones multiplanares curvas. D) Reconstrucción volumétrica. La arteria coronaria derecha (A), descendente anterior (B) y circunfleja (C) fueron normales, descartándose enfermedad coronaria.
CD: arteria coronaria derecha; Cx: arteria coronaria circunfleja; DA: arteria coronaria descendente anterior.
Las conclusiones más importantes que se pueden extraer de los trabajos descritos son: 1) si bien los resultados observados en los estudios dependen en gran medida de la prevalencia de enfermedad coronaria en los pacientes incluidos, la coronariografía por TCMC es capaz de confirmar o descartar lesiones coronarias hemodinámicamente significativas en la mayoría de los sujetos con riesgo bajo o intermedio; 2) una minoría de los pacientes estudiados mediante TCMC requiere un test de provocación de isquemia debido a que en la TCMC se han detectado lesiones indeterminadas o los estudios de TCMC no han sido concluyentes; 3) la TCMC posee un elevado valor predictivo negativo para el despistaje del dolor torácico, y 4) el desenlace final de los pacientes en los que se realizó una TCMC fue similar al que se hubiera obtenido de acuerdo con el estándar clínico habitual empleado para evaluar el SCA en el Servicio de Urgencias. Entre los estudios que actualmente se están llevando a cabo o han sido diseñados para analizar la utilidad de la TCMC en los pacientes con dolor torácico destacan el CT-STAT, ROMICAT-II (http://www.romicat.org) y el promocionado por la Red de Imagen del Colegio Americano de Radiología (American College of Radiology Imaging Network-ACRIN, http://www.acrin.org), ACRIN PA 4005. Por supuesto, además de patología coronaria, este tipo de estudio también permite diagnosticar otras causas cardíacas de dolor torácico como miocarditis, pericarditis (fig. 3), etc.
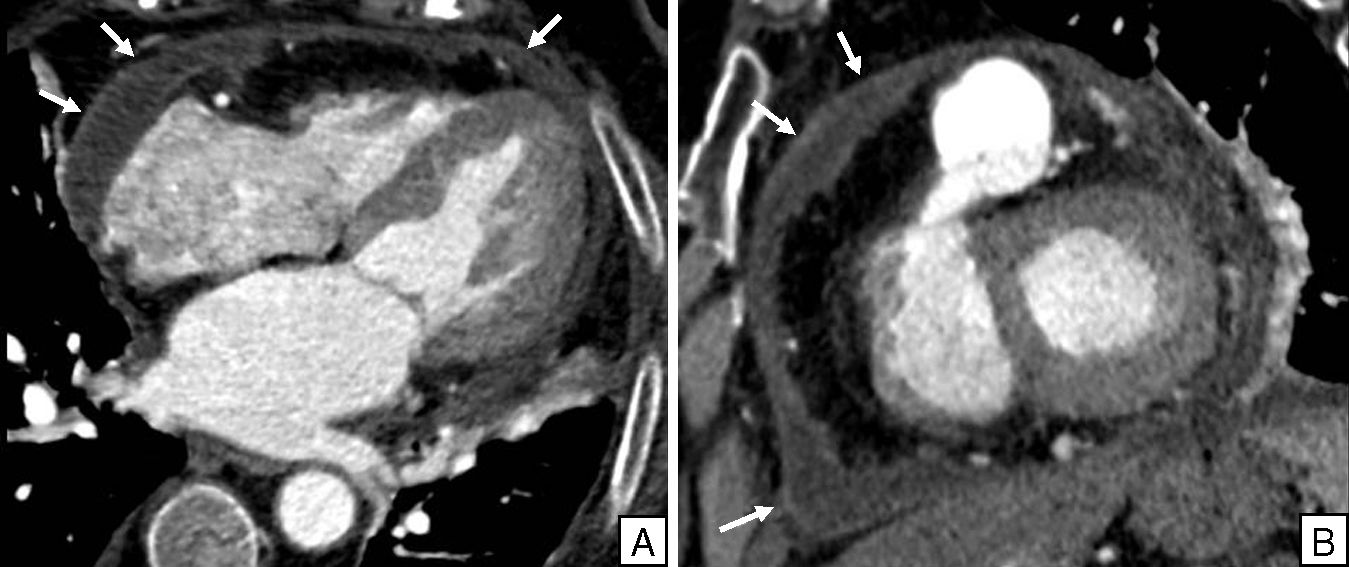
Coronariografía por TCMC en mujer de 64 años que acudió al Servicio de Urgencias por dolor torácico, malestar y fiebre de dos días de evolución. A) Plano de cuatro cámaras. B) Plano eje corto. El estudio cardiaco mostró derrame pericárdico circunferencial con captación de contraste por parte del pericardio (flechas), sugestivo de pericarditis aguda.
No obstante, a pesar del gran potencial que posee la coronariografía por TCMC, subrayado en numerosas publicaciones, se deben señalar algunos aspectos que limitan la generalización del empleo de la TCMC en pacientes con dolor torácico. Por una parte, como se ha descrito, un número de pacientes precisará exploraciones complementarias, habitualmente técnicas de perfusión miocárdica, debido a que los resultados de la TCMC son indeterminados o no concluyentes. Así, una lesión significativa puede tratarse de un hallazgo incidental y no ser necesariamente la causa del dolor torácico referido por el paciente. Por otra parte, considerando que la estenosis coronaria es un hallazgo morfológico, en las lesiones intermedias es preciso realizar pruebas de provocación de isquemia para determinar su repercusión fisiológica o funcional. Además, existen limitaciones inherentes a la propia técnica de TCMC como son por ejemplo las arritmias, las frecuencias cardiacas elevadas, la calcificación coronaria extensa o los stents coronarios de pequeño tamaño (< 3mm), situaciones que impiden obtener estudios de calidad diagnóstica o realizar una valoración óptima en todos los pacientes. Más aún, como se ha comentado, la dosis de radiación de este tipo de estudios no se debe ignorar, aunque cabe señalar que la dosis administrada se encuentra en el rango de las dosis empleadas en la pruebas de detección de isquemia basadas en técnicas de Medicina Nuclear81. Por tanto, la coronariografía por TCMC parece que va a ser una herramienta de gran utilidad en el cribado del dolor torácico en los Servicios de Urgencias pero el rendimiento diagnóstico de la técnica dependerá en gran medida del adecuado uso de la misma.
Estudio cardiotorácico (Triple descarte o «Triple-rule-out»)Si bien con generaciones anteriores de equipos de TC se requería realizar protocolos complejos para estudiar el tórax, los nuevos TCMC permiten estudiar toda la cavidad torácica en una apnea de duración corta, optimizando aún más la utilización del material de contraste82,83, de manera que es posible evaluar todos los vasos de interés con calidad diagnóstica. La gran ventaja de utilizar un protocolo que incluya todo el tórax y no únicamente el corazón en el paciente con dolor torácico atípico viene dada por la posibilidad de detectar hallazgos no vasculares como etiología de dicho dolor84.
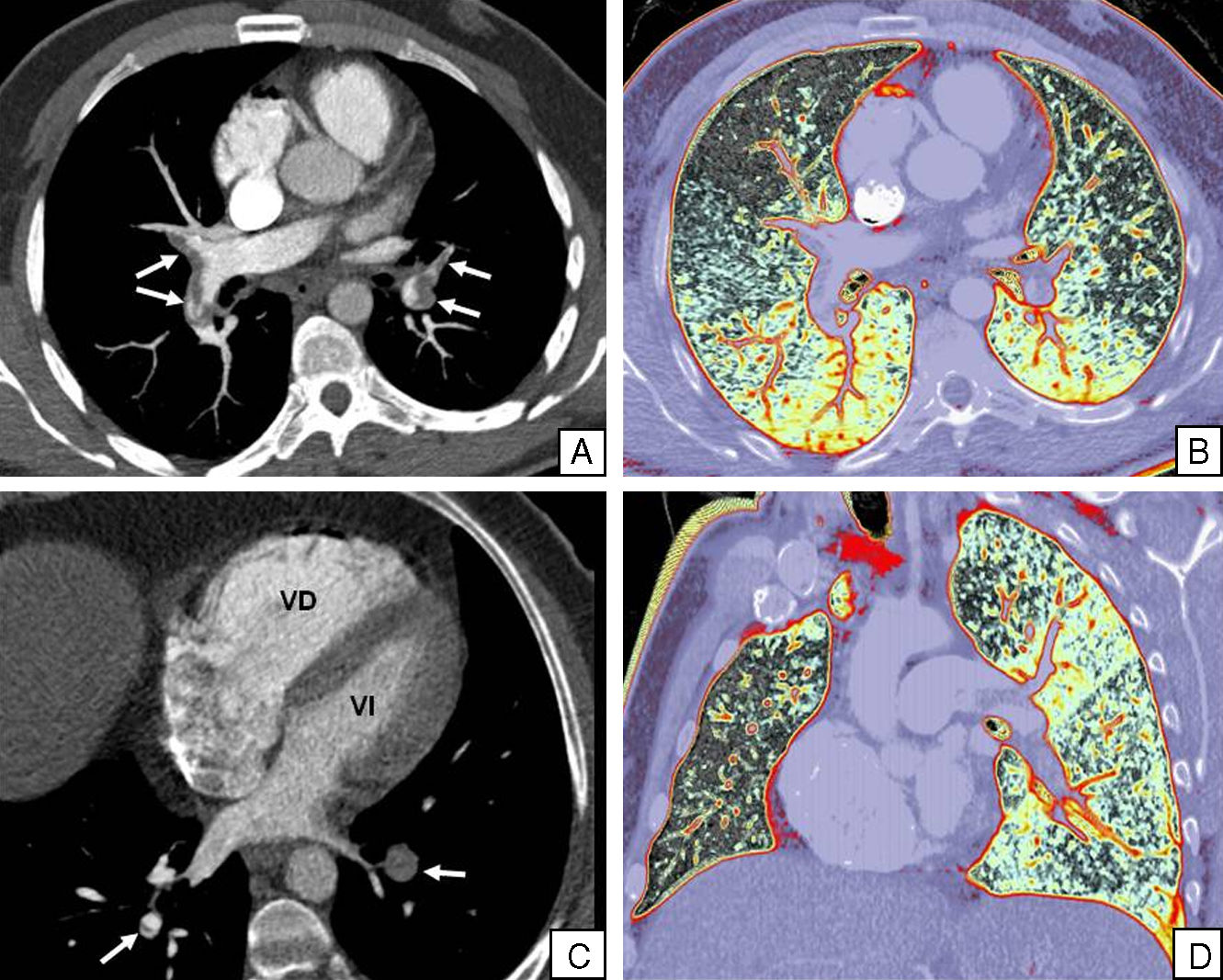
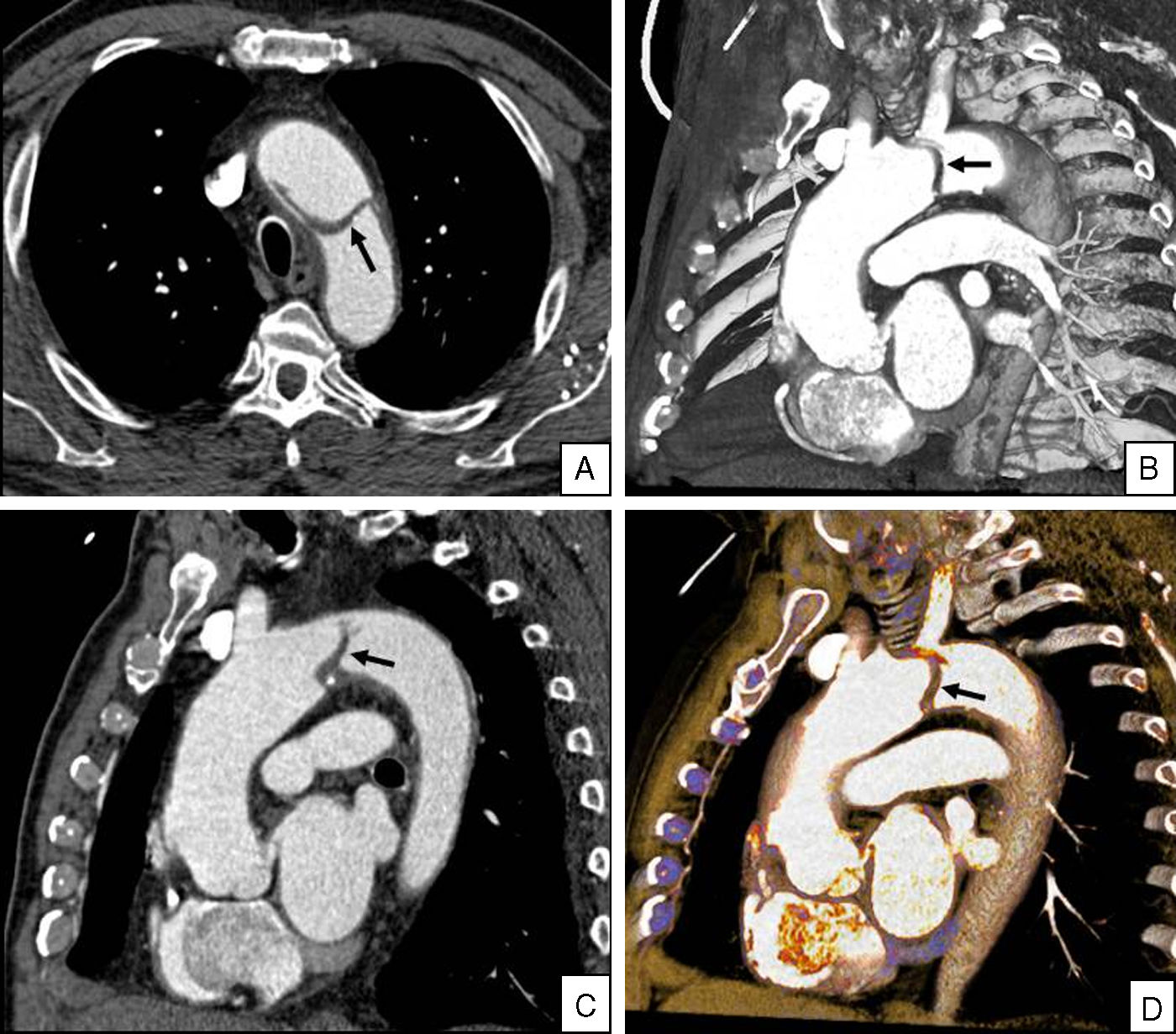
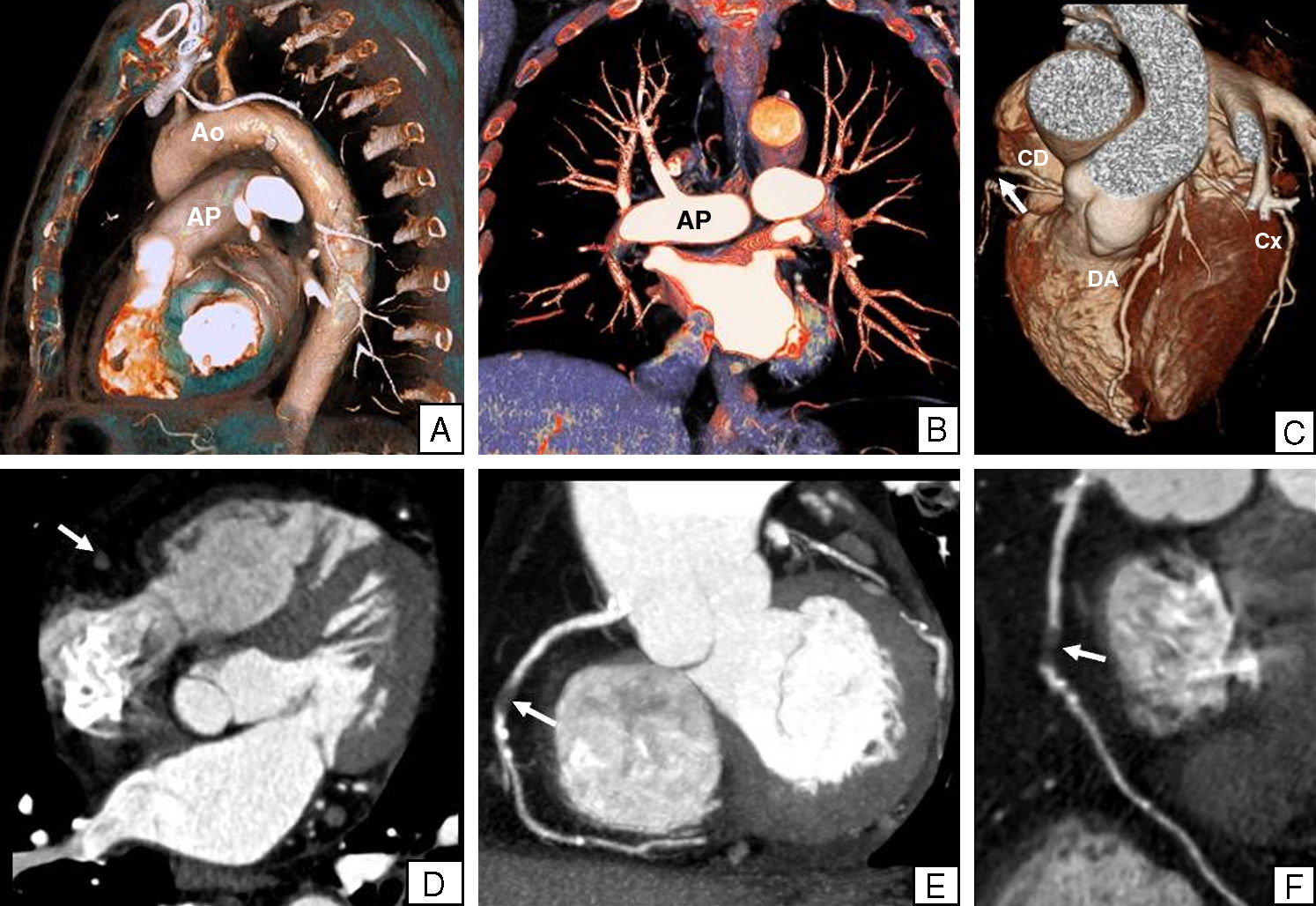
Desde hace años, la TCMC se ha consolidado como técnica de primera elección para diagnosticar el tromboembolismo pulmonar18–20 y el síndrome aórtico agudo21,22. La sincronización con el ECG ha aportado el valor añadido de permitir diagnosticar enfermedad coronaria en pacientes con dolor torácico. Así, en el caso de la embolia pulmonar, además de detectar el trombo, la TCMC también puede mostrar dilatación comparativa del ventrículo derecho (diámetro VD/VI>1,5), signo que aporta valor pronóstico (fig. 4); la sincronización con el ECG es especialmente útil en este entidad, dado que de esta manera se puede cuantificar con exactitud la función ventricular derecha85, más allá de la mera medición de diámetros. En el caso de la disección aórtica (fig. 5), la sincronización con el ECG permitirá establecer la extensión de la disección en casos de disecciones tipo A, que afectan a la aorta ascendente, al demostrar si el «flap» intimal se extiende o no al plano valvular aórtico o al ostium de las arterias coronarias. Por tanto, la TCMC con sincronización con el ECG es una herramienta diagnóstica potencialmente capaz de descartar las causas de dolor torácico de mayor morbimortalidad. Este abordaje, conocido como «Triple estudio», «estudio de triple descarte» o «Triple-rule-out» constituye, por tanto, una aproximación diagnóstica única para diferenciar la etiología cardiovascular de la no cardiovascular en los pacientes que acuden a urgencias por dolor torácico. Por tanto, a diferencia de los protocolos arriba descritos, es decir, los basados únicamente en realizar un estudio cardiaco dirigido (coronariografía por TC), este tipo de estudio posee la ventaja de poder excluir la patología aórtica aguda, el tromboembolismo pulmonar y la enfermedad coronaria en una única exploración (fig. 6), así como otras posibles causas de dolor torácico que aunque no suponen un riesgo vital para el paciente, sí pueden justificar la sintomatología clínica referida. Entre las mismas destacan las causas musculoesqueléticas (fracturas, hernias discales, etc.), lesiones pleurales o pulmonares, hernia de hiato y procesos que afectan al tracto digestivo superior como colecistitis, pancreatitis, pielonefritis, etc.
Estudio de TCMC de triple descarte en paciente de 48 años con dolor torácico y disnea de cinco horas de evolución. A) Imagen axial. B) Reconstrucción volumétrica axial. C) Reconstrucción multiplanar en el plano cuatro cámaras. D) Reconstrucción volumétrica coronal oblicua. El estudio mostró tromboembolismo pulmonar bilateral central y periférico (flechas), con signos de sobrecarga de presión y disfunción ventricular derecha (nótese en C, el aumento comparativo del diámetro del ventrículo derecho –VD, respecto al diámetro del ventrículo izquierdo –VI) y defectos de perfusión pulmonar, más evidentes en las reconstrucciones volumétricas (B, D).
Estudio de TCMC de triple descarte en paciente hipertenso de 68 años con dolor centrotorácico súbito. A) Imagen axial. B) Reconstrucción volumétrica sagital oblicua. C) Reconstrucción multiplanar sagital oblicua. D) Reconstrucción volumétrica sagital oblicua. Disección aórtica con «flap» intimal localizado en el cayado aórtico (flechas), extendiéndose al origen de la arteria subclavia izquierda.
Estudio de TCMC de triple descarte en paciente fumador de 57 años con antecedentes familiares de cardiopatía isquémica. A, B, C) Reconstrucciones volumétricas de la aorta (A), arterias pulmonares (B) y corazón (C). D) Imagen axial. E) Reconstrucción multiplanar MIP. F) Reconstrucción multiplanar curva. La aorta (Ao) y las arterias pulmonares (AP) no mostraron alteraciones significativas. El estudio cardiaco puso de manifiesto una estenosis significativa, con práctica oclusión (flechas) de la arteria coronaria derecha en su tercio medio.
CD: arteria coronaria derecha; Cx: arteria coronaria circunfleja; DA: arteria coronaria descendente anterior.
Los primeros trabajos que demostraron el potencial de este tipo de protocolos de adquisición se realizaron con equipos TCMC-1684. Posteriormente, debido a la mayor resolución espacial y temporal de los equipos de TCMC-64, el número de estudios llevados a cabo con el fin de demostrar la utilidad de esta técnica diagnóstica se incrementó de manera significativa86. Como ejemplo, Savino et al82 demostraron que en pacientes con dolor torácico, la TCMC cardiotorácica permitía disminuir los costes asistenciales en los Servicios de Urgencias y acortar los días de hospitalización. Los mayores inconvenientes de este tipo de exploraciones son, sin embargo, que los protocolos de adquisición no se encuentran totalmente establecidos y varían entre los distintos centros en función de la experiencia adquirida, que es necesario administrar mayor cantidad de contraste y radiación que al realizar un estudio cardiaco específico87 y que la resolución temporal de los equipos de TCMC-64 puede resultar insuficiente, particularmente para estudiar las arterias coronarias88. En este sentido, los trabajos realizados con TC-dual han demostrado que esta técnica puede superar en parte las limitaciones descritas, sobre todo al reducir el número de segmentos coronarios no evaluables89–91.
ConclusionesLa TCMC, particularmente los equipos de TCMC-64 o superiores, se vislumbra como una herramienta de gran utilidad clínica para el diagnóstico del paciente con dolor torácico atípico. El estudio de este grupo de pacientes se puede realizar desde distintas perspectivas, utilizando protocolos sencillos que únicamente se basan en la cuantificación de la calcificación coronaria, o protocolos que tras administrar contraste intravenoso permiten estudiar el corazón y los vasos coronarios o realizar un estudio exhaustivo de la patología cardiotorácica y pulmonar. La elección de cada protocolo dependerá de las características propias de cada paciente y de la sospecha clínica inicial, manteniendo siempre en el mínimo posible los posibles efectos adversos de esta tecnología, particularmente en cuanto a la dosis de radiación y cantidad de contraste se refiere. El beneficio potencial de la angiografía por TCMC con sincronización con el ECG realizada en el paciente apropiado parece superar sus riesgos y la introducción de esta tecnología en los Servicios de Urgencias se perfila como una herramienta coste-efectiva al permitir realizar el diagnóstico de manera rápida y exacta, disminuyendo el número de ingresos inapropiados y por tanto, reduciendo los costes derivados.
AutoríaConcepción del estudio: Bastarrika, Schoepf.
Redacción y revisión crítica del trabajo: Bastarrika.
Aprobación final de la versión enviada para publicar: Bastarrika, Schoepf.
Conflicto de interesesEl D. G. Bastarrika declara percibir financiación de Bayer-Schering, General Electric, Medrad y Siemens. El Dr. U.J. Schoepf es consultor médico de Bayer-Schering, Bracco, General Electric, Medrad y Siemens.