La evaluación del dolor torácico con electrocardiograma y biomarcadores negativos representa un desafío para el clínico. Como estrategia adicional se utilizan varias escalas para la estratificación pronóstica. Se describe el rendimiento diagnóstico de dichas escalas para los síndromes coronarios agudos en pacientes de alta probabilidad, con electrocardiograma y biomarcadores negativos.
MetodologíaEstudio de pruebas diagnósticas en una cohorte de pacientes mayores de 18 años ingresados a 2 hospitales de tercer nivel por dolor torácico y sospecha de síndrome coronario agudo, sin cambios electrocardiográficos ni elevación de biomarcadores. Como referente diagnóstico se utilizaron diversas pruebas de estratificación coronaria y para la prueba índice se incluyeron las diferentes escalas para la evaluación del pronóstico en dolor torácico. Se calcularon las características operativas en diferentes puntos de corte y se compararon las áreas bajo la curva ROC.
ResultadosSe incluyó a 86 pacientes cuyo promedio de edad fue 63 años (DE: 12); el 61,6% fueron hombres y 51,2% tuvieron diagnóstico de angina. La escala HEART tuvo el mejor desempeño, con un área bajo la curva de 0,65, seguida por la GRACE con 0,61. Los intervalos de confianza se sobreponían entre las diferentes escalas evaluadas.
ConclusiónLas escalas de predicción de riesgo en pacientes con dolor torácico, evaluadas con fines diagnósticos, mostraron un pobre poder discriminatorio en una población de pacientes de alto riesgo pese a tener electrocardiograma y troponina negativos.
The evaluation of chest pain in cases where electrocardiogram and biomarkers are negative represent a challenge for the clinician. Severe scales are now being used as an additional strategy for the prognosis stratification. The objective of the present study is to describe the diagnostic performance of the diagnostic scales for acute coronary symptoms in patients with high probability and in whom the electrocardiogram and biomarkers are negative.
MethodologyA study of the diagnostic tests in a cohort of patients older than 18 years old, who were admitted into 2level-3 hospitals due to chest pain and suspicion of acute coronary syndrome with no changes in the electrocardiogram or increases in biomarkers. Different coronary stratification tests were used as a diagnostic reference, and the different scales for evaluating the prognosis in chest pain were included for the index test. The operational characteristics were calculated for different cut-off points, and the areas under the ROC curve were compared.
ResultsThe study included a total of 86 patients. The mean age was 63 years old, with 61.6% men, and 51.2% of the patients had a diagnosis of angina. The HEART scale gave a better performance, with an area under the curve of 0.65, followed by the GRACE scale with 0.61. The confidence intervals overlapped the different evaluation scales.
ConclusionThe scales of risk prediction in patients with chest pain, evaluated for diagnostic purposes, showed a lower discriminatory power in a population of patients with high risk, despite having a negative electrocardiogram and troponin.
El dolor torácico representa la segunda causa de consulta en los servicios de urgencias de acuerdo con una encuesta realizada en el 2006 por el NHAMCS en EE. UU.1. De estos casos, menos del 5% representan un infarto con elevación de ST y alrededor del 20% son debidos a síndromes coronarios agudos (SCA) sin elevación de ST2. La mayor parte de las veces el dolor torácico es causado por otras condiciones3, que con frecuencia son de curso benigno. Durante su evaluación prima el descartar los SCA, lo que conlleva el consumo de una gran cantidad de recursos4.
Así pues, un aspecto que ha sido considerado fundamental en la valoración de los dolores torácicos es la correcta identificación de pacientes con bajo riesgo para desarrollar eventos adversos cardiovasculares, con el fin de darlos de alta del servicio de urgencias de manera temprana y segura, para disminuir la congestión y limitar la necesidad de hospitalizaciones innecesarias, con la carga económica que esto acarrea2. Si bien la incursión de las troponinas de alta sensibilidad en los últimos años ha favorecido que se cometan menos errores al descargar pacientes5, aún no está perfectamente establecido cuáles son los lineamientos finales en esta dirección.
Es por ello por lo que se han intentado desarrollar y aplicar diversas escalas para evaluar el riesgo de eventos cardiovasculares, algunas de ellas extrapoladas de su experiencia con los SCA, aplicadas para evaluar el dolor torácico, como TIMI, GRACE6,7 y una variación del TIMI con 3de sus variables llamada CARdiac8; otras, diseñadas específicamente para los dolores torácicos de baja probabilidad como la de Florencia9 y Sanchís10 y una para una población más diversa de dolor torácico, la de HEART11. Todas ellas han demostrado aumentar el poder discriminatorio que ostenta la troponina.
El objetivo del presente trabajo es evaluar el rendimiento de diversas escalas de riesgo para el diagnóstico de SCA en pacientes sin cambios electrocardiográficos isquémicos ni elevación de los niveles de troponinas.
MétodosSe realizó un estudio de pruebas diagnósticas en una cohorte prospectiva en la que se incluyó de manera consecutiva a pacientes mayores de 18 años de edad que ingresaron por dolor torácico con sospecha de SCA, en los que no se evidenciaran cambios isquémicos electrocardiográficos (desviación del segmento ST de más de 0,5mm, cambios de la onda T o presencia de ondas Q patológicas en 2o más derivaciones) ni elevación de la troponina, hospitalizados en el Servicio de Urgencias o en la Unidad de Cuidado Coronario de 2hospitales universitarios de tercer nivel de atención, el Hospital de San José y el Hospital Infantil Universitario de San José, ambos localizados en Bogotá, durante el periodo comprendido entre el 1 de junio de 2014 y el 29 de febrero de 2016.
El estándar de referencia para el diagnóstico consistió en diferentes estrategias de estratificación coronaria invasiva (arteriografía coronaria) o no invasiva de imagen (perfusión miocárdica o ecoestrés) realizadas durante la hospitalización del paciente en cualquiera de los servicios del hospital. Se tuvieron en cuenta, además, algunos casos en los que a través de algún otro medio diagnóstico se lograra, de manera inequívoca, la asignación diagnóstica de otras causas del dolor torácico, por ejemplo, una tomografía de tórax para un embolia pulmonar.
Como prueba índice se tomaron las diferentes escalas o nomogramas utilizados para la evaluación del riesgo de presentar eventos cardiovasculares mayores en pacientes con dolor torácico. Dichas escalas se basan en componentes de la historia clínica, en especial los demográficos, las características del dolor torácico, los antecedentes, algunos datos del examen físico y los resultados del electrocardiograma y de los biomarcadores de lesión miocárdica. Se tuvieron en cuenta las escalas de TIMI y la GRACE originadas para la evaluación del riesgo en pacientes con SCA; las de Florencia y Sanchís, específicamente desarrolladas para la evaluación de riesgo en pacientes con dolor torácico de bajo riesgo (por lo que no se incluyen datos del electrocardiograma ni de los biomarcadores) y, por último, la escala HEART para evaluar una población no seleccionada con dolores torácicos.
A partir de la revisión de las historias aportadas por cada uno de los pacientes, se extrajeron los datos demográficos, de presentación del dolor torácico, antecedentes, examen físico, electrocardiograma y biomarcadores de lesión miocárdica para el cálculo de cada una de las escalas, así como datos de los resultados de las diferentes formas de estratificación coronaria con los cuales se llegó al diagnóstico del SCA. Para el análisis de la información se construyó una base de datos en Excel 2010.
Las variables categóricas se expresan con frecuencias absolutas y relativas, las cuantitativas con medidas de tendencia central y dispersión según su distribución. Se realizó el análisis univariado para evaluar la asociación de cada uno de los factores de riesgo descritos con el desenlace de presentar angina. Después se calcularon las características operativas para el diagnóstico de angina de cada una de las escalas evaluadas a partir de diferentes tablas de contingencia (de 2×2) en diferentes puntos de corte, y se obtuvieron las sensibilidades, especificidades, valores predictivos y razones de verosimilitud (likelihood ratio [LR]), para luego realizar la comparación de las áreas bajo la curva (AUC) ROC no paramétrica; además, se calculó para cada una de ellas los intervalos de confianza del 95%. El análisis estadístico se realizó en STATA 13.
El estudio fue aprobado por el Comité de Investigaciones y el Comité de Ética en Investigación de la Facultad de Medicina de la Fundación Universitaria Ciencias de la Salud y del Hospital de San José de Bogotá.
ResultadosSe recolectó a 86 sujetos de investigación cuyo promedio de edad fue 63 años (DE 12 años); 54 (62,8%) eran de sexo masculino, 44 (51,2%) pacientes fueron catalogados con angina mientras que a los 42 (48,8%) restantes se les descartó SCA. La estrategia diagnóstica más usada fue a través de los métodos no invasivos en 37 (43%) pacientes, seguida por la coronariografía en 35 (40%). La distribución de comorbilidades indicó que en el 26,7% había antecedente de diabetes de tipo 2; que el 10,5% tenían enfermedad renal crónica y en el 48,8% de los casos había historia de enfermedad coronaria.
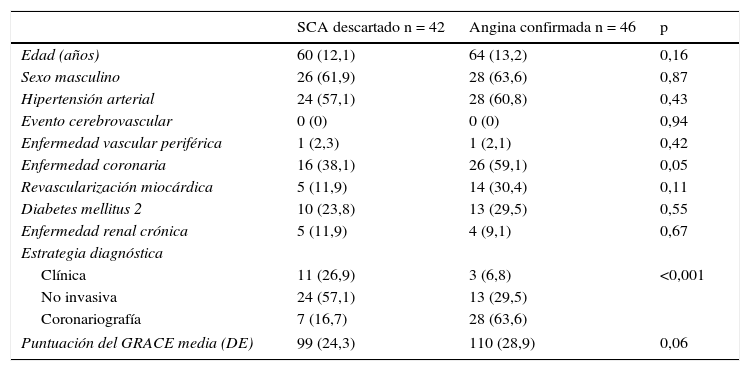
A diferencia de los pacientes en los que se descartó un SCA, se encontró que en los que se diagnosticó angina tenían una mayor presencia del antecedente de enfermedad coronaria previa, fueron evaluados con coronariografía de manera más frecuente y tuvieron una tendencia hacia una mayor puntuación en la escala de GRACE y a ser de mayor edad (tabla 1).
Características demográficas de la población
| SCA descartado n = 42 | Angina confirmada n = 46 | p | |
|---|---|---|---|
| Edad (años) | 60 (12,1) | 64 (13,2) | 0,16 |
| Sexo masculino | 26 (61,9) | 28 (63,6) | 0,87 |
| Hipertensión arterial | 24 (57,1) | 28 (60,8) | 0,43 |
| Evento cerebrovascular | 0 (0) | 0 (0) | 0,94 |
| Enfermedad vascular periférica | 1 (2,3) | 1 (2,1) | 0,42 |
| Enfermedad coronaria | 16 (38,1) | 26 (59,1) | 0,05 |
| Revascularización miocárdica | 5 (11,9) | 14 (30,4) | 0,11 |
| Diabetes mellitus 2 | 10 (23,8) | 13 (29,5) | 0,55 |
| Enfermedad renal crónica | 5 (11,9) | 4 (9,1) | 0,67 |
| Estrategia diagnóstica | |||
| Clínica | 11 (26,9) | 3 (6,8) | <0,001 |
| No invasiva | 24 (57,1) | 13 (29,5) | |
| Coronariografía | 7 (16,7) | 28 (63,6) | |
| Puntuación del GRACE media (DE) | 99 (24,3) | 110 (28,9) | 0,06 |
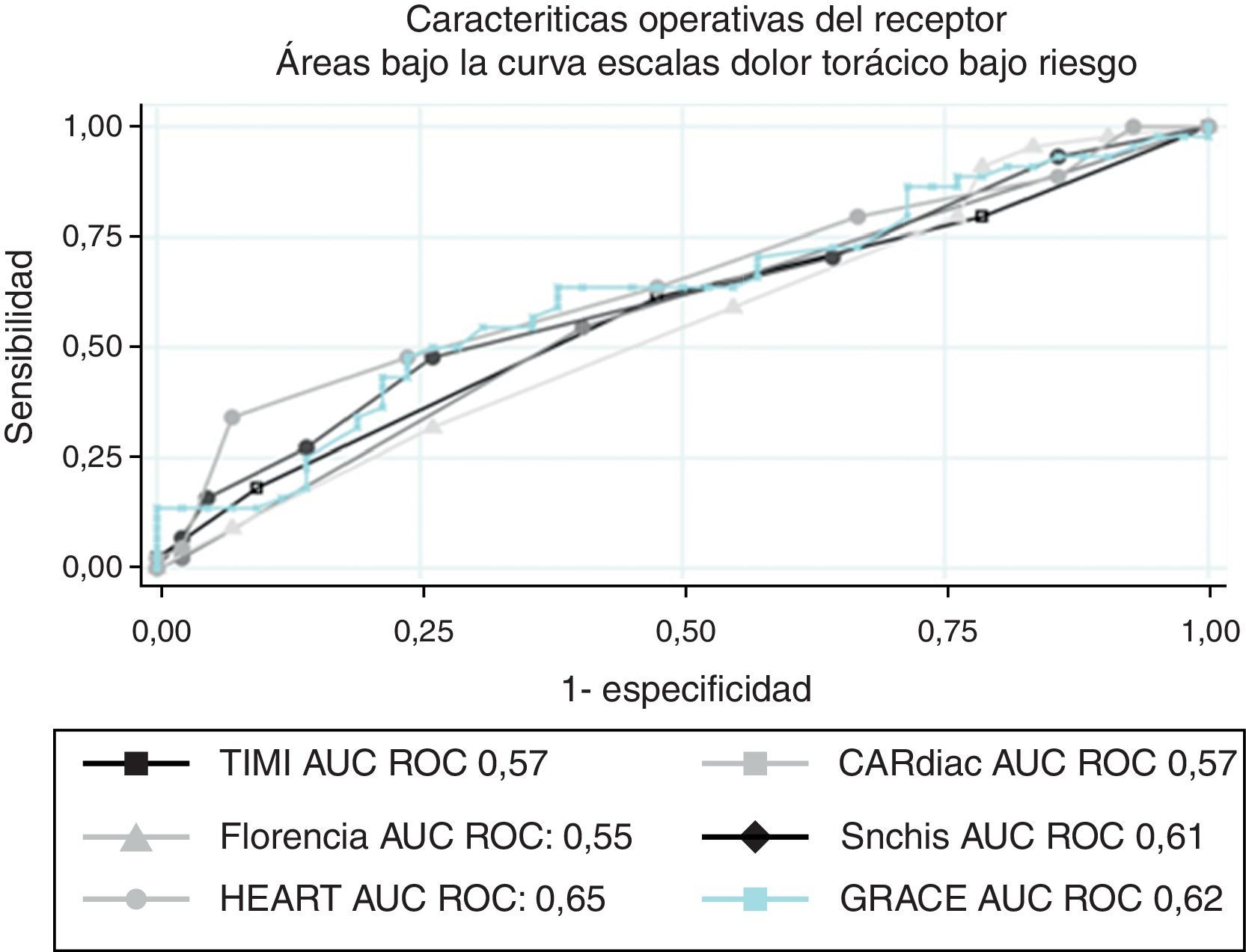
Al evaluar las AUC ROC (fig. 1) se encuentra que todas las escalas muestran un pobre poder de discriminación (AUC por debajo de 0,7): la escala de HEART fue la que tuvo el mejor desempeño para el diagnóstico de angina inestable, con 0,65. Se evidencia además una superposición en los intervalos de confianza, por lo que no puede hablarse de diferencias sustanciales en el rendimiento de cada una de ellas.
En las tablas 2 y 3 se exponen los resultados del desempeño de cada una de las escalas TIMI y HEART. De ellas podemos resumir que existe una relación entre la puntuación y una mayor probabilidad de diagnóstico de angina: casi podría descartarse el diagnóstico de angina, al considerar las puntuaciones más bajas de todas las escalas evaluadas, y que existe en cada una de ellas una puntuación a partir de la cual se tiene un alto grado de certeza para el diagnóstico de angina.
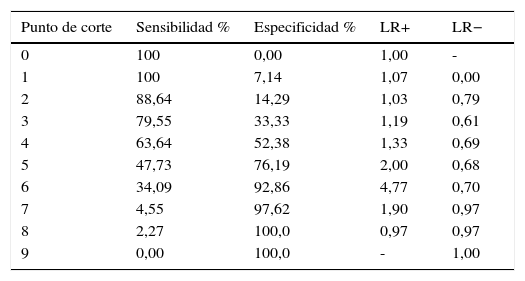
Desempeño diagnóstico de la escala HEART
| Punto de corte | Sensibilidad % | Especificidad % | LR+ | LR− |
|---|---|---|---|---|
| 0 | 100 | 0,00 | 1,00 | - |
| 1 | 100 | 7,14 | 1,07 | 0,00 |
| 2 | 88,64 | 14,29 | 1,03 | 0,79 |
| 3 | 79,55 | 33,33 | 1,19 | 0,61 |
| 4 | 63,64 | 52,38 | 1,33 | 0,69 |
| 5 | 47,73 | 76,19 | 2,00 | 0,68 |
| 6 | 34,09 | 92,86 | 4,77 | 0,70 |
| 7 | 4,55 | 97,62 | 1,90 | 0,97 |
| 8 | 2,27 | 100,0 | 0,97 | 0,97 |
| 9 | 0,00 | 100,0 | - | 1,00 |
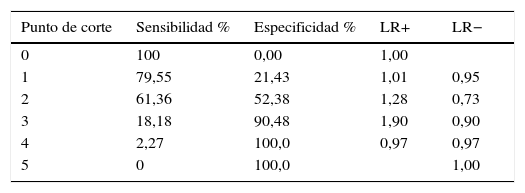
Para la escala de TIMI (tabla 2) se obtuvo la mayor precisión diagnóstica con un punto de corte de 2, una sensibilidad del 61,4% y una especificidad del 52,4%. Con una puntuación de 3, se obtenía el LR+ más alto con una especificidad 90,5%. La escala CARdiac tuvo su mejor precisión con una puntuación de 1, con una sensibilidad de 54,6% y especificidad de 59,5%. La escala de Florencia obtuvo la precisión más alta con una puntuación de 5 en la que la sensibilidad fue 59,1% y la especificidad 45,2%; con una puntuación mayor de 7 se alcanzaba el LR+ más alto.
La escala Sanchís, la de mayor precisión con 2 puntos, tuvo una sensibilidad del 70,5% y una especificidad del 35,7%; el LR+ más alto se tuvo a los 5 puntos con 5,5 y una especificidad del 95,2%. La escala HEART (tabla 3) alcanzó su mayor precisión a los 4 puntos, con una sensibilidad de 63,6% y una especificidad de 52,4%. El LR+ más alto se obtuvo a los 6 puntos, con 4,8. La escala de GRACE tuvo la mayor precisión a los 105 puntos con una sensibilidad de 61,4% y especificidad de 61,9%; el LR+ más alto fue de 5,7 con 147 puntos y una especificidad de 97,6%.
DiscusiónLa evaluación de los pacientes con dolor torácico encaminada a descartar un SCA en poblaciones de bajo riesgo, es decir, cuando el electrocardiograma no presenta cambios, los biomarcadores de lesión miocardiaca son negativos y no presentan otro factor de riesgo para enfermedad coronaria, representa un área de intensa búsqueda en la investigación médica. Si bien el electrocardiograma es una excelente herramienta diagnóstica con una sensibilidad del 49% y una especificidad que se acerca al 92%, cerca de 40% de los pacientes con dolor torácico tienen un trazado normal12. Si adicionamos biomarcadores negativos durante un seguimiento de 24 h, se estima que la probabilidad de muerte o infarto ronda al 2%13, aunque existen reportes en los que se ubica en el 3% a 30 días y en el 4,8% a 6 meses14.
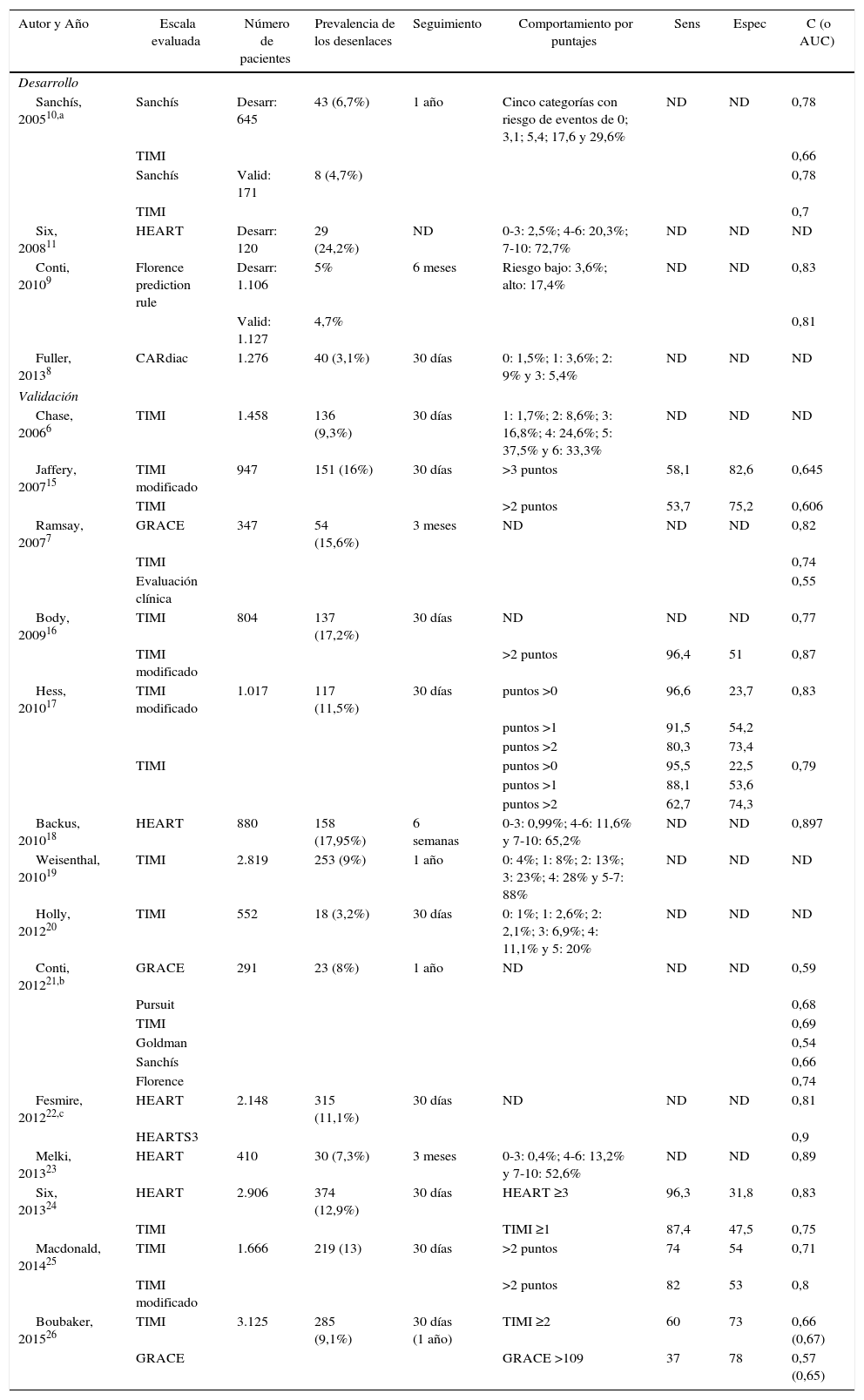
Es por esto por lo que se han intentado desarrollar herramientas que soporten las decisiones en este grupo de pacientes. En la tabla 4 se expone, en orden cronológico, un resumen de algunos de los trabajos en los que se desarrollan8–11 y validan6,15–26 algunas escalas para la evaluación del riesgo de eventos cardiovasculares en pacientes con dolor torácico y su pronóstico. Pese a encontrarse grandes variaciones en las diferentes poblaciones exploradas, la gran mayoría muestran un adecuado poder predictor. En esta tabla podemos observar cómo la escala más evaluada (12 trabajos) es la de TIMI, que en el presente trabajo muestra un muy discreto poder de predicción, de manera similar a lo encontrado en algunos reportes15,21,26 aunque tuvo un peor desempeño que un número superior de trabajos7,16,17,25. En algunos de estos trabajos solo se demuestra cómo con el incremento de su puntuación aumenta la presencia de desenlaces6,19,20. Para el caso del GRACE, 2de los reportes concuerdan con nuestro hallazgo de una baja AUC21,26 y uno reporta un valor mucho más alto7.
Comparación entre los diferentes estudios que desarrollan o validan escalas de riesgo para la evaluación del dolor torácico en pacientes de urgencias
| Autor y Año | Escala evaluada | Número de pacientes | Prevalencia de los desenlaces | Seguimiento | Comportamiento por puntajes | Sens | Espec | C (o AUC) |
|---|---|---|---|---|---|---|---|---|
| Desarrollo | ||||||||
| Sanchís, 200510,a | Sanchís | Desarr: 645 | 43 (6,7%) | 1 año | Cinco categorías con riesgo de eventos de 0; 3,1; 5,4; 17,6 y 29,6% | ND | ND | 0,78 |
| TIMI | 0,66 | |||||||
| Sanchís | Valid: 171 | 8 (4,7%) | 0,78 | |||||
| TIMI | 0,7 | |||||||
| Six, 200811 | HEART | Desarr: 120 | 29 (24,2%) | ND | 0-3: 2,5%; 4-6: 20,3%; 7-10: 72,7% | ND | ND | ND |
| Conti, 20109 | Florence prediction rule | Desarr: 1.106 | 5% | 6 meses | Riesgo bajo: 3,6%; alto: 17,4% | ND | ND | 0,83 |
| Valid: 1.127 | 4,7% | 0,81 | ||||||
| Fuller, 20138 | CARdiac | 1.276 | 40 (3,1%) | 30 días | 0: 1,5%; 1: 3,6%; 2: 9% y 3: 5,4% | ND | ND | ND |
| Validación | ||||||||
| Chase, 20066 | TIMI | 1.458 | 136 (9,3%) | 30 días | 1: 1,7%; 2: 8,6%; 3: 16,8%; 4: 24,6%; 5: 37,5% y 6: 33,3% | ND | ND | ND |
| Jaffery, 200715 | TIMI modificado | 947 | 151 (16%) | 30 días | >3 puntos | 58,1 | 82,6 | 0,645 |
| TIMI | >2 puntos | 53,7 | 75,2 | 0,606 | ||||
| Ramsay, 20077 | GRACE | 347 | 54 (15,6%) | 3 meses | ND | ND | ND | 0,82 |
| TIMI | 0,74 | |||||||
| Evaluación clínica | 0,55 | |||||||
| Body, 200916 | TIMI | 804 | 137 (17,2%) | 30 días | ND | ND | ND | 0,77 |
| TIMI modificado | >2 puntos | 96,4 | 51 | 0,87 | ||||
| Hess, 201017 | TIMI modificado | 1.017 | 117 (11,5%) | 30 días | puntos >0 | 96,6 | 23,7 | 0,83 |
| puntos >1 | 91,5 | 54,2 | ||||||
| puntos >2 | 80,3 | 73,4 | ||||||
| TIMI | puntos >0 | 95,5 | 22,5 | 0,79 | ||||
| puntos >1 | 88,1 | 53,6 | ||||||
| puntos >2 | 62,7 | 74,3 | ||||||
| Backus, 201018 | HEART | 880 | 158 (17,95%) | 6 semanas | 0-3: 0,99%; 4-6: 11,6% y 7-10: 65,2% | ND | ND | 0,897 |
| Weisenthal, 201019 | TIMI | 2.819 | 253 (9%) | 1 año | 0: 4%; 1: 8%; 2: 13%; 3: 23%; 4: 28% y 5-7: 88% | ND | ND | ND |
| Holly, 201220 | TIMI | 552 | 18 (3,2%) | 30 días | 0: 1%; 1: 2,6%; 2: 2,1%; 3: 6,9%; 4: 11,1% y 5: 20% | ND | ND | ND |
| Conti, 201221,b | GRACE | 291 | 23 (8%) | 1 año | ND | ND | ND | 0,59 |
| Pursuit | 0,68 | |||||||
| TIMI | 0,69 | |||||||
| Goldman | 0,54 | |||||||
| Sanchís | 0,66 | |||||||
| Florence | 0,74 | |||||||
| Fesmire, 201222,c | HEART | 2.148 | 315 (11,1%) | 30 días | ND | ND | ND | 0,81 |
| HEARTS3 | 0,9 | |||||||
| Melki, 201323 | HEART | 410 | 30 (7,3%) | 3 meses | 0-3: 0,4%; 4-6: 13,2% y 7-10: 52,6% | ND | ND | 0,89 |
| Six, 201324 | HEART | 2.906 | 374 (12,9%) | 30 días | HEART ≥3 | 96,3 | 31,8 | 0,83 |
| TIMI | TIMI ≥1 | 87,4 | 47,5 | 0,75 | ||||
| Macdonald, 201425 | TIMI | 1.666 | 219 (13) | 30 días | >2 puntos | 74 | 54 | 0,71 |
| TIMI modificado | >2 puntos | 82 | 53 | 0,8 | ||||
| Boubaker, 201526 | TIMI | 3.125 | 285 (9,1%) | 30 días (1 año) | TIMI ≥2 | 60 | 73 | 0,66 (0,67) |
| GRACE | GRACE >109 | 37 | 78 | 0,57 (0,65) | ||||
La escala HEART parece ser la más evaluada en los estudios recientes y obtiene resultados consistentemente altos, con AUC por encima de 0,818,22–24. Si bien en el presente reporte tuvo el mejor desempeño, su resultado, y por ende el de las demás escalas, parece que no permite su aplicación en esta población. El estudio del grupo desarrollador de la escala de Florencia, que además evalúa varias escalas que no incluye la del HEART, obtiene resultados cercanos al presente estudio, aunque la única con un adecuado poder de discriminación fue la de Florencia21.
Es nuestro deber hacer notar que la población motivo del presente estudio es altamente seleccionada: el clínico había establecido que, pese a la negatividad del electrocardiograma y la troponina, se requería una evaluación intrahospitalaria, por lo que ya no constituía un bajo riesgo, hecho que se refleja en la altísima proporción de casos de SCA diagnosticados.
Al considerar las razones para explicar los pobres resultados obtenidos en el presente estudio, tenemos varias custiones. Primero, nuestro estudio se centra en el diagnóstico y no en el pronóstico: este tipo de enfoque no es la primera vez que se intenta. Es así como en el trabajo de Fersmire et al. del 2012 usaron como desenlace el diagnóstico de SCA dentro de la hospitalización y a los 30 días, evaluando las escalas HEART y una nueva, el HEARTS3, con un desempeño bastante bueno22. Por otro lado, el trabajo de Conti et al. del 2012 incluyó en el punto compuesto de los desenlaces la confirmación angiográfica de la estenosis coronaria21. Desde el punto de vista del clínico que aborda a un paciente con dolor torácico, el llegar a conocer el diagnóstico es tan importante como el análisis pronóstico, por lo tanto, no es descabellado este análisis; por otro lado, otros desenlaces cardiovasculares podrían ser causados por otros diagnósticos diferentes al SCA.
Un segundo aspecto, que al mismo tiempo es una limitación importante, es el pequeño tamaño de la muestra, lo que conlleva una escasa representación de algunos grupos o puntuaciones en algunas escalas, lo que limita la capacidad del estudio para realmente discriminar la precisión diagnóstica y hace que no se pueda hablar de una verdadera validación de las escalas contempladas.
Las escalas pronósticas, en especial el TIMI y GRACE, cumplen un papel importante en la práctica diaria del clínico de urgencias para tomar decisiones en el enfoque del paciente con dolor torácico y ayudan a decidir qué acciones tomar en un determinado caso al intentar identificar situaciones de riesgo. En el presente estudio buscamos explorar su desempeño para el diagnóstico, siendo conscientes de que existe una gran limitación para alcanzar este objetivo sin la inclusión de alguna estrategia de estratificación coronaria, además de suponer que dicha clasificación diagnóstica se correlaciona con el riesgo de eventos cardiovasculares.
ConclusiónLas escalas de predicción de riesgo de desarrollar un evento cardiovascular mayor en pacientes con dolor torácico, evaluadas con fines diagnósticos, mostraron un pobre poder discriminatorio en una población de pacientes de alto riesgo con electrocardiograma y troponina negativos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflictos de interesesLos autores declaramos que no existe ningún conflicto de interés.
Los autores agradecemos a los estudiantes de Medicina Maritza Peña y Javier Torres, y al residente de Medicina Interna Luis Muñoz, quienes participaron en un análisis preliminar del presente estudio.
Este estudio fue presentado en el XXIII Congreso Colombiano de Medicina Interna, Cartagena 7 al 10 de agosto de 2014, y obtuvo el premio al mejor póster.