Relatamos o caso de um paciente portador de hipertensão pulmonar de origem esquistossomótica, que procurou pronto atendimento por apresentar quadro de dor torácica em repouso. A apresentação clínica e os demais dados referentes ao caso levantaram a suspeita de insuficiência coronariana aguda, e foi diagnosticada uma obstrução grave do tronco da coronária esquerda. O relato do caso teve por objetivo destacar a necessidade do diagnóstico diferencial da queixa de dor torácica nestes pacientes e ressaltar a opção da intervenção coronariana percutânea como tratamento eficaz e seguro neste cenário.
This report describes a patient with pulmonary hypertension secondary to schistosomiasis, who sought emergency care due to chest pain at rest. The clinical presentation and other information related to the case raised the suspicion of acute coronary failure, and a severe obstruction was identified in the left main coronary artery. The case report aimed to highlight the need for a differential diagnosis of chest pain complaints in these patients, and emphasizes the choice of percutaneous coronary intervention as an effective and safe treatment in this scenario.
Obstruções significativas do tronco da artéria coronária esquerda são encontradas em 5 a 7% dos pacientes submetidos à coronariografia.1 O acometimento aterosclerótico é a causa mais frequente, mas outras causas podem ocorrer, como a obstrução extrínseca por dilatação da artéria pulmonar, secundária à hipertensão pulmonar.
A esquistossomose é a terceira doença parasitária endêmica no mundo, com cerca de 5% dos pacientes infectados apresentando também hipertensão arterial pulmonar.2 Assim, uma das principais causas de hipertensão pulmonar é secundária à esquistossomose. A dor torácica é uma das queixas mais comuns nesses pacientes, sendo usualmente considerada secundária à hipertensão pulmonar.
O relato de caso a seguir chama a atenção para uma outra causa possível da dor torácica nestes pacientes e torna claro o importante papel da intervenção percutânea em seu tratamento.
Relato do casoEAB, 66 anos, recebeu o diagnóstico de esquistossomose mansônica aos 10 anos de idade. Aos 38 anos, teve diagnóstico de hipertensão pulmonar após apresentar quadro transitório de dispneia. Permaneceu assintomático até os 53 anos, quando apresentou novo quadro de dispneia intensa, associada à fibrilação atrial. Houve reversão espontânea para ritmo sinusal, e o paciente permaneceu em uso de varfarina, em acompanhamento com pneumologista. Na época, a cintilografia pulmonar foi negativa para tromboembolismo, e a espirometria mostrou‐se normal. Realizou cateterismo direito, neste mesmo período, que evidenciou pressão sistólica na artéria pulmonar de 107mmHg (pressão sistólica sistêmica de 175mmHg), sem resposta à prova vasodilatadora. Ecocardiogramas periódicos mostraram dilatação e disfunção sistólica ventricular direita, dilatação da artéria pulmonar e ramos principais, e hipertensão pulmonar. Avaliações anuais da capacidade funcional com o teste de caminhada de 6 minutos mostraram valores entre 450 e 500 m de distância percorrida (valores de referência para a idade: 550 a 600).
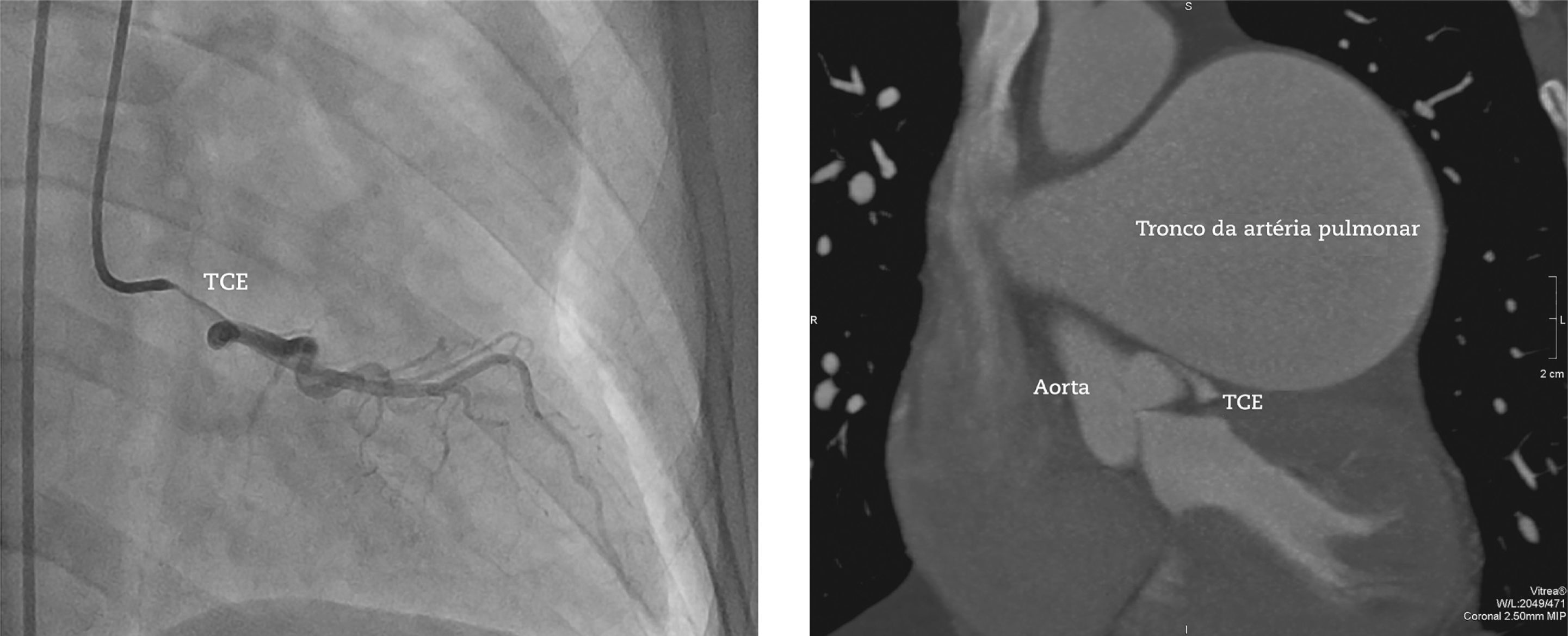
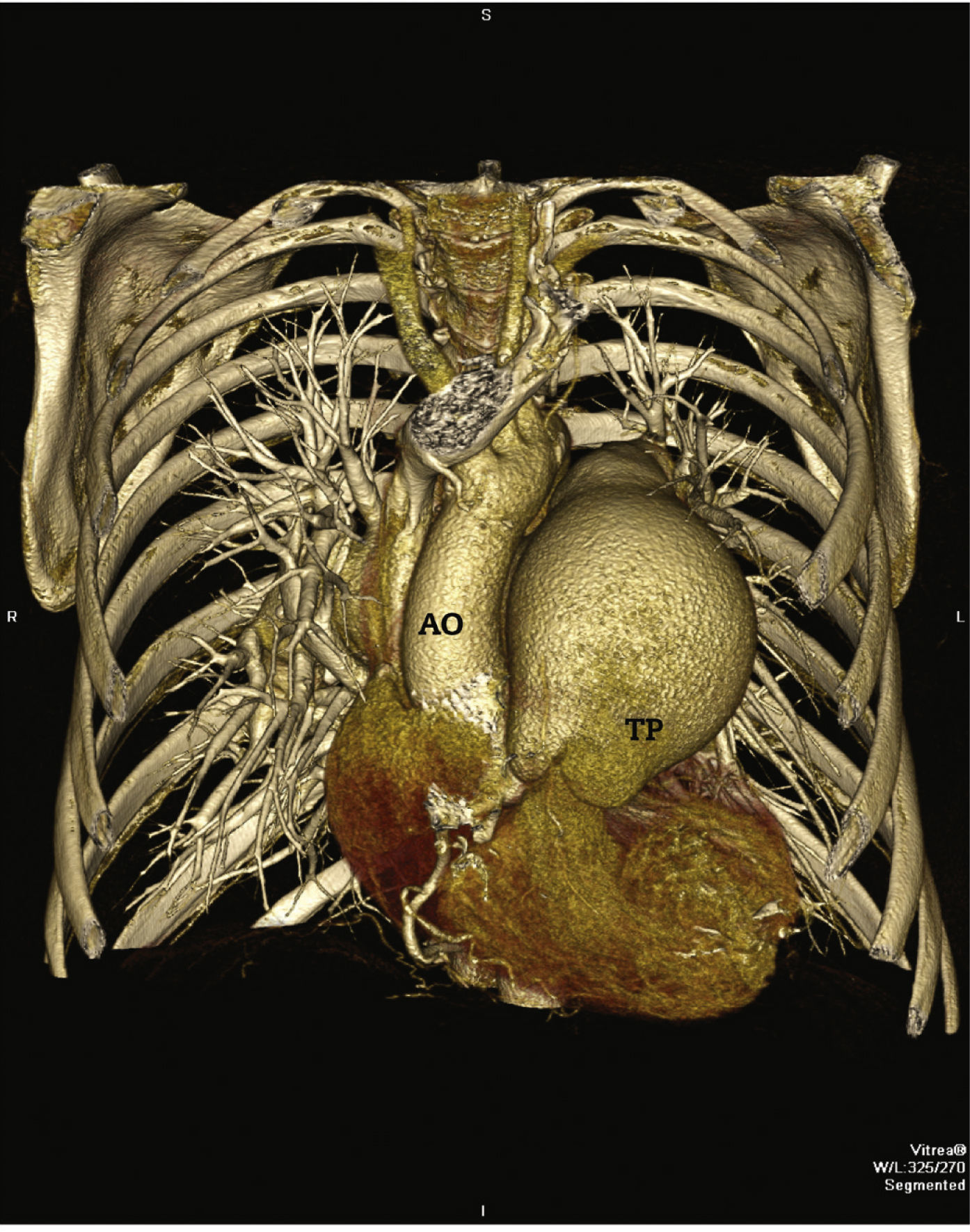
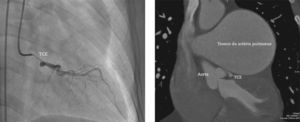
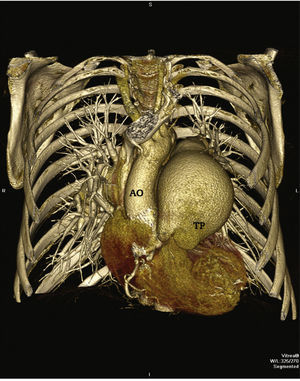
Em 2011, aos 62 anos, apresentou piora da dispneia, desta vez associada à dor torácica atípica. Foi iniciado tratamento com sildenafil, com importante melhora do quadro para classe funcional II da New York Heart Association (NYHA). Em julho de 2014, apresentou episódio agudo de dor torácica em repouso. Procurou o pronto atendimento, e o eletrocardiograma evidenciou bloqueio de ramo direito, infradesnivelamento do segmento ST e onda T negativa de V1 a V5 (alterações presentes previamente), com valores sequenciais de troponina I de 34,7 pg/mL, 44,8 pg/mL e 46,2 pg/mL (VR < 34,2 pg/mL). Foi encaminhado para nosso serviço com diagnóstico de síndrome coronariana aguda. Cineangiocoronariografia evidenciou tronco da coronária esquerda com lesão grave, suboclusiva, sem outras obstruções significativas, além de ventriculografia esquerda com função sistólica preservada (fig. 1). Considerando a história prévia de dilatação da artéria pulmonar importante e poucos sinais angiográficos de aterosclerose coronariana, optamos pela realização de angiotomografia coronariana, que evidenciou dilatação da artéria pulmonar de 80,4mm (VR < 26mm), exercendo compressão extrínseca no tronco da coronária esquerda (fig. 2). O caso foi discutido com o pneumologista assistente e o cirurgião cardiovascular. Considerando o alto risco operatório, optamos por revascularização percutânea. Foi implantado stent farmacológico PROMUS Element® 4,0 x 28mm (Boston Scientific, Natick, EUA) no tronco da coronária esquerda. Realizado ultrassom intracoronário após o implante, que evidenciou má aposição do stent, resolvida após dilatação do stent com cateter balão 4,5 15mm (fig. 3). A alta hospitalar ocorreu 2 dias após o procedimento.
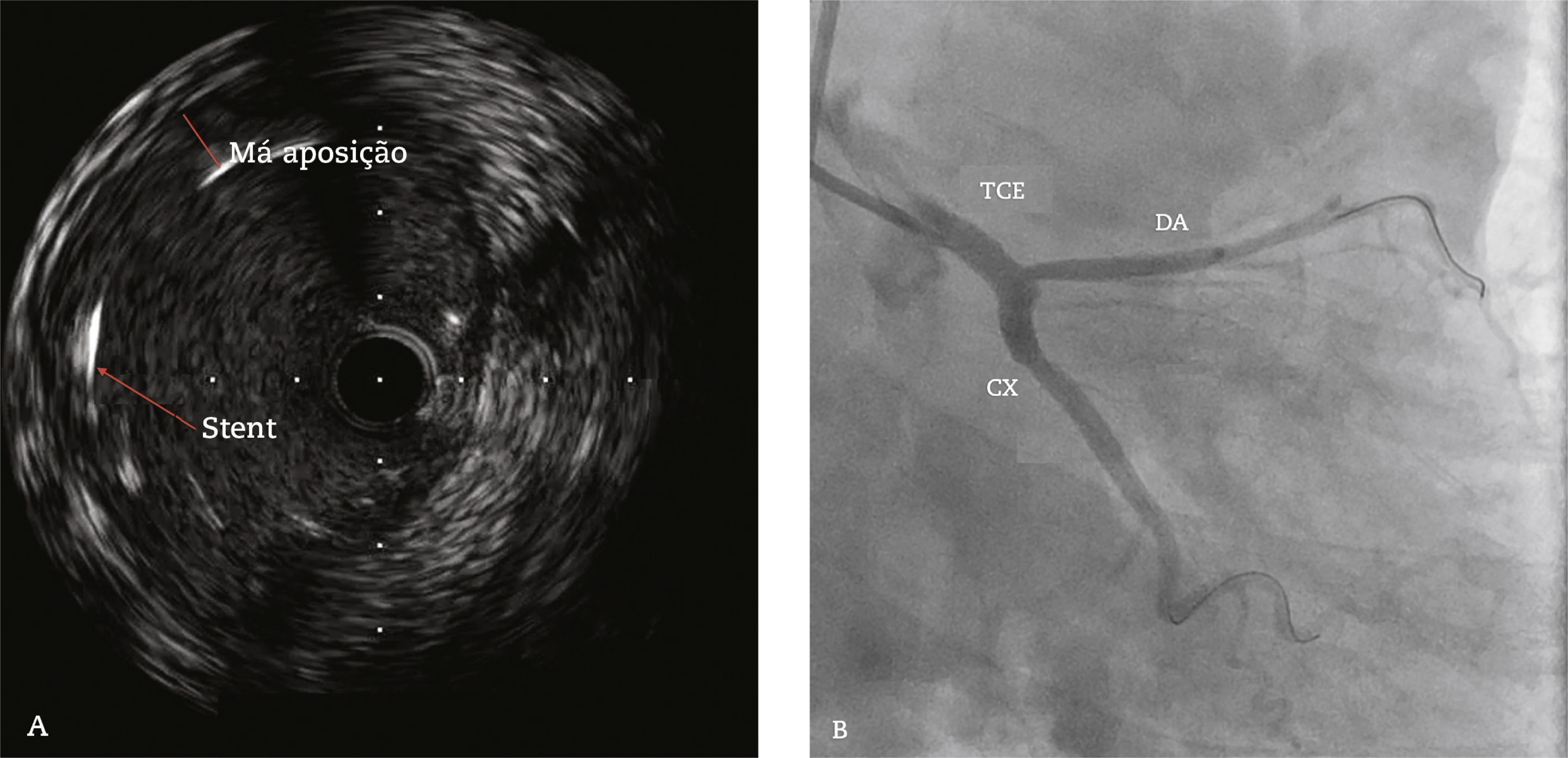
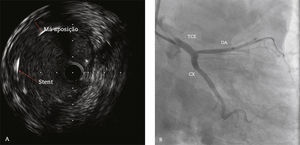
Ultrassom intracoronariano realizado após o implante do stent no tronco da coronária esquerda (TCE) com imagem sugestiva de má aposição das hastes do stent (A). Coronariografia (projeção oblíqua anterior direita caudal) após o implante de stent farmacológico 4,0 28mm no TCE, seguido de pós‐dilatação com cateter balão não complacente 4,5 15mm (B). DA: artéria descendente anterior; CX: artéria circunflexa.
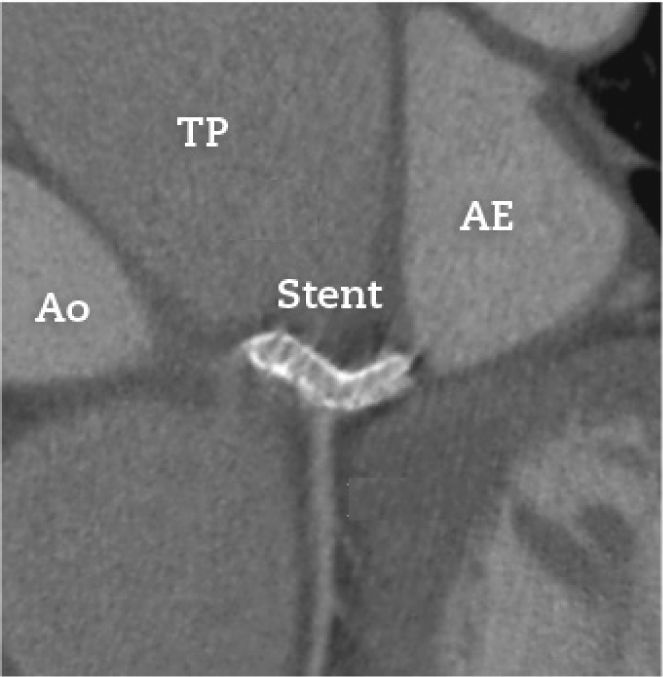
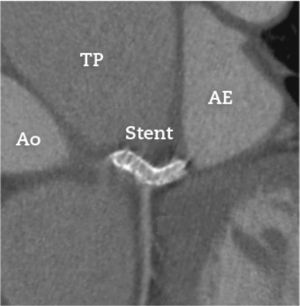
O paciente evoluiu sem recorrência de dor torácica, com melhora da dispneia para classe funcional I (NYHA). Atualmente, encontra‐se assintomático, em uso de metoprolol, furosemida, sinvastatina, clopidogrel, varfarina e sildenafil. Usou aspirina por 30 dias após o procedimento. Foi realizado acompanhamento por exame de imagem, com angiotomografia de coronárias realizada 8 meses após o procedimento (fig. 4), que evidenciou stent bem posicionado, com lúmen preservado, sem sinais de deformação ou reestenose.
DiscussãoA hipertensão pulmonar é desencadeada por um remodelamento das camadas íntima e média do leito arterial pulmonar, com consequentes aumento na resistência vascular, aumento do diâmetro da artéria pulmonar, aumento e disfunção do ventrículo direito, podendo causar insuficiência cardíaca (cor pulmonale) e óbito.2 As causas mais comuns de hipertensão pulmonar são hipertensão pulmonar primária, cardiopatias congênitas, doença tromboembólica crônica e doença parenquimatosa pulmonar avançada. Já as causas de compressão extrínseca do tronco da artéria pulmonar são síndrome do desfiladeiro torácico, sífilis, carcinoma metastático e cisto broncogênico.3 No entanto, nos países onde a esquistossomose é endêmica, por sua alta prevalência, essa parasitose é uma das principais causas de hipertensão pulmonar.
A dilatação da artéria pulmonar pode exercer compressão extrínseca sobre o tronco da coronária esquerda, determinando redução significativa de seu lúmen. A incidência precisa desse achado não é conhecida, podendo ocorrer em 5 a 44% dos pacientes portadores de hipertensão pulmonar.3 Seu desenvolvimento depende de um aumento crônico no diâmetro da artéria pulmonar, geralmente associado à hipertensão pulmonar grave. A compressão do tronco torna‐se provável quando o diâmetro da artéria pulmonar ultrapassa 55mm ou quando a relação entre esse diâmetro e o diâmetro da raiz da aorta é de pelo menos 1,98.3
A apresentação clínica mais comum é a ocorrência de dor torácica anginosa, associada ou não à dispneia. Porém, também podem estar presentes síncope, arritmias graves, infarto do miocárdio ou disfunção ventricular.3 Na ocorrência de qualquer um desses sinais ou sintomas em pacientes portadores de hipertensão pulmonar grave, deve‐se suspeitar da possibilidade de obstrução do tronco da coronária esquerda.
O diagnóstico definitivo da compressão se faz pela angiografia, associada ou não ao ultrassom intracoronário.3 A projeção mais indicada é a oblíqua anterior esquerda cranial. A angiotomografia coronariana possui vantagens: além de evidenciar a obstrução, é capaz de avaliar a artéria pulmonar, sua relação com o tronco da coronária esquerda e a função ventricular esquerda. Possui a desvantagem de expor o paciente à radiação e ao contraste iodado. A ressonância magnética cardíaca é capaz de avaliar as características do músculo miocárdico, acrescentando pouco ao diagnóstico da compressão extrínseca. Por seu caráter não invasivo, a angiotomografia deve ser o exame inicialmente solicitado e utilizada para acompanhamento após o tratamento. Os exames de imagem que pesquisam isquemia miocárdica não se mostraram eficazes na avaliação de alterações de perfusão miocárdica nesses pacientes.3 Uma hipótese provável seria que a extensa isquemia provocada pela obstrução levaria a uma alteração balanceada na perfusão miocárdica em diversos segmentos do ventrículo esquerdo, o que desencadearia dificuldades na análise dessas imagens.
O melhor tratamento da obstrução extrínseca do tronco da coronária esquerda pela dilatação da artéria pulmonar não está definido. A realização de estudos randomizados e controlados é difícil pelo pequeno número de casos.
A revascularização do miocárdio pode ser feita pela cirurgia convencional ou pelo implante percutâneo de stents. Vários autores consideram o último a melhor opção por algumas razões.3–6 Primeiro, o risco inerente à cirurgia convencional nesses pacientes é aumentado, devido à presença da hipertensão pulmonar grave. Segundo, a fisiopatologia da obstrução não é aterosclerótica. Isso pode significar menores taxas de reestenose dos stents e maior facilidade durante o tratamento percutâneo. De acordo com os relatos de casos descritos, essa modalidade de tratamento se mostrou eficaz e segura durante a fase hospitalar e o seguimento tardio.3,4,6
A escolha entre a utilização dos stents convencionais e os farmacológicos também não está definida. Alguns autores escolhem os stents convencionais pela natureza não aterosclerótica da lesão e pelo grande diâmetro do tronco da coronária esquerda, o que tornaria a reestenose pouco provável.4,6 No entanto, a alta eficácia e a segurança do uso dos stents farmacológicos no tratamento das lesões ateroscleróticas do tronco da coronária esquerda fazem desses dispositivos os mais empregados nos casos relatados.3 Não se tem estabelecido se é necessário o controle angiográfico de rotina durante o seguimento dos casos. Pelo descrito acima, a angiotomografia de coronárias provavelmente seria suficiente para descartar reestenose ou complicações tardias, considerando os avanços recentes no método. De qualquer maneira, levando em conta a morbidade e a grande área de miocárdio em risco, o uso da terapia antiplaquetária dupla por pelo menos 1 ano é recomendada.
O tratamento da hipertensão pulmonar deve ser guiada pela causa. O controle clínico com vasodilatadores associados ao tratamento percutâneo da lesão de tronco também foi descrito.3 Nos casos com etiologia esquistossomótica, o tratamento deve envolver as medidas específicas para a parasitose. As medidas farmacológicas incluem o tratamento antiparasitário (praziquantel e artemeter), mesmo nas formas crônicas recentemente diagnosticadas. O tratamento elimina os parasitas adultos, produtores de ovos, diminuindo a agressão ao parênquima pulmonar. No entanto, o remodelamento vascular estabelece um ponto de irreversibilidade, no qual o tratamento antiparasitário isolado é ineficaz na prevenção da piora progressiva. O tratamento definitivo é o transplante coração‐pulmão.7
Fonte de financiamentoNão há.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
A revisão por pares é da responsabilidade Sociedade Brasileira de Hemodinâmica e Cardiologia Intervencionista.