Defeitos congênitos múltiplos são tradicionalmente corrigidos cirurgicamente, mas, atualmente, podem ser tratados percutaneamente. Existem poucos relatos na literatura atestando sua eficácia e segurança. Objetivamos descrever uma experiência com a realização de procedimentos combinados para tratar diferentes defeitos, congênitos e estruturais, numa mesma sessão terapêutica.
MétodosDesde 2007, foram tratados, numa mesma sessão terapêutica, diferentes defeitos. Todos foram selecionados por ecocardiograma. Os procedimentos foram realizados segundo as técnicas tradicionais já descritas para cada defeito encontrado.
ResultadosForam tratados dez pacientes, cinco do sexo masculino, com idades de 1 a 67 anos, e pesos de 11 a 90kg. O defeito mais prevalente de forma isolada foi a persistência do canal arterial (PCA, n = 5), seguido da comunicação interatrial ostium secundum (CIA OS, n = 4) e da comunicação interventricular (CIV, n = 4). As combinações mais frequentes foram CIV com PCA (n = 2) e CIV com CIA OS (n = 2). Foram dilatadas duas estenoses valvares pulmonares com CIA OS e com forame oval patente (FOP), e uma coarctação de aorta com PCA. Adicionalmente, foi ocluído um apêndice atrial esquerdo com FOP e foi embolizada uma fístula aortopulmonar com PCA. Todos os procedimentos foram bem‐sucedidos. O tempo médio de seguimento foi de 31 ± 28,1 meses, havendo apenas duas complicações. Não houve nenhum óbito.
ConclusõesA pequena série de casos relatada mostrou que os procedimentos combinados foram seguros e eficazes, podendo ser reproduzidos por operadores experientes em centros especializados, podendo vir a se constituir como primeira opção terapêutica para esses pacientes.
Multiple congenital defects are traditionally corrected surgically, but nowadays can be treated percutaneously. There are few reports in the literature attesting to its efficacy and safety. We aimed to describe an experience with combined procedures to treat different congenital and structural defects, in a single therapeutic session.
MethodsSince 2007, different defects were treated in a single treatment session. All were selected by echocardiography. The procedures were performed using traditional techniques already described for each defect.
ResultsTen patients were treated, five males, aged 1‐67 years, weighting 11‐90 kilograms. The most prevalent isolated defect was patent ductus arteriosus (PDA, n = 5), followed by ostium secundum atrial septal defects (ASD, n = 4) and ventricular septal defects (VSD, n = 4). The most common combinations were VSD with PDA (n = 2) and VSD with osASD (n = 2). Two pulmonary valve stenosis were dilated with ASD and patent foramen ovale (PFO), and one aorta coarctation with PDA. Additionally, a left atrial appendage with PFO was occluded and an aortopulmonary fistula with PDA was embolized. All procedures were successful. The mean follow‐up was 31 ± 28.1 months, with only two complications. There were no deaths.
ConclusionsThe small number of reported cases showed that the combined procedures were safe and effective and can be reproduced by experienced operators in specialized centers and may be considered as the first therapeutic option in these patients.
A intervenção percutânea constituiu‐se na modalidade terapêutica de escolha para a maioria das cardiopatias congênitas simples e também para alguns defeitos estruturais, apresentando resultados semelhantes e até mesmo, por vezes, alguma vantagem sobre a cirurgia convencional.1,2
Defeitos congênitos múltiplos são tradicionalmente corrigidos por meio de técnicas cirúrgicas. No entanto, embora a exequibilidade da intervenção percutânea de diferentes defeitos em um mesmo procedimento tenha sido descrita em alguns relatos de caso, sua eficácia e segurança não foram avaliadas de forma consistente.3–6
No presente manuscrito, analisamos a experiência do grupo com procedimentos combinados realizados para tratamento de diferentes defeitos congênitos e estruturais, e discutimos aspectos técnicos e indicações para sua realização. Por fim, tecemos considerações sobre a eficácia e a segurança dos procedimentos realizados.
MétodosForam analisados, retrospectivamente, os registros de todos os pacientes submetidos a procedimentos percutâneos para tratar diferentes defeitos cardíacos em uma mesma sessão terapêutica. Foram excluídos desta análise os casos de implante de mais de um dispositivo para tratar o mesmo tipo anatômico de defeito, além de casos em que foram ocluídos a comunicação interatrial (CIA) e o forame oval patente (FOP) no mesmo procedimento.
ProcedimentosTodos os procedimentos foram realizados sob anestesia geral e intubação orotraqueal, após jejum mínimo de 8 horas. Os pacientes foram submetidos a cateterismo cardíaco direito e esquerdo, por punção femoral. Foram realizadas as angiografias pertinentes a cada caso.
Heparina foi administrada nas doses de 100 UI/kg em crianças, e de 5.000 a 10.000 UI em adultos, após ter sido obtido o acesso venoso e introduzido o transdutor transesofágico. Profilaxia antimicrobiana com cefazolina (50mg/kg em crianças ou 2g em adultos) foi rotineiramente administrada.
Como regra geral, foram realizados, inicialmente, os procedimentos julgados mais complexos, demorados ou trabalhosos, seguidos daqueles considerados mais simples ou que tecnicamente demandassem menos. No caso de estenoses valvares associadas, estas foram abordadas inicialmente.
Todos os procedimentos de oclusão e as dilatações foram realizadas segundo as técnicas habituais, previamente detalhadas.2,7–11 Os procedimentos de oclusão foram monitorados por ecocardiograma transesofágico (ETE), além da fluoroscopia tradicional.
Os pacientes foram seguidos em unidade de tratamento intensivo após o procedimento e receberam alta após realizarem ecocardiografia transtorácica (ETT) de controle 24 horas após o procedimento índice.
SeguimentoOs pacientes nos quais foram realizadas oclusões de CIA, FOP, comunicação interventricular (CIV) e apêndice atrial esquerdo (AAE) foram orientados a usar aspirina (3 a 5mg/kg/dia em crianças ou 200mg/dia em adultos) por 6 meses, somada a 75mg de bissulfato de clopidogrel, em adultos, por 3 meses, nos casos em que havia indicação. Nos pacientes cujo procedimento envolveu apenas o uso de stents, terapia antiplaquetária com aspirina foi recomendada por 6 meses. A todos foi feita a recomendação de observar a profilaxia para endocardite infecciosa por um período de 6 meses, quando necessário.
Seguimento clínico foi realizado nos meses 1, 3, 6 e 12 após o procedimento, e anualmente a partir de então. Acompanhamento de imagem com ETT foi realizado nas consultas de 1, 3 e 12 meses, e anualmente a seguir, enquanto na consulta de 6 meses, a avaliação do resultado do procedimento foi realizada com ETE.
Além do exame clínico e dos ecocardiogramas de rotina, os stents foram avaliados com angiotomografia após 6 meses.
ResultadosDesde 2007, foram realizados procedimentos em 982 pacientes, tendo sido tratados 2 diferentes defeitos numa mesma sessão em 10 pacientes (1,0%). Cinco pacientes eram do sexo masculino, as idades variaram de 1 a 67 anos (14 ± 24,3 anos) e os pesos, de 11 a 90kg (50 ± 26,9kg).
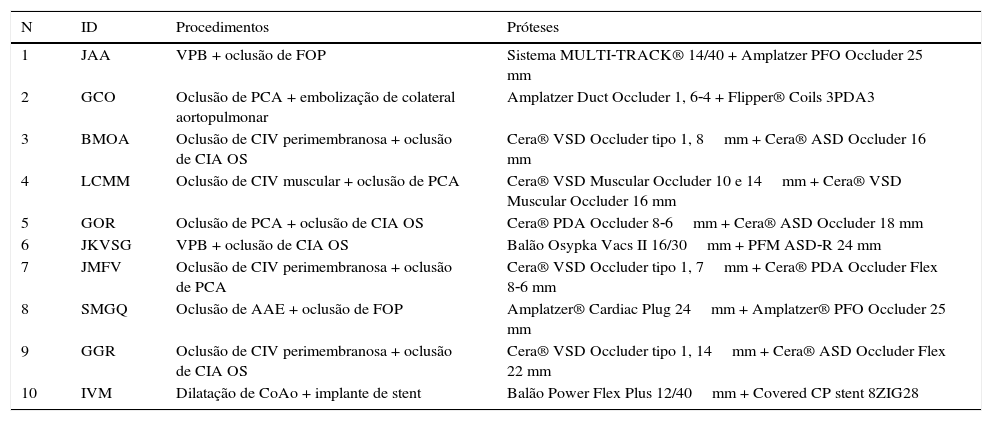
A tabela 1 apresenta os dados demográficos dos dez pacientes incluídos, assim como as combinações de defeitos estruturais tratados. No total, foram tratados 20 defeitos congênitos e estruturais, com a persistência do canal arterial (PCA) sendo o mais prevalente (n = 5) de forma isolada, seguido por CIA OS (n = 4) e CIV (n = 4). As combinações mais frequentes foram CIV com PCA (n = 2) e CIV com CIA OS (n = 2).
Dados demográficos e defeitos estruturais
| N | ID | Sexo | Idade (anos) | Peso (kg) | Defeitos |
|---|---|---|---|---|---|
| 1 | JAA | M | 57 | 90 | EP + FOP |
| 2 | GCO | M | 1 | 11 | PCA + colateral aortopulmonar |
| 3 | BMOA | F | 14 | 50 | CIV perimembranosa + CIA OS |
| 4 | LCMM | F | 35 | 59 | CIVs musculares múltiplas + PCA |
| 5 | GOR | F | 29 | 56 | PCA + CIA OS |
| 6 | JKVSG | M | 3 | 14 | EP + CIA OS |
| 7 | JMFV | M | 4 | 15 | CIV perimembranosa + PCA |
| 8 | SMGQ | F | 67 | 65 | FA crônica com AVC + FOP |
| 9 | GGR | M | 10 | 42 | CIV perimembranosa + CIA OS |
| 10 | IVM | F | 7 | 24 | CoAo + PCA |
ID: identificação do paciente; M: masculino; EP: estenose valvar pulmonar; FOP: forame oval patente; PCA: persistência do canal arterial; F: feminino; CIV: comunicação interventricular; CIA OS: comunicação interatrial tipo ostium secundum; FA: fibrilação atrial; AVC: acidente vascular cerebral; CoAo: coarctação de aorta.
Dos 20 procedimentos realizados nos 10 pacientes, a combinação de 2 procedimentos de oclusão foi realizada na maioria dos casos (n=7). Em 2 casos, foi realizada valvoplastia pulmonar com balão (VPB) em combinação com oclusão de FOP (n = 1) e CIA OS (n = 1). Outro paciente portador de coarctação de aorta (CoAo) e PCA teve sua CoAo tratada com dilatação com balão e implante de stent recoberto por politetrafluoretileno (PTFE), posicionado de forma a ocluir também a origem do canal arterial. Para a realização dos procedimentos, foi utilizada uma variedade de dispositivos com diferentes características e de diversos fornecedores, conforme a tabela 2.
Procedimentos realizados e dispositivos utilizados
| N | ID | Procedimentos | Próteses |
|---|---|---|---|
| 1 | JAA | VPB + oclusão de FOP | Sistema MULTI‐TRACK® 14/40 + Amplatzer PFO Occluder 25 mm |
| 2 | GCO | Oclusão de PCA + embolização de colateral aortopulmonar | Amplatzer Duct Occluder 1, 6‐4 + Flipper® Coils 3PDA3 |
| 3 | BMOA | Oclusão de CIV perimembranosa + oclusão de CIA OS | Cera® VSD Occluder tipo 1, 8mm + Cera® ASD Occluder 16 mm |
| 4 | LCMM | Oclusão de CIV muscular + oclusão de PCA | Cera® VSD Muscular Occluder 10 e 14mm + Cera® VSD Muscular Occluder 16 mm |
| 5 | GOR | Oclusão de PCA + oclusão de CIA OS | Cera® PDA Occluder 8‐6mm + Cera® ASD Occluder 18 mm |
| 6 | JKVSG | VPB + oclusão de CIA OS | Balão Osypka Vacs II 16/30mm + PFM ASD‐R 24 mm |
| 7 | JMFV | Oclusão de CIV perimembranosa + oclusão de PCA | Cera® VSD Occluder tipo 1, 7mm + Cera® PDA Occluder Flex 8‐6 mm |
| 8 | SMGQ | Oclusão de AAE + oclusão de FOP | Amplatzer® Cardiac Plug 24mm + Amplatzer® PFO Occluder 25 mm |
| 9 | GGR | Oclusão de CIV perimembranosa + oclusão de CIA OS | Cera® VSD Occluder tipo 1, 14mm + Cera® ASD Occluder Flex 22 mm |
| 10 | IVM | Dilatação de CoAo + implante de stent | Balão Power Flex Plus 12/40mm + Covered CP stent 8ZIG28 |
ID: identificação do paciente; VPB: valvoplastia pulmonar com balão; FOP: forame oval patente; PCA: persistência de canal arterial; CIV: comunicação interventricular; CIA OS: comunicação interatrial tipo ostium secundum; AAE: apêndice atrial esquerdo; CoAO: coarctação de aorta.
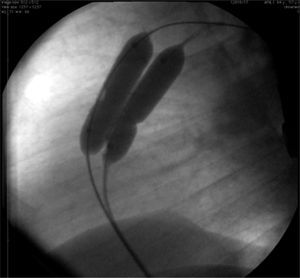
VPB foi realizada em dois casos como primeiro procedimento. O gradiente transvalvar pulmonar encontrado foi de 40 e 60mmHg, e se reduziu para 8 e 28mmHg, respectivamente, após a dilatação.
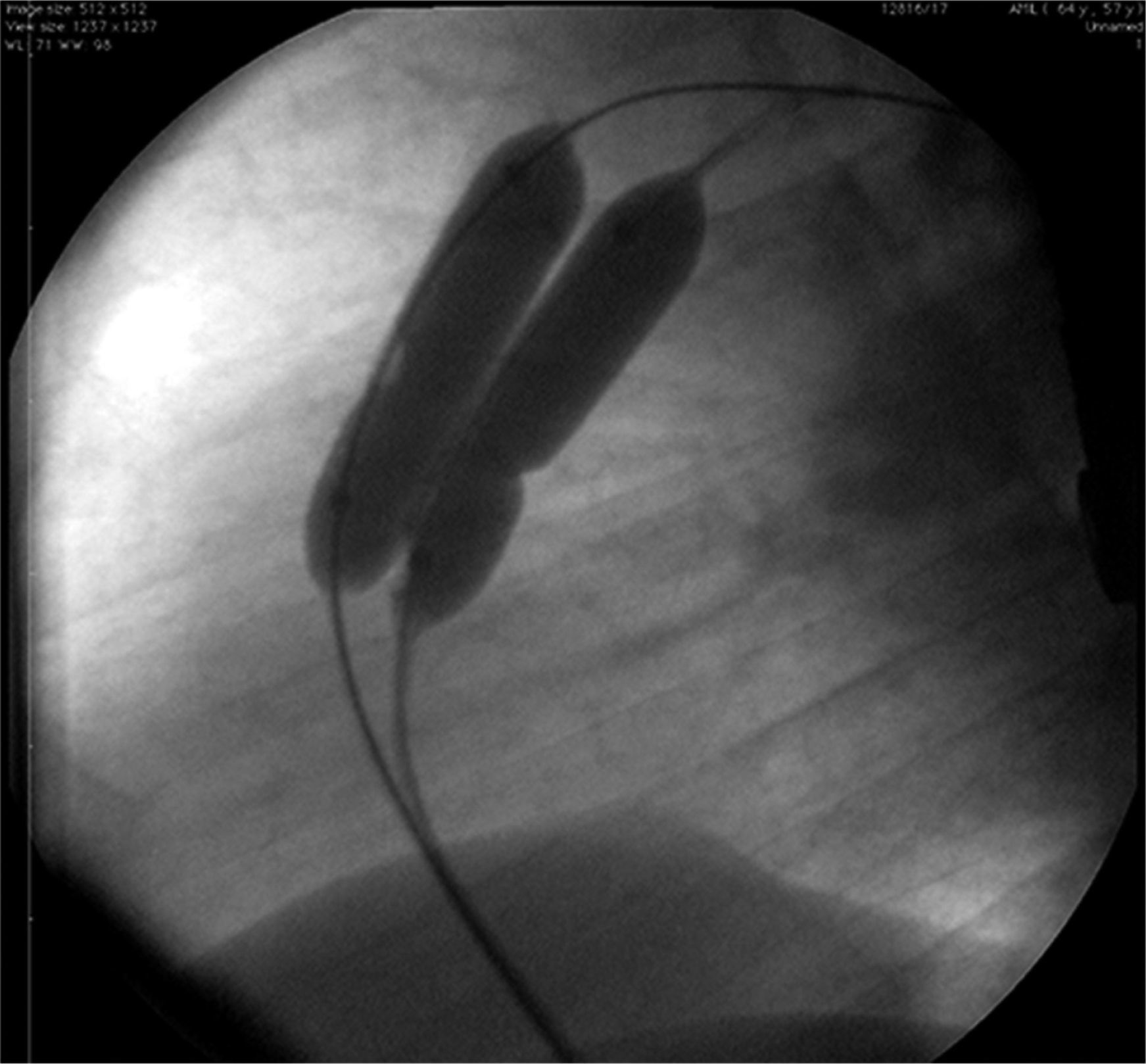
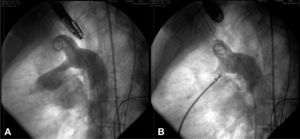
No caso 1, um paciente adulto, utilizamos a técnica de duplo balão sobre um único fio‐guia (sistema MULTI‐TRACK®, NuMed, H‐opkinton, Estados Unidos) com dois balões 14/40mm, com bom resultado (fig. 1) No caso 6, uma criança de 3 anos, foi utilizado um balão Osypka Vacs II de 16mm (Osypka AG, Rheinfelden‐Herten, Alemanha). Em ambos os casos, a lesão valvar foi abordada primeiro, para, em seguida, ser realizada a oclusão septal com próteses Amplatzer® PFO Occluder de 25mm (St. Jude Medical, St. Paul, Estados Unidos) (caso 1) e PFM ASD‐R de 22mm (PFM AG, Köln, Alemanha) (caso 6). Ambos os casos tiveram resultados satisfatórios.
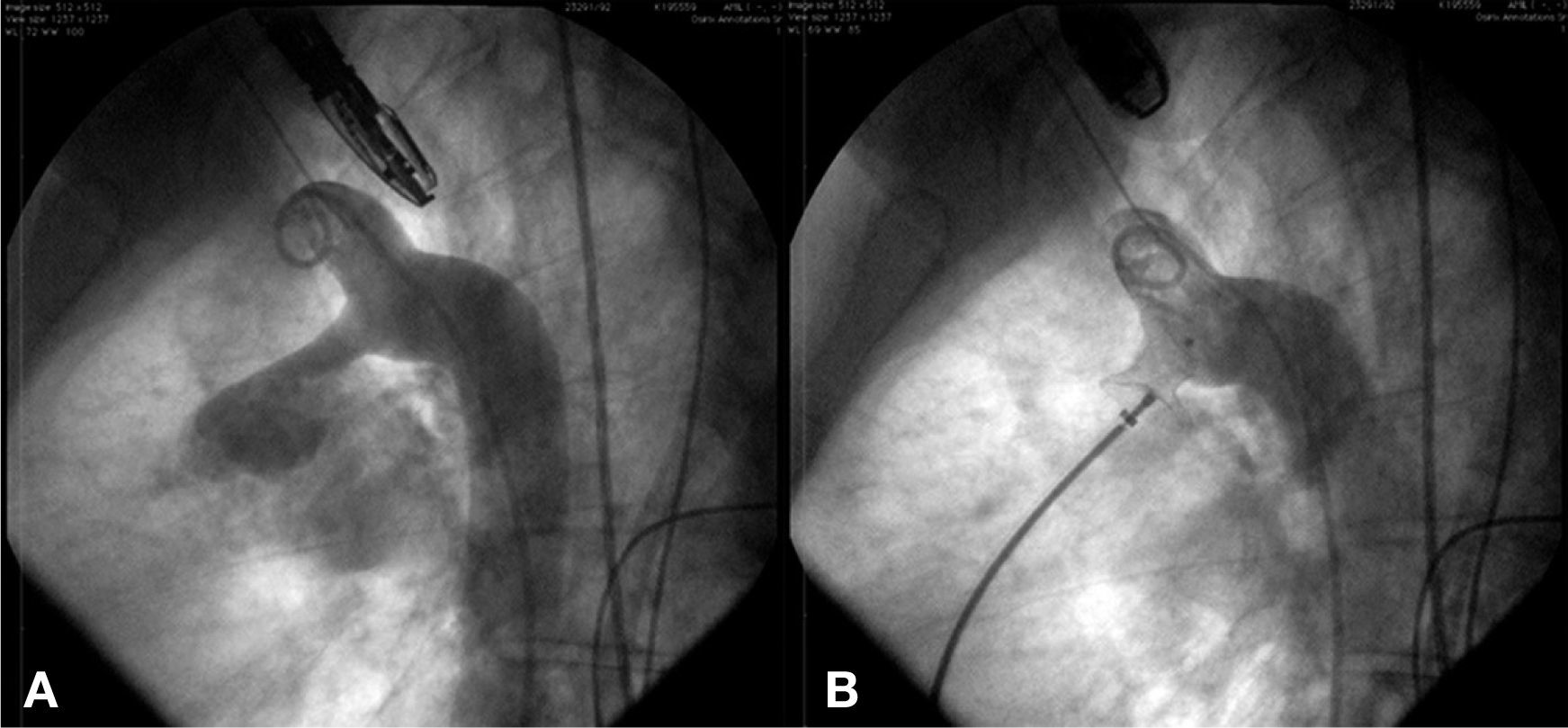
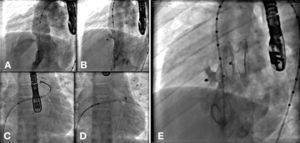
Oclusão de persistência de canal arterialForam ocluídos canais arteriais como primeiro procedimento, em três casos (casos 2, 4 e 5) pela técnica tradicional, utilizando‐se próteses Amplatzer® Duct Occluder tipo I 6‐4mm (St. Jude Medical, St. Paul, Estados Unidos), Cera® Muscular VSD Occluder 16mm e Cera® PDA Occluder Flex 6‐8mm (Lifetech, Shenzhen, China). No caso 2, foi realizada a oclusão de um vaso colateral como segundo procedimento, utilizando‐se duas molas Flipper® 3PDA3 (Cook Medical, Bloomington, Estados Unidos), liberadas sequencialmente. No caso 4, foram ocluídas duas CIV musculares (descrito a seguir). O caso 5 teve também ocluída uma CIA OS com prótese Cera® ASD Occluder de 18 mm (Lifetech, Shenzhen, China). Ambos os casos foram bem‐sucedidos e nenhum apresentou obstrução da aorta descendente ou do ramo esquerdo pulmonar (fig. 2).
Oclusão de comunicação interventricular perimembranosaOclusão de CIV perimembranosa foi realizada como primeiro procedimento em três casos. Todos apresentavam pressão sistólica pulmonar normal e algum grau de aumento nos diâmetros diastólicos do ventrículo esquerdo por sobrecarga volumétrica. Nenhum caso apresentou regurgitação aórtica antes ou após o procedimento. A CIV do paciente do caso 3 era um pertuito residual pós‐operatório por deiscência do patch cirúrgico, e os demais eram defeitos congênitos (casos 7 e 9). Os defeitos mediram, respectivamente, 7, 5 e 8mm na extremidade ventricular direita. Foram ocluídos com próteses Cera® VSD Occluder tipo I de 8, 7 e 10mm. No mesmo procedimento, foram realizadas também a oclusão de CIA OS em dois pacientes (casos 3 e 9) e a PCA no caso 7. As CIA OS foram ocluídas como segundo procedimento, sendo utilizadas, respectivamente, próteses Cera® ASD Occluder de 16mm e Cera® ASD Occluder Flex de 22mm. A PCA foi ocluída com prótese Cera® PDA Occluder Flex 6‐8mm.
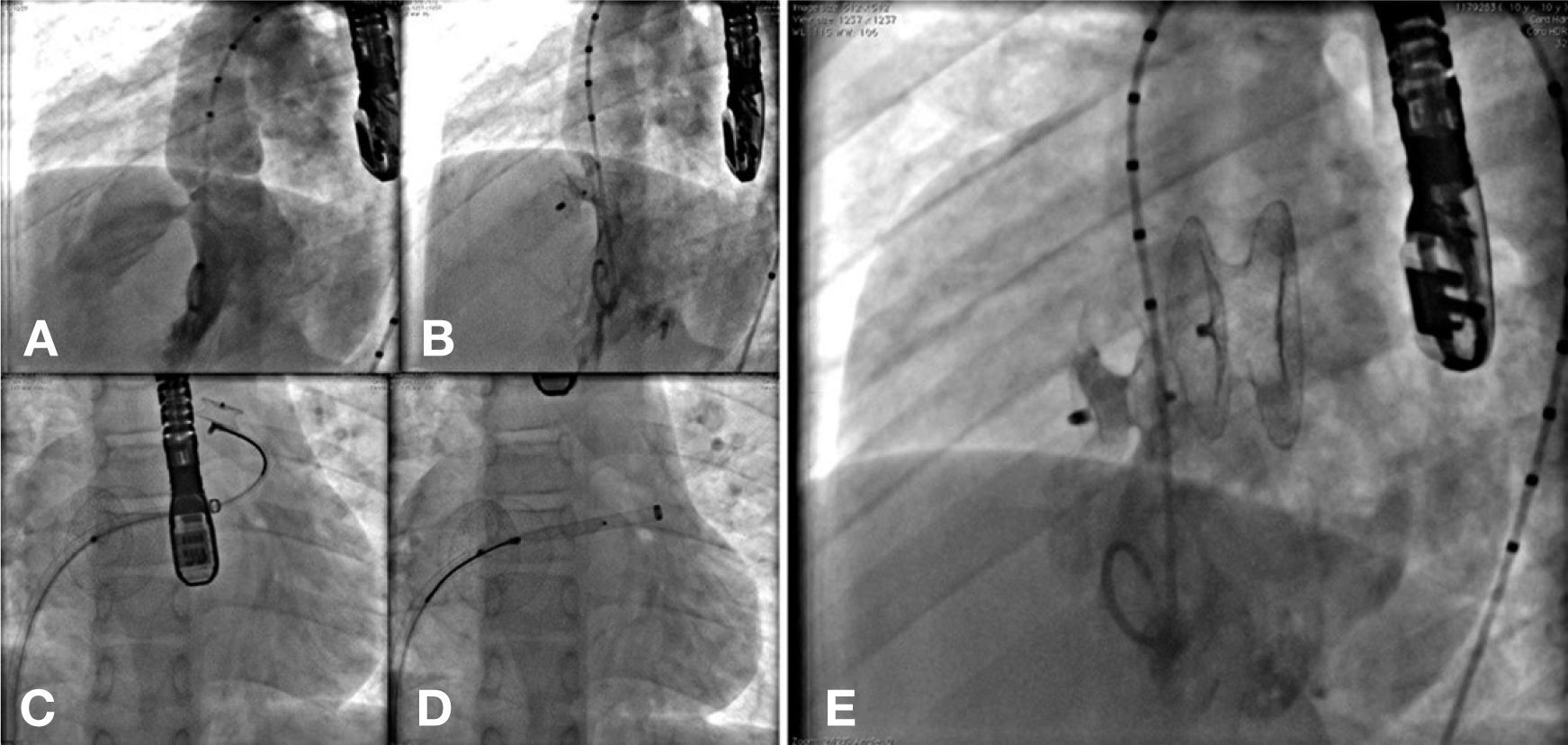
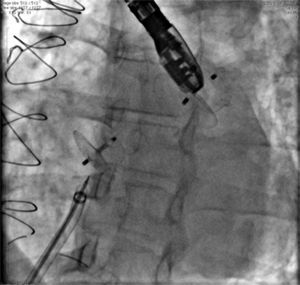
No caso 9, após a oclusão da CIA OS, observou‐se que a prótese de CIV havia embolizado para o ramo esquerdo pulmonar. Ela foi, então, capturada com cateter laço de 20mm e retirada pelo interior da bainha longa de 12mm, utilizada para o implante da prótese de CIA OS. Ambos os defeitos estavam ocluídos ao final do procedimento, que foi encerrado sem novas intercorrências (fig. 3).
Em A, ventriculografia esquerda em oblíqua anterior esquerda, eixo longo, mostra comunicação interventricular abaixo da valva aórtica. Em B, a comunicação interventricular ocluída por uma prótese Cera® VSD Occluder tipo I. Em C, nota‐se a presença de prótese Cera® ASD Occluder Flex ocluindo a comunicação interatrial tipo ostium secundum e a prótese de comunicação interventricular embolizada para o ramo esquerdo pulmonar. Observa‐se que o pino de conexão está capturado pelo cateter laço. Em D, a prótese de comunicação interventricular sendo retirada pelo interior da bainha longa. Em E, observam‐se a prótese de comunicação interatrial em posição e a segunda prótese de comunicação interventricular, ocluindo completamente o defeito.
Em nenhum caso houve interferência na valva tricúspide e nem ocorrência de regurgitação aórtica. Nenhum paciente apresentou distúrbios na condução atrioventricular após o procedimento.
Oclusão de comunicação interventricular membranosaA paciente do caso 4 apresentava hipertensão arterial pulmonar grave por CIVs musculares múltiplas. Durante o cateterismo de rotina, foi percebida uma PCA tubular medindo 10mm e que não tinha sido diagnosticada ao ecocardiograma transtorácico. Foi ocluída, como primeiro procedimento, com uma prótese Cera® Muscular VSD Occluder de 16mm. Na sequência, foram ocluídas duas CIV musculares medindo 8 e 11mm com próteses Cera® Muscular VSD Occluder de 10 e 14mm. Ao final do procedimento, não houve redução apreciável da pressão pulmonar e a paciente permaneceu em tratamento ambulatorial, em protocolo específico para hipertensão arterial pulmonar.
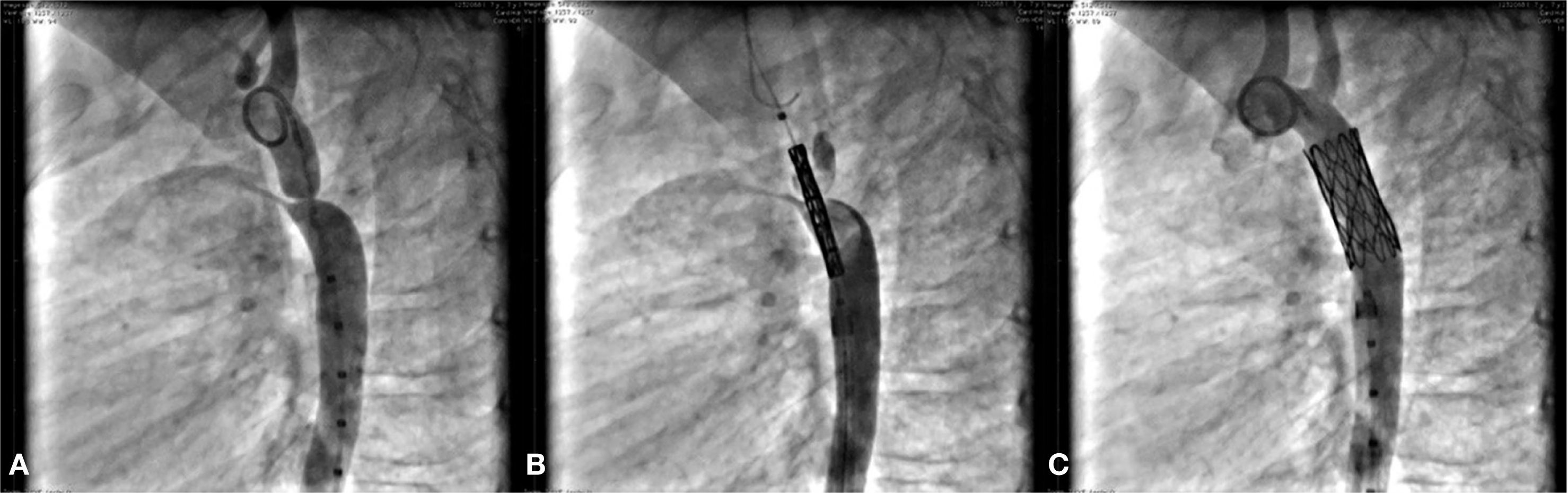
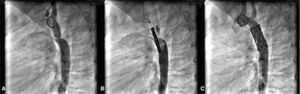
Dilatação de coarctação de aortaO paciente do caso 10, de 7 anos de idade, apresentava CoAo e PCA cônico. A CoAo foi dilatada e a PCA ocluída simultaneamente pelo implante de stent CP Recoberto 8ZIG28, montado sobre balão Power Flex Plus 12/40, introduzido pelo interior de bainha de Mullins 10 F sobre fio‐guia rígido posicionado na artéria subclávia esquerda. O gradiente através da área estreitada mediu 64mmHg e reduziu‐se para 5mmHg após o implante do stent. O procedimento foi bem‐sucedido e ambas as lesões foram tratadas adequadamente, sem complicações (fig. 4).
Em A, aortografia descendente em perfil esquerdo mostra a presença de coarctação de aorta. Observa‐se, também, um canal arterial cônico opacificando o tronco pulmonar. Em B, na mesma incidência, nota‐se o stent recoberto posicionado através da coarctação já no exterior e acima da bainha de entrega. Em C, o stent totalmente expandido, promovendo a dilatação da coarctação e a oclusão completa do canal arterial.
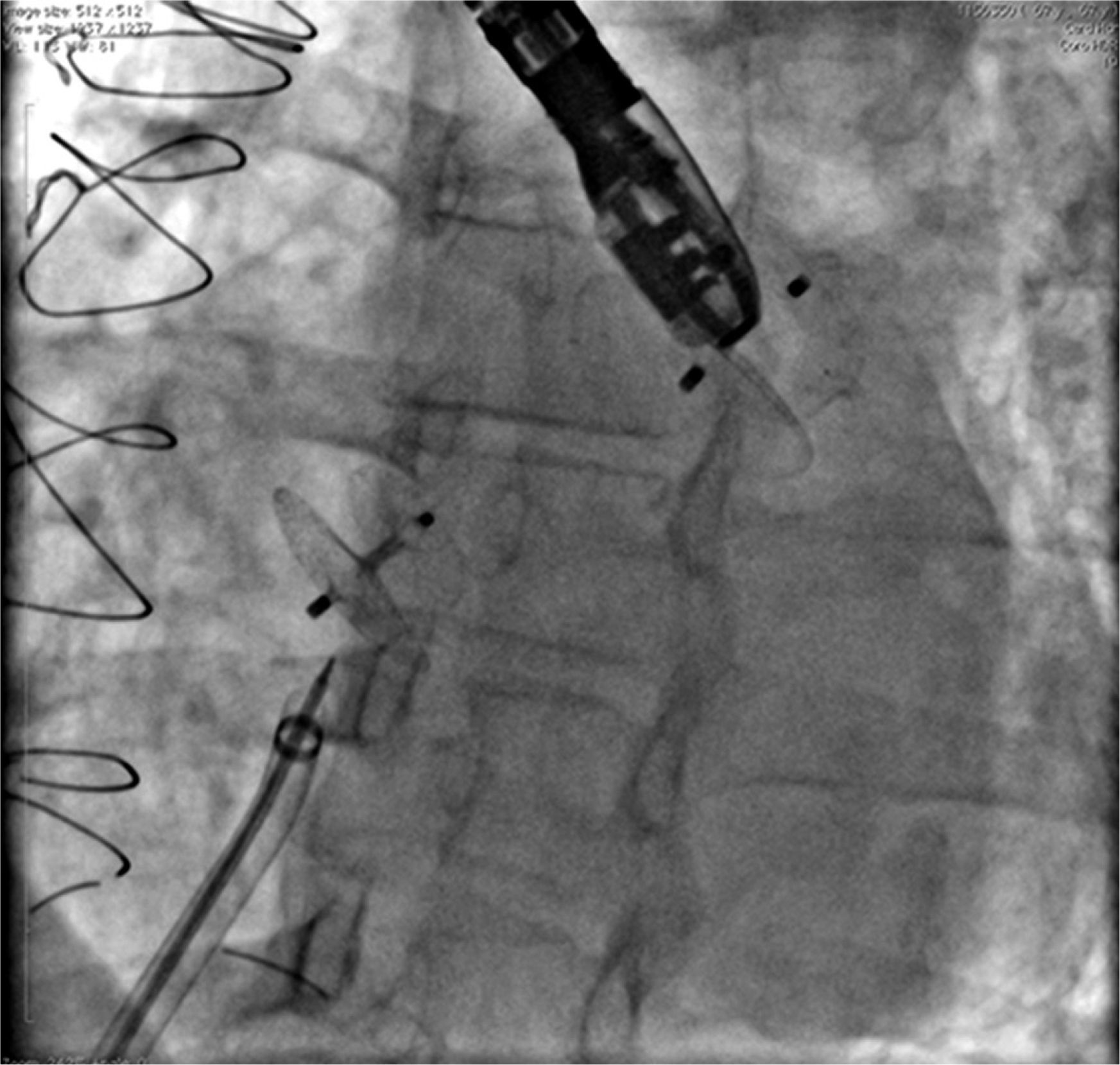
A paciente do caso 8, de 67 anos de idade, portadora de doença arterial coronariana crônica, sofreu dois infartos do miocárdio aos 32 e 33 anos, tendo sido submetida à cirurgia de revascularização miocárdica em 1983 e 2000. Desde 2013 apresentava ritmo de fibrilação atrial. Apresentou acidente vascular cerebral isquêmico em maio de 2014, quando foi diagnosticado FOP em ETE. Foi instituída anticoagulação oral com varfarina, suspensa por apresentar hemorragia retiniana. O AAE foi acessado através do forame oval, sem necessidade de punção transeptal, e ocluído com prótese Amplatzer® Cardiac Plug de 24mm. O FOP foi fechado com prótese Amplatzer® PFO Occluder de 25mm, usando‐se o mesmo cabo e a mesma bainha de entrega. Ambos os defeitos foram ocluídos com sucesso (fig. 5).
Observa‐se a presença do Amplatzer® Cardiac Plug no interior do apêndice atrial esquerdo, em posição mais superior e, mais inferiormente, o Amplatzer® PFO Occluder ocluindo o forame oval. Notam‐se também a bainha longa com dupla curvatura e o cabo de entrega em seu interior, imediatamente após liberar a segunda prótese.
O tempo médio de seguimento foi de 31 ± 28,1 meses (1 a 84 meses).
Não houve shunts residuais nos casos de colateral aortopulmonar, PCA, CIA OS, FOP, CIV perimembranosa e AAE ocluídos. Restou pequeno shunt residual na porção superior da segunda prótese de CIV muscular implantada na paciente do caso 4.
Não houve gradiente residual significativo na CoAo do caso 10.
Ocorreram duas complicações menores: a embolização de uma prótese de CIV muscular (caso 9), retirada sem dificuldades do ramo esquerdo pulmonar, e uma pequena fístula arteriovenosa no local da punção na paciente do caso 8, reparada por rafia cirúrgica e que foi, provavelmente, causada por lesão arterial ocorrida durante as coronariografias realizadas previamente.
Não houve óbitos nessa pequena série de casos.
DiscussãoA correção de associação de mais de um defeito cardíaco era, tradicionalmente, realizada pela cirurgia. O desenvolvimento de técnicas percutâneas de tratamento possibilitou a abordagem da maioria dos defeitos cardíacos mais simples e, em alguns casos, tornou‐se o tratamento de escolha para os defeitos mencionados, nos centros que dispõem de profissionais especializados.3–6,12–16
A realização de procedimentos combinados não é simples e demanda planejamento antes de sua execução. Alguns princípios básicos devem ser seguidos com o maior rigor: quando há associação de defeitos cardíacos, é fundamental que todos sejam passíveis de abordagem por via percutânea, por meio de técnicas estabelecidas e com resultados universalmente comprovados. Caso contrário, o paciente deve ser referido para correção cirúrgica, o que promove a completa e adequada resolução dos defeitos encontrados.
Da mesma forma, não se deve tratar percutaneamente um defeito antes de esgotada a possibilidade de resolução espontânea.
Com respeito a aspectos técnicos, a maioria dos autores norteia seus procedimentos com base em dogmas sobre como abordar primeiramente as lesões valvares12 abordar o defeito mais difícil ou mais complexo em primeiro lugar e, depois, o mais simples ou menos complicado,14 e levar em consideração a possibilidade de acesso aos defeitos. Os defeitos mais remotos devem ser abordados em primeiro lugar. Dessa forma, não se deve ocluir um defeito septal em primeiro lugar, sabendo‐se que será necessário acessar o átrio esquerdo para abordar o apêndice atrial ou a valva mitral posteriormente.
Nos procedimentos aqui apresentados, procuramos seguir as ponderações acima expostas. No entanto, invertemos a sequência de abordagem em dois casos, sem prejuízo dos resultados. No caso 4, foi fechado o canal arterial antes das CIVs musculares, o que não acarretou qualquer tipo de dificuldade para o fechamento dos defeitos do septo ventricular. No caso 9, ocluímos primeiramente a CIV perimembranosa, seguida pela CIA OS, como preconizado. Após a liberação da prótese de CIA OS, foi observada a embolização da prótese de CIV perimembranosa, que foi retirada. Na sequência, foi implantada nova prótese, do mesmo tipo, no septo ventricular, mas de tamanho maior que a anterior, sem que houvesse qualquer tipo de interferência ou dificuldade provocada pela presença da prótese em septo atrial. Como regra geral, as normas aqui citadas são bastante adequadas, mas pode haver espaço para improvisações, a critério da experiência do operador, desde que não dificultem e nem impeçam a completa resolução dos defeitos em questão.
A vantagem do tratamento simultâneo de defeitos combinados é bastante óbvia. Além de oferecer uma alternativa de tratamento para pacientes tradicionalmente abordados de forma cirúrgica, com todos seus riscos e inconvenientes, evita a ocorrência de múltiplos procedimentos intervencionistas, minimiza a exposição radiológica, impede o risco de procedimentos anestésicos repetidos, reduz o número de punções vasculares e corta custos.
ConclusõesNa pequena experiência demonstrada, todos os procedimentos realizados se mostraram seguros, eficazes e potencialmente reproduzíveis por operadores experimentados. No estado atual da Cardiologia Intervencionista, a realização de procedimentos simultâneos em defeitos combinados é uma realidade e pode ser a primeira opção de tratamento em centros especializados.
Fonte de financiamentoNão há.
Conflitos de interesseFrancisco Chamié é consultor técnico e proctor da Boynton, representante dos produtos Lifetech. Os demais autores declaram não haver conflitos de interesse.