La craneosinostosis es un trastorno congénito que requiere intensas cirugías reconstructivas que implican alta probabilidad de hemorragia severa, transfusión masiva y difícil abordaje de la vía aérea. Debido a que el manejo anestésico previsto para este procedimiento presenta particularidades y metas de prioritario alcance, la presentación de la experiencia del departamento de anestesiología en el programa de cirugía de anomalías craneofaciales toma gran importancia.
ObjetivoDescribir el comportamiento de variables anestésicas en el perioperatorio de pacientes llevados a corrección de craneosinostosis en el Hospital Infantil Universitario de San José.
MétodosEstudio observacional de cohorte retrospectiva en pacientes intervenidos entre el 1 de enero de 2008 y el 31 de enero del 2012. Se realizó extracción de datos de historias clínicas electrónicas y registros anestésicos.
ResultadosLos datos de mayor relevancia fueron la hemorragia y la transfusión. La hemorragia quirúrgica fue de 35,6cc/kg (DE=17,4), lo cual consideramos como hemorragia severa; allí los casos que utilizaron ácido tranexámico no presentaron inferiores volúmenes hemorrágicos o transfusionales de glóbulos rojos empaquetados (GRE) intraoperatorios, menor tiempo de ventilación mecánica o estancia en la unidad de cuidados intensivos (UCI). Observamos menor cantidad de GRE transfundidos en la UCI en los casos que recibieron desmopresina.
ConclusionesSugerimos que probablemente el ácido tranexámico (14mg/kg) y la desmopresina (0,36mg/kg) en esta cohorte no se relacionaron con disminución de la hemorragia, ni menor cantidad de GRE transfundidos durante el intraoperatorio; solo describimos menor cantidad de GRE transfundidos en la UCI asociados al empleo de desmopresina.
Craniosynostosis is a congenital disorder requiring extensive reconstructive surgery that entails a high probability of severe bleeding, massive transfusion and difficult airway management. Considering that the anaesthetic management for this procedure has special requirements and priority targets, presenting the experience of the anaesthesiology department working under the programme for surgery of craniofacial abnormalities is of the greatest importance.
ObjectiveDescribe the behaviour of anaesthetic variables during the perioperative period inpatients taken to craniosynostosis correction at Hospital Infantil Universitario de San José.
MethodsRetrospective observational cohort study in patients taken to surgery between January 1st 2008 and January 31st 2012. Data were collected from electronic clinical records and anaesthesia records.
ResultsThe most relevant data were haemorrhage and transfusion. Blood loss was 35.6 cc/kg (SD = 17.4), considered as severe haemorrhage. Patients receiving tranexamic acid did not show lower intra-operative levels of blood loss or packed red blood cell (PRBC) transfusions, shorter mechanical ventilation or ICU (intensive care unit) length of stay. We observed a smaller number of PRBC transfusions in patients in the ICU who received desmopressin.
ConclusionsThe high rate of consumption of nutritional supplements in patients about to undergo surgery, possible drug interactions and adverse effects of perioperative consumption of some herbs, should be a warning to the anesthesiologist who performed the pre-anesthetic consultation; is necessary to include this in the interview and take decisions about it. We recommend to request always packing of the products.
La craneosinostosis es reconocida en el ámbito médico por su difícil tratamiento, habitualmente condicionado a la ejecución de procedimientos invasivos de alto impacto para la reserva funcional del paciente y la economía de nuestro sistema de salud; es allí donde el programa quirúrgico de anomalías craneofaciales del Hospital Infantil Universitario de San José se encamina a devolver al niño una expectativa funcional y de convivencia en el medio que lo rodea. Los resultados en los últimos años nos hacen pensar que el ejercicio realizado podría marcar diferencias con respecto a desenlaces de impacto vital con respecto a otros centros de referencia encargados de casos similares. Este estudio describe el resultado de las variables perioperatorias de los pacientes intervenidos de craneosinostosis entre el 1 de enero de 2008 y el 31 de enero del 2012 por el Departamento de Anestesiología del Hospital Infantil Universitario de San José, Bogotá, Colombia.
Materiales y métodosLa presente investigación se desarrolló previa aprobación del Comité de Ética e Investigación y la División de Investigaciones de la facultad de Medicina de la Fundación Universitaria de Ciencias de la Salud (FUCS) para desarrollarse en el Hospital Infantil Universitario de San José; debido a su naturaleza, no requirió consentimiento informado. Se realizó descripción por género de datos demográficos, anestésicos y críticos; se estimaron medias y desviaciones estándar para variables continuas, así como frecuencias y porcentajes para variables nominales; se compararon valores de media para desenlaces como hemorragia, transfusión, días de ventilación mecánica y estancia en UCI; se estratificaron diversas variables, y por último se postularon hipótesis para nuevos trabajos.
Se tomaron como diferencias estadísticamente significativas aquellas con una p<0,05. Se realizó búsqueda no sistemática de la literatura médica y se discutieron nuestros datos con los existentes en la literatura internacional; paquete estadístico STATA10.
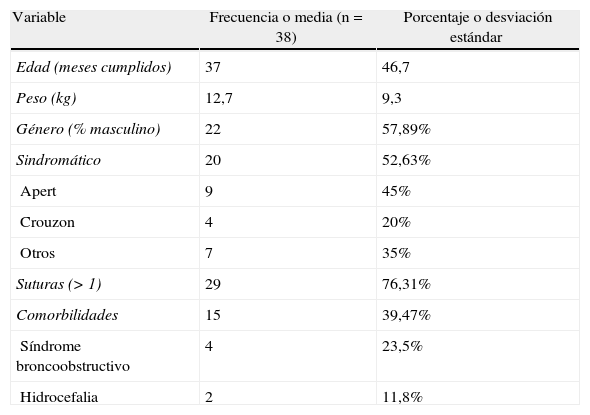
ResultadosEntre el 1 de enero de 2008 y el 31 de enero de 2011 se identificaron 41pacientes intervenidos. Se excluyeron 3 por no cumplir los criterios de inclusión, y en 3casos no se pudieron extraer los datos anestésicos intraoperatorios. Los 35restantes aportaron el 100% de los datos (tabla 1).
Datos demográficos
| Variable | Frecuencia o media (n=38) | Porcentaje o desviación estándar |
| Edad (meses cumplidos) | 37 | 46,7 |
| Peso (kg) | 12,7 | 9,3 |
| Género (% masculino) | 22 | 57,89% |
| Sindromático | 20 | 52,63% |
| Apert | 9 | 45% |
| Crouzon | 4 | 20% |
| Otros | 7 | 35% |
| Suturas (> 1) | 29 | 76,31% |
| Comorbilidades | 15 | 39,47% |
| Síndrome broncoobstructivo | 4 | 23,5% |
| Hidrocefalia | 2 | 11,8% |
Comorbilidades: condiciones presentes en los pacientes previo a la cirugía.
La valoración preanestésica de la vía aérea no demostró una importante prevalencia de predictores de vía aérea difícil. Solo el 17,6% de pacientes de esta cohorte se tipificaron como Cormack 3, el 2,9% presentaron dificultad para la apertura oral y solo el 5,2% fueron considerados como verdadera vía aérea difícil en la intubación, a pesar de que el 50% presentaban Mallampati mayor o igual a iii (iv=8,3%).
En todos los casos se utilizó monitorización básica e invasiva de la presión arterial, en el 60% de los casos la menor temperatura media fue de 35,09°C (DE=0,78) y el 94,7% de los casos recibieron monitorización y terapia a través de catéter venoso central.
Los anestésicos más utilizados durante la inducción fueron sevoflurano (64,7%) y propofol (32,4%). Solo el 71,4% usó un analgésico específico en esta fase (remifentanilo en el 88% de las ocasiones). Se realizó bloqueo neuromuscular en el 91,2% de los casos, siendo el pancuronio y el rocuronio los más empleados (37,5 y 25%, respectivamente). Para el mantenimiento anestésico la combinación remifentanilo-sevoflurano fue la elección en el 88,6%, mientras que sevoflurano se constituyó como el anestésico inhalatorio más utilizado (94,3%).
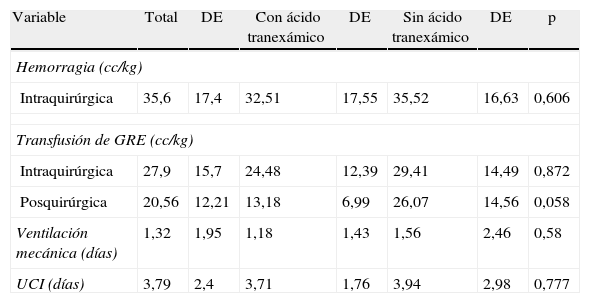
En cirugía, los pacientes sangraron en promedio 35,6cc/kg (DE=17,4), requirieron transfusión de 27,9cc/kg (DE=15,7) de glóbulos rojos empaquetados (GRE) en quirófano y 20,55cc/kg (DE=12,21) de GRE en la UCI. Además se encontró una importante diferencia en la cantidad de otros hemoderivados (diferentes a GRE) transfundidos entre quirófanos y la UCI (cirugía 2,7% vs UCI 36,8%, correspondiente a 1 vs 14casos) (tabla 2). Al ingreso en cirugía los pacientes presentaron una hemoglobina (Hb) de 13,27g/dl (DE=1,14), mientras que al egreso una Hb de 11,46g/dl (DE=2,04) y una base exceso (BE) de –8,55 (DE=2,98) diagnóstica de acidemia metabólica a pesar de existir solo una diferencia media de 1,69g/dl entre la Hb al ingreso a salas e ingreso a la UCI.
Pérdidas sanguíneas, transfusión de GRE, días de ventilación mecánica y estancia en la UCI
| Variable | Total | DE | Con ácido tranexámico | DE | Sin ácido tranexámico | DE | p |
| Hemorragia (cc/kg) | |||||||
| Intraquirúrgica | 35,6 | 17,4 | 32,51 | 17,55 | 35,52 | 16,63 | 0,606 |
| Transfusión de GRE (cc/kg) | |||||||
| Intraquirúrgica | 27,9 | 15,7 | 24,48 | 12,39 | 29,41 | 14,49 | 0,872 |
| Posquirúrgica | 20,56 | 12,21 | 13,18 | 6,99 | 26,07 | 14,56 | 0,058 |
| Ventilación mecánica (días) | 1,32 | 1,95 | 1,18 | 1,43 | 1,56 | 2,46 | 0,58 |
| UCI (días) | 3,79 | 2,4 | 3,71 | 1,76 | 3,94 | 2,98 | 0,777 |
DE: desviación estándar; GRE: glóbulos rojos empaquetados; UCI: unidad de cuidados intensivos.
Se empleó ácido tranexámico en el 44,7% de los casos, a una dosis media de 14mg/kg bolo y una dosis media de infusión de 1,1mg/kg/h; solo a 8pacientes se les aplicó adicionalmente desmopresina a una dosis de 0,36μg/kg bolo. De los 17pacientes (44,7%) que recibieron ácido tranexámico, al 41,2% le fue aplicado solo bolo, mientras que al 47,1% le fue administrada la combinación bolo e infusión a dosis ya descritas.
Como medida indirecta del efecto del ácido tranexámico, se calculó la volemia de cada paciente según la edad y el peso, y se trazaron metas de hemorragia al 25, 33, 40 y 50% de lo deducido; al describir los volúmenes de hemorragia y compararlos entre los que recibieron el medicamento y los no expuestos, no se encontraron diferencias significativas entre los pacientes que sangraron menos del 40 y del 50% de la volemia calculada (9 vs 4; p=0,105, para hemorragia menor del 40%, y 9 vs 9; p=0,746, para hemorragia menor del 50%). Tampoco se encontraron diferencias significativas para hemorragias menores del 25 y del 33% de la volemia calculada (tabla 2).
Tampoco se observó disminución de la hemorragia en grupo de pacientes para los que recibieron desmopresina. Por el contrario, la mayor proporción de pacientes que presentaron sangrado menor del 50% de la volemia calculada correspondió al grupo sin dicho medicamento (p=0,001); a su vez, tampoco describimos diferencias para pérdidas calculadas por debajo del 25, del 33 y del 40% de la volemia.
Al estratificar las medias de transfusión en quirófano con la colocación de ácido tranexámico, los promedios variaron de 24,48cc/kg (DE=12,39) en los pacientes expuestos a ácido tranexámico a 29,41cc/kg (DE=14,49) en los que no recibieron dicho medicamento, pero sin diferencias significativas (p=0,872); mientras que en la UCI las medias de transfusión presentaron diferencias marginales pero no consideradas como significativas para el uso de GRE (13,18cc/kg [DE=6,99] vs 26,07cc/kg [DE=14,56] para una p=0,058), lo cual de ningún modo rechaza su uso por el origen de los datos y por lo contrario soporta la decisión de generar experimentos que evalúen dicha hipótesis.
Al estratificar el efecto de la desmopresina, no hallamos diferencias en los promedios de transfusión de GRE en quirófanos (29,17cc/kg [DE=12,92] vs 26,26 [DE=13,85] para una p=0,949), pero al estratificar los volúmenes de transfusión de GRE en la UCI se hallaron diferencias significativas (15,82cc/kg [DE=3,01] vs 22,81cc/kg [DE=16,32] para una p=0,027), lo cual sugiere que la desmopresina podría reducir el sangrado microcirculatorio en la UCI, y por lo tanto los requerimientos transfusionales de GRE, los cuales observamos que no estaban relacionados con la transfusión de otros derivados sanguíneos.
El 13,5% requirieron soporte hemodinámico en quirófanos, siendo habitual el uso de norepinefrina (66,7%), mientras que el 42,1% de los pacientes durante su estancia en la UCI recibieron soporte con dopamina y/o norepinefrina (87,5%).
El tiempo quirúrgico fue de 303,1min (DE=92) y no se asoció con incremento en la tasa de hemorragia en quirófano o UCI. Se presentaron comorbilidades postoperatorias en el 42,1% de los casos, siendo la coagulación intravascular diseminada (CID) la complicación más frecuente (35%), seguida del croup postextubación y la insuficiencia renal aguda (con un 10,5% cada uno). El tiempo medio de ventilación mecánica fue de 1,32días (DE=1,94). La duración media en la UCI fue de 3,79días (DE=2,39), y ninguno de los pacientes falleció durante la hospitalización.
Para esta cohorte no observamos relación entre craneosinostosis sindrómica e incremento en los volúmenes de hemorragia, morbilidad o mortalidad; en cambio, describimos un leve incremento en los días de estancia en la UCI (2,78 [DE=1.22] vs 4,7 [DE=2,83] para una p=0,011) y en el tiempo de ventilación mecánica (0,39 [DE=1,03] vs 2,15 [DE=2,21] para una p=0,004). Al analizar las variables independientes número de suturas y complejidad (cirugía de avance vs corrección de varias suturas y avances) no se hallaron diferencias con respecto a desenlaces hemorrágicos y/o transfusionales, ni con modificación del tiempo quirúrgico.
DiscusiónLos procedimientos quirúrgicos desarrollados para la corrección de la craneosinostosis son reconocidos por su alto volumen de sangrado y máximo riesgo de transfusión masiva, así como lo describen Kho1 y Soriano2; usualmente los pacientes son lactantes o escolares y presentan comorbilidades que a su vez están asociadas a medicamentos para su adecuado control, factores que afectan el resultado de este tipo de procedimientos3.
En la literatura mundial se referencia al manejo de la vía aérea difícil y al control de la hemorragia como los principales ítems de intervención anestesiológica. En este estudio, si bien el 17,6% de los pacientes fueron tipificados como Cormack3 y el 5,9% considerados como vía aérea difícil, en el momento de la intubación no se presentó ninguna complicación. No sugerimos la no presencia de vía aérea difícil en estos pacientes, por lo contrario queremos expandir el gran respeto y protocolización que tenemos en el Departamento de Anestesiología al acceso de la vía aérea probablemente difícil en dimorfismo craneofacial pediátrico.
La tasa de hemorragia intraoperatoria fue acorde a lo reportado por otros autores, pero al analizar los sangrados publicados asociados a diferentes estrategias procoagulantes hallamos algunas diferencias; para Goobie et al.4 (en un experimento que empleó ácido tranexámico para pacientes en corrección de craneosinostosis) la hemorragia fue menor en el grupo de ácido tranexámico (62cc/kg [DE=22]) vs placebo (101cc/kg [DE=63]). A su vez Dadure y Sauter5, en un estudio similar, encontraron tasas de hemorragia homogéneas (grupo ácido tranexámico: 51,4cc/kg [DE=28,3] versus grupo placebo: 61,1cc/kg [DE=16,8]; p=0,25), sin embargo, calcularon una reducción del 85% en la transfusión intraoperatoria en el grupo de ácido tranexámico (p=0,02), de la mano de un protocolo riguroso con eritropoyetina y suplencia de hierro.
El volumen intraoperatorio transfundido en este estudio fue de 27,9cc/kg (DE=15,7), lo cual se correlaciona con los requerimientos transfusionales publicados a nivel mundial; para Goobie et al.4, el valor medio de transfusión en quirófanos fue de 33cc/kg (DE=13), allí mismo los GRE usados en el posoperatorio fueron 3cc/kg (IC95% entre 0 y 25), mientras que en el artículo de Dadure y Sauter5 el volumen transfundido intraoperatorio fue de 1,6cc/kg en el grupo de ácido tranexámico vs 11cc/kg en el grupo placebo, con un valor de p=0,01.
En la literatura mundial el ácido tranexámico se emplea con dosis bolo (10 a 100mg/kg) e infusión (1 a 10mg/kg/h); para estos pacientes se empleó una dosis bolo promedio de 14mg/kg y ocasionalmente se relacionó con una infusión de 1mg/kg/h, lo cual no se relacionó con un menor volumen de hemorragia, ni a más baja cantidad de GRE transfundidos en cirugía o en la UCI. El presente análisis abre un interrogante sobre la real eficacia de ácido tranexámico a las dosis empleadas para prevención de hemorragia mayor y reducción en el empleo de hemoderivados, lo cual es concordante con lo demostrado por Neilipovitz et al.6.
Dadure y Sauter5 utilizaron dosis de ácido tranexámico similares a las empleadas en este grupo de pacientes (15mg/kg seguido de infusión a 1mg/kg/h), pero combinado con eritropoyetina subcutánea preoperatoria y suplemento de hierro, no hallando disminución en la tasa de hemorragia, pero sí del volumen de hemotransfusión, similar a lo reportado por Meneghini et al.7 y Fearon y Weinthal8.
En una interesante reflexión sobre la metodología y los resultados publicados por los anteriores autores, Holcomb9 discute la solvencia y la profundidad de sus conclusiones, aconsejando al criterio médico tener un mejor fundamento a la hora de iniciar este antifibrinolítico para dichos pacientes; seguramente el discernimiento de las dosis específicas (en bolo o infusión), la construcción de protocolos y la proyección de metas transfusionales, junto con la diversidad de efectos de cierta manera controlables asesorados por una monitorización simultánea (en tiempo real) y moderna de la coagulación, podría conducirnos a un establecimiento preciso de indicaciones, seguimiento y metas a alcanzar con el ácido tranexámico9.
La utilización de desmopresina como medicamento coadyuvante o como terapia única para esta cohorte de pacientes tampoco disminuyó el volumen hemorrágico ni la cantidad de GRE usados en cirugía. Llama la atención que los volúmenes de transfusión de GRE observados en la UCI fueron significativamente menores (15,82 vs 22,81; p=0,027), lo cual sugiere un posible beneficio relacionado con su aplicación en quirófanos y por lo tanto nos recomienda la comprobación experimental de dichas observaciones. Es claro que el modelo de hemorragia presente en el postoperatorio inmediato y temprano presenta diversas etiologías, se diferencia según el grupo etario y es producto en mayor proporción de un defecto intrínseco de la coagulación que una disrupción vascular persistente en el paciente pediátrico, bases que podrían justificar su posible eficacia en estos pacientes10.
Si bien el empleo de hemoderivados restrictivamente han disminuido la tasa de complicaciones con respecto a las medidas liberales, no necesariamente previenen su morbilidad; además, a diferencia de la incidencia de complicaciones transfusionales en adultos (13:100.000 unidades de GRE), en los infantes esta se triplica (37:100.000 unidades de GRE)11, siendo muy importante el estudio de alternativas como hemodilución normovolémica/hipervolémica, hipotensión deliberada, antifibrinolíticos, salvador de células sanguíneas, concentrado de fibrinógeno y autotransfusión entre otros métodos de conservación hemática, pero que en la actualidad permanecen sin investigación y aplicación para este grupo etario11-15.
El presente estudio esboza el modelo de anestesia empleada en el Hospital Infantil Universitario de San José para craneosinostosis, el cual incluye en inducción y mantenimiento agentes intravenosos e inhalados ratificados en la literatura mundial dada la ventaja de una pronta y confortable evaluación neurológica después de cirugía16. Sus conclusiones nos permiten crear hipótesis acerca del manejo preventivo de la hemorragia severa para población pediátrica de alto riesgo.
La premisa de que el ácido tranexámico a dosis promedio de 14mg/kg puede ofrecer las mismas bondades que dosis mayores podría no ser cierta; para esta cohorte retrospectiva, los volúmenes de hemorragia y transfusión en diferentes momentos con respecto a la aplicación de ácido tranexámico fueron similares.
Si bien la transfusión masiva contribuyó a mejorar los índices de perfusión y se optimizaron los niveles de hemoglobina, no significó la prevención de CID, ni la disminución de acidosis metabólica, igual a lo mencionado por Choi et al.17. Solo uno de nuestros pacientes recibió PFC durante la cirugía, lo cual es similar a lo reportado por Kerner et al.18, quienes publicaron que la aplicación de PFC intraoperatorio no disminuye el volumen hemorrágico, el requerimiento transfusional ni el tiempo de estancia en la UCI. En nuestra investigación la alta tasa de CID asociada a transfusión agresiva con GRE, una reanimación hídrica con cristaloides libre de importante acidemia metabólica y la presencia de hipotermia leve sugieren reconsiderar la administración temprana de PFC y PLA guiadas por monitorización moderna de la coagulación (tromboelastografía), de la misma forma que la oportuna reposición de calcio iónico sérico.
En consonancia con lo descrito a nivel mundial, la estrategia de abordaje de la vía aérea en el paciente con anormalidades faciales debe estar soportada a un planeamiento preoperatorio meticuloso; para De Beer y Bingham19 la clave del éxito radica en identificar el sitio de la anormalidad, el grado de apertura oral y la movilidad del cuello, además del control de todos los factores que puedan exacerbar la presión intracraneal y/o descompensar las condiciones cardiacas patológicas; para estos mismos autores la técnica invasiva de la vía aérea debe ser seleccionada individualmente19. En nuestro estudio los casos rara vez se correlacionaron con intubación difícil o complicaciones respiratorias perioperatorias, hallazgos similares a los de Barnett et al.20, quienes hallaron en el síndrome de Apert una incidencia de complicación baja (4,5%). A diferencia de la dificultad reportada para el abordaje de la vía aérea en pacientes con hipoplasia mediofacial por sus proporciones intermaxilares irregulares y reducción del movimiento temporomandibular19, en nuestra cohorte la minoría de los casos (17,6%) correspondió a un Cormack gradoiii, y solo el 5,26% correspondió a vía aérea difícil, lo cual esta posiblemente relacionado con la incursión de técnicas avanzadas y modernas de manejo (videolaringoscopia e intubación fibroóptica).
El embolismo aéreo durante la craniectomía del paciente con craneosinostosis es bastante frecuente y su incidencia va del 36 al 82,6%21-23; en esta cohorte no se hizo el estudio ni el diagnóstico, lo cual representa un punto débil a la hora de analizar la causa del soporte hemodinámico en la UCI.
Al igual que lo referenciado por la literatura mundial, la etiología sindrómica de la craneosinostosis, las comorbilidades, los fármacos utilizados hasta la cirugía, el número de suturas y la complejidad tampoco se correlacionaron con aumento en el volumen de hemorragia, en la transfusión de hemoderivados o en la morbilidad, hallando solamente con etiología sindrómica un leve incremento en el tiempo de ventilación mecánica y en los días de estancia en cuidados intensivos.
En esta cohorte, el medio anestésico aparentemente no modificó la hemorragia, la transfusión, las horas de ventilación, la estrategia de fast-tracking ni los días de estancia en la UCI.
ConclusionesNuestras observaciones en relación con la hemorragia y el requerimiento transfusional nos hace sospechar que el ácido tranexámico (a dosis media de 14mg/kg) en población pediátrica llevada a corrección de craneosinostosis podría no prevenir la hemorragia masiva ni disminuir el volumen de transfusión de GRE, así como los días de ventilación mecánica y los días de estancia en la UCI; sugerimos que su uso debe estar sujeto a la disponibilidad de la mejor evidencia sobre dosis pediátrica, esquema de administración y monitorización de la coagulación.
Sugerimos que la monitorización invasiva, el planeamiento apropiado de la vía aérea y la transfusión temprana restrictiva basada en metas de perfusión celular y coagulación son los pilares del manejo anestésico, los cuales creemos pudieron disminuir la frecuencia de efectos adversos y la mortalidad de esta cohorte con respecto a la reportada a nivel mundial.
Recomendamos fuertemente la realización de estudios clínicos aleatorizados para determinar la efectividad de diferentes dosis de antifibrinolíticos para la prevención de la hemorragia severa y los altos volúmenes de transfusión, así como la investigación de alternativas a la transfusión y conservación hemática en pacientes pediátricos llevados a cirugías de alto riesgo de hemorragia. De la misma forma apreciamos la necesidad de una guía de práctica clínica para dicho reto anestésico.
FinanciaciónDivisión de Investigaciones de la Fundación Universitaria de Ciencias de la Salud, Bogotá, Colombia.
Conflicto de interesesNinguno declarado.
A la Fundación Universitaria de Ciencias de la Salud, al Hospital Infantil Universitario de San José y a sus Departamentos de Anestesiología, Cirugía Plástica, Neurocirugía y al programa de Cirugía Reconstructiva de Anomalías Craneofaciales (CSAP).