La levobupivacaína y la ropivacaína son anestésicos locales relativamente nuevos, desarrollados con el fin de abordar la cuestión de la toxicidad de la bupivacaína. Aunque existen ciertas diferencias entre sus perfiles farmacológicos, su relevancia clínica en dosis equipotentes no es evidente hasta ahora.
ObjetivoComparar la eficacia y las características de las dosis equipotentes de levobupivacaína por vía intratecal con las de ropivacaína.
MetodologíaA sesenta pacientes de grado ASAI/II de 18 a 60años y de ambos sexos, programados para cirugía ortopédica del miembro inferior bajo anestesia espinal, se les administró al azar o bien 15mg de levobupivacaína o 22,5mg de ropivacaína. El bloqueo motor, el bloqueo sensorial, las características hemodinámicas y cualquier otro efecto secundario fueron registrados.
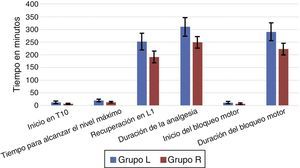
ResultadosEl inicio del bloqueo sensorial en T10 fue más rápido en el grupo R que en el grupo L (p<0,0001). El nivel mediano (rango) alcanzado en el grupo R fue T7 (T5-T10), mientras en el grupo L fue T7 (T4-T10). El tiempo para alcanzar el nivel máximo y para alcanzar un grado 3 en la escala de Bromage fue más breve en el grupo R en comparación con el grupo L (p<0,0001). La levobupivacaína produce una duración significativamente más larga (290,50±34,67min) del bloqueo motor que la ropivacaína (222,50±23,00min). La duración de la analgesia fue significativamente más larga en el grupo L (309,83±36,45min) que en el grupo R. No se registraron efectos adversos graves.
ConclusiónLa levobupivacaína produce una duración de la analgesia significativamente más larga que la ropivacaína cuando se utiliza en una proporción de 0,6:1. La eficacia, la toxicidad y el perfil hemodinámico hacen de la ropivacaína un agente adecuado para cirugías con un umbral bajo de hipotensión.
Levobupivacaine and ropivacaine are relatively new local anaesthetics developed in order to address the issue of bupivacaine toxicity. Although certain differences do exist between their pharmacological profiles, its clinical relevance at equipotent doses is not evident so far.
ObjectiveTo compare the efficacy and characteristics of equipotent doses of intrathecal levobupivacaine with ropivacaine.
MethodologySixty ASA gradeI/II patients of 18-60years, either sex posted for lower limb orthopaedic surgery under spinal anaesthesia were randomly given either 15mg levobupivacaine or 22.5mg ropivacaine. Sensory and motor block, haemodynamic characteristics, as well as any side effects, were recorded.
ResultsOnset of sensory block to T10 was more rapid in group R than group L (P<.0001). The median (range) height achieved in group R was T7 (T5-T10) while in group L was T7 (T4-T10). Time to reach maximum height and time to modified bromage grade 3 was shorter in group R as compared to group L (P<.0001). Levobupivacaine produced significantly longer (290.50±34.67min) duration of motor block compared to ropivacaine (222.50±23.00min). Duration of analgesia was significantly longer in group L (309.83±36.45min) than group R (249.50±22.83). No serious adverse effects were recorded.
ConclusionLevobupivacaine produces significantly longer duration of analgesia than ropivacaine when used in a ratio of 0.6:1. Efficacy, toxicity and haemodynamic profile make ropivacaine suitable agent for surgeries with low threshold for hypotension.
La bupivacaína ha sido, tradicionalmente, el fármaco elegido para el bloqueo subaracnoideo. Sin embargo, la duración significativamente larga de su acción retrasa la recuperación de la función motora y programa la estancia del paciente en la unidad de cuidados postanestésicos. Además, varios estudios han demostrado que la bupivacaína produce una mayor toxicidad neurológica y cardiaca en comparación con otros anestésicos locales1. Los problemas asociados con la toxicidad de la bupivacaína racémica motivaron el desarrollo de agentes anestésicos locales alternativos adecuados de tipo «enantiómeros aislados» con bajo riesgo de toxicidad en el sistema nervioso central (SNC) y cardiaca. La levobupivacaína y la ropivacaína son 2 agentes anestésicos amidas relativamente nuevos que se han producido con el fin de evitar los problemas de toxicidad de la bupivacaína.
La levobupivacaína es un anestésico local de alta potencia y larga duración con un inicio de acción relativamente lento2. Es menos propensa a bloquear los canales de sodio y potasio inactivados y su grado de disociación es más veloz comparado con su forma racémica3. La mayoría de los estudios in vitro, in vivo y en farmacodinámica humana del bloqueo de nervio indican que la levobupivacaína tiene una potencia similar a la bupivacaína, pero que su riesgo de toxicidad cardiovascular o del SNC es menor4. Así, tener un umbral más elevado de toxicidad cardiaca y neurotoxicidad, comparado con la bupivacaína racémica, brinda a los anestesistas mayor seguridad al trabajar con levobupivacaína5, y esta tiene el potencial de reemplazar a la bupivacaína como fármaco estándar6.
La ropivacaína es el isómero S del propilo análogo de la bupivacaína con mayor duración de la acción, baja solubilidad en lípidos, potencia baja y bajo riesgo de toxicidad cardiovascular y del SNC7. La ropivacaína bloquea las fibras nerviosas implicadas en la transmisión del dolor (fibras Aδ y C) en un grado mayor que las que controlan la función motora (fibras Aβ)8. Por eso, se ha encontrado que la ropivacaína induce un bloqueo motor menos intenso que la bupivacaína. Dada su duración relativamente más corta, la recuperación más rápida de la función motora y el menor nivel de toxicidad, este fármaco se ha identificado como un beneficio potencial para la cirugía de duración intermedia, así como para la cirugía ambulatoria en centros de cuidados ambulatorios.
En la era actual de medicina basada en la evidencia, cada paso de nuestro manejo se evalúa a fondo de acuerdo con la investigación médica revisada por pares, y el bloqueo subaracnoideo no es una excepción. La idea de que una sola inyección de bupivacaína puede hacerlo todo está en entredicho y se requiere el uso cuidadoso de sustitutos más seguros. Para Casati y Putzu9 las diferencias teóricas y experimentales sí existen en toxicología y en perfiles clínicos debido a las diferentes potencias anestésicas de esas formas isoméricas de bupivacaína, pero hasta ahora estas características no se han reflejado de manera evidente en la práctica clínica. Es por esta razón que tenemos que explorar las características típicas y los usos potenciales de estos nuevos fármacos. Se han realizado muchos estudios que comparan distintas formas de bupivacaína, ropivacaína y levobupivacaína; sin embargo, la mayoría de ellos han usado dosis que pueden resultar inadecuadas para cirugías de cadera10. Además, por lo general han empleado formas hiperbáricas11,12, y no se ha considerado la relación de potencia entre la levobupivacaína y la ropivacaína13.
Por lo tanto, este estudio fue realizado para comparar la eficacia y las características de formas isobáricas de levobupivacaína intratecal al 0,5% y ropivacaína al 0,75% en dosis equipotentes para cirugía ortopédica de miembros inferiores.
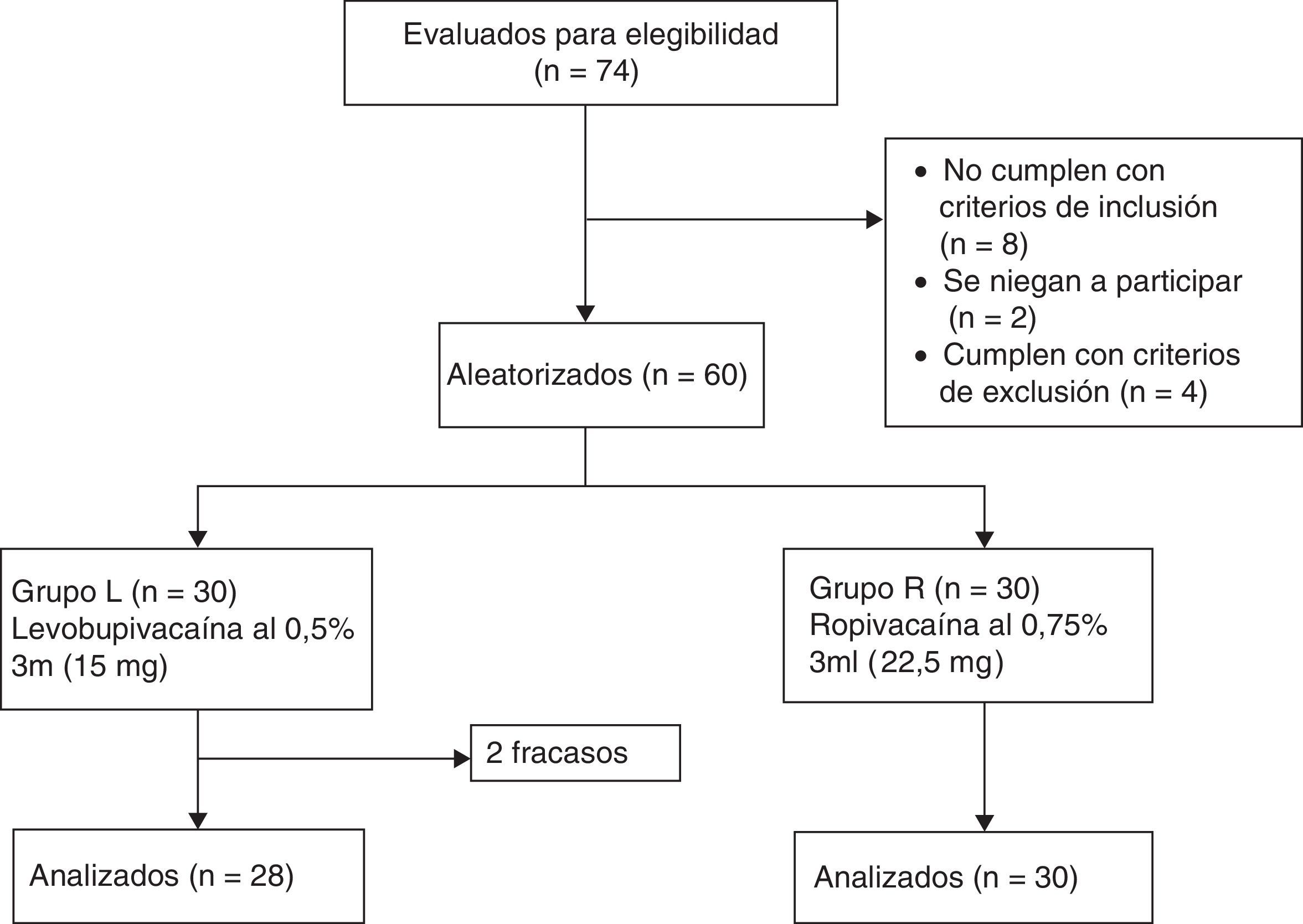
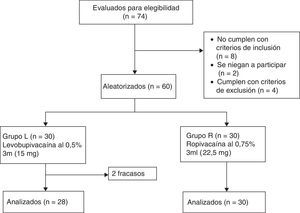
MetodologíaLuego de la aprobación del comité de ética institucional (referencia n.¿ D1303/FM y registro de ensayo clínico n.¿ NCT02201784) y del consentimiento informado por escrito, este ensayo clínico de equivalencia, prospectivo, aleatorizado, doble ciego y controlado fue llevado a cabo en sesenta pacientes de grado ASAI/II de ambos sexos entre los 18 y los 60años sometidos a anestesia espinal para cirugía ortopédica de los miembros inferiores. Se excluyeron pacientes con contraindicación para anestesia espinal, con alergia conocida a anestésicos locales y, finalmente, pacientes con antecedentes de diabetes y enfermedades neurológicas o musculoesqueléticas que pudieran dificultar la técnica. Los pacientes fueron divididos de manera aleatoria en 2 grupos de 30 personas cada uno (grupo L y grupo R) por la aleatorización generada por el computador (fig. 1). Los pacientes del grupo L recibieron 3ml de levobupivacaína a 5mg/ml (15mg de LEVO-ANAWIN® 0,5%, Neon Laboratories Ltd.), mientras el grupo R recibió 3ml de ropivacaína a 7,5mg/ml (22,5mg de ROPIN® 0,75%, Neon Laboratories Ltd.). Todos los fármacos fueron preparados por un anestesiólogo que no estaba involucrado en la valoración posterior de los pacientes, mientras que otro anestesiólogo administró la anestesia y evaluó a todos los participantes. Los pacientes fueron monitoreados según el estándar, incluyendo electrocardiografía, oximetría de pulso y monitoreo de la presión arterial no invasiva (PANI). Se midieron la frecuencia cardíaca (FC) basal, la saturación arterial de oxígeno (SaO2) y PANI. Todos los pacientes recibieron oxígeno vía máscara de Hudson a razón de 6l/min hasta finalizada la cirugía. Se aseguró el acceso intravenoso, y los pacientes fueron premedicados con 0,1mg/kg de ondansetrón por vía intravenosa y precarga realizada con 15ml/kg de solución del lactato de Ringer. Tomando precauciones asépticas estrictas, se infiltró la piel de los pacientes con lidocaína al 2% y la punción lumbar se realizó en posición sentada con una aguja espinal punta Quincke calibre 25 (Becton Dickinson, Madrid, España), utilizando un abordaje por línea media en el espacio intervertebral L3-4. Se verificó la colocación correcta de la aguja por la circulación libre de líquido cefalorraquídeo (LCR) y se confirmó por aspiración y reinyección de LCR antes y después de la administración de la solución del fármaco estudiado. El fármaco fue inyectado durante un periodo de 20s. Después de la inyección del fármaco espinal, los pacientes fueron colocados en posición supina de inmediato, momento en el cual el tiempo fue registrado como «cero». El nivel de bloqueo sensorial fue evaluado cada 5min hasta la pérdida de sensación de pinchazo, usando una aguja hipodérmica calibre 22 con 2mm de protrusión a través del capuchón de seguridad de la aguja. Después de finalizada la cirugía continuaron las evaluaciones en intervalos de 30min hasta que la sensación normal retornó. Después de confirmar la pérdida de sensación en el dermatoma T10 en comparación con la del dermatoma C5-6, se administró 0,03mg/kg de midazolam por vía intravenosa a los pacientes, y a los cirujanos se les permitió proceder con la cirugía. La incapacidad de alcanzar el nivel sensorial en T10 en 30min fue considerada como un «fracaso». A estos pacientes se les administró anestesia general, y no fueron incluidos en el análisis sino reportados como número total de «fracasos» de acuerdo con el análisis por protocolo. El bloqueo motor en las extremidades inferiores fue clasificado según la escala modificada de Bromage14 (grado 0=sin bloqueo motor; grado 1=incapacidad de elevar la pierna extendida, capaz de mover las rodillas y los pies; grado 2=incapacidad de elevar la pierna extendida y mover la rodilla, capaz de mover los pies; grado 3=bloqueo motor completo de miembros inferiores). La evaluación del bloqueo motor se llevó a cabo cada 5min hasta que se alcanzó el grado 3 y luego cada 30min hasta lograr la recuperación completa (grado 0). La FC basal, SaO2 y PANI se registraron antes de la inducción, cada 3min hasta alcanzar los 15min, y luego cada 15min hasta el alta de la sala de recuperación. La hipotensión se definió como presión arterial sistólica <90mm Hg y fue tratada con inyección intravenosa en bolo de mefenteramina de 6mg con fluidos. La bradicardia se definió como FC<50latidos/min y se trató con la administración intravenosa de atropina de 0,5mg cuando era sintomática. Para evaluar el inicio de la anestesia se tuvieron en cuenta el tiempo requerido para que el bloqueo sensorial se desarrollara en T10, el nivel máximo del bloqueo y el tiempo para alcanzar dicho nivel. Para evaluar la duración del bloqueo sensorial se compararon el tiempo para la regresión a L1 y la duración de la analgesia (resultado primario). También se observaron el tiempo para alcanzar el bloqueo motor máximo, la duración del bloqueo motor y cualquier otro efecto secundario.
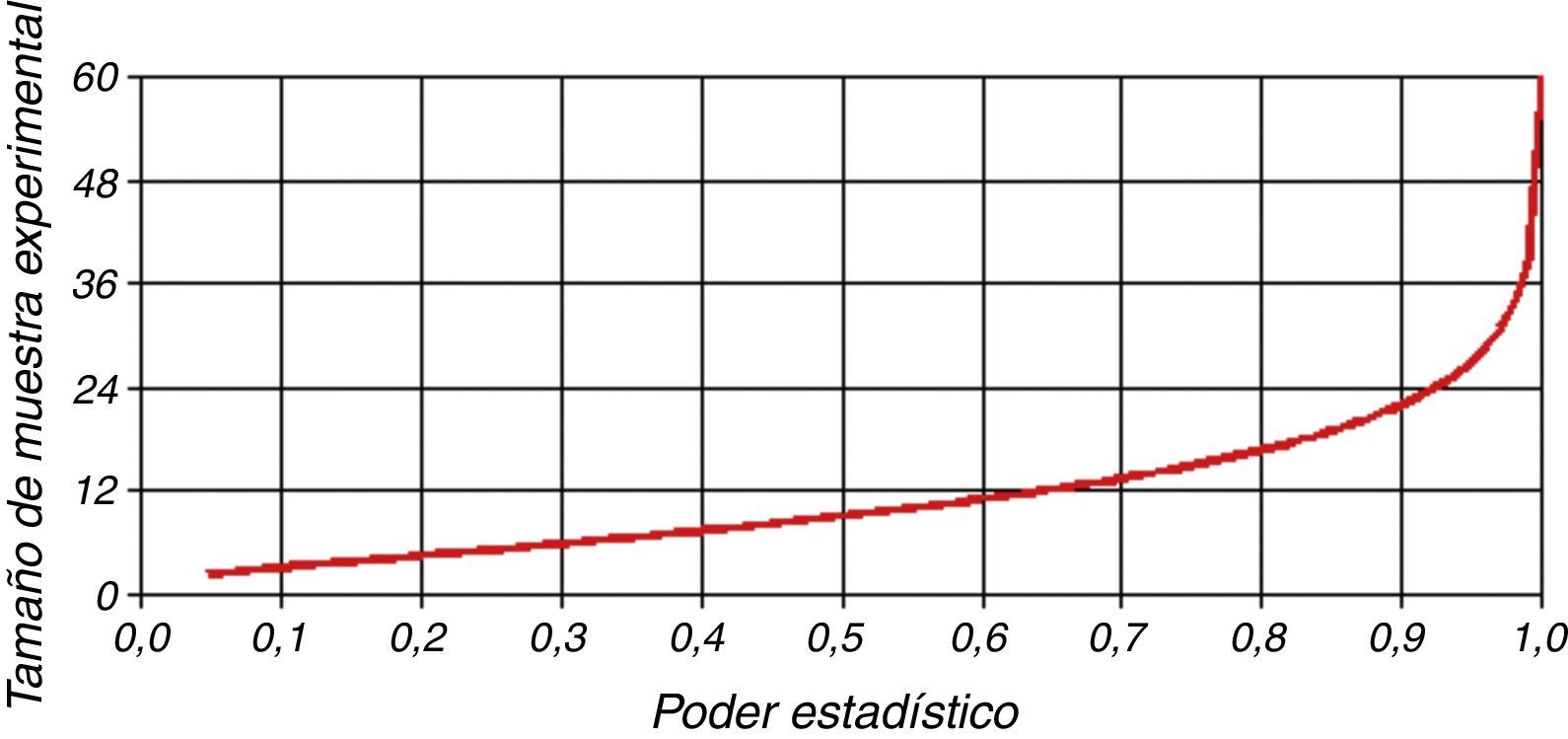
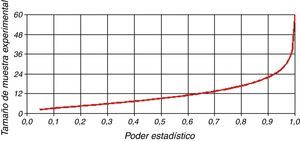
Análisis estadísticoEl análisis de poder estadístico estimó que un tamaño de muestra de 30 pacientes por grupo arrojaría un poder de 95% para probar la hipótesis a un margen de equivalencia de 30min de diferencia en el tiempo medio hasta la primera necesidad de analgésicos (PS Power and Sample Size Calculator-Version 3.0.43; William D. Dupont, Walton D. Plummer). La probabilidad de error tipoi asociada con esta prueba para la hipótesis nula de que la levobupivacaína y la ropivacaína en dosis equipotentes son similares en cuanto a la duración de la analgesia fue de α=0,05 (fig. 2). El análisis estadístico se llevó a cabo usando Excel 2013 (Microsoft, Redmond, VA), software SPSS (Versión 19, SPSS Inc., Estados Unidos) y Graph Pad Prism 5.00 (Graph Pad Software, San Diego, CA). Los datos son presentados en forma de media (±DE), mediana (rango) o frecuencias (%) según el caso. Los datos demográficos de grupo y los eventos adversos fueron comparados mediante prueba t no pareada o prueba de chi-cuadrado (χ2), la que resultara pertinente. Las características de bloqueo, la duración de la analgesia y la hemodinámica fueron comparadas con prueba t no pareada. Para comparar las variaciones intragrupo desde la línea de base se utilizaron ANOVA unidireccional y la prueba de comparaciones múltiples de Dunnett. Un valor de p<0,05 fue considerado estadísticamente significativo.
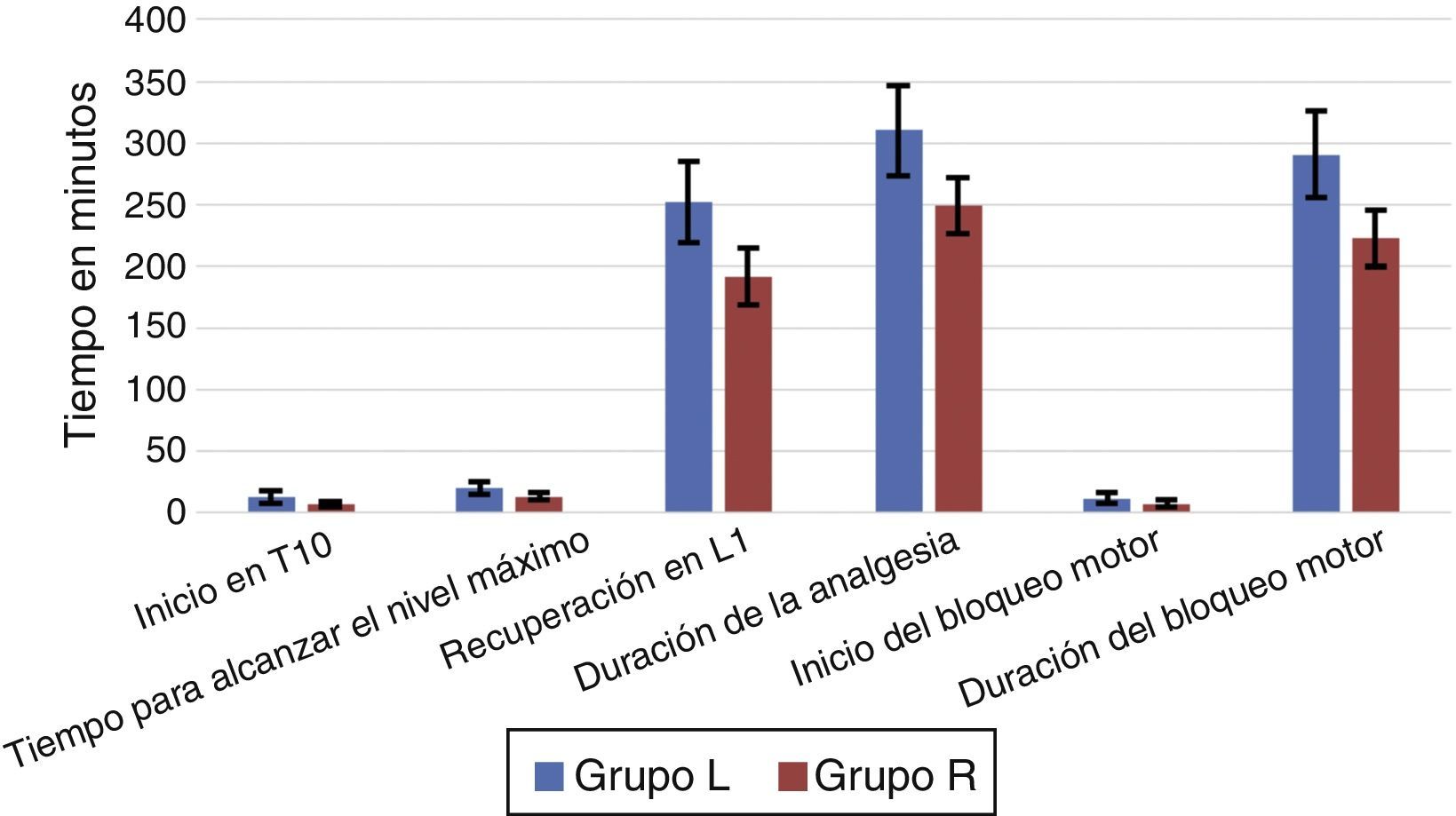
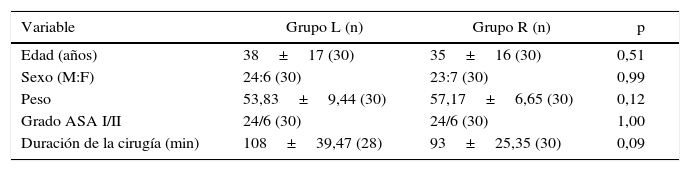
ResultadosNo se observaron diferencias significativas entre los 2 grupos con respecto a edad, sexo, peso, grado ASA o duración de la cirugía (tabla 1). La anestesia fue exitosa en todos los pacientes, a excepción de 2 «fracasos» en el grupo L. El inicio de la anestesia en T10 fue de 7,33±2,49min en el grupo R y 13,50±4,86min en el grupo L (p<0,0001). La mediana (rango) del nivel máximo alcanzado en el grupo R (en términos de dermatomas) fue T7 (T5-T10), mientras que en el grupo L fue T7 (T4-T10). El tiempo para alcanzar el nivel máximo fue más breve en el grupo R (13,17±3,02min) que en el grupo L (20,33±5,31min), p<0,0001 (tabla 2, fig. 3).
Características de los pacientes
| Variable | Grupo L (n) | Grupo R (n) | p |
|---|---|---|---|
| Edad (años) | 38±17 (30) | 35±16 (30) | 0,51 |
| Sexo (M:F) | 24:6 (30) | 23:7 (30) | 0,99 |
| Peso | 53,83±9,44 (30) | 57,17±6,65 (30) | 0,12 |
| Grado ASA I/II | 24/6 (30) | 24/6 (30) | 1,00 |
| Duración de la cirugía (min) | 108±39,47 (28) | 93±25,35 (30) | 0,09 |
M:F: masculino:femenino; n: número de pacientes.
p≤0,05 es considerado estadísticamente significativo.
Fuente: autores
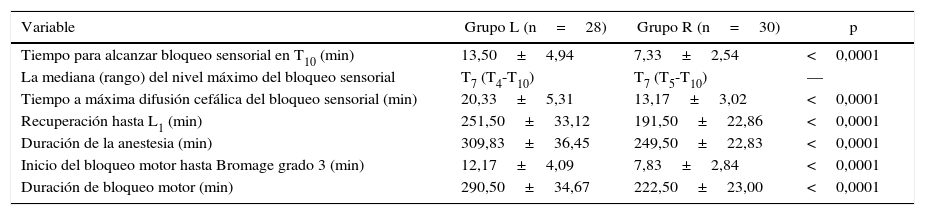
Características del bloqueo
| Variable | Grupo L (n=28) | Grupo R (n=30) | p |
|---|---|---|---|
| Tiempo para alcanzar bloqueo sensorial en T10 (min) | 13,50±4,94 | 7,33±2,54 | <0,0001 |
| La mediana (rango) del nivel máximo del bloqueo sensorial | T7 (T4-T10) | T7 (T5-T10) | — |
| Tiempo a máxima difusión cefálica del bloqueo sensorial (min) | 20,33±5,31 | 13,17±3,02 | <0,0001 |
| Recuperación hasta L1 (min) | 251,50±33,12 | 191,50±22,86 | <0,0001 |
| Duración de la anestesia (min) | 309,83±36,45 | 249,50±22,83 | <0,0001 |
| Inicio del bloqueo motor hasta Bromage grado 3 (min) | 12,17±4,09 | 7,83±2,84 | <0,0001 |
| Duración de bloqueo motor (min) | 290,50±34,67 | 222,50±23,00 | <0,0001 |
n: número de pacientes; T: nivel de dermatoma.
Los datos se expresan como media±DE o mediana (rango).
p≤0,05 es considerado estadísticamente significativo.
Fuente: autores.
El tiempo hasta el grado 3 en la escala modificada de Bromage (MB-3) fue de 7,83±2,84min en el grupo R y de 12,17±4,09min en el grupo L, p<0,0001. La duración del bloqueo motor por levobupivacaína fue significativamente más larga (290,50±34,67min) que la causada por la ropivacaína (222,50±23,00min), p<0,0001. El tiempo de regresión del bloqueo sensorial a L1 fue más prolongado en el grupo L que en el grupo R (251,50±33,12min versus 191,50±22,86min; p<0,0001). La duración de la analgesia también fue significativamente más larga en el grupo L (309,83±36,45min) que en el grupo R (249,50±22,83min), p<0,0001.
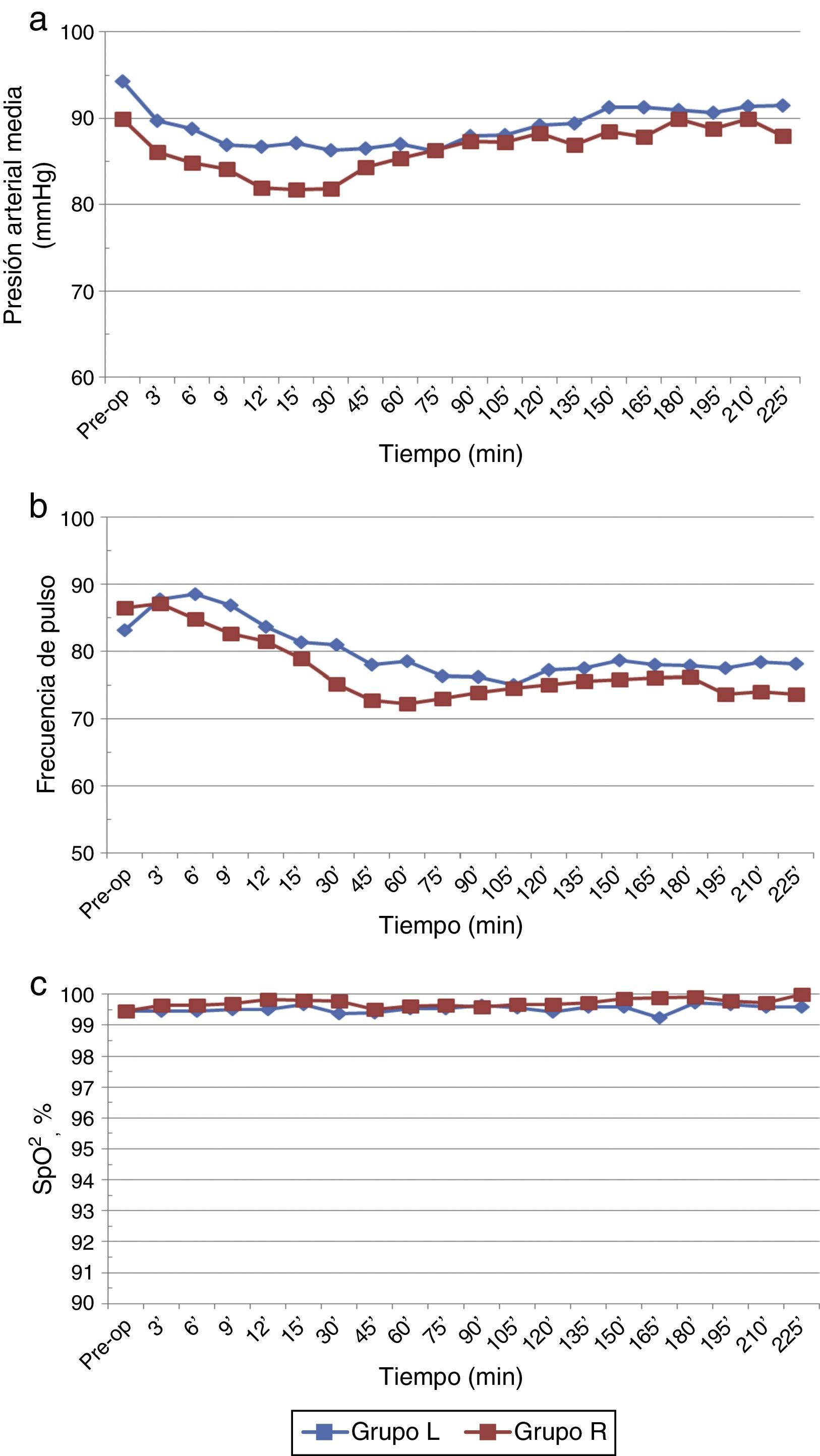
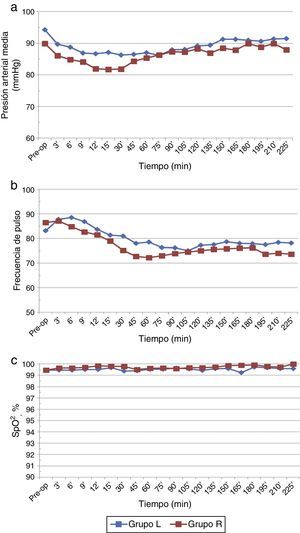
Los parámetros hemodinámicos de base fueron comparables en ambos grupos. La media de la presión arterial media (PAM) se redujo de manera significativa en ambos grupos si se compara con los valores preoperatorios/de base (p<0,05), pero la incidencia general de hipotensión no fue significativamente diferente (fig. 4a). Además, fue transitoria en el grupo de ropivacaína (30min) en comparación con el grupo de levobupivacaína, en el cual se mantuvo (100min). No existieron diferencias significativas entre los 2 grupos con respecto a la frecuencia del pulso y SaO2 (p>0,05) (fig. 4b y c).
No se observó incidencia de Post Dural Puncture Headache (PDPH) o de otros efectos adversos significativos en ninguno de los grupos (tabla 3). La hipotensión fue el efecto secundario más común en ambos grupos; no obstante, la cantidad total de mefentermina utilizada no fue significativamente diferente (p>0,05). Se presentó bradicardia en 2 pacientes de cada grupo durante el periodo intraoperatorio.
Efectos adversos
| Variable | Grupo L (n=28) | Grupo R (n=30) | p |
|---|---|---|---|
| Náuseas y vómitos | 4/0 (14/%) | 2/0 (7%) | 0,42 |
| Hipotensión | 7 (25%) | 10 (33%) | 0,57 |
| Bradicardia | 2 (7%) | 2 (7%) | 0,99 |
| Escalofríos | 3 (11%) | 5 (17%) | 0,71 |
n: número de pacientes.
p≤ 0,05 es considerado estadísticamente significativo.
Fuente: autores.
En nuestro estudio, la levobupivacaína isobárica mostró un inicio del bloqueo sensorial y motor significativamente más lento pero con una duración de la anestesia más prolongada que la ropivacaína.
No se observaron diferencias significativas en las características de los pacientes ni en los parámetros hemodinámicos de base entre los 2 grupos.
La levobupivacaína y la ropivacaína han sido producidas con el fin de abordar los problemas de toxicidad de la bupivacaína10,15. Varios estudios han sido llevados a cabo en el pasado con el fin de evaluar la eficacia clínica y toxicológica de estos anestésicos locales en diferentes dosis y baricidad. La mayoría de estos estudios clínicos ha sugerido que la levobupivacaína era ligeramente menos potente que la bupivacaína pero más potente que la ropivacaína16. Esta mayor potencia de la levobupivacaína en comparación con la ropivacaína podría ser explicada, de manera parcial, por su mayor solubilidad de lípidos y formulación17 que subestima por 12,6% las moléculas activas en comparación con su racemato18. Sin embargo, muchos estudios recientes19,20 han encontrado una diferencia en potencia mayor al 30%, lo que implica que la levobupivacaína es, de hecho, más potente que la ropivacaína. Su potencia, comparada con la de la ropivacaína, se mantuvo inconsistente y variaba entre 1-1,6717. Así, con base en los hechos expuestos anteriormente y en los distintos estudios previos7,19,21,22, asumimos que la levobupivacaína es 1,5 veces más potente que la ropivacaína.
Autores anteriores han usado diferentes dosis (5-17,5mg) de levobupivacaína11,12,23,24. Teniendo en cuenta estudios previos11-13, la concentración analgésica mínima de un anestésico local y la relación de potencia analgésica, usamos 15mg (5mg ml−1) de levobupivacaína y lo comparamos con 22,5mg (7,5mg ml−1) de ropivacaína, con el fin de lograr el bloqueo motor y sensorial adecuado para la mayoría de los procedimientos ortopédicos.
Las conclusiones de varios autores con respecto al tiempo de inicio del bloqueo sensorial varían mucho. De acuerdo con algunos autores, no existe una diferencia significativa en el tiempo de inicio11-13,24. Por el contrario, algunos opinan que sí existe una diferencia significativa en el tiempo de inicio entre los 2 fármacos23,25,26. Sin embargo, en el presente estudio la ropivacaína alcanzó el nivel sensorial de T10 significativamente más rápido que la levobupivacaína, en concordancia con investigaciones pasadas23,25,26. Las variaciones en los hallazgos de estos estudios pueden deberse al tamaño de la muestra, al perfil demográfico, a la metodología, a la dosis usadas y a la baricidad. Cuvas et al.27 solo han estudiado varones de edad avanzada (>60años), mientras que Sananslip et al.28 reclutaron únicamente mujeres programadas para cirugía ginecológica.
En el presente estudio, la mediana del nivel dermatomal que alcanzaron ambos grupos fue T7, pero a la levobupivacaína le tomó más tiempo alcanzar el máximo nivel de bloqueo sensorial que a la ropivacaína. Además, la levobupivacaína (T4-T10) mostró ligeramente mayor variabilidad en comparación con la ropivacaína (T5-T10). Según la mayoría de los autores12,21,23,26-29, la mediana del nivel alcanzado estuvo en el rango T8-T9, con una dosificación y una técnica similares. Sin embargo, algunos autores11,12 obtuvieron resultados variados que podrían ser atribuidos a la diferencia en la dosis y la baricidad de la ropivacaína usada en sus estudios.
Así como en el bloqueo sensorial, la ropivacaína también mostró un inicio del bloqueo motor más rápido, comparado con la levobupivacaína. No obstante, Khaw et al.30 usaron una preparación medida de ropivacaína isobárica para anestesia espinal en posición lateral derecha administrada durante 60s y no encontraron ninguna diferencia significativa. Como no hemos medido la densidad relativa de los fármacos en nuestro estudio, y tomando en cuenta el hecho de que la bupivacaína y la ropivacaína son hipobáricas a 37°C31, puede asumirse que la naturaleza hipobárica de los fármacos utilizados, la posición sentada32,33 y la comparativamente más rápida velocidad de inyección29 han resultado en un inicio del bloqueo motor más rápido.
La regresión sensorial (L1) y motora de la ropivacaína fue más rápida comparada con la de la levobupivacaína en nuestro estudio. Varios autores obtuvieron resultados similares en el pasado con la ropivacaína, evidenciando una recuperación sensorial11,24,25 y motora más breve13,23,27.
La ropivacaína y la levobupivacaína, aparte de ser un poco diferentes en términos de potencias, se consideran casi iguales en la práctica clínica9. Pero el presente estudio mostró que, incluso en dosis equipotentes de 1,5:1(ropi:levo), la ropivacaína ofrece una duración de la analgesia significativamente más corta que la levobupivacaína. Este resultado es similar al de estudios de previos que mostraron una regresión más temprana de la ropivacaína en comparación con la levobupivacaína12,23,34. Sin embargo, Gautier et al.35 no documentaron diferencia alguna cuando compararon 12mg de ropivacaína con 8mg de levobupivacaína en cesáreas. Una respuesta farmacodinámica diferente ocasionada por una dosis más baja y una población de estudio diferente parece ser la explicación más razonable para esta discrepancia.
La disminución de la PAM y de la frecuencia del pulso son 2 de las complicaciones encontradas con mayor frecuencia en el bloqueo neuroaxial. En nuestro estudio observamos que la caída de la presión arterial fue transitoria en el grupo de ropivacaína pero se mantuvo en el grupo de la levobupivacaína. A pesar de esto, no existió una diferencia significativa en la incidencia general de la hipotensión, y estos casos fueron tratados de manera oportuna y sin consecuencias graves. Asimismo, la dosis total requerida de mefentermina para ambos grupos fue comparable (p>0,05). Sin embargo, la mayor incidencia de hipotensión transitoria observada con la ropivacaína pudo haber surgido debido a un alcance más rápido del nivel máximo del bloqueo con este fármaco en comparación con la levobupivacaína, lo que resulta en una caída en la presión arterial; esto de acuerdo con la opinión de Carpenter et al.36.
Se tomó extremo cuidado y vigilancia para evitar sesgos al hacer el estudio aleatorizado y doble ciego. No obstante, los sesgos y las limitaciones aparecen con frecuencia en las investigaciones, y este estudio no es la excepción. El diseño del estudio podría haber permitido cierto grado de sesgo, sobre todo en el análisis del protocolo. Una limitación importante de nuestro estudio fue que no se midió la densidad específica de cada uno de los fármacos. El mantenimiento de la temperatura podría ser un problema en países tropicales, lo que podría haber influido en los resultados generales de este estudio30. Adicionalmente, la concentración mayor de sodio y la osmolalidad de la levobupivacaína aumentan más su densidad. La calidad de la anestesia tampoco fue medida en este estudio.
ConclusiónAsí, concluimos que las dosis de levobupivacaína y la ropivacaína isobáricas usadas en este estudio producen la analgesia y anestesia adecuadas para cirugía ortopédica de miembros inferiores sin efectos secundarios graves. La duración de la analgesia es significativamente más prolongada con la levobupivacaína que con la ropivacaína cuando se usa en una proporción de 0,6:1. Por lo tanto, los fármacos deben ser usados tomando en cuenta la condición del paciente, la duración y el tipo de cirugía. La eficacia, la toxicidad y el perfil hemodinámico hacen de la ropivacaína un agente adecuado para cuidados ambulatorios y otras cirugías con un umbral bajo de hipotensión. La levobupivacaína, por otro lado, es un agente más adecuado para cirugías prolongadas.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciaciónNinguna.
Conflictos de interesesLos autores declaran no tener conflicto de intereses.